Семейная ламинопатия: один ген, два белка, три различных сценария предсердной манифестации фенотипа кардиомиопатии, ассоциированной с новой мутацией в гене ламина A/C (LMNA)
Аннотация
Варианты в гене ламина А/С (LMNA), ответственные за кодирование ядерных белков ламина A и C, являются второй по частоте (после вариантов гена титина) причиной семейной дилатационной кардиомиопатии (КМП). Ламины A и C являются структурными белками, которые играют решающую роль в поддержании целостности и стабильности ядра, а также в регуляции ядерной функции.
Клинические проявления патогенных вариантов LMNA варьируют от фенотипа дилатационной КМП до аритмогенной КМП с нарушениями проводимости, предсердной и/или желудочковой аритмией. Ламинопатии ассоциированы с повышенным риском внезапной сердечной смерти даже у бессимптомных носителей при отсутствии признаков КМП. Для ранней стадии LMNA-ассоциированной КМП характерно развитие атриальной миопатии с клиническими проявлениями брадиаритмии и/или предсердной тахиаритмии с нарушением функции левого предсердия (ЛП) при отсутствии дилатации и систолической дисфункции левого желудочка, которые развиваются на поздней стадии заболевания.
В представленной серии клинических наблюдений у родственников с семейным анамнезом внезапной сердечной смерти была диагностирована атриальная электромеханическая дисфункция при нормальных размерах ЛП, фракции выброса и геометрии левого желудочка. Три признака — межпредсердная блокада, брадиаритмия и снижение деформации ЛП — указывали на предсердную миопатию как первый тревожный сигнал ранней манифестации семейной КМП. Так, в случае пробанда, бессимптомного 36-летнего мужчины, обнаружение далеко зашедшей межпредсердной блокады на электрокардиограмме инициировало комплекс обследований, включающих спекл-трекинг эхокардиографию, холтер-мониторирование, магнитно-резонансную томографию и генетический скрининг. Выявленные специфические признаки — семейный брадиаритмический синдром, снижение пиковой деформации ЛП и продольной деформации межжелудочковой перегородки, линейный септальный фиброз — свидетельствовали в пользу генетической КМП. В результате таргетного секвенирования идентифицирован новый вероятно патогенный вариант в гене LMNA (c.276del; p.Asp93Thrfs*3), и установлен диагноз кардиоламинопатии, связанной с делецией в 1 экзоне, приводящей к варианту сдвига рамки считывания. Результаты каскадного скрининга и сегрегационного анализа подтвердили диагноз ламинопатии еще у 2 членов семьи (один из них асимптомный, другой — с симптомами нераспознанной «горячей фазы» КМП давностью 1 год) с признаками предсердной миопатии.
Введение
Ламины — это ядерные белки промежуточных филаментов V типа, которые составляют структуру внутренней ядерной мембраны и классифицируются на типы A и B. Ламиновые протеины типа A (ламины A и C) кодируются геном ламина A/C (LMNA), который расположен на хромосоме 1 (1q21.2-q21.3) [1]. Ламины A и C обладают множественными функциями и плейотропными эффектами, которые обеспечивают структурную целостность ядра с поддержанием его стабильности, регулируют форму, размеры и жесткость оболочки ядра; кроме того, эти протеины активно участвуют в организации хроматина и модуляции связей ядро-цитоскелет, что оказывает влияние на экспрессию других генов [1-3].
Патогенные варианты LMNA ассоциированы с различными фенотипами, большинство из них приводят к кардиомиопатии (КМП), нередко с вовлечением поперечнополосатых мышц, другие приводят к мультисистемным прогероидным и перекрывающимся синдромам с поражением жировой ткани и периферической нервной системы [3].
LMNA ассоциированные КМП (LMNA-КМП) характеризуются механическими и электрическими нарушениями в сердце, приводящими к развитию разных фенотипов — рестриктивной, дилатационной, некомпактной и аритмогенной леводоминантной КМП. С 2023г согласно рекомендациям рабочей группы Европейского общества кардиологов по диагностике и лечению КМП определены дефиниции для выделения нового фенотипа КМП — недилатационной КМП (НДКМП) левого желудочка (ЛЖ), который критериально и клинически соответствует фенотипу леводоминантной аритмогенной КМП и включает недилатационные формы структурного/фиброзного поражения ЛЖ с нарушением его контрактильности или без нарушения сократительной функции [4].
Варианты в гене LMNA являются причиной семейной дилатационной КМП (ДКМП) в 5-9%, занимая вторую по частоте генетическую позицию после укорачивающих вариантов в гене титина [5-7]. LMNA мутации обычно наследуются по аутосомно-доминантному типу с высоким риском (50%) передачи варианта потомству, также ламинопатии имеют высокую сердечную пенетрантность — до 86% среди носителей LMNA генотипов. Так, фенотип LMNA-ДКМП в двух третях случаев развивается в возрасте 20-40 лет с полной пенетрантностью к 60 годам [8][9].
Клинические проявления ламинопатий варьируют от классического кардиального фенотипа ДКМП и аритмогенной КМП (с нарушениями проводимости, предсердной и/или желудочковой аритмией, которые наблюдаются и при нормальной фракции выброса (ФВ) ЛЖ) до нейромышечной патологии (мышечная дистрофия Эмери-Дрейфуса) и «воспалительной» КМП, имитирующей сердечный саркоидоз или инфаркт-подобный миокардит [3][7-9]. Патогенные варианты LMNA ассоциируются с жизнеопасными желудочковыми тахиаритмиями (ЖТА), прогрессирующей сердечной недостаточностью (СН), которая у каждого пятого носителя трансформируется в терминальную стадию и требует трансплантации сердца [5]. Однако даже бессимптомные LMNA носители без морфофункциональных признаков КМП имеют повышенный риск внезапной сердечной смерти (ВСС) [6-9], и преждевременная смерть часто является первым клиническим проявлением ламинопатий.
Так, клинические проявления LMNA-КМП отличаются специфическими особенностями — поражением проводящей системы сердца (у каждого третьего LMNA носителя) и желудочковыми аритмиями [6-9]. Фибрилляция предсердий (ФП) также часто наблюдается при LMNA-КМП, примерно у 60% пациентов ФП развивается в молодом возрасте (12-20 лет) как первое клиническое проявление кардиоламинопатии с нейромышечными симптомами или без них [10]. У пациентов с LMNA-ДКМП распространенность ФП превышает 90%. В то время как ФП нередко встречается и при других наследственных КМП, ранняя ФП при LMNA-КМП может развиваться задолго до начала ремоделирования желудочков, что позволяет предположить, что отличительной особенностью ламинопатий является раннее атриальное ремоделирование (электрическое, структурное, механическое) с развитием предсердной миопатии и вовлечением желудочков на конечной стадии формирования фенотипа КМП [10].
В представленной серии клинических наблюдений диагностика семейной ламинопатии была проведена в результате каскадного скрининга семьи пробанда — бессимптомного 36-летнего мужчины, у которого обнаружение далеко зашедшей межпредсердной блокады (МПБ) на электрокардиограмме (ЭКГ) инициировало комплекс исследований, включающих эхокардиографию (ЭхоКГ) со спекл-трекингом, холтеровское мониторирование (ХМ), магнитно-резонансную томографию (МРТ) и генетическое тестирование. Интегральная оценка ранней предсердной патологии у пробанда позволила провести КМП-ориентированную диагностику семейной ламинопатии.
Клинический случай 1
Пациент ДII-1, мужчина в возрасте 36 лет, был направлен врачом общей практики на консультацию к кардиологу для оценки состояния сердца с учетом наличия у него семейного анамнеза ВСС и изменений на ЭКГ, выявленных в результате профилактического осмотра перед допуском к работе. Известно, что отец пациента умер внезапно в возрасте 45 лет, а ранее, в 40-летнем возрасте, ему был имплантирован электрокардиостимулятор (ЭКС). У пациента на момент осмотра не было жалоб, отсутствовала индивидуальная и семейная медицинская информация о наличии хронических заболеваний.
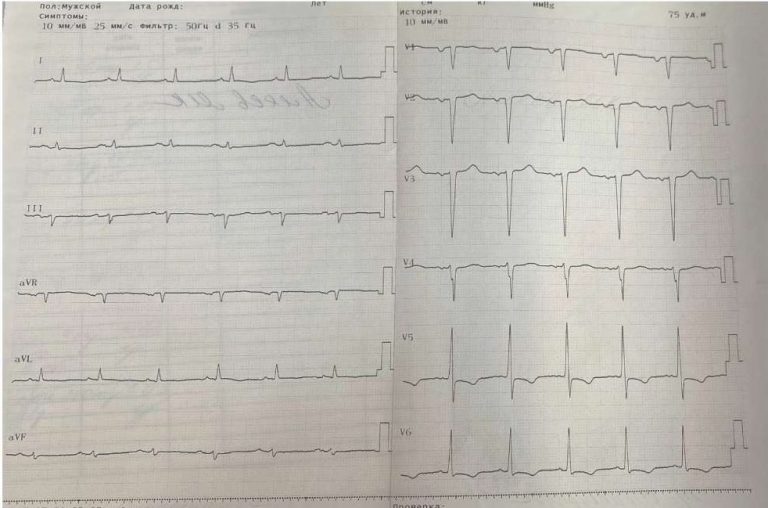
При физикальном обследовании видимых отклонений не выявлено. На ЭКГ регистрировался синусовый ритм с частотой сердечных сокращений (ЧСС) 50 уд./мин, отмечались удлинение интервала PR (280 мс) и значительное увеличение длительности зубца P до 184 мс (в норме <120 мс) с низковольтной (амплитуда Р в отведении I <0,1 мВ) и трехфазной бимодальной (+/-/+) морфологией в 6 отведениях с выраженным отрицательным компонентом в отведениях II, III, aVF и V1. Патологические изменения соответствовали атриовентрикулярной (АВ) блокаде 1 ст. и атипичной МПБ 3 ст., или атипичной далеко зашедшей МПБ по критериям Silvestrini TL и Bayes De Luna, et al. (2023) [11], обусловленной полной блокадой пучка Бахмана и потенциально связанной с увеличением и дисфункцией левого предсердия (ЛП). В отведениях V1 и V2-3 визуализировались эпсилон-подобные волны, ЭКГ пациента представлена на рисунке 1.

Рис. 1. Поверхностная ЭКГ пробанда ДII-1 в покое: А) стандартная ЭКГ-12 (масштаб 10 мм/мВ, скорость 50 мм/c) c ЧСС 50 уд./мин; Б) фрагмент ЭКГ в увеличенном масштабе (40 мм/мВ при скорости 100 мм/c) демонстрирует признаки атипичной далеко зашедшей МПБ, удлинение интервала PR и нарушение проводимости по наджелудочковому гребешку.
При стандартной трансторакальной ЭхоКГ существенных отклонений в геометрии, морфологии и функции желудочков не было выявлено: ФВ ЛЖ 59%, конечно-диастолический диаметр (КДД) ЛЖ 54 мм, индекс объема ЛЖ 77 мл/м², индекс объема ЛП 33 мл/м², ФВ правого желудочка (ПЖ) 55%, TAPSE 20 мм. Обнаружен пролапс митрального клапана 2 ст. (А2 =7 мм, А3 =8 мм) с митральной регургитацией 2 ст., при спекл-трекинг визуализации выявлено локальное снижение продольной деформации в септальной области (GLS =-12,6%) — в зоне базальных и средних сегментов межжелудочковой перегородки (МЖП) с незначительным снижением глобальной продольной деформации ЛЖ (GLS =-15,9%). Выявлено также снижение пиковой продольной деформации ЛП в фазах резервуара (PALS =22%), кондуита и контрактильности (PALC =-10,2%).
При ХМ зарегистрированы эпизоды синусовой брадикардии с ЧСС 40 уд./мин в дневное время (средняя ЧСС днем 56 уд./мин), МПБ 3 ст., АВ блокада 1 ст.; желудочковая экстрасистолия состояла из 736 одиночных желудочковых экстрасистол (ЖЭС), 5 парных ЖЭС и 1 триплета; суправентрикулярная экстрасистолия (СВЭС) состояла из 936 одиночных, 63 групповых и 176 парных предсердных сокращений; максимальная постэктопическая пауза не превышала 2 сек. Фрагменты ХМ с эктопической активностью представлены на рисунке 2.

Рис. 2. Фрагменты ЭКГ, демонстрирующие предсердную и желудочковую эктопию у пробанда при физической активности по данным ХМ.
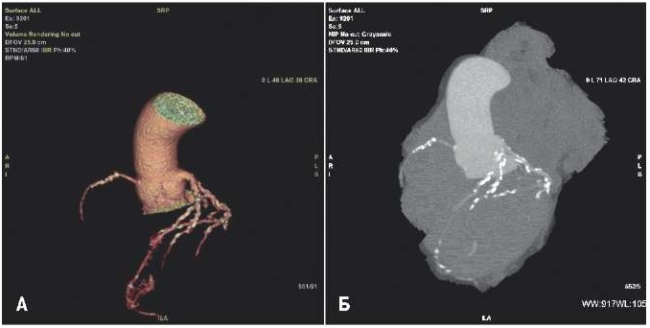
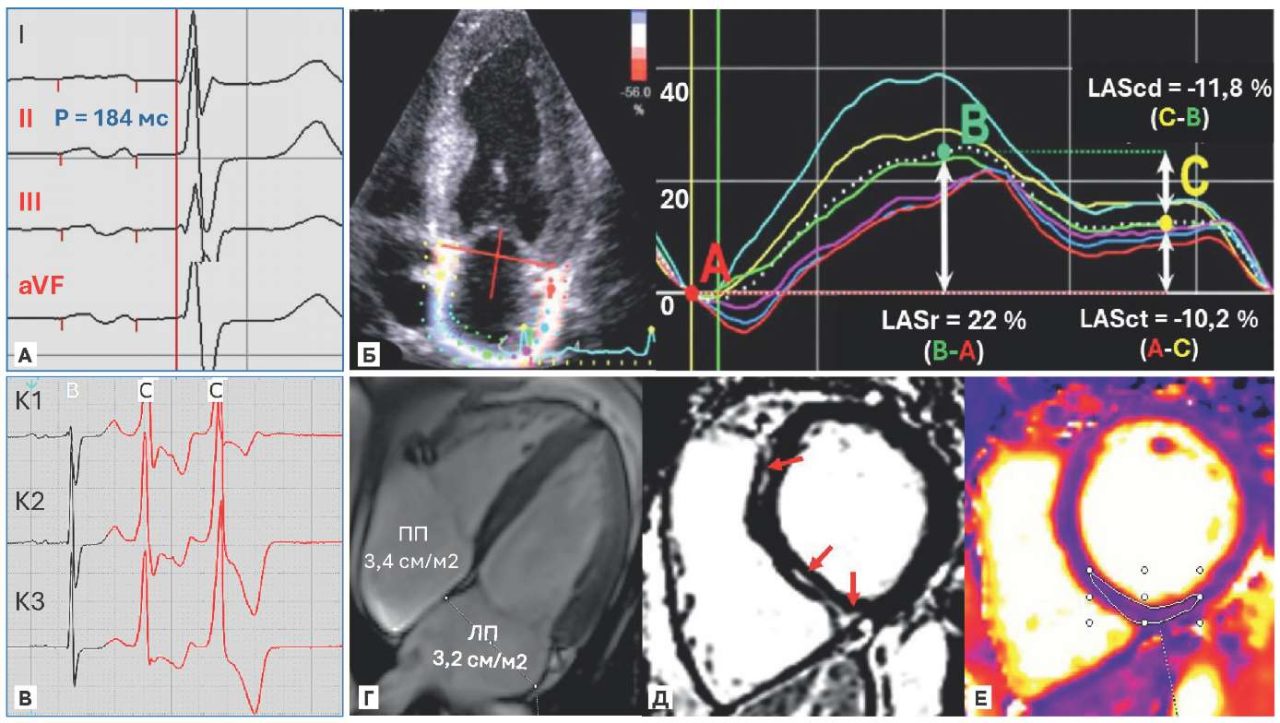
При МРТ сердца обнаружено интрамуральное накопление контрастного вещества в базальных и средних сегментах МЖП; очаговая задержка контраста выявлена в нижних точках прикрепления свободной стенки ПЖ без нарушения глобальной сократительной функции ЛЖ и без изменений тканевых характеристик при Т1 и Т2 картировании; также обнаружено снижение локальной сократимости в базальных отделах МЖП и незначительное расширение полости ЛП; объем и линейные размеры ЛЖ соответствовали верхним значениям МРТ-референтных показателей. Данные комплексной оценки кардиального статуса пробанда (с прецизионной визуализацией Р волны, параметрами продольной деформации ЛП и МРТ с контрастированием) представлены на рисунке 3.

Рис. 3. Графическое представление результатов комплексного мультимодального обследования пробанда: А) признаки атипичной МПБ 3 ст. с ретроградной активацией ЛП в каудально-краниальном направлении; Б) признаки дисфункции ЛП по данным спекл-трекинга со снижением продольной деформации в фазах резервуара — LASr, кондуита — LAScd и сокращения — LASct; В) фрагмент ХМ с желудочковым куплетом; Г) МРТ изображение в 4-камерной проекции; Д) позднее постконтрастное усиление МРТ с изображением в 2-камерной проекции и признаками отсроченного накопления контраста в области МЖП (зоны указаны стрелками); Е) преконтрастное Т1-картирование без признаков тканевых нарушений релаксации.
Сокращения: ЛП — левое предсердие, ПП — правое предсердие.
С учетом клинического подозрения на наследственную КМП согласно результатам анализа тревожных сигналов — «красных флагов», таких как: семейный анамнез ранней ВСС (и имплантации ЭКС), специфические изменения ЭКГ (АВ блокада 1 ст., МПБ 3 ст.), асимптомные нарушения ритма (предсердная и желудочковая экстрасистолия в патологическом количестве), данные МРТ (срединный линейный фиброз МЖП), пациенту предложили генетическое тестирование и, в соответствии с полученным письменным информированным согласием, было проведено молекулярно-генетическое исследование. В результате секвенирования NGS/Sanger был идентифицирован новый вариант в гене ламина A/C (LMNA: chr1-156115192 CT>C; c.276del; p.Asp93Thrfs*3; NM_170707.4) и подтвержден диагноз кардиоламинопатии, связанной с делецией в 1 экзоне, приводящей к варианту сдвига рамки считывания.
Новый вариант LMNA расценили как «вероятно патогенный» согласно биоинформационному инструменту прогнозирования Franklin (https://franklin.genoox.com) в соответствии с критериями классификации вариантов Американской коллегии медицинской генетики/геномики и Ассоциации молекулярной патологии (критерии PVS1, PM2) [12]. Критерий PVS1 соответствует вредоносным вариантам нуклеотидной последовательности (например, сдвиг рамки считывания, как в данном случае) и относится к очень сильным патогенным критериям. Такой LOF-вариант нарушает функцию гена (LOF, от англ. Loss-of-Function — потеря функции) и приводит к прекращению синтеза белка ламина А. Идентифицированный вариант встречается крайне редко, он не зарегистрирован в контрольных базах данных gnomAD (если вариант отсутствует в общей популяции или контрольной когорте >1000 человек, его обнаружение можно считать умеренным доказательством патогенности — критерий PM2).
При динамическом наблюдении пробанда ДII-1, получавшего терапию ангиотензиновых рецепторов и неприлизина ингибитором, бета-блокатором (низкие дозы сукцинат-метопролола) и антагонистом альдостерона, через 23 мес. отмечалось локальное и глобальное снижение сократительной функции ЛЖ (ФВ ЛЖ 47%) с увеличением желудочковой эктопии и неустойчивой желудочковой тахикардии (нЖТ) по данным ХМ. Принимая во внимание новые рекомендации Европейского общества кардиологов [4], учитывая прогноз КМП, связанный с нон-миссенс мутацией LMNA, наличием нЖТ и снижением ФВ, проведена реклассификация прогнозируемого 5-летнего риска жизнеугрожающих ЖТА. Расчетный риск опасных для жизни ЖТА (на основании он-лайн калькулятора риска https://lmna-risk-vta.fr) составил 57,6%. С учетом рекомендованного экспертами порогового значения ≥10% для первичной профилактики ВСС у пациентов с LMNA-КМП, многопрофильной командой врачей (кардиолог/хирург-аритмолог/генетик) было принято согласованное с пациентом решение об имплантации кардиовертер-дефибриллятора (КВД).
Красные флаги и диагностический процесс, ориентированный на поиск КМП, представлены на рисунке 4.

Рис. 4. Центральная иллюстрация. Пошаговая диагностика с выявлением «красных флагов» ламинопатии.
Сокращения: ВСС — внезапная сердечная смерть, ИКД — имплантируемый кардиовертер-дефибриллятор, ЛП — левое предсердие, МПБ — межпредсердная блокада, МРТ — магнитно-резонансная томография, ЭКГ — электрокардиография, ЭКС — электрокардиостимулятор, ЭхоКГ — эхокардиография.
Каскадный семейный скрининг
На основании семейного и генотип-фенотипического анализа, с учетом критериев патогенности LOF-варианта был проведен семейный каскадный скрининг (с клиническим и генетическим тестированием), который подтвердил наличие аналогичного LMNA генотипа у бессимптомной младшей сестры ДII-3 и симптомной старшей сестры ДII-2, которая годом ранее уже обследовалась у терапевта и невролога в связи с болями в грудной клетке и повышением уровней высокочувствительных тропонинов Т/I (hs-TnТ и hs-TnI). Положительные результаты сегрегационного анализа в семье (отец, трое детей) подтвердили предположение о патогенности нового варианта (критерий РР1). Генеалогическое древо семьи ДII-1 представлено на рисунке 5.

Рис. 5. Генеалогическое древо семьи пробанда ДII-1.
Примечание: квадратные символы обозначают членов семьи мужского пола, круглые — женского пола, стрелкой указан пробанд ДII-1, заштрихованные символы обозначают носителей патогенного LMNA+ генотипа c фенотипом LMNA-КМП.
Сокращения: АВБ — атриовентрикулярная блокада, ВСС — внезапная сердечная смерть, ЖЭС — желудочковая экстрасистолия, КМП — кардиомиопатия, КФК — креатинфосфокиназа, МПБ — межпредсердная блокада, нЖТ — неустойчивая желудочковая тахикардия, ПМК — пролапс митрального клапана, СВЭС — суправентрикулярная экстрасистолия, ЭКС — электрокардиостимулятор, hsTnI — высокочувствительный тропонин I.
Клинический случай 2
Старшая сестра пробанда (ДII-2) ранее в течение 12 мес. амбулаторно обследовалась (последовательно) у терапевта, невролога, кардиолога и аритмолога. Так, в возрасте 36 лет она впервые обратилась к терапевту с жалобами на боли в области сердца ноющего и колющего характера, не связанные с физической нагрузкой (ФН), слабость и быструю утомляемость. Указанные симптомы появились после нескольких эпизодов 7-мин острой боли в грудной клетке, по поводу которых пациентка обращалась к врачам.
В рамках семейного скрининга пациентка ДII-2 была обследована многопрофильной командой (кардиолог, аритмолог, невролог, генетик) через 12 мес. после дебюта указанных симптомов в возрасте 37 лет. Представленные данные медицинской документации включали результаты ранее проведенного обследования: ЭКГ-12, ЭхоКГ и МРТ сердца; у пациентки был выявлен пролапс митрального клапана 1 ст., синусовая брадикардия и признаки гипертрабекулярного миокарда верхушки и нижнебоковой стенки ЛЖ. Со слов пациентки, МРТ выполнялось из-за несоответствия устойчивого повышения сердечных биомаркеров — тропонинов hs-TnI/hs-TnT — жалобам и «нормальным» параметрам ЭКГ и ЭхоК Г. На представленных ЭКГ (динамика 8 мес.), кроме аномально низковольтной Р волны, частичной МПБ и брадикардии, значимых отклонений не наблюдалось.
При физикальном осмотре отмечалась синусовая брадикардия с ЧСС 45-47 уд./мин, артериальное давление 120/77 мм рт.ст., температура тела — 36,8 °C; пациентка отрицала предшествующие респираторные симптомы, желудочно-кишечные инфекции, COVID-19 или укус клеща. Признаков СН (периферические отеки, диспноэ) не было обнаружено. Однако при выполнении теста 6-минутной ходьбы (520 м) были отмечены некоторые «перонеальные» особенности походки (степпаж). Пациентка ДII-2 не знала о хронических заболеваниях в семье, отрицала анамнез семейной миопатии, не замечала затруднений при выполнении ФН (домашней и на уроках физкультуры в школьные годы), не предъявляла жалобы на слабость в ногах и других мышцах. При R-графии органов грудной клетки отклонений от нормы не обнаружено. На ЭКГ выявлена синусовая брадикардия с ЧСС 45 уд./мин, низковольтная бифазная Р волна (Р <0,1 мВ), МПБ 2 ст., АВ блокада 1 ст. (PR 377 мс), предсердная одиночная и парная экстрасистолия, незначительный прирост зубца R в отведениях V1-V3. Следует отметить, что МПБ 2 ст., или интермиттирующая МПБ, крайне редко регистрируется на короткой записи ЭКГ в покое; у пациентки наблюдалась трансформация исходной МПБ 1 ст. (с расширенным Р зубцом до 150 мс) в постэктопическую далеко зашедшую МПБ 3 ст. (с 2-фазной морфологией Р во всех нижних отведениях), ЭКГ пациентки ДII-2 в модифицированном масштабе (для более четкой визуализации Р волны и R зубцов) представлена на рисунке 6.

Рис. 6. ЭКГ пациентки ДII-2 (масштаб модифицирован для визуализации низковольтной Р волны).
Сокращения: ЧСС — частота сердечных сокращений, ЭКГ — электрокардиография.
При ХМ регистрировался преимущественно синусовый ритм со средней ЧСС 57 уд./мин (макс. 128, мин. 33), выявлены эпизоды синоатриальной блокады 2 ст. Мобитц 1, МПБ 1-3 ст., АВ блокада 1 ст., СВЭС состояла из 23140 одиночных, парных и групповых сокращений с постэктопическим угнетением функции синусового узла и выскальзывающими супрагисовыми сокращениями; зарегистрировано 15 пауз от 2,5 до 3,2 секунд и 242 одиночные ЖЭС.
По данным ЭхоКГ патологических морфофункциональных изменений камер сердца не выявлено: размеры, объемы, толщина стенок и кинетика миокарда были в пределах референтных значений; ФВ ЛЖ в В-режиме составила 59%; глобальная продольная деформация ЛЖ (GLS =-21,3%) соответствовала возрастной норме; обнаружено незначительное снижение продольной деформации базальных сегментов МЖП (GLS =-14,7%) — типичный признак КМП, связанной с LMNA мутациями, а также снижение пиковой деформации ЛП (PALS =23,5%; PACS =-11,4%); изменений перикарда и перикардиального выпота не обнаружено.
В результате лабораторной диагностики PATHFAST обнаружено 2-3-кратное повышение hs-TnI от 95 до 62 нг/л в динамике (норма 0-29 нг/л), увеличение N-концевого промозгового натрийуретического пептида (259 пг/мл при норме <125 пг/мл) и сывороточной креатинфосфокиназы до 235 ед./л (норма <126 ед./л). Воспалительные биомаркеры (С-реактивный белок 0,70 мг/л; лейкоциты 8,1×10³/мкл; прокальцитонин 0,03 мкг/л), полимеразная цепная реакция и серологические тесты к антигенам 9 кардиотропных вирусов (включая SARS-CoV-2) были отрицательными.
При МРТ сердца выявлены признаки умеренного отека в области базальных и средних сегментов МЖП с повышением значений преконтрастной Т1-релаксометрии до 1105 мс за счет расширения межклеточных пространств (интерстициального фиброза); линейный срединный паттерн интрамурального накопления контраста обнаружен в базальных сегментах перегородки и в нижней точке прикрепления свободной стенки ПЖ. Признаков гипокинеза и дилатации камер сердца не выявлено, обнаружена гипертрабекулярность миокарда в области верхушки и нижнебоковой области ЛЖ. Конечно-диастолический объем ЛЖ составил 138 мл (индекс 77 мл/м²), а конечно-систолический объем — 53 мл (индекс 29,9 мл/м²), ФВ ЛЖ — 62%, тогда как конечно-диастолический объем ПЖ составил 118 мл (66,7 мл/м²), а конечно-систолический объем ПЖ — 49 мл (индекс 27,7 мл/м²), ФВ ПЖ — 58%. Для исключения миокардита и саркоидоза выполнена позитронно-эмиссионная томография с 18F-фтордезоксиглюкозой, в результате которой у пациентки не было обнаружено аномальной метаболической активности, признаков саркоидной инфильтрации и миокардита. Данные комплексной оценки кардиального статуса пациентки ДII-2 (с прецизионной визуализацией Р волны, фрагментами ХМ и МРТ изображениями) представлены на рисунке 7.

Рис. 7. ЭКГ и МРТ визуализация сердца пациентки ДII-2: А) фрагмент ХМ с постэктопической паузой 3,2 сек; Б) фрагмент ХМ с предсердной эктопией (групповая и одиночная); В) признаки МПБ 3 ст. с ретроградной активацией ЛП; Г) повышение значений преконтрастной Т1-релаксометрии до 1105 мс при МРТ картировании (синей стрелкой указана зона отека/интерстициального фиброза); Д) МРТ изображение в 2-камерной поперечной проекции с отсроченным накоплением контраста в септальной области (красная стрелка).
После назначения антинейрогуморальной (рамиприл 2,5 мг/сут., верошпирон 25 мг/сут.) и противовоспалительной (колхицин 0,5 мг/сут.) терапии, повторное обследование проведено через 3 мес. К этому сроку уже были известны положительные результаты семейного генотипирования. При ХМ отмечалась положительная динамика бинодальной функции сердца и эктопической активности: пауз >2,5 сек не выявлено, средняя ЧСС днем составляла 65 уд./мин, экстрасистолия представлена в виде 546 СВЭС и 63 одиночных ЖЭС.
С целью оценки хронотропной функции синусового узла пациентке проведен ступенчатый тест с ФН на велоэргометре (протокол 25 Вт × 3 мин с непрерывным мониторингом ЭКГ без оценки потребления O2): на высоте выполняемой работы 75 Вт максимальная ЧСС составила 116 уд./мин с аллоритмической ЖЭС (в т.ч. с бигеминией), за которой последовала симптомная 10-мин АВ блокада 2 ст. Мобитца 2 со снижением ЧСС до 30 уд./мин. При повторном ХМ на высоте ФН (быстрая ходьба) у пациентки зарегистрирован эпизод далеко зашедшей АВ блокады 2 ст., сопровождающийся жалобами (по дневнику пациентки) на головокружение и предобморочное состояние, а также два желудочковых триплета после пробуждения.
Принимая во внимание неблагоприятный прогноз НДКМП ЛЖ, связанный с механизмом нон-миссенс мутации LMNA, наличием значимых нарушений АВ проводимости и нЖТ, проведена оценка риска ВСС с применением он-лайн калькулятора риска (https://lmna-risk-vta.fr) — расчетный прогнозируемый 5-летний риск жизнеугрожающих ЖТА составил 34,9%.
Согласно текущим рекомендациям, у пациентов с ДКМП и НДКМП ЛЖ с 5-летним расчетным показателем прогнозируемого риска ≥10%, связанным с нЖТ, ФВ ЛЖ <50% или АВ блокадой, присутствуют показания класса IIa для имплантации КВД с целью первичной профилактики. Более того, при стандартных показаниях к имплантации ЭКС пациентам с ламинопатиями рекомендована имплантация КВД [4][13]. После совместного (пациент-врач) принятия решения на основе анализа полученных клинических данных и информированного согласия пациентке был имплантирован двухкамерный КВД.
Клинический случай 3
Младшая сестра пробанда (ДII-3) в рамках каскадного скрининга впервые была обследована в возрасте 21 года. Результаты комплексного исследования (нейромышечного, лабораторного, ЭКГ, ЭхоКГ и МРТ) не показали отклонений от физиологической нормы. При контрольном клиническом скрининге в возрасте 25 лет у LMNA-носительницы впервые были выявлены ранние признаки атриальной КМП — частичная МПБ (или МПБ 1 ст.) и сократительная дисфункция ЛП (снижение деформации в фазу сократимости LASct =-14,5%) без дилатации ЛП (индексированный объем ЛП 28 мл/м²) при нормальной геометрии и сократительной функции ЛЖ и ПЖ (КДД ЛЖ 45 мм, ФВ ЛЖ 67%, TAPSE 22 мм). При ХМ у пациентки регистрировался синусовый ритм со средней ЧСС 67 уд./мин (макс. 160, мин. 43), СВЭС состояла из 562 одиночных и парных СВЭС, выявлены эпизоды синоатриальной блокады 2 степени Мобитц 1 и транзиторной АВ блокады 1 степени.
Пятилетняя эволюция фенотипов семейной КМП, представленная в таблице 1, раскрывает уникальную патофизиологию предсердной миопатии и суправентрикулярной тахиаритмии (СВЭС, предсердные тахикардии и неустойчивые пароксизмы ФП) при LMNA-КМП, которые развивались на фоне сохранной функции желудочков без дилатации ЛП и ЛЖ.
Таблица 1
Эволюция семейной ламинопатии — от дебюта предсердной миопатии и фенотипа НДКМП ЛЖ к полной пенетрантности ДКМП через 5 лет
|
Члены семьи, год рождения |
Фенотипы семейной кардиоламинопатии — 5-летняя эволюция |
||||
|
2020 |
2021 |
2022 |
2023 |
2025 |
|
|
Пробанд ДII-1, 1985 |
Атриальная миопатия |
Атриальная миопатия → НДКМП ЛЖ |
НДКМП ЛЖ (ФВ 47%; иКДО ЛЖ 77 мл/м²) |
НДКМП ЛЖ (ФВ 50%; иКДО ЛЖ 79 мл/м²), неуст. ФП |
ДКМП (ФВ 43%; индекс КДО ЛЖ 84 мл/м²), неуст. ФП |
|
Калькулятор риска ЖТА/ВСС (lmna/risk) |
– |
22,8% |
57,6% → Имплантация КВД |
Аппаратная терапия ЖТ |
Шоковая терапия полиморфной ЖТ (1) |
|
Сестра ДII-2, 1984 |
Атриальная миопатия + «горячая фаза» КМП |
Атриальная миопатия → НДКМП ЛЖ (ФВ 62%) |
НДКМП ЛЖ (ФВ 56%; иКДО 55 мл/м²), неуст. пароксизмы ФП |
НДКМП ЛЖ (ФВ 59%; индекс КДО 58 мл/м²), неуст. ФП, уст. ФП пароксизмы |
ДКМП (ЛЖ: ФВ 46%; индекс КДО 61 мл/м²), уст. ФП пароксизмы |
|
Калькулятор риска ЖТА/ВСС (lmna/risk) |
– |
14,3% |
34,9% → Имплантация КВД |
As-Vp 4,6% Аппаратная терапия ЖТ |
As-Vp 11,2% Аппаратная терапия ЖТ |
|
Сестра ДII-3, 2000 |
Нет симптомов |
Асимптомный носитель LMNA мутации (ФВ 68%; индекс объема ЛП 22 мл/м², индекс КДД ЛЖ 27 мм/м², индекс КДО ЛЖ 57 мл/м²) |
Предсердная КМП (МПБ 1 ст., СВЭС, LASct =-14,5%) |
||
|
Калькулятор риска ЖТА/ВСС (lmna/risk) |
– |
5,4% |
11,9% |
||
Сокращения: ВСС — внезапная сердечная смерть, ДКМП — дилатационная кардиомиопатия, ЖТ — желудочковая тахикардия, ЖТА — желудочковые тахиаритмии, иКДО — индексированный конечно-диастолический объем, КВД — кардиовертер-дефибриллятор, КДД — конечно-диастолический диаметр, КДО — конечно-диастолический объем, КМП — кардиомиопатия, ЛЖ — левый желудочек, ЛП — левое предсердие, МПБ — межпредсердная блокада, НДКМП ЛЖ — недилатационная кардиомиопатия левого желудочка, СВЭС — суправентрикулярная экстрасистолия, ФВ — фракция выброса, уст. ФП — пароксизмы устойчивой фибрилляции предсердий (>30 сек), неуст. ФП — пароксизмы неустойчивой фибрилляции предсердий (≤30 сек), As-Vp — вариант Р-управляемой стимуляции желудочков при сенсированном спонтанном ритме предсердий, LASct — деформация левого предсердия в фазу сокращения.
Так, у пробанда первые пароксизмы неустойчивой ФП были зарегистрированы через 9 мес. после имплантации КВД при контрольном интеррогировании устройства. При этом отрицательной динамики размеров и функции ЛП и ЛЖ не было обнаружено. У старшей сестры ДII-2 пароксизмы устойчивой и неустойчивой ФП были зафиксированы имплантированным устройством через 6 мес. наблюдения (также при отсутствии отрицательной ЭхоКГ динамики). В то время как эпизоды обоснованной аппаратной терапии желудочковой тахикардии зарегистрированы у обоих родственников через 19 мес. после имплантации КВД.
Обсуждение
Представленный семейный случай подчеркивает важную роль тщательного ЭКГ анализа как отправной точки для мультимодального подхода, ведущего к диагностике генетической КМП. Полная блокада Бахмана (МПБ 3 ст.) на ЭКГ встречается крайне редко у молодых пациентов и может быть первым проявлением (красным флагом) предсердной КМП. Так, в греческой когорте пациентов в возрасте до 35 лет распространенность МПБ 1 ст. с длительностью зубца P ≥120 мс составила 1,6%, а в испанской когорте 100-летних долгожителей распространенность частичной МПБ составила 21%, далеко зашедшей МПБ — 26% [14][15]. В датской когорте (при первичном обращении 152759 пациентов в возрасте 50-90 лет за медицинской помощью в г. Копенгаген) распространенность частичной МПБ составила 16%, а далеко зашедшей МПБ — 0,5% [16]. Различные исследования показали схожие результаты относительно распространенности МПБ 3 ст. в общей популяции — в диапазоне от 0,5% до 1%, при этом частота МПБ увеличивалась с возрастом и зависела от факторов риска и степени блокады [17][18]. Частичная и полная блокада Бахмана продемонстрировали высокую распространенность среди пациентов с КМП [19]; тем не менее в литературе описаны единичные случаи частичной МПБ у пациентов с дебютом ламинопатии [20], а публикации с наблюдением МПБ 3 ст. не представлены.
Брадиаритмии и наджелудочковые тахиаритмии являются распространенными признаками ламинопатий и часто на десятилетия опережают развитие ДКМП и СН. Наджелудочковые аритмии включают трепетание предсердий, ФП и предсердную тахикардию и могут быть связаны с дисфункцией синусового узла (синдромом тахикардии-брадикардии). Синусовая брадикардия в молодом возрасте (с начала второго десятилетия до четвертого десятилетия) с последующим развитием ФП или АВ блокады высокой степени являются типичными для LMNA-КМП [10].
Для кардиоламинопатий характерно развитие ранней предсердной миопатии, клинически проявляющейся предсердной эктопией (и/или ФП) со снижением индексов продольной деформации ЛП при отсутствии дисфункции и дилатации ЛЖ, даже без дилатации ЛП [10]. Снижение продольной деформации в базальных сегментах МЖП является частой и ранней находкой при кардиоламинопатиях при наличии септального фиброза, который определяет повышенный риск аритмий и дефектов проводимости. LMNA ассоциированные КМП характеризуются ранним началом, частым возникновением нарушений сердечной проводимости, аритмий и крайне неблагоприятным прогнозом [21]. Основные клинические проявления при манифестации LMNA-КМП представлены на рисунке 8.

Рис. 8. Схематическое представление основных клинических проявлений при манифестации LMNA-КМП.
Сокращения: АВ — атриовентрикулярный, ВСС — внезапная сердечная смерть, ЛЖ — левый желудочек, МПБ — межпредсердная блокада, СА — синоатриальный, СН — сердечная недостаточность, ТП — трепетание предсердий, ФП — фибрилляция предсердий.
В представленной клинической ситуации генетический тест и МРТ визуализация продемонстрировали решающую роль в ранней диагностике, стратификации риска ВСС и выборе тактики лечения. Комплекс признаков, характерных для ранних стадий КМП, таких как предсердная электромеханическая дисфункция, наличие неишемического паттерна фиброза в области МЖП без дилатации ЛЖ при сохранной ФВ ЛЖ, позволили диагностировать НДКМП ЛЖ у пробанда и провести семейный каскадный скрининг.
В представленном наблюдении подтверждена значительная индивидуальная фенотипическая вариабельность ламинопатий, которая характерна не только для неродственных носителей LMNA мутаций, но для членов одной семьи. И хотя МПБ, как ранний маркер субклинической предсердной миопатии, наблюдалась у всех носителей нового варианта LMNA со сдвигом рамки считывания, степень вовлечения/поражения ЛЖ, симптомы дебюта и динамика заболевания были различными. Так, двое членов семьи были асимптомны, но у пробанда ДII-1 атипичная далеко зашедшая МПБ сопровождалась нарушением резервуарной и сократительной деформации ЛП с незначительной (по данным МРТ) дилатацией ЛП, легким снижением локальной сократимости и линейным срединным фиброзом в области МЖП, в то время как у младшей сестры ДII-3 частичная МПБ ассоциировалась с умеренной контрактильной дисфункцией ЛП, предсердной экстрасистолией без изменений локальной сократимости ЛЖ, геометрии и тканевых характеристик ЛЖ и ЛП (по данным МРТ).
У симптомной старшей сестры ДII-2 интермиттирующая МПБ 2 ст. сопровождалась нарушением деформации ЛП в фазу резервуара и сокращения, рестриктивной гемодинамикой и признаками НДКМП ЛЖ. И хотя манифестация НДКМП ЛЖ у ДII-2 была наиболее типичной для ламинопатии — с повышением креатинфосфокиназы и hs-TnI, признаками субклинической миопатии нижних конечностей, специфическими изменениями ЭКГ (низковольтный Р зубец, малый прирост амплитуды зубца R в V1-3, АВ блокада 1-2 ст., клинически значимая СВЭС) и МРТ (срединный линейный фиброз МЖП), однако миокардиальный отек, обнаруженный в перифокальной зоне линейного фиброза МЖП и миокардит-подобные симптомы в дебюте болезни, свидетельствовали в пользу сценария «горячей фазы» генетически обусловленной КМП (с запуском каскада генно-программируемых механизмов апоптоза кардиомиоцитов с индукцией последующего воспаления и фиброза миокарда), тогда как «горячие фазы» с воспалительным компонентом являются более характерными для активных фаз десмоплакиновых КМП. Новый термин «горячие фазы» КМП принят недавно для характеристики эпизодов повреждения миокарда с воспалительным компонентом, которые являются сложными клиническими проявлениями генетической КМП со специфическими симптомами — острой болью в груди, повышением сердечных тропонинов (при отсутствии коронарной обструкции) и желудочковыми аритмиями. Эти эпизоды клинически проявляются как миокардит-псевдокоронарные симптомы, чаще встречаются у молодых пациентов, сопряжены с повышенным риском злокачественных аритмий и прогрессированием заболевания [22].
В представленном наблюдении подчеркивается клиническая важность специфических ЭКГ показателей и спекл-трекинг ЭхоКГ параметров (МПБ и снижение индексов деформации ЛП, указывающих на предсердную миопатию) в качестве клинического диагностического инструмента у пациентов, не имеющих в остальном никаких симптомов и отклонений стандартной ЭхоКГ, для направленного поиска КМП с ориентацией на генетическую диагностику. В семье молодых LMNA носителей индексы деформации предсердий и локальная продольная деформация желудочков были изменены при наличии (в остальном) нормальных морфофункциональных показателей ЭхоК Г. Следует отметить, что о сократительной дисфункции предсердий и снижении пиковой сократительной деформации ЛП ранее сообщалось при исследовании когорты пациентов с вариантами LMNA, у которых развивались пароксизмы ФП; авторы отмечали о непропорционально высокой распространенности наджелудочковых аритмий у пациентов с вариантами LMNA на ранних стадиях болезни, задолго до появления дисфункции и дилатации ЛЖ [10]. Более того, наличие МПБ было связано с повышенным риском злокачественных аритмий и ВСС у пациентов с ДКМП [19].
Клиническая картина на ранних стадиях LMNA-КМП обычно ограничена малыми признаками, и единственными установленными отклонениями могут быть только нарушения ритма в виде брадиаритмии или суправентрикулярной эктопии и дефекты проводимости различной степени (реже повышение креатинфосфокиназы и hs-TnI/T), в то время как полный фенотип КМП развивается на более поздних стадиях заболевания [5-7]. У носителей LMNA генотипа нередко при МРТ исследовании можно наблюдать типичную интрамиокардиальную задержку гадолиния в области МЖП. В литературе представлены единичные случаи обнаружения «горячих фаз» при ламинопатиях, однако о выявлении более высоких значений тропонинов у пациентов с ламинопатиями ранее уже сообщалось в исследовании Chmielewski P, et al. (2024) [23]. При LMNA-КМП повышенные уровни TnT/I могут отражать продолжающиеся процессы повреждения кардиомиоцитов, а следствием длительного повреждения кардиомиоцитов является неспецифический заместительный фиброз, который является причиной развития электрической нестабильности, приводящей к аритмиям [24], а со временем и к механическим нарушениям. Авторы Topriceanu С, et al. (2025) впервые предоставили убедительные доказательства того, что повреждение миокарда и отек являются основными признаками LMNA-КМП (но не миокардита), опубликовав результаты проспективного многоцентрового исследования с детальной оценкой МРТ картирования миокарда (Т1 и Т2) и анализом циркулирующих сывороточных биомаркеров [24]. Ученые обнаружили увеличение длительности миокардиальной Т1- и T2- релаксации у носителей LMNA мутаций как с сохранной ФВ, так и со сниженной ФВ, а также более высокие уровни тропонинов и С-реактивного белка по сравнению с другими генотипами (TTN и RBM20) ДКМП. Используя многопараметрическое МРТ картирование и 4D-анализ морфологии сердца, авторы определили характерные признаки ламинопатий — пролонгированную релаксацию при Т1 и Т2 картировании, более высокую фракцию внеклеточного объема, большую степень накопления контраста и худшую миокардиальную динамику у LMNA-носителей вне зависимости от ФВ ЛЖ [24], что предполагает наличие очагового и интерстициального фиброза. Эти данные поддерживают концепцию аритмического риска ламинопатий — профибротические пути, связанные с дефектным ламином, способны активироваться на ранней стадии заболевания, а фиброзное ремоделирование может служить аритмогенным субстратом и одной из причин непропорционально высоких показателей ЖТА, АВ блокад и ВСС при LMNA-КМП.
В представленном наблюдении дисфункция предсердий при ранней LMNA-КМП (с клинически значимой суправентрикулярной эктопией при сохранной ФВ ЛЖ) демонстрирует геноспецифическую миопатию предсердий со снижением сократительной деформации ЛП, которая предшествует увеличению ЛП, дилатации и дисфункции ЛЖ. Почему на молекулярно-клеточном и тканевом уровне ЛП поражается раньше, чем ЛЖ, остается открытым вопросом, который можно объяснить различной толщиной стенок. Например, тонкостенное предсердие может быть более чувствительным к нарушению механотрансдукции, контролируемой каскадом взаимодействий «ядерная оболочка-цитоскелет-клеточная мембрана». В исследовании Owais А, et al. (2025) авторы открыли новый механизм (на моделях индуцированных плюрипотентных стволовых клеток, полученных из предсердных кардиомиоцитов), с помощью которого редкий патогенный миссенс вариант LMNA нарушает доступность хроматина и регуляцию других генов в локусах, связанных с атриальной миопатией и ФП. В частности, доказано снижение доступности энхансера SCN5A, приводящее к электрофизиологическим дефектам — снижению тока натрия, нарушениям проводимости и ФП [25].
Так, для все большего числа сердечных заболеваний генетическое тестирование предоставляет важную диагностическую и прогностическую информацию. Для ламинопатий молекулярная диагностика является критически важной, т.к. LMNA-КМП независимо от ФВ ЛЖ имеют крайне неблагоприятный аритмический прогноз, что смещает рекомендации в сторону более низкого порога (с повышением класса показаний) для имплантации КВД с целью первичной профилактики ВСС.
Заключение
Обнаружение семейных предсердных аритмий без значимого желудочкового поражения у нескольких членов семьи отражает потенциальное присутствие генетического компонента болезни, особенно если аритмии возникают у молодых людей при отсутствии других факторов риска. Далеко зашедшая МПБ встречается крайне редко у молодых пациентов и может быть первым проявлением предсердной миопатии. Таких пациентов целесообразно обследовать с помощью метода спекл-трекинг ЭхоКГ и, в случае выявления аномальных индексов продольной деформации ЛП и/или ЛЖ, ориентировать на мультимодальное дообследование (и/или на генетический скрининг) с целевым поиском ранней КМП.
Врачам общей практики и кардиологам важно осознавать необходимость проведения регулярных кардио-скрининговых исследований при наличии в семейном анамнезе КМП или ранней ВСС и учитывать любые ЭКГ и/или ЭхоКГ аномалии, включающие признаки, указывающие на предсердную миопатию или миокардит, которые требуют дополнительного обследования.
У бессимптомных носителей LMNA мутаций оценка продольной деформации ЛП и ЛЖ является клинически полезной опцией при динамическом наблюдении, эти измерения практически не увеличивают временных затрат к рекомендуемой ЭхоКГ визуализации, но при этом значительно расширяют неинвазивный диагностический потенциал.
Информированное согласие. У всех участников исследования было получено письменное информированное согласие.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Вайханская Т.Г., Геворкян Т.Т., Левданский О.Д. Семейная ламинопатия: один ген, два белка, три различных сценария предсердной манифестации фенотипа кардиомиопатии, ассоциированной с новой мутацией в гене ламина A/C (LMNA) — серия случаев. Российский кардиологический журнал. 2026;31(1S):6465. https://doi.org/10.15829/1560-4071-2026-6465. EDN: VWMNBH
Скопировать