Метаболическая аэстивация как новое патогенетическое звено саркопении при хронической сердечной недостаточности: систематический обзор и метаанализ
Аннотация
Цель. Систематически оценить влияние водного дефицита, диуретической терапии и осмотического стресса на изменение осмолитного профиля плазмы (осмолярность, концентрации натрия и мочевины) и их связь с клиническими исходами, включая мышечный катаболизм.
Материал и методы. Систематический обзор выполнен в соответствии с PRISMA-2020. Поиск проводился в октябре 2025г в базах SciSpace, PubMed, EMBASE, Google Scholar, Cochrane Library, Web of Science, а также в регистрах ClinicalTrials.gov, WHO ICTRP, EU-CTR (всего 1680 записей + 124 регистра + 45 дополнительных источников). После удаления дубликатов (n=118) и двухэтапного скрининга включено 18 исследований (2017-2025гг): 7 клинических, 6 экспериментальных, 3 обзорных и 2 смешанных. В анализ включались взрослые ≥18 лет с маркерами дегидратации или осмостресса. Основные показатели: плазменная осмолярность, доля Na+ и мочевины в eOSM, уровни копептина/вазопрессина, аминокислотный профиль, показатели мышечного катаболизма, гемодинамики, функции почек. Оценка риска предвзятости проводилась с использованием ROB 2.0 и ROBINS-I.
Результаты. В систематический обзор включено 18 исследований, из которых 6 клинических исследований вошли в количественный метаанализ. Метаанализ показал, что водный дефицит, диуретическая терапия и применение SGLT2-ингибиторов ассоциированы с увеличением осмолярности плазмы (SMD 0,63 [0,19; 1,07], модель случайных эффектов; I2=93,8%). Отмечено повышение концентрации мочевины (SMD 0,44 [0,12; 0,75]) и снижение концентрации натрия (SMD -0,17 [-0,27; -0,06], p=0,0029). Анализ относительного вклада мочевины в осмолярность плазмы, доступный в 2 исследованиях, показал статистически значимое увеличение её доли (SMD 1,00 [0,64; 1,36]).
Заключение. Метаболическая аэстивация является универсальной адаптивной программой водосбережения у человека, активируемой при дегидратации, высокой солевой нагрузке, терапии диуретиками. Перераспределение осмолитов в пользу мочевины сопровождается мышечным катаболизмом, ростом артериального давления, ремоделированием миокарда и может способствовать прогрессированию хронической сердечной недостаточности и возникновению саркопении. Результаты систематического обзора указывают на необходимость мониторинга осмолярности, вклада Na+ и мочевины, а также осторожности при ограничении жидкости у пациентов, получающих диуретики. Контроль признаков метаболической аэстивации может улучшить безопасность терапии и прогноз при сердечно-сосудистых и кардиоренальных заболеваниях.
Эволюционный переход от жизни в водной среде к существованию на суше потребовал формирования сложных механизмов сохранения воды и натрия — элементов, чья роль в гомеостазе неразрывно связана. В океане вода и натрий присутствуют в избытке, тогда как на суше их дефицит стал мощным эволюционным стимулом для развития адаптаций, направленных на их удержание. У наземных животных основным органом регуляции водно-солевого равновесия стали почки, чья энергетическая активность преимущественно расходуется на канальцевую реабсорбцию натрия. При этом виды, обитающие в засушливых регионах, выработали дополнительные стратегии экономии воды — от удлинения нефронов и повышения концентрационной способности почек до перехода к выделению азота в виде мочевой кислоты и развития кожных барьеров, минимизирующих трансэпидермальную потерю жидкости [1].
Традиционно поддержание осмотического гомеостаза у человека рассматривается преимущественно через призму почечной экскреции натрия и воды. Однако в последние годы накоплены данные, указывающие на более сложную, многоуровневую регуляцию осмолярности, включающую перераспределение осмолитов между неорганическими (прежде всего натрий и калий) и органическими компонентами, такими как мочевина и глюкоза [1-3].
Ряд экспериментальных и клинических исследований продемонстрировал, что при состояниях, сопровождающихся относительным дефицитом воды или ограничением её доступности, может наблюдаться сдвиг в структуре осмолярности плазмы с увеличением вклада органических осмолитов [4-6]. Этот метаболический ответ ассоциирован с активацией катаболических путей, в т.ч. распадом белков скелетной мускулатуры, усилением синтеза мочевины и изменениями энергетического обмена. В отдельных публикациях данный феномен описывается с использованием термина «аэстивация», заимствованного из физиологии, где он обозначает адаптацию к дефициту воды [6-9].
Аэстивация (лат. aestivatio, от aestivare — «проводить лето», aestas — «лето») — древняя адаптивная программа выживания, обеспечивающая сохранение воды у организмов в условиях засухи. В природе она реализуется через переход к синтезу органических осмолитов (прежде всего мочевины), снижение метаболизма и ограничение кожных и почечных потерь жидкости.
Аналогичные механизмы были выявлены и у млекопитающих, включая человека, где они реализуются в форме метаболической перестройки (метаболическая аэстивация), направленной на эндогенное сохранение воды при хронической или ятрогенной гипогидратации [4]. Этот феномен характеризуется сдвигом от неорганических к органическим осмолитам, прежде всего мочевине и аминокислотам, а также активацией катаболизма скелетной мускулатуры как основного источника азотистых субстратов для синтеза мочевины [10]. Переход от неорганических к органическим осмолитам (мочевина) описан при различных патологических состояниях у животных и человека — от кожных заболеваний до сердечной [11] и почечной недостаточности [12].
Наблюдения у пациентов с хроническими заболеваниями подтверждают универсальность этого механизма. В работе Hultström M, et al. (2022) [5] и последующих исследованиях Barrueta Tenhunen A, et al. 2024 [13] показано, что повышение осмоляльности плазмы сопровождается сдвигом в сторону органических осмолитов, ростом мочевины, что отражает дегидратационно-индуцированный мышечный катаболизм и способствует развитию саркопении у пациентов после перенесенных критических состояний. Несмотря на растущий интерес к данной концепции, опубликованные данные характеризуются значительной гетерогенностью: исследования различаются по дизайну, клиническим моделям (интенсивная терапия, сердечная недостаточность (СН), инфекционные заболевания и т.д.), используемым показателям дегидратации и методам оценки осмолярного сдвига. Кроме того, отсутствует систематизированный анализ, позволяющий оценить, в какой степени описываемые изменения осмолитного профиля воспроизводимы, клинически значимы и сопоставимы между различными популяциями пациентов.
Цель: систематически оценить влияние водного дефицита, диуретической терапии и осмотического стресса на изменение осмолитного профиля плазмы (осмолярность, концентрации натрия, калия, мочевины и глюкозы) и их связь с клиническими исходами, включая мышечный катаболизм.

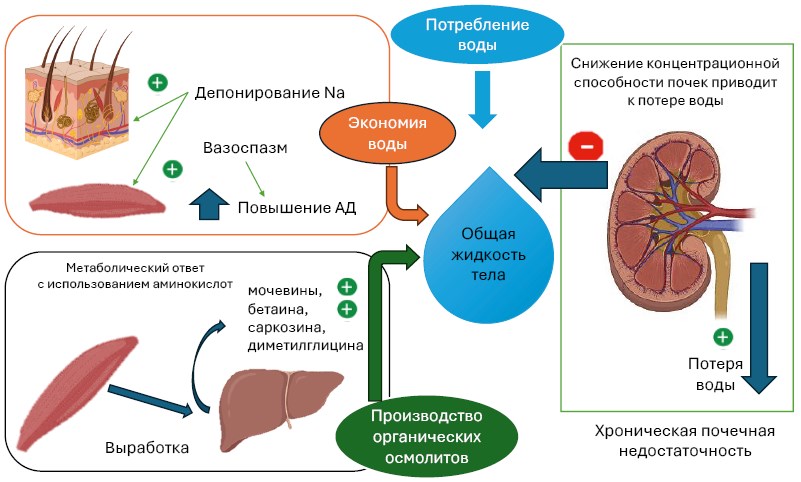
ЦЕНТРАЛЬНАЯ ИЛЛЮСТРАЦИЯ
Сокращение: АД — артериальное давление.
Методология исследования
Данный систематический обзор литературы был представлен в соответствии с рекомендациями по предпочтительным элементам отчетности для систематических обзоров и метаанализов [14].
Критерии включения и исключения исследований
В обзор включались статьи, сообщающие о результатах исследований, целью которых было изучение эффекта или ассоциации водного дефицита, осмотического стресса или изменений в осмолярности плазмы с ≥1 клиническим показателем здоровья — показатели катаболизма и их связь с осмолитными индексами.
Исследования были отобраны, если они соответствовали критериям популяции, вмешательства, сравнения, исхода, времени и дизайна исследования (PICOTS) (табл. 1).
Таблица 1
Критерии включения (PICOTS, Population, Intervention, Comparator, Outcomes, Timing, Study design)
|
Элемент |
Описание |
|
Population (P) |
Взрослые (≥18 лет) участники с признаками водного дефицита, гиперосмолярности или осмотического стресса, натриевой нагрузкой. Включались пациенты с хронической сердечной недостаточностью, хронической болезнью почек, острыми инфекциями (включая COVID-19), критическими состояниями, а также лица с повышенными потерями воды через кожу (псориаз, и др.) |
|
Intervention (I) |
Воздействия или состояния, индуцирующие осмостресс: дегидратация, ограничение жидкости, диуретическая терапия (петлевые, тиазидные диуретики), приём SGLT2-ингибиторов, высокосолевая диета, гипернатриемия, снижение свободного клиренса воды |
|
Comparator (C) |
Группы с нормальной гидратацией и нормальными осмолитными индексами или отсутствием признаков осмостресса |
|
Outcomes (O) |
Первичные исходы: аминокислотный профиль, изменения соотношения мочевины к осмолярности или Na к осмолярности плазмы. |
|
Time (T) |
Исследования, оценивающие острые (часы-дни) и эффекты водного дефицита, осмостресса, перегрузка солью. Включались как краткосрочные госпитальные наблюдения, так и долговременные когортные исследования |
|
Study design (S) |
Клинические исследования (рандомизированные и нерандомизированные), когортные и обсервационные исследования, вторичные анализы, метаболомные исследования, экспериментальные исследования, а также систематические обзоры и метаанализы, включающие данные по осмолярности плазмы и осмолитным соотношениям у человека |
Сокращения: COVID-19 — новая коронавирусная инфекция, SGLT2 — натрий-глюкозный котранспортер 2 типа.
Критерии исключения исследований
- Отсутствие данных об осмолярности или концентрациях осмолитов. Исключались публикации, не содержащие количественных значений Na+, K+, глюкозы или мочевины, либо не позволявшие рассчитать eOSM (расчетная осмолярность плазмы) или долю мочевины к eOSM (PropUrea/eOSM).
- Неопределённый эффект водного дефицита или осмостресса. Исключались работы, где невозможно выделить независимое влияние дегидратации, диуретиков, соли или натрий-глюкозного котранспортера 2 типа (SGLT2)-ингибиторов на исследуемые исходы.
- Отсутствие взрослой популяции. Работы, включавшие детей и подростков (<18 лет), исключались, если не проводился отдельный анализ взрослых.
- Дубликаты и вторичные публикации без новых данных. Если одно исследование публиковалось несколько раз, учитывалась наиболее полная версия данных.
- Публикации без доступа к полному тексту или без рецензирования. Исключались тезисы конференций, препринты, материалы без проверяемых данных.
Извлечение данных
Извлечение данных проводилось одним автором с последующей независимой проверкой другим исследователем. Информация из включённых публикаций переносилась в унифицированные таблицы, соответствующие дизайну каждого исследования. Для всех работ регистрировались основные характеристики выборки, демографические параметры, клинический контекст, методы оценки водно-осмолитного статуса и изучаемые исходы.
Особое внимание уделялось показателям, отражающим перераспределение осмолитов при водном дефиците: концентрациям натрия, калия, глюкозы и мочевины, а также расчетной осмолярности плазмы и доле органических осмолитов. При необходимости значения осмолярности пересчитывались по стандартным формулам, а все единицы измерения приводились к единому формату.
Для каждого исследования оценивались клинические исходы, связанные с мышечным катаболизмом, функцией почек, артериальным давлением (АД) и общим состоянием пациентов. При наличии нескольких публикаций из одной когорты использовалась наиболее полная версия данных. Разногласия при интерпретации информации разрешались путем обсуждения до достижения консенсуса между авторами.
Стратегия поиска
Поиск проводился в октябре 2025г с языковыми ограничениями: английский, русский, немецкий, французский; временной охват — 1980-2025гг. Включались исследования на людях (возраст ≥18 лет). Работы на животных и фундаментальные механистические исследования использовались вспомогательно — для описания или подтверждения правдоподобного механизма, объясняющего наблюдаемые клинические эффекты. Протокол соответствовал PRISMA-2020. Протокол исследования предварительно не регистрировался.
Информационные источники
Мы систематически искали публикации в электронных базах и регистрах клинических исследований, а также дополняли поиск ручными методами.
- Электронные базы (n=1680 записей): SciSpace (n=420), PubMed (n=380), EMBASE (n=340), Google Scholar (n=280), Cochrane Library (n=180), Web of Science (n=80).
- Регистры клинических исследований (n=124): ClinicalTrials.gov (n=75), World Health Organization, ICTRP (n=32), EU-CTR (n=17).
- Другие источники (n=45): перекрёстные ссылки из включённых статей, экспертные рекомендации (нефрология/эндокринология), материалы конференций (European Society of Cardiology, American Society of Nephrology, European Renal Association — European Dialysis and Transplant Association, American Heart Association), препринты.
Концептуальная схема и поисковые термины
Запросы строились по пяти тематическим блокам с последующим логическим объединением (AND) блоков и синонимов (OR) внутри блока. Ключевые понятия:
- Метаболическая аэстивация и осмолиты: «metabolic aestivation», «aestivation», «osmolyte metabolism», «urea cycle», «water conservation», «osmotic stress», «hyperosmolality».
- Клинические состояния: «heart failure», «chronic kidney disease», «COVID-19», «ICU», «dehydration», «loop diuretics», «SGLT2 inhibitors».
- Биомаркеры: «urea», «estimated osmolality», «eOSM», «copeptin», «vasopressin».
- Клинические исходы: «sarcopenia», «muscle catabolism», «long-COVID», «physical weakness».
- Популяция: «humans», «adult».
Итоговая поисковая формула (базовая, для PubMed): («metabolic aestivation» OR «aestivation» OR «osmolyte metabolism» OR «urea cycle» OR «water conservation» OR «osmotic stress» OR «hyperosmolality») AND («heart failure» OR «chronic kidney disease» OR «COVID-19» OR «ICU (Intensive Care Unit)» OR «dehydration» OR «loop diuretics» OR «SGLT2 inhibitors») AND («urea» OR «estimated osmolality» OR «eOSM» OR «copeptin» OR «vasopressin») AND («sarcopenia» OR «muscle catabolism» OR «long-COVID» OR «physical weakness») AND («humans» OR «adult»).
Для PubMed использовались MeSH-термины и поля [tiab]; для EMBASE — Emtree-термины; синтаксис адаптирован к каждой базе. В Google Scholar применяли экранирование точных фраз и минус-операторы для отсечения нерелевантных источников.
Обработка результатов поиска и удаление дубликатов
Все результаты экспортировались в менеджер библиографии (Zotero) с последующей дедупликацией (совпадение DOI/PMID/названия/года/авторов). Повторные версии препринта/журнала маркировались и приоритет отдавался рецензированному полному тексту.
Скрининг и отбор
Двое рецензентов независимо выполняли двухэтапный скрининг: (1) заголовок/аннотация; (2) полнотекстовый просмотр. Несогласия решались консенсусом; при необходимости привлекался третий рецензент.
Оценка риска предвзятости
Совокупность доказательств, включённых в настоящий обзор, основана преимущественно на данных хорошо спланированных когортных и клинических исследований, что позволяет рассматривать выявленные ассоциации между водным дефицитом, осмолитным сдвигом и клиническими исходами как потенциально причинно-следственные. В связи с этим была проведена оценка риска предвзятости (Risk of Bias, ROB) для включённых работ.
Поскольку анализ охватывал широкий спектр исходов — от биохимических показателей осмолярности и метаболизма до клинических конечных точек (саркопения, АД, функция почек, смертность), подход к оценке ROB был адаптирован к типу исследования. Для рандомизированных клинических испытаний использовались критерии инструмента Cochrane ROB 2.0, для нерандомизированных и когортных исследований — инструмент ROBINS-I (Risk Of Bias In Non-randomized Studies).
При оценке учитывались следующие домены риска предвзятости:
- Качество подбора участников и адекватность критериев включения;
- Контроль смешивающих факторов (возраст, пол, функция почек, потребление соли, объём диуретиков, терапия SGLT2-ингибиторами);
- Точность измерения биомаркёров (Na+, K+, глюкоза, мочевина, eOSM, копептин);
- Достоверность методов оценки исходов (мышечная масса и сила, показатели гемодинамики, расчетная скорость клубочковой фильтрации (СКФ), острое повреждение почек, смертность);
- Полнота данных наблюдения и риск выборочного отчёта результатов.
Результаты
Характеристика включённых исследований
В ходе поиска было выявлено 120 публикаций, из которых 118 остались после удаления дубликатов. После анализа аннотаций и полнотекстового скрининга 18 исследований соответствовали критериям включения (рис. 1, табл. 2). В анализ вошло 18 исследований, опубликованных с 2017 по 2025гг, Из них: 7 клинических (в т.ч. 2 рандомизированных и 3 когортных исследования); 6 экспериментальных на животных моделях (мыши, крысы, свиньи); 3 обзорных и 2 смешанных (люди + животные). В окончательный анализ вошли 6 клинических исследований.

Рис. 1. PRISMA-диаграмма отбора исследований.
Таблица 2
Дополнительная характеристика включённых исследований
|
№ |
Автор (год) |
Страна/центр |
Дизайн исследования |
Модель/участники |
N |
Интервенция/условие |
Основная цель |
doi/источник |
|
1 |
Marton A, et al. (2024) |
Германия, США |
клиническое |
люди |
33 пациента (в группе анализа 29) |
SGLT2 |
изучить механизмы водосбережения при ограничении воды |
10.1152/physiol.2024.39.S1.1461 [26] |
|
2 |
Kitada K, et al. (2017) |
Германия/США |
экспериментальное |
люди + мыши |
28 животных и 20 человек |
проверить роль осмотического стресса в АД |
10.1172/JCI88532 [17] |
|
|
3 |
Wild J, et al. (2021) |
Германия |
экспериментальное |
мыши |
N/A (обзор) |
изучить влияние кожной потери воды |
10.1111/apha.13628 [10] |
|
|
4 |
Kovarik J, et al. (2021) |
Германия, Япония |
экспериментальное |
крысы |
18 животные |
адаптивное водосбережение при ХПН |
10.1111/apha.13629 [12] |
|
|
5 |
Nihlén S, et al. (2021) |
Германия, Сингапур |
клиническое |
люди |
241 пациент |
фуросемид |
вклад мочевины в осмолярность при дегидратации |
10.1093/function/zqab055 [4] |
|
6 |
Marton A, et al. (2021) |
Германия |
обзорное |
– |
N/A (обзор) |
обзор эффектов SGLT2-ингибиторов |
10.1038/s41581-020-00350-x [26] |
|
|
7 |
Hultström M, et al. (2022) |
Швеция (многоцентровое) |
наблюдательное |
люди |
374 пациента |
COVID-19 |
связь дегидратации и симптомов |
10.1186/s13054-022-04203-w [5] |
|
8 |
Dragunov DO, et al. (2025) |
Россия |
клиническое |
люди |
102 пациента |
фуросемид |
оценить влияние соли и диуретиков |
10.3389/fnut.2025.1538962 [15] |
|
9 |
Barrueta A, et al. (2024) |
Германия, Швеция |
наблюдательное |
люди |
824 пациента (571 + 284 подвыборки) |
COVID-19 |
метаболомный профиль дегидратации |
10.1152/physiolgenomics.00021.2024 [13] |
|
10 |
Carty J, et al. (2024) |
Германия |
обзорное |
– |
N/A (обзор) |
осморегуляция при гипернатриемии |
10.1097/MNH.0000000000001012 [21] |
|
|
11 |
Barrueta Tenhunen A, et al. (2025) |
Германия |
экспериментальное |
свиньи |
14 свиней |
роль свободной воды при натрийнагрузке |
10.1186/s40635-025-00800-5 [24] |
|
|
12 |
Hultström M, et al. (2022) |
Германия |
экспериментальное |
– |
N/A (размер выборки не указан) |
метаболическое водосбережение |
10.1096/fasebj.2022.36.S1.R4420 [27] |
|
|
13 |
Eccles R, et al. (2019) |
Швеция |
наблюдательное |
люди |
55 участников |
ОРВИ |
влияние инфекции на гидратацию |
10.1186/s40248-019-0200-9 [28] |
|
14 |
Da Cruz-Filho J, et al. (2025) |
Германия |
экспериментальное |
мыши |
12 мышей |
обезвоживание и мышечный катаболизм |
10.1152/ajpregu.00187.2024 [29] |
|
|
15 |
Imoto K, et al. (2022) |
Бразилия |
смешанное |
люди + мыши |
16 мышей + 2 клинических случая |
цикл мочевины и аммоний |
10.1186/s12876-022-02213-0 [30] |
|
|
16 |
Kameda M, et al. (2021) |
США |
наблюдательное |
люди |
19 участников |
ХБП |
метаболомика саркопении |
10.18632/aging.203498 [31] |
|
17 |
Rugg C, et al. (2020) |
Германия |
обзорное |
– |
размер выборки требует доступа к полному тексту |
ICU-гипернатриемия и PICS |
10.3390/jcm9093017 [32] |
|
|
18 |
Marton A, et al. (2024) |
Германия |
клиническое |
люди |
40 |
SGLT2 |
целью данного исследования была проверка гипотезы о том, что концентрация мочи, обусловленная вазопрессином, преобладает над осмотическим диуретическим эффектом глюкозурии, вызванной лечением дапаглифлозином |
10.1016/j.jacc.2024.02.020 [26] |
Сокращения: АД — артериальное давление, ОРВИ — острая респираторная вирусная инфекция, ХБП — хроническая болезнь почек, ХПН — хроническая почечная недостаточность, COVID-19 — новая коронавирусная инфекция, ICU — Intensive Care Unit, PICS — Persistent Inflammation, Immunosuppression and Catabolism Syndrome, SGLT2 — натрий-глюкозный котранспортер 2 типа.
Анализ включал 3 подгруппы (рис. 2): пациенты, получавшие диуретики (n=45/284), пациенты с дегидратацией различной этиологии (n=1000) и пациенты, получавшие ингибиторы SGLT2 (n=15/15).

Рис. 2. Forest plot метаанализа влияния различных моделей водного дефицита и диуретической терапии на изменение осмолярности плазмы.
В группе диуретиков Dragunov DO, et al. (2025) и Nihlén S, et al. (2021) [4][15] демонстрируют положительный сдвиг осмолярности в сторону увеличения по сравнению с контролем (Standardized Mean Difference (SMD) 0,24 [ -0,24; 0,71] и 0,88 [ 0,39; 1,38], соответственно). Объединённая оценка по модели с фиксированными эффектами составила SMD 0,55 [ 0,20; 0,89], в то время как при модели случайных эффектов — 0,56 [ -0,08; 1,19], однако при выраженной гетерогенности (I²=70,6%, τ²=0,1488).
В подгруппе дегидратации три исследования продемонстрировали существенное повышение осмолярности (Eccles R, et al., 2019: SMD 0,18 [ -0,20; 0,55]; Hultström M, et al., 2022: SMD 0,80 [ 0,65; 0,95]; Barrueta Tenhunen A, et al., 2024: SMD 1,41 [ 1,28; 1,54]). Объединённый эффект по фиксированной модели составил 1,08 [ 0,99; 1,18], а по модели случайных эффектов — 0,81 [ 0,12; 1,50], при высокой межисследовательской вариабельности (I²=96,7%, τ²>=0,3532; p<0,0001).
Подгруппа терапии SGLT2-ингибиторами включала одно исследование с отсутствием статистически значимого изменения осмолярности (Marton A, et al., 2024: 0,00 [ -0,72; 0,72]).
В совокупности по всем исследованиям общий объединённый эффект по модели фиксированных эффектов составил SMD 1,03 [ 0,94; 1,12] (p<0,0001), тогда как при применении модели случайных эффектов — 0,63 [ 0,19; 1,07] (p=0,0049). Гетерогенность между исследованиями была значительной (I²=93,8%, τ²=0,2555). Интервал прогноза для будущих исследований варьировал от -0,79 до 2,05, отражая высокую вариабельность осмотического ответа в зависимости от клинического контекста.
В анализ (рис. 3) включено 6 исследований с общей выборкой 1060 пациентов в группах воздействия и 1299 в контрольных группах. Исследования Nihlén S, et al. (2021) и Dragunov DO, et al. (2025) продемонстрировали разнонаправленные величины эффекта с общей тенденцией к увеличению концентрации мочевины в плазме (SMD 0,10 [ -0,39; 0,59] и SMD 0,82 [ 0,32; 1,31], соответственно). Объединённый эффект по фиксированной модели показал статистически значимое повышение уровня мочевины (SMD 0,46 [ 0,11; 0,80]), при этом по модели случайных эффектов ассоциация не достигла статистической значимости (SMD 0,46 [ -0,24; 1,16]). Гетерогенность была высокой (I²=75,3%, τ²=0,1933; p=0,0443). Для исследований Hultström M, et al. (2022), Barrueta Tenhunen A, et al. (2024) и Eccles R, et al. (2019) не были представлены количественные данные для расчёта SMD, поэтому они не внесли вес в итоговые модели. Единственное исследование Marton A, et al. (2024) показало отсутствие значимого эффекта вмешательства (SMD 0,36 [ -0,36; 1,09]).

Рис. 3. Forest plot метаанализа влияния диуретической терапии, дегидратации и SGLT2-ингибиторов на концентрацию мочевины в плазме. Эффект вмешательства выражен в виде SMD между группами вмешательства и контроля.
Совокупный анализ по фиксированной модели показал достоверное повышение уровня мочевины в плазме при воздействиях, направленных на усиление водного дефицита (SMD 0,44 [ 0,12; 0,75], p=0,0063). Однако по модели случайных эффектов статистическая значимость была пограничной (SMD 0,43 [ -0,03; 0,90], p=0,0653). Гетерогенность исследований умеренная (I²=51,2%, τ²=0,0847). Прогностический интервал лежит в пределах от -1,18 до 2,04, что указывает на значительную вариабельность мочевины.
Несмотря на различия между исследованиями, результаты демонстрируют тенденцию к повышению концентрации мочевины в случаях, сопровождающихся водным дефицитом. Это может подтверждать концепцию перераспределения осмолитов и увеличения вклада мочевины в поддержание тоничности плазмы при осмотическом стрессе. Однако нестабильность оценок указывает на необходимость дальнейших исследований.
Исследования Nihlén S, et al. (2021) и Dragunov DO, et al. (2025) (рис. 4) показали разнонаправленные величины SMD (-0,83 [ -1,33; -0,33] и 0,06 [ -0,42; 0,53], соответственно). Совокупный анализ по фиксированной модели выявил статистически значимое снижение концентрации натрия в плазме (SMD -0,37 [ -0,71; -0,02]). Однако использование модели случайных эффектов нивелировало значимость (SMD -0,38 [ -1,25; 0,48]). Гетерогенность — высокая (I²=84,2%, τ²=0,3289; p=0,0118). Единственное исследование Barrueta Tenhunen A, et al. (2024), внесшее вес в итоговый анализ, продемонстрировало небольшое, но статистически значимое снижение уровня натрия по сравнению с контролем (SMD -0,15 [ -0,26; -0,03]). Данные Hultström M, et al. (2022) и Eccles R, et al. (2019) не позволили рассчитать SMD и не повлияли на общий вес.

Рис. 4. Forest plot метаанализа изменения концентрации натрия в плазме при вмешательствах, сопровождающихся изменением водного баланса (диуретики, дегидратация, SGLT2-ингибиторы).
В исследовании Marton A, et al. (2024) не выявлено значимого эффекта терапии на уровень натрия (SMD 0,00 [ -0,72; 0,72]). Совокупный анализ по фиксированной модели показал небольшое, но статистически значимое снижение концентрации натрия в плазме под влиянием вмешательств, связанных с изменением водного баланса (SMD -0,17 [ -0,27; -0,06], p=0,0029). По модели случайных эффектов эффект не достиг статистической значимости (SMD -0,23 [ -0,60; 0,14], p=0,2183), что обусловлено межисследовательской вариабельностью (I²=62,3%, p=0,0467). Прогностический интервал варьирует от -1,36 до 0,90, что демонстрирует высокую неопределённость ожидаемого эффекта в будущих исследованиях.
В анализ включены 2 исследования, представляющие данные по 45 пациентам в группе фуросемида и 284 — в контрольной группе (рис. 5). Оба исследования рассматривали состояние осмотического стресса, возникающего на фоне применения диуретиков. В исследовании Nihlén S, et al. (2021) отмечено достоверное повышение вклада доли мочевины в поддержание плазменной осмолярности по сравнению с контролем (SMD 0,72 [ 0,22; 1,22]). Результаты Dragunov DO, et al. (2025) демонстрируют ещё более выраженный эффект (SMD 1,31 [ 0,78; 1,83]). Объединённый анализ показал статистически значимое увеличение доли мочевины в осмотическом балансе по фиксированной модели (SMD 1,00 [ 0,64; 1,36]) и по модели случайных эффектов (SMD 1,01 [0,43; 1,58]). Гетерогенность между исследованиями умеренная (I²=60,5%, τ²=0,1038; p=0,1117), что допускает частичное влияние клинических и методологических различий. Прогностический интервал варьировал от -4,52 до 6,54, что отражает широкий ожидаемый диапазон физиологических ответов в будущих выборках, однако его ширина обусловлена малым числом включённых работ. Терапия диуретиками приводит к перераспределению водно-осмотического баланса с увеличением вклада мочевины в поддержание плазменной осмолярности. Это согласуется с концепцией адаптивного усиления продукции органических осмолитов как защитного механизма водосбережения при снижении объёма циркулирующей крови. Представленные данные отражают системный компонент феномена метаболической аэстивации у пациентов под действием диуретиков.

Рис. 5. Forest plot метаанализа влияния диуретической терапии на относительный вклад мочевины в расчётную плазменную осмолярность (доля мочевины в pOSM).
Обсуждение
Молекулярные механизмы метаболической аэстивации
Ключевым механизмом метаболической аэстивации является активация орнитинового цикла мочевинообразования в печени [16]. При котором происходит накопление аминокислот, повышение уровней α-кетоглутарамата (маркёра перегрузки NH4+) и N-ацетил-глутамата (аллостерического активатора карбамоилфосфатсинтетазы), а также рост активности аргиназы и содержания мочевины в печени. Эти изменения свидетельствуют о перераспределении азота из аминокислот в мочевину, выполняющую роль органического осмолита, стабилизирующего водный баланс.
Источником азота и энергии при активации этих механизмов служит скелетная мускулатура. Отмечено усиление катаболизма разветвлённых аминокислот (валин, лейцин, изолейцин) с падением их концентрации и соответствующих оксокислот (KMV, KIC, KIV), а также рост β-гидроксибутирата в мышцах при отсутствии признаков усиленного кетогенеза в печени. Это указывает на использование мышечных белков как доноров азота для печёночного синтеза мочевины [12].
В совокупности печёночно-мышечные, пуриновые и аргинин-NO-зависимые сдвиги, подкреплённые нейрогормональными и сосудистыми реакциями, формируют программу метаболической аэстивации — механизма удержания воды за счёт перехода от неорганических к органическим осмолитам и использования мышечного азота как источника субстрата для их синтеза, ценой усиленного катаболизма и повышения АД [12].
В исследовании Kitada K, et al. (2017) [17] было показано, что выведение избытка поваренной соли не ограничивается осмотическим диурезом и потерей воды. При высоком потреблении натрия организм поддерживает отрицательный свободный водный клиренс и накапливает мочевину в почках, способствуя сохранению воды. Почки, печень и скелетные мышцы функционируют как единая регуляторная сеть, обеспечивая баланс между экскрецией соли и эндогенным водосбережением за счёт усиленного синтеза мочевины.
Было показано, что при высоком потреблении соли водосбережение обеспечивается не только почечной рециркуляцией мочевины, но и её активным синтезом в печени и скелетных мышцах. Содержание мочевины в этих органах объясняет до 87% вариабельности её уровня в плазме, при этом ведущая роль принадлежит печени. Повышение активности аргиназы в печени и мышцах служит ключевым механизмом этого процесса, а её фармакологическое ингибирование предотвращает солеиндуцированное накопление мочевины. Эти данные подтверждают существование гепато-ренально-мышечной системы регуляции водного баланса, в которой образование и рециркуляция мочевины играют центральную роль, хотя и сопровождаются значительными энергетическими затратами [17].
Hultström M, et al. показали, что обезвоживание активирует у реанимационных пациентов в состоянии дегидратации «аэстивационноподобный» ответ при высокой осмоляльности плазмы [5][13]. У пациентов в тяжёлом состоянии, с новой коронавирусной инфекцией и без него, высокая осмоляльность плазмы ассоциировалась со сдвигом метаболизма в сторону продукции аминокислот вследствие распада мышечных белков и усиленного синтеза мочевины [5][13]. В ряде работ было показано, что «аэстивационноподобный» ответ сопровождается повышением секреции вазопрессина и индуцированным глюкокортикоидами усилением мышечного катаболизма [18][19]. Однако до конца остаётся неясным, оказывает ли вазопрессин прямое влияние на мышечный катаболизм и как этот процесс запускается [18].
Следует также отметить, что гипогидратация у пожилых людей имеет прямую связь с развитием саркопении. В исследовании, проведённом на основе национального корейского опроса здоровья и питания (n=3656; 1582 мужчин и 2074 женщин), было показано, что у лиц с саркопенией суточное потребление воды из пищи и напитков, а также отношение фактического водного потребления к рекомендованному уровню (1000 мл для мужчин и 900 мл для женщин) были значительно ниже, чем у лиц без саркопении. Таким образом, недостаточное потребление воды в пожилом возрасте является независимым фактором, повышающим риск саркопении, и требует учёта при профилактике саркопении для сохранения мышечной массы и ее нормального функционирования [20][21].
В исследовании Dmitrieva NI, et al. (Atherosclerosis Risk in Communities Study (ARIC Study)) [11] была продемонстрирована тесная связь между хронической гипогидратацией и повышенным риском развития СН. В выборке из 11814 участников среднего возраста (45-66 лет), наблюдаемых на протяжении 25 лет, выявлено, что повышение концентрации натрия в сыворотке крови выше 143 ммоль/л — даже в пределах «нормального» диапазона — ассоциировалось с увеличением риска хронической СН (ХСН) на 39% и гипертрофии левого желудочка (ЛЖ) на 62-107% по сравнению с лицами с более низкими значениями натрия. Эти данные интерпретированы как отражение хронического дефицита воды, эквивалентного примерно 1% массы тела, что указывает на метаболическую перестройку, направленную на эндогенное водосбережение.
Продолжением этого исследования стало более крупное популяционное исследование Rabinowitz J, et al. (2025) [22], основанное на анализе электронных медицинских карт 407187 взрослых пациентов (18-104 лет) из базы данных израильской системы Leumit Healthcare Services за 20-летний период. В исследование включались лица без выраженных хронических заболеваний и нарушений водного баланса, с нормальными значениями натрия в сыворотке (135-146 ммоль/л).
Результаты показали, что даже «высоконормальные» уровни натрия и тоничности плазмы связаны с существенным повышением риска артериальной гипертензии (АГ) и СН. Так, при концентрации натрия 140-142 ммоль/л риск АГ возрастал на 13%, а при уровне выше 143 ммоль/л — на 29% (отношение рисков (HR) 1,29; 95% доверительный интервал (ДИ): 1,25-1,33). Аналогично, тоничность плазмы >287 мосм/кг ассоциировалась с 19%-м увеличением риска гипертензии (HR 1,19; 95% ДИ: 1,17-1,22). Для СН риск возрастал на 20% при натрии >143 ммоль/л (HR 1,20; 95% ДИ: 1,12-1,29) и на 15% при тоничности >289 мосм/кг (HR 1,16; 95% ДИ: 1,08-1,21).
Данные этого исследования подтверждают, что даже умеренно повышенные уровни натрия и гипогидратация даже в пределах нормы могут служить предрасполагающим фактором развития АГ и ХСН. С точки зрения концепции метаболической аэстивации, эти изменения отражают адаптивное смещение метаболизма к эндогенному водосбережению — активации вазопрессина, усиленному синтезу мочевины и катаболизму мышечной ткани, что при длительном воздействии способствует ремоделированию миокарда и прогрессированию СН и развитию саркопении.
Важно отметить, что гипернатриемия является классическим маркером водного дефицита и отражает состояние гипогидратации и осмотического стресса. Однако абсолютные и относительные изменения осмолитов могут иметь различную направленность. Даже при сохранении или повышении абсолютной концентрации натрия в плазме может происходить непропорционально более выраженное увеличение концентрации органических осмолитов, прежде всего мочевины, вследствие усиленного уреогенеза и мышечного катаболизма. В результате относительный вклад натрия в общую осмолярность плазмы может снижаться, несмотря на наличие гипернатриемии или нормонатриемии. Этот феномен отражает перераспределение осмолитного баланса в сторону органических осмолитов как части адаптивного ответа, направленного на эндогенное сохранение воды при гипогидратации.
В исследовании Dragunov DO, et al. (2025) [15] показано, что у госпитализированных пациентов с ХСН интенсивная терапия петлевыми диуретиками вызывает рост осмолярности плазмы и увеличение доли мочевины при одновременном снижении вклада натрия, что отражает активацию метаболической аэстивации — переход от неорганических к органическим осмолитам, направленный на эндогенное водосбережение. Наиболее выраженный эффект наблюдался у пациентов, потреблявших более 10 г соли в сутки1.
Мы предположили, что выраженность метаболической аэстивации зависит в т.ч. и от уровня потребления соли. У лиц, длительно находящихся на высокосолевой диете, возможно накопление осмотически неактивного натрия, связанного с гликозаминогликанами [23], что усиливает метаболическую перестройку при диуретической стимуляции. В нашем исследовании именно у таких пациентов через 7 дней терапии отмечался более выраженный осмолитный сдвиг: повышение вклада мочевины в суммарную осмолярность с 2,2% до 2,5% (p=0,015) и снижение вклада натрия в суммарную осмолярность с 46,4% до 46,3% (p=0,014), тогда как при потреблении <6 г соли подобный эффект отсутствовал.
Эффект интенсивной терапии петлевыми диуретиками на метаболическую перестройку в сторону метаболической аэстивации, ранее продемонстрированный в исследовании Nihlén S, et al. (2021) [4], подтверждён данными о выраженной положительной корреляции между кумулятивной дозой фуросемида в дни нахождения в отделении реанимации и интенсивной терапии и увеличением доли мочевины в осмолярности плазмы (r=0,61; P<0,001).
Аналогичные закономерности были продемонстрированы в экспериментальном исследовании Barrueta Tenhunen A, et al. (2025) [24], где на модели гипернатриемии у свиней изучалось влияние фуросемида (5 мг/ч) в группах потребляющих воду и нет. При этом стоит отметить, что гипернатриемическое состояние достигалось за счет нахождения животных на высокосолевой диете (250 ммоль, что соответствует примерно 14 г соли в сутки с минимальным доступом к воде). Было показано, что избыточное повышение концентрации Na+ в плазме (>150 ммоль/л) вызывает выраженный гиперосмотический и катаболический ответ. Применение фуросемида без коррекции водного дефицита усугубляло гипернатриемию и метаболический стресс, тогда как его сочетание с инфузией свободной воды способствовало нормализации осмолярности, усиливало натрийурез (99±20 ммоль vs 70±18 ммоль; p=0,00056) и снижало выраженность катаболических изменений (глютамин 1084±110 мкмоль/л vs 1305±209 мкмоль/л; p=0,029). Повышение уровня глутамина в плазме при отсутствии инфузии воды отражает активацию его синтеза и усиление распада белка в ответ на гиперосмолярность. Глутамин, образующийся преимущественно в скелетных мышцах, участвует в транспорте азота в печень для синтеза мочевины, что подтверждает его ключевую роль в адаптации. Эти результаты подтверждают ключевую роль водно-электролитного дисбаланса и терапии петлевыми диуретиками как триггера метаболической перестройки в сторону аэстивации. СКФ, в группе получающей воду достигала плато к концу исследования, составив в среднем 46±4 мл/мин, тогда как в группе без инфузии воды отмечалось постепенное снижение СКФ на протяжении всего эксперимента — с 56±10 до 40±8 мл/мин, что соответствовало среднему снижению на 16±12% по сравнению с исходными значениями. Метаболическая аэстивация может способствовать снижению клубочковой фильтрации и, следовательно, повышать риск прогрессирования хронической болезни почек (ХБП).
В исследовании Duan S, et al. (2024) [25] была подробно проанализирована взаимосвязь между потреблением соли, водным балансом и структурно-функциональными изменениями сердца у пациентов с ХБП, не находящихся на диализе. В исследование были включены 409 пациентов с ХБП стадий C1-C4, у которых суточное потребление соли оценивали по 24-часовому выведению натрия с мочой, а водный баланс — по отношению внеклеточной воды (ECW) к общей воде организма (TBW). Пациенты были разделены на четыре группы в зависимости от уровня потребления соли (порог 6 г/сут.) и медианного значения ECW/TBW (0,439).
Результаты показали, что у пациентов с высоким потреблением соли и повышенным содержанием внеклеточной жидкости риск формирования гипертрофии ЛЖ и/или повышенного давления наполнения ЛЖ был в 2,4 раза выше (отношение шансов =2,396; 95% ДИ: 1,171-4,902; p=0,017), чем у пациентов с низкими показателями обоих параметров, даже после коррекции на основные факторы риска (расчетная СКФ, протеинурия). Таким образом, сочетание высокого потребления соли (>6 г/сут.) и избыточного внеклеточного объёма (ECW/TBW >0,439) независимо предсказывает развитие гипертрофии и диастолической дисфункции миокарда у пациентов с ХБП без диализа. Эти данные подтверждают, что избыточное потребление соли и задержка жидкости приводят к хронической осмолярной и объёмной перегрузке, стимулирующей адаптивные, но энергозатратные водосберегающие механизмы, сходные с метаболической аэстивацией, которые в конечном итоге способствуют ремоделированию миокарда. По-видимому, несмотря на наличие перегрузки жидкостью, аэстивация развивалась вследствие высокой концентрации натрия в моче, которая в группе пациентов с избыточным потреблением соли и ХБП составляла в среднем 154,4 (127,35-194,60) ммоль/сут., что приводит к потере свободной воды, тем самым активируя эндогенные механизмы водосбережения.
Эта концепция получила подтверждение в исследовании Marton A, et al. (2024)2, в котором была экспериментально продемонстрирована связь между потреблением воды и соли. В когорте из 108 участников в условиях повседневной жизни аналогичные зависимости подтвердились: повышение АД сопровождалось ростом осмолярности плазмы, увеличением уровня вазопрессина и снижением экскреции свободной воды. У лиц с более высоким АД наблюдалось преобладание органических осмолитов (мочевина, глюкоза) при меньшей роли неорганических ионов натрия, что свидетельствует о переключении метаболизма в аэстивационный режим — сохранение воды за счёт эндогенного синтеза органических осмолитов.
В контексте концепции метаболической аэстивации результаты исследования Marton A, et al. (2024) [26] представляют особый интерес, поскольку демонстрируют, что даже фармакологическая стимуляция осмотического диуреза с помощью SGLT2-ингибиторов не приводит к потере воды, а, напротив, активирует вазопрессин-зависимый механизм эндогенного водосбережения.
Повышение концентрации мочи, рост уровней копептина (маркёра секреции вазопрессина) и усиление синтеза мочевины у пациентов с ХСН, получающих SGLT2i, указывают на включение тех же адаптивных путей, которые ранее были описаны при физиологической или патологической дегидратации. Таким образом, лечение ингибиторами SGLT2 парадоксально воспроизводит аэстивационноподобное состояние, при котором организм стремится сохранить воду за счёт увеличения доли органических осмолитов — прежде всего мочевины.
Заключение
Результаты настоящего систематического обзора и метаанализа показывают, что водный дефицит, диуретическая терапия, сопровождающиеся осмотическим стрессом, ассоциированы с изменением осмолитного профиля плазмы, включая увеличение концентрации мочевины и её вклада в общую осмолярность, а также тенденцию к снижению относительного вклада натрия.
Выявленные изменения согласуются с описанным в экспериментальных и клинических исследованиях феноменом метаболической аэстивации, который рассматривается как потенциальный адаптивный метаболический ответ, направленный на эндогенное сохранение воды за счёт перераспределения осмолитов и усиления синтеза органических осмолитов, прежде всего мочевины.
Вместе с тем высокая гетерогенность между исследованиями, вариабельность величин эффекта и ограниченное число клинических работ не позволяют окончательно подтвердить клиническое значение и универсальность данного феномена у пациентов с ХСН.
Полученные результаты указывают на необходимость дальнейших проспективных клинических исследований с унифицированной методологией для уточнения механизмов, клинической значимости и прогностической роли феномена метаболической аэстивации при состояниях, сопровождающихся нарушением водного баланса.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Арутюнов Г. П., Драгунов Д. О., Соколова А. В., Артюков И. А. Фундаментальные и прикладные аспекты метаболизма натрия при сердечно-сосудистых заболеваниях. Общероссийская общественная организация «Общество специалистов по сердечной недостаточности», Москва, 2025.
2. Marton A, Rauh M, Takase-Minegishi K, et al. Elevated blood pressure follows physiological body-water conservation. Physiology 2024 39(S1). doi:10.1152/physiol.2024.39.S1.147.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Арутюнов Г.П., Драгунов Д.О., Соколова А.В. Метаболическая аэстивация как новое патогенетическое звено саркопении при хронической сердечной недостаточности: систематический обзор и метаанализ. Российский кардиологический журнал. 2026;31(1S):6650. https://doi.org/10.15829/1560-4071-2026-6650. EDN: TNJUJD
Скопировать