Интраоперационная эхокардиографическая визуализация и ее влияние на клинические исходы повторной катетерной аблации типичного трепетания предсердий
Аннотация
Цель. Сравнить эффективность повторной катетерной аблации кавотрикуспидального перешейка (КТП) у пациентов с типичным трепетанием предсердий (ТП) при стандартном подходе и с использованием внутрисердечной эхокардиографии (ВСЭхоКГ).
Материал и методы. В исследование включено 112 пациентов с рецидивом ТП после катетерной аблации КТП. В соответствии с технической возможностью применения ВСЭхоКГ пациенты разделены на две группы: в первой группе аблация проводилась с использованием ВСЭхоКГ (54 пациента), во второй группе, контрольной, 58 пациентам аблация выполнялась по стандартной методике, только под контролем флюороскопии. ВСЭхоКГ позволила определить особенности строение КТП у пациентов с рецидивами ТП: утолщение проксимальной части КТП >7 мм (35%), утолщение основания евстахиева клапана >7 мм (48%), неоднородная центральная часть КТП (13%). Проводилась оценка достижения двунаправленной блокады проведения в КТП: в группе ВСЭхоКГ — 52/54 (96,3%), в контрольной группе — 52/58 (89,7%), Р=0,27. Срок наблюдения пациентов составил 24 мес.
Результаты. Средняя продолжительность процедуры аблации была выше в группе ВСЭхоКГ (54,0±16,8 мин) в сравнении с группой контроля (46,9±11,9 мин), однако среднее время флюороскопии было существенно ниже в группе ВСЭхоКГ: 2,9±1,1 мин и 6,3±1,8 мин, соответственно, Р=0,003. Повторные рецидивы трепетания предсердий встретились у 3 (5,8%) пациентов группы ВСЭхоКГ и у 8 (13,8%) лиц в контрольной группе (P=0,21).
Заключение. При повторной катетерной аблации КТП у пациентов с рецидивом типичного ТП выявлены особенности строения КТП, вероятно ассоциированные со снижением эффективности аблации. Использование ВСЭхоКГ при повторной аблации ТП ассоциировано со снижением времени флюороскопии, однако вероятность повторного рецидива ТП одинаково невысока как при стандартной визуализации во время аблации, так и при использовании ВСЭхоКГ.
Трепетание предсердий (ТП) — одно из наиболее распространенных нарушений ритма сердца, по частоте встречаемости занимающее второе место после фибрилляции предсердий. На долю этой аритмии приходится ~15% от всех наджелудочковых тахикардий [1]. Типичное истмус-зависимое ТП представляет собой правопредсердную тахикардию, реализующуюся по механизму macro re-entry с обязательным прохождением цикла по кавотрикуспидальному перешейку (КТП) [2-4]. Данная аритмия достоверно снижает качество жизни пациентов и ассоциирована с риском тромбоэмболических осложнений, аналогичных рискам при фибрилляции предсердий. В настоящее время первой линией лечения истмус-зависимого ТП является катетерная аблация (КА) КТП, значительно превосходящая медикаментозное лечение по эффективности. Целью КА является формирование двунаправленной блокады проведения в КТП [2][5]. Частота рецидивов ТП после КА КТП, согласно литературным данным, находится в диапазоне 5-10% [6-9]. Рецидивы аритмии обусловлены восстановлением проведения через зону аблации в области КТП. Снижение эффективности аблации может быть связано как с локальными анатомическими особенностями нижней части правого предсердия (ПП) и КТП в виде значительного удлинения перешейка, повышенной трабекулярности из-за продолжения гребенчатых мышц на область КТП, локальным утолщением тканей и формированием карманов, в зоне которых выполняется линия воздействия, так и недостаточным контактом электрод-эндокард [10-13]. Сравнительный анализ применяемых катетеров (катетеры с датчиком давления, орошаемые, с увеличенным размером электродов, высокомощные методики) не выявил достоверных преимуществ в достижении двунаправленной блокады проведения в КТП [7]. Широко применяемое в современной интервенционной аритмологии трехмерное навигационное картирование не позволяет детализировать локальные особенности стенок сердца [10]. Внутрисердечная эхокардиография (ВСЭхоКГ) является инвазивным методом ультразвуковой (УЗ) диагностики, выполняемым при помощи УЗ катетера, введенного в полости сердца. Наиболее частой сферой применения ВСЭхоКГ является КА фибрилляции предсердий для контроля пункции межпредсердной перегородки [14] и интраоперационного мониторинга, но данная методика может быть использована для визуализации при интервенционном лечении любых нарушений ритма сердца. Роль визуализации в интервенционном лечении истмус-зависимого ТП показана в работах отечественных и зарубежных авторов [10][11][15][16].
Целью исследования явилось сравнение эффективности повторной КА КТП у пациентов с рецидивом типичного ТП при использовании ВСЭхоКГ по сравнению со стандартной рентгеноскопической навигацией, с акцентом на анатомические параметры перешейка, длительность и исходы процедуры, изучение практической значимости использования ВСЭхоКГ при катетерном лечении ТП.
Материал и методы
Проведено проспективное нерандомизированное сравнительное наблюдение у 112 пациентов с рецидивом типичного ТП после первичной аблации. Перед проведением повторной аблации ТП пациенты были распределены в одну из двух групп: с использованием ВСЭхоКГ и без использования УЗ визуализации. Последовательные пациенты распределялись в группы на основании наличия или отсутствия в медицинском учреждении расходного материала для выполнения ВСЭхоКГ: группа I с ВСЭхоКГ состояла из 54 пациентов, группу II — без ВСЭхоКГ — составили 58 пациентов; проведение повторной аблации проводилось стандартно под контролем рентгеноскопии.
Критерии включения: возраст ≥18 лет; радиочастотная аблация КТП в течение предыдущих 24 мес. с достижением критериев двунаправленной блокады проведения; клинически значимый рецидив типичного ТП (по электрокардиографическим (ЭКГ) критериям); согласие пациента на участие в исследовании.
Критерии невключения: сердечная недостаточность выше 2А стадии по классификации Стражеско-Василенко, сердечная недостаточность выше III функционального класса по классификации New-York Heart Association, фракция выброса левого желудочка <50% по методу Simpson, атипичное ТП по ЭКГ-критериям, стенокардия напряжения >II функционального класса, хроническая почечная недостаточность с клиренсом креатинина <50 мл/мин, хроническая болезнь почек выше 3 Б стадии, тяжелый обструктивный бронхит, декомпенсированный сахарный диабет, пациенты с показаниями к открытым операциям на сердце, пациенты с имплантированным электрокардиостимулятором, кардиовертером-дефибриллятором.
Критерии исключения: подтверждение не истмус-зависимого механизма тахикардии во время эндокардиального электрофизиологического исследования (ЭФИ) в течение процедуры повторной аблации; отказ пациента от участия в исследовании.
Оцениваемые параметры
Первичной конечной точкой исследования явилось отсутствие рецидива ТП к 24 мес. наблюдения. Вторичные конечные точки включали следующие параметры: время рентгеноскопии во время процедуры КА, общее время процедуры, достижений электрофизиологических критериев двунаправленной блокады проведения в КТП, наличие неблагоприятных событий во время процедуры КА и сразу после нее.
Дополнительными оцениваемыми параметрами являлись особенности анатомического строения КТП, определяемыми при УЗ сканировании.
ЭФИ и КА
В ходе ЭФИ у всех пациентов проводилась оценка критериев достижения двунаправленной блокады проведения через КТП путем регистрации проведения возбуждения в ПП при стимуляции из устья коронарного синуса и нижне-бокового отдела ПП, а также анализа локальных потенциалов с дистального полюса аблационного катетера, расположенного в нижнем КТП. Аблация проводилась в неорошаемом режиме с использованием катетера для аблации Blazer large curve 4 мм (Boston Scientific, США). Параметры наносимых воздействий: мощность 45-50 Вт, максимальная температура 60 °C. В ходе работы в группе I использовался УЗ катетер AcuNav 8/10 Fr, (Biosence Webster, США), УЗ аппараты Cypress (Siemens, США), Vivid IQ (General Electric, США). УЗ катетер вводился через бедренную вену в ПП и устанавливался в «базовую позицию», при которой визуализировались структуры трикуспидального клапана (ТК), диагностическим 10-полюсным катетером катетеризировался коронарный синус. В ПП вводился электрод для аблации, устанавливался на нижний полюс фиброзного кольца ТК, из данной области начиналось нанесение радиочастотных воздействий. Далее позиция для УЗ визуализации изменялась вслед за смещением аблационного катетера по КТП от кольца ТК до устья нижней полой вены. Критериями эффективности КА были купирование ТП, появление локальных критериев блокады проведения по данным регистрации потенциалов с аблационного катетера (формирование двойных низкоамплитудных потенциалов с интервалом между фазами ≥110 мс), а также изменение последовательности активации ПП при стимуляции из коронарного синуса и нижне-боковой зоны ПП, время достижения активации ПП при стимуляции из устья коронарного синуса — не менее 160 мс, невозможность индукции ТП 1 типа стимуляцией.
Оценка характеристик КТП
По данным УЗ визуализации оценивались следующие параметры: длина КТП от кольца ТК до устья нижней полой вены, толщина КТП, наличие углубления/»кармана» КТП, размер и конфигурацию евстахиева клапана. Значительным утолщением КТП считалось значение >7 мм.
Обследование и наблюдение
До операции всем пациентам проводилось обследование, включающее трансторакальную эхокардиографию, ЭКГ, холтеровское мониторирование ЭКГ, другие методы обследования по показаниям. После операции пациентам проводилось суточное мониторирование ЭКГ через 3, 6, 12, 24 мес., регистрация ЭКГ при симптомах, подозрительных на нарушение ритма сердца, а также внеплановые обследования при наличии клинических показаний.
Работа выполнена с использованием ресурсов Центра коллективного пользования «Центр доклинических и трансляционных исследований» на базе ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России.
Статистический анализ. Полученные данные обрабатывались методами статистического анализа с использованием параметрических способов обработки. Для определения достоверности различий количественных признаков применялся t-критерий Стьюдента. Для определения влияния фактора использовался однофакторный дисперсионный анализ с расчетом точного критерия Фишера. Значения различий параметров р<0,05 считались статистически достоверными. Данные были представлены в виде среднего значения и его стандартного отклонения. Для оценки статистической значимости нескольких факторов использовался многофакторный дисперсионный и корреляционный анализ. Статистический анализ проводился с использованием программного обеспечения Excel 2019 (Microsoft corp., США), Statistica 7 (StatSoft, США).
Результаты
Анализ клинических и демографических характеристик показал сопоставимость групп, также не было различий в средней длине цикла рецидивирующего ТП (табл. 1).
Таблица 1
Клиническая характеристика пациентов
|
Показатель |
Группа I (n=54) |
Группа II (n=58) |
Критерии достоверности |
|
Возраст, лет |
60,2±6,5 |
62,1±5,8 |
Р=0,26 |
|
Мужчины, % |
58,6 |
57,9 |
|
|
Женщины, % |
41,4 |
42,1 |
|
|
Сопутствующая патология: артериальная гипертензия, % |
75,9 |
70,7 |
|
|
Сопутствующая патология: сахарный диабет, % |
20,4 |
15,5 |
|
|
Длина цикла тахикардии, мс |
248,0±9,8 |
245,5±8,7 |
р=0,23 |
Интраоперационные результаты повторной аблации
Средняя длительность цикла тахикардии равнялась 248,0±9,8 мс в I группе, 245,9±8,8 мс во II группе. Длительность операции была больше в группе с использованием ВСЭхоКГ в среднем на 7,7 мин (54,0±16,8 мин в I группе, 46,9±11,9 мин во II группе). В группе с УЗ контролем длительность рентгеноскопии была достоверно меньше и составила 2,9±1,1 мин vs 6,3±1,8 мин (Р=0,003). Критерии достижения двунаправленной блокады проведения через КТП были достигнуты у 52/54 (96,3%) пациентов в группе с УЗ контролем и у 52/58 (89,7%) в группе с использованием рентгеноскопии (P=0,27). У 2 пациентов в I группе и 8 во второй не удалось достичь критериев блокады проведения через КТП, несмотря на длительные воздействия и формирование альтернативных линий аблации (латеральной, медиальной).
УЗ характеристика КТП
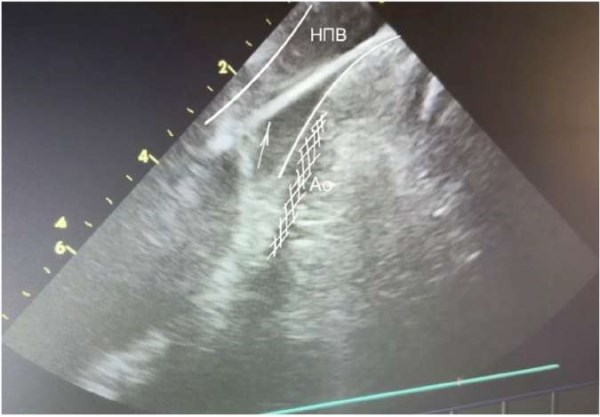
В группе с УЗ визуализацией была оценена морфология КТП, длина КТП составляла от 18 до 50 мм, в среднем 28±6,4 мм, максимальная длина 50 мм у пациента со значительной дилатацией ПП. У 49 (90,7%) отмечалось утолщение миокарда в проксимальной части КТП >7 мм, у 42 (77,8%) — в области основания евстахиева клапана >7 мм, при этом клапан имел конусовидную форму, достигал в длину ≥14 мм (табл. 2, рис. 1 А, Б).
Таблица 2
Результаты эхокардиографической визуализации
|
Показатель |
Группа I (n=54) |
|
Длина КТП в диастолу, мм |
31,8±6,6 |
|
Толщина в проксимальной части КТП, мм |
7,3±0,8 |
|
Толщина в проксимальной части КТП >7 мм |
26 (48%) |
|
Толщина в средней части КТП, мм |
4,3±0,4 |
|
Неоднородность КТП в средней части |
7 (13%) |
|
Наличие углубления/»кармана» в средней части КТП |
3 (5,6%) |
|
Наличие углубления/»кармана» в дистальной части КТП |
2 (3,7%) |
|
Толщина в дистальной части КТП (основание евстахиева клапана), мм |
7,1±0,7 |
|
Толщина в дистальной части КТП (основание евстахиева клапана) >7 мм |
21 (35%) |
|
Длина евстахиева клапана, мм |
10,9±3,3 |
Сокращение: КТП — кавотрикуспидальный перешеек.
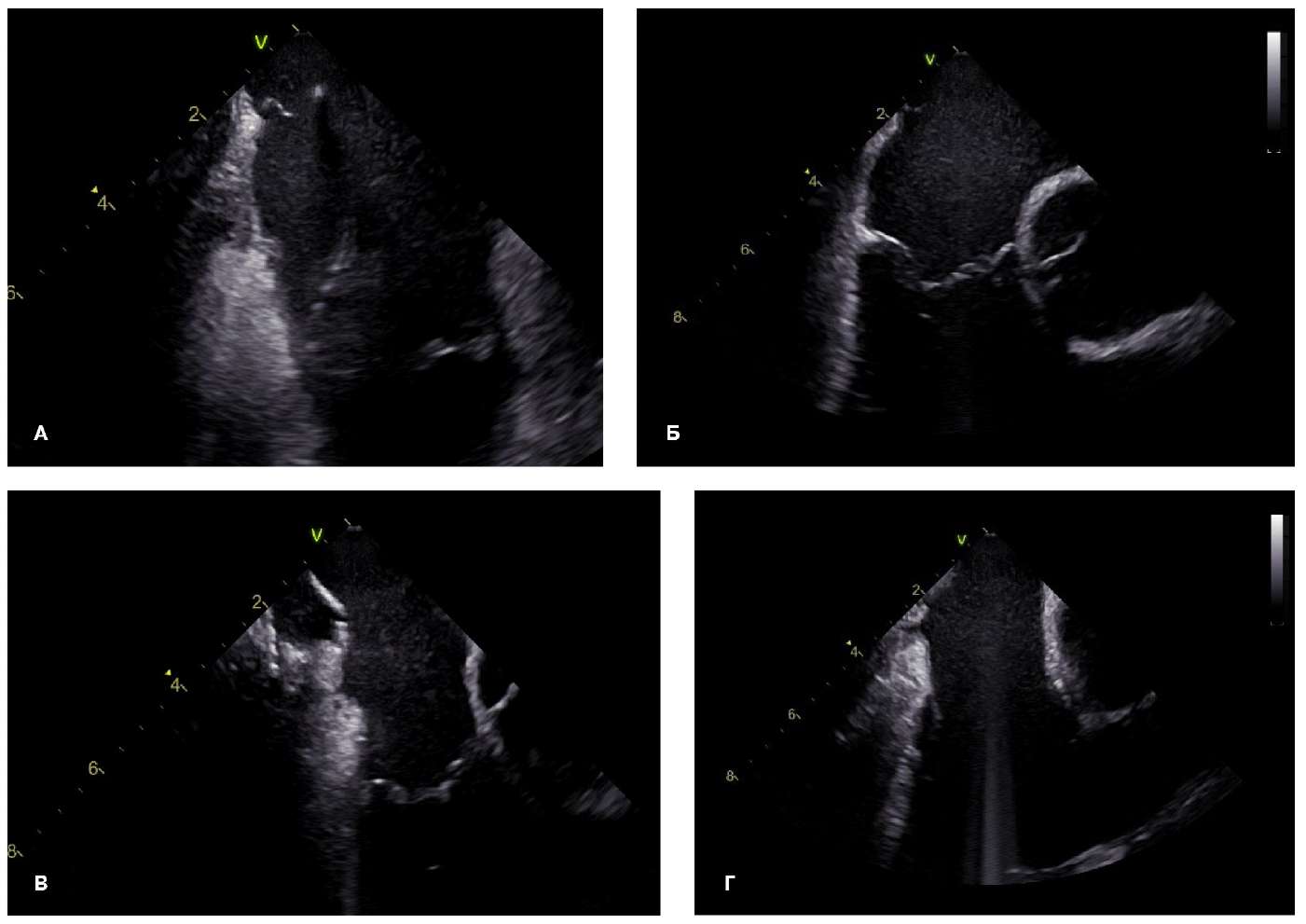
Рис. 1. Полиморфизм центральной части КТП.
У 5 (9,3%) пациентов отмечались затруднения при позиционировании аблационного катетера и достижения блокады проведения по причине наличия углубления/»кармана» КТП: у 3 пациентов (5,6%) — в средней части КТП (при этом наблюдалась наименьшая толщина КТП в этой зоне (до 2,2 мм); у 2 (3,7%) пациентов — в дистальной части КТП перед евстахиевым клапаном, глубиной до 7 мм (рис. 1, В, Г).
Полиморфизм евстахиева клапана — еще одна особенность, выявленная в группе ВСЭхоКГ (рис. 2 А, Б, В, Г). Длина евстахиева клапана варьировалась от 0 (полное отсутствие) до 16,6 мм, в среднем 10,9±3,3 мм, с утолщением основания до 11,8 мм (среднее значение 7,1±0,7 мм). В большинстве случаев евстахиев клапан имел конусовидную форму (рис. 2 А, Б, В), в 2 случаях (3,7%) имел лентовидную форму («сеть Хиари»).

Рис. 2. Полиморфизм евстахиева клапана.
На панелях А, Б визуализируется утолщение эндокарда на протяжении перешейка с участком резкого истончения тканей в центральной части. Подобные участки, не визуализирующиеся при рентгеноскопическом подходе, могут подвергаться диссекции при КА, что может приводить к риску перфорации стенки и развитию осложнений.
Панель В — центральная часть перешейка без патологических углублений или дубликатур эндокарда. На панели Г визуализируются углубления («карманы») в центральной и дистальной частях перешейка.
На панелях А-Г представлены варианты евстахиева клапана в виде гиперэхогенной уплотненной конусовидной структуры, длиной до 15 мм, толщиной до 10 мм. На панели Г евстахиев клапан значительно тоньше и короче, но с резко удлиненной концевой створкой («сеть Хиари»). За счет значительного утолщения тканей в данной области необходимо нанесение воздействий с большей мощностью и длительностью, чем в центральной части перешейка. При рентгеноскопическом подходе данная анатомическая структура не визуализируется, и оценить толщину стенки невозможно. При недостаточном воздействии при КА может формироваться отек тканей, нарушение электрофизиологических свойств клеток, что будет проявляться положительными критериями блока КТП; впоследствии, после купирования отека проведение в данной части может восстановиться, что приведет к рецидиву тахикардии. В то же время избыточные воздействия у пациентов без значительного утолщения эндокарда в данной зоне также создают повышенный риск диссекции.
Анализ ассоциации анатомических характеристик КТП с внутриоперационными результатами
Проведен анализ ассоциации анатомических параметров (длина КТП в диастолу, толщина в проксимальной части, толщина в средней части, толщина основания евстахиева клапана, длина евстахиева клапана) с внутриоперационными данными: длительность операции и длительность рентгеноскопии. Анализ включал последовательную проверку линейных и нелинейных связей с использованием линейной регрессии и обобщенно аддитивной модели. Построены корреляционные матрицы с целью выявления ассоциаций между зависимыми и независимыми переменными (рис. 3).
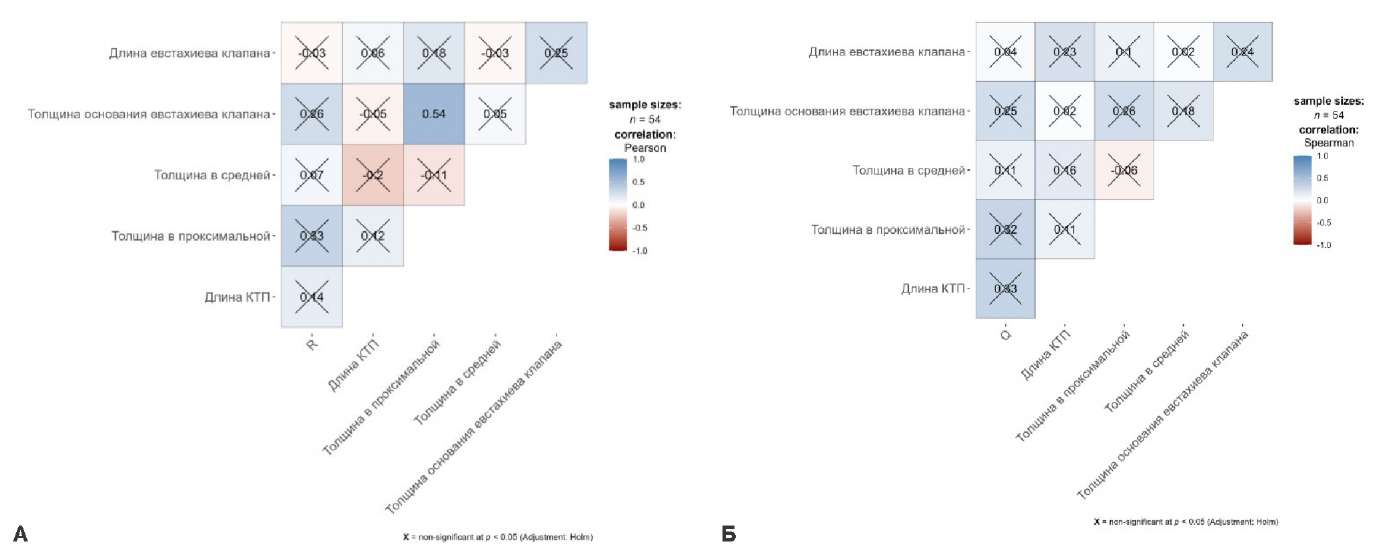
Рис. 3. Корреляционные матрицы показателей «длительность рентгеноскопии» (панель А) и показателя «длительность операции» (панель Б) с анатомическими характеристиками КТП.
Корреляционный анализ не выявил значимых взаимосвязей между изучаемыми переменными и исходом (p>0,05), отмечена лишь ассоциация между толщиной основания евстахиева клапана с проксимальной толщиной. Множественная линейная регрессия с пошаговым исключением предикторов также не продемонстрировала статистически значимых эффектов, а объясняющая способность модели оказалась минимальной (Adjusted R² ≈0,03). Для выявления возможных сложных нелинейных зависимостей была построена обобщённая аддитивная модель (GAM). Ни один из предикторов не достиг статистической значимости (p=0,10-0,71), а общая объяснимость модели оставалась низкой (Adjusted R² ≈0,09).
Отдаленные результаты аблаций
Все пациенты обеих групп выполнили полный протокол наблюдения.
Интраоперационные и отдаленные результаты аблации КТП представлены в таблицах 3, 4. Частота повторных рецидивов имела тенденцию к снижению в группе I в сравнении с группой контроля, однако не имела статистически значимой разницы (5,8 vs 13,8%, P>0,05), таблица 3.
Таблица 3
Интраоперационные и отдаленные результаты аблации
|
Показатель |
Группа I (n=54) |
Группа II (n=58) |
Показатель достоверности |
|
Длительность операции, мин |
53,2±15,3 |
47,2±11,2 |
р=0,03 |
|
Длительность рентгеноскопии, мин |
2,9±1,1 |
6,3±1,8 |
р=0,003 |
|
Достижение блока проведения через КТП, абс. |
52 |
49 |
|
|
Достижение блока проведения через КТП, % |
96,3 |
89,7 |
p=0,89 |
|
Рецидив трепетания предсердий, n (%) |
3 (5,8%) |
8 (13,8) |
p=0,78 |
Примечание: р — показатель достоверности абсолютных величин.
Сокращение: КТП — кавотрикуспидальный перешеек.
Таблица 4
Частотный анализ контрольных точек в группе исследования и контроля
|
Контрольная точка |
Группа I |
Группа II |
χ² |
p-value |
|
0 (выписка из стационара) |
0 |
0 |
– |
1,000 |
|
1 (3 мес.) |
1 (1,9%) |
3 (5,2%) |
0,895 |
0,345 |
|
2 (6 мес.) |
1 (1,9%) |
2 (3,4%) |
0,273 |
0,602 |
|
3 (12 мес.) |
1 (1,9%) |
2 (3,4%) |
0,273 |
0,602 |
|
4 (24 мес.) |
0 |
1 (1,7%) |
0,939 |
0,333 |
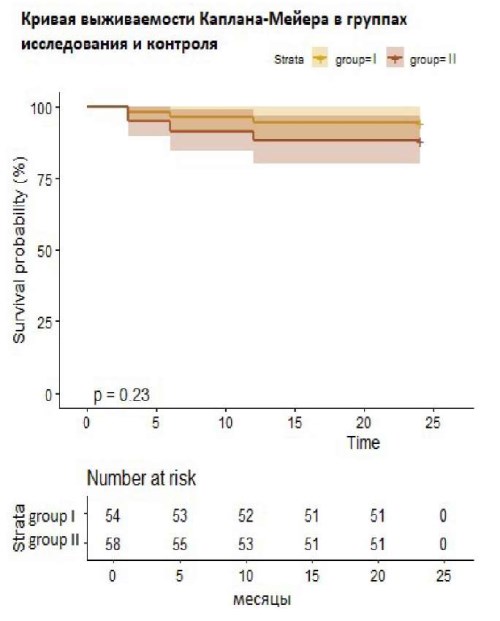
Проведен частотный анализ контрольных точек в группах исследования после выполнения операции с использованием χ² Пирсона, проведен анализ «выживаемости» с построением кривых Каплана-Мейера по контрольным точкам, определяемым в течение 24 мес. после вмешательства в группах исследования и контроля (рис. 4). Частотный анализ по контрольным точкам после вмешательства продемонстрировал сопоставимые результаты в группе исследования (ВСЭхоКГ) и группе контроля (табл. 4).
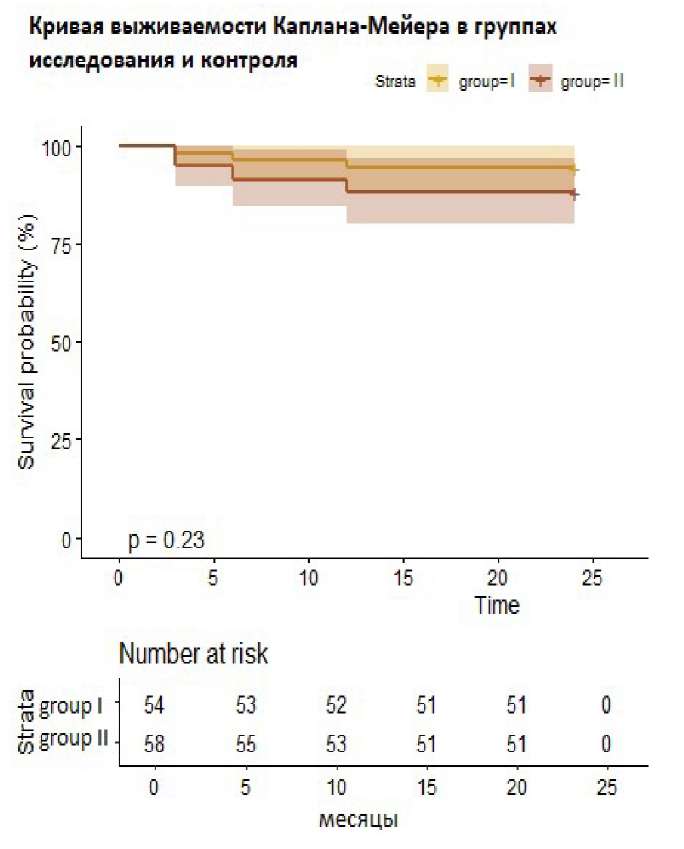
Рис. 4. Кривые выживаемости Каплана-Майера, отражающие время возникновения рецидивов ТП и различия в рецидивах между группами.
Имеется тенденция к большему количеству рецидивов в группе II, однако статистической значимости различия не достигали.
Анализ выживаемости также не выявил достоверных различий между исследуемыми группами.
Обсуждение
Полученные результаты свидетельствуют о высокой технологической и клинической состоятельности метода ВСЭхоКГ при повторных КА КТП при рецидивном ТП. Несмотря на отсутствие статистически значимых различий по основным клиническим исходам между сравниваемыми когортами, установлены важные тенденции: достоверное сокращение времени рентгеноскопии и улучшение качества визуализации анатомического субстрата, что может способствовать оптимизации наносимых воздействий и формирования линий аблации, минимизации воздействий в истонченных участках КТП, минимизации участков, не затронутых аблацией («слепые зоны»), традиционно ассоциирующихся с развитием рецидивов аритмии.
Использование ВСЭхоКГ контроля позволяет значительно уменьшить интраоперационную рентгеноскопию, вплоть до ее отмены («zero fluoro») при полном переключении оператора (хирурга) на УЗ визуализацию. ВСЭхоКГ обеспечивает визуализацию дистальной части катетера, контроля положения в режиме реального времени, а также прилегания аблирующего сегмента электрода к эндокарду по всей протяжённости проксимального КТП вплоть до кольца ТК; электрофизиологически это подтверждается характерной электрограммой. УЗ оценка структуры перешейка позволяет точно учитывать анатомические особенности КТП в каждом клиническом случае, избегать лишних воздействий в зонах истончения миокарда и контролировать перегрев тканей, предотвращая феномен «steam-pop», связанный с диссекцией и повреждением сердечной стенки. В переходной части КТП, прилежащей к фиброзному кольцу ТК, утолщение стенки может затруднять достижение устойчивой трансмуральной блокады даже при длительном воздействии. Критическая зона сфокусирована на терминальной части КТП, где располагается евстахиев клапан. Это рудиментарное анатомическое образование отличается выраженным морфологическим разнообразием: у отдельных пациентов наблюдается его значительное удлинение и утолщение [10].
В нашем исследовании показана вариабельность евстахиева клапана, что позволяет предположить его ключевую роль в восстановлении проведения в КТП после аблации в связи с особенностями строения данной зоны. Обзор отечественной литературы подтверждает, что ВСЭхоКГ при аблации ТП рассматривается как метод визуализации и анализа морфологии субстрата аблации [17]. Анализ морфологии КТП позволил выявить значительное число случаев утолщения миокарда и вариабельности евстахиева клапана, что, по данным современной литературы, расценивается как возможный фактор риска технической неуспешности и последующих рецидивов. Этот аспект вновь акцентирует актуальность индивидуализации интервенционной тактики при выполнении КА с опорой на объективные эхокардиографические параметры. Зарубежными авторами также показано достоверное уменьшение длительности рентгеноскопии при использовании ВСЭхоКГ без достоверного влияния на эффективность аблации и количество осложнений [18].
При выраженной дилатации ПП, удлиненном КТП и несоответствии радиуса кривизны катетера не формируется достаточно плотный контакт электрода и эндокарда, при этом биполярная электрограмма с дистального полюса может иметь вполне удовлетворительные для электрофизиолога характеристики, соответствующие положению катетера в области КТП. Данный феномен ранее изучался, была показана значимость контроля прижатия электрода к эндокарду при выполнении КА [19][20]. При аблации тканей сердца температура на дистальной части может повышаться, но эффективной трансмуральной деструкции тканей может не происходить за счет распределения мощности энергии между тканью сердца и окружающей циркулирующей кровью [21].
Наличие анатомических особенностей КТП, таких как значимое утолщение основания евстахиева клапана, наличие выраженной неоднородности перешейка усложняет достижение блокады проведения, несмотря на значительное повышение температуры аблируемых тканей, а длительная аблация в одной точке может привести к перфорации миокарда и развитию тампонады сердца. УЗ визуализация позволяет контролировать изменения тканей во время аблации путем оценки изменений локальной эхогенности миокарда. Для достижения эффективных воздействий в области евстахиева клапана может быть изменение направления движения катетера с каудального на краниальное в дистальной части КТП, при этом при ВСЭхоКГ визуализируется «выворачивание» ТК и прилегание катетера к венозной его части. Эффективным может быть применение нестандартных позиций катетера — максимальное сгибание перпендикулярно плоскости перешейка для аблации в углублениях КТП, выполнение которого возможно под визуальным УЗ контролем. Необходимо отслеживать, чтобы катетер последовательно прилегал к евстахиеву клапану и эндокарду в области углублений на всем протяжении линии аблации. Эти приёмы позволяют добиться появления критериев наличия блокады проведения в этой анатомически сложной области.
Необходимо также учитывать, что применение ВСЭхоКГ требует большей настороженности в отношении осложнений сосудистого доступа (постпункционных гематом, ложных аневризм, артериовенозных фистул) в связи с необходимостью использования интродьюсеров большего диаметра (8,5 и 10 Fr). Среди пациентов обеих групп осложнений в виде гемоперикарда и со стороны сосудистого доступа не наблюдалось.
Ограничения исследования. Необходимо подчеркнуть, что нерандомизированный дизайн исследования и относительно небольшое число событий накладывают известные ограничения на качество и широту экстраполяции результатов. Тем не менее предложенный подход позволяет рассматривать ВСЭхоКГ как значимый инструмент индивидуализации, повысивший информированность и управляемость процедуры. Методика имеет ограничения, связанные с необходимостью получения дополнительных навыков в УЗ визуализации и управления УЗ катетером.
Заключение
Исследование выявило, что повторная аблация КТП у пациентов с рецидивом типичного ТП под контролем ВСЭхоКГ позволяет более детально определить морфологические особенности КТП, влияющие на особенности позиционирования аблационного катетера, особенности нанесения аблационных воздействий. Использование ВСЭхоКГ достоверно снижает время рентгеноскопии, но не влияет на частоту повторных рецидивов ТП по сравнению со стандартным подходом. Представленные данные демонстрируют, что индивидуальная морфология КТП определяет сложность процедуры КА и подчеркивают целесообразность дополнительной УЗ визуализации у пациентов с рецидивом ТП.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Богачевский А.Н., Богачевская С.А., Михайлов Е.Н. Интраоперационная эхокардиографическая визуализация и ее влияние на клинические исходы повторной катетерной аблации типичного трепетания предсердий. Российский кардиологический журнал. 2025;30(4S):6675. https://doi.org/10.15829/1560-4071-2025-6675. EDN: OYQEQK
Скопировать