Высокоплотное электроанатомическое картирование при катетерной аблации нарушений ритма сердца
Аннотация
На сегодняшний день катетерные методы являются ведущим подходом к лечению нарушений ритма сердца. Актуальным направлением при проведении аблации является применение навигационного картирования, обладающего высокой точностью в локализации аритмий. Целью обзора явилось представление современных навигационных систем и катетеров, их характеристик и возможностей. Представлены результаты исследований применения высокоплотного картирования при таких нарушениях ритма сердца, как фибрилляция предсердий, желудочковая тахикардия и предсердные тахиаритмии, подтверждена эффективность подхода в реальной клинической практике.
Смена парадигмы в электрофизиологии сердца: как все начиналось
За последние два десятилетия сфера интервенционной электрофизиологии сердца претерпела революционные изменения, обусловленные, главным образом, достижениями в катетерных методах лечения нарушений ритма сердца. Одним из ведущих направлений при проведении аблации на сегодняшний день является применение навигационного картирования для элиминирования различных нарушений ритма сердца, в т.ч. фибрилляции предсердий (ФП) и желудочковой тахикардии (ЖТ) [1][2]. Традиционные методики точечного картирования, доминировавшие в этой области до начала 2000-х годов, основывались на последовательном сборе данных с помощью катетеров, оснащенных ограниченным набором электродов. Этот подход имел существенные ограничения, которые снижали эффективность процедуры и ухудшали клинические результаты. Основными проблемам являлись: высокая продолжительность процедуры (часто превышающая 4-6 ч для сложных субстратных аритмий), пространственные погрешности, возникавшие из-за артефактов дыхания и движения сердца, и критически недостаточная плотность выборки для точной характеристики сложных механизмов аритмии, особенно в случае таких субстратов, как фиброзные изменения предсердного миокарда при кардиомиопатиях или гетерогенный желудочковый рубец [3].
Внедрение систем высокоплотного электроанатомического картирования (High-Density Electroanatomic Mapping) в начале 2010-х годов стало настоящим прорывом в электрофизиологических технологиях. Эти системы позволили одновременно получать тысячи единиц данных с помощью сложных катетеров, включавших в себя от 16 до 64 электродов в различных геометрических конфигурациях. Это технологическое достижение фундаментально изменило понимание механизмов аритмий, особенно в случае персистирующей формы ФП, субстратных ЖТ и постинцизионных предсердных тахикардий [4]. Улучшенное пространственное и временное разрешение позволило выявить ранее неоцененные аспекты электрофизиологии сердца, включая контуры микро ри-энтри, локализованную роторную активность и сложную архитектуру рубцов с критическими областями проводящих каналов [5].
Современные навигационные системы высокоплотного картирования обеспечивают комплексную трехмерную электроанатомическую реконструкцию сердца с исключительными параметрами разрешения: пространственное разрешение 1-2 мм, временное разрешение <1 мс и точность локализации катетера в реальном времени 0,6-0,8 мм [6]. Этот беспрецедентный уровень детализации облегчил переход от анатомически ориентированных стратегий аблации к электрофизиологически ориентированным подходам, кардинально повлияв на показатели успеха и долгосрочные результаты по всему спектру аритмий.
Современные картирующие катетеры: принципы проектирования и клиническое применение
Многополюсный катетер PentaRay NAV оснащен 20 электродами, стратегически распределенными по пяти гибким сплайнам с оптимизированным межэлектродным расстоянием 2-6-2 мм. Такая конфигурация обеспечивает одновременный многонаправленный сбор данных из нескольких эндокардиальных участков [7]. Конструкция на основе сплайнов обеспечивает исключительную маневренность и панорамный охват, что делает ее особенно подходящей для комплексного картирования предсердий. Однако для достижения оптимальной производительности требуется тщательное манипулирование для поддержания постоянного контакта со стенками предсердия и предотвращения пролапса сплайнов в более крупных камерах сердца (рис. 1).

Рис. 1. Диагностические катетеры для высокоплотного картирования.
Примечание: сверху вниз: Orion (Boston Scientific), PentaRay (Johnson & Johnson), HD Grid (Abbott) (материалы архива лаборатории хирургических и рентгенхирургических методов лечения нарушений ритма сердца отдела сердечно-сосудистой хирургии института клинической кардиологии ФГБУ «НМИЦК им. акад. Е. И. Чазова» Минздрава России).
Катетер HD Grid имеет уникальную схему расположения электродов 4×4 с 16 индивидуально контролируемыми электродами, расположенными с интервалом 3 мм. Эта инновационная конструкция облегчает многонаправленную биполярную регистрацию сигналов, позволяя идентифицировать как поперечные, так и продольные паттерны проводимости, которые часто имеют решающее значение для анализа диастолических проводящих путей в рубцовой ткани. Уникальная модель катетера позволяет адекватно оценивать электрограмму вне зависимости от направленности фронта активации [8]. Клинические исследования продемонстрировали, что эта конфигурация обеспечивает превосходную возможность идентификации фракционированных электрограмм, поздних потенциалов и диссоциированных потенциалов в областях рубца [9][10] (рис. 1).
Катетер Mini-Basket (IntellaMap Orion, Constellation) состоит из 64 электродов, расположенных на восьми сплайнах (каждый содержит 8 электродов) с точным межэлектродным расстоянием 2,5 мм. Каждый платиноиридиевый электрод сечением 0,4 мм² поддерживает технологию оценки расстояния до эндокарда на основе импеданса, которая обеспечивает информацию о контакте в режиме реального времени без необходимости измерения силы прямого контакта. Конструкция «корзинки» позволяет безопасное манипулирование в сложных анатомических структурах, таких как ушко левого предсердия (ЛП), устья легочных вен (ЛВ) и трабекулярные поверхности желудочков [11] (рис. 1).
Навигационные системы электроанатомического картирования
Навигационная система CARTO 3 с модулем CONFIDENSE использует магнитную технологию, обеспечивая точную визуализацию катетера в полости сердца. Алгоритм «Fast Anatomical Mapping» (FAM) обеспечивает наиболее быстрое (до 2-3 мин) построение геометрии одной камеры сердца, а обработка сигналов с автоматизированной аннотацией с определением «Stable Local Activation Time» (SLAT) значительно сокращает время картирования и повышает точность. Модуль «PRIME» включает в себя новые инструменты, такие как возможность параллельного картирования, «Coherent Mapping» — для более детального анализа распространения фронта возбуждения, «Carto Finder Module» — для выявления очагов роторной активности, а также «LAT Hybrid» для более прецизионного картирования экстрасистол1.
Система EnSite X EP была представлена в США в конце 2022г в период растущего спроса на системы трехмерного картирования с использованием технологии магнитного поля. Разработка предоставляет широкий спектр вариантов аннотации электрограмм, возможность их настройки в зависимости от различных типов аритмий или субстрата. Стандарт аннотации электрограмм по времени основан на униполярных/биполярных электрограммах с использованием максимального отрицательного наклона (–dV/dT) для локального времени активации. Хотя этот метод точен при нормальном проведении импульса через здоровый миокард, в случае сложных фракционированных и низкоамплитудных электрограмм эффективность страдает. Система EnSiteX EP поддерживает возможность выбора аннотации электрограмм по началу (первое отклонение) или концу (последнее отклонение) биполярного сигнала, что повышает универсальность при картировании «самого раннего участка» аритмии или при оценке областей медленного проведения в аномальном субстрате с помощью поздних потенциалов. Технология «OT Near Field» автоматизирует точечную аннотацию сигналов путем выделения истинно локализованных потенциалов, что позволяет мгновенно дифференцировать прорывы изоляции ЛВ от сигналов far-field2.
Навигационная система RHYTHMIA HDx относится к гибридной технологии магнитного поля и импеданса [12]. При использовании данной навигационной системы возможна одновременная автоматическая аннотация по девяти критериям для каждого сердечного сокращения: стабильность длины цикла (±10 мс), стабильность катетера (смещение <3 мм), синхронизация с дыханием, стабильность электрограммы сердца и несколько фильтров качества сигнала. Вычислительная способность системы позволяет обрабатывать в режиме реального времени массивные наборы данных, превышающие 20 тыс. точек, сохраняя при этом стабильность системы и адаптивную визуализацию [13] (табл. 1).
Таблица 1
Обзор современных навигационных систем (адаптировано из [14])
|
Abbott NavX |
Biosense-Webster |
Boston Scientific |
|
|
Торговое название |
— Ensite Precision (старая версия) — Ensite X (новая версия) |
— Carto 3 — Несколько предыдущих версий |
— Rhythmia |
|
Технология навигации |
— Импеданс (Ensite Precision) или магнитное поле (Ensite X) |
— Магнитное поле |
— Гибридная технология импеданса и магнитного поля |
|
Преимущества |
— Гибкая система, открытая платформа для установки необходимых катетеров — Ensite X: локализация основана на стабильном наружном патче — Устранение артефактов, связанных с дыханием/движением |
— Точность локализации, обеспечиваемая закрытой системой (только катетеры собственной разработки) — Локализация основана на стабильном наружном патче |
— Гибкая система: может использовать фирменные (Orion) и другие катетеры — Заявленная точность маркировки сигнала, высокая достоверность даже для слабых высокочастотных сигналов |
|
Недостатки |
— Ограниченное применение при неустойчивых аритмиях — Ensite Precision: локализация зависит от стабильности референтного катетера; может потребоваться повторное построение карты при его смещении |
— Ограниченное применение при неустойчивых аритмиях — Несовместимость с катетерами других производителей — Ограниченное использование диагностических референтных катетеров |
— Ограниченное применение при неустойчивых аритмиях |
|
Обеспечение локализации |
— Ensite Precision: электрический ток частотой 8 кГц от ортогональных патчей, местоположение катетера определяется по импедансу на кончике электрода — Ensite X: магнитное поле, излучаемое патчами, воспринимаемое катетером |
— Магнитный эмиттер под столом создает слабое магнитное поле (5×10⁻⁶–5×10⁻⁵ Тл) — Шесть патчей на груди |
|
|
Точность локализации |
<1-2 мм |
<1 мм |
<2 мм |
Современные методы картирования и алгоритмы обработки сигналов
Высокоточное картирование активации: алгоритмические инновации. Современные системы высокоплотного картирования используют всё более сложные вычислительные алгоритмы для точного определения времени активации. Традиционный алгоритм (максимальное отклонение -dV/dt) остаётся стандартом для анализа биполярных сигналов, в то время как анализ униполярных электрограмм, использующий метод минимального -dV/dt или метод пикового отрицательного наклона, предоставляет важную информацию о направлении распространения фронта возбуждения. Современные системы включают в себя алгоритмы «обнаружения столкновений различных фронтов возбуждения» и «адаптивные методики подавления сигналов far-field», которые значительно повышают точность аннотации в сложных областях, таких как пограничные зоны рубцов, где множественные сигналы far-field часто усложняет анализ. Также активно используются «алгоритмы морфологической корреляции», которые сравнивают полученные электрограммы с шаблонными сигналами для выявления достоверной локальной активации на фоне шума и артефактов [14].
Оценка характеристик миокарда с помощью вольтажного картирования. В ходе исследований, посвященных высокоплотному картированию, стандартные параметры биполярных карт были тщательно проанализированы, что позволило детерминировать пороговые значения, специфичные для определенных тканей.
Для предсердного миокарда установлено пороговое значение <0,5 мВ для рубца ЛП и фиброзированной ткани. Диапазон 0,1-0,5 мВ обычно используется для обозначения «пограничной зоны», при этом здоровой тканью обычно считается диапазон >1,0-1,5 мВ. Для желудочков значение <1,5 мВ было определено как патологическое, а <0,5 мВ — как сформировавшийся рубец. Диапазон 0,2-1,5 мВ повсеместно используется для определения пограничной зоны инфаркта, критически важной для аблации субстрата ЖТ [15].
Специализированные методы картирования для сложных субстратов. Алгоритмы фазового картирования для идентификации роторов используют математические изменения, включая преобразование Гильберта или «комплексный анализ распространения фронтов возбуждения», для выявления фазовых сингулярностей и паттернов вращательной активации. Хотя клиническая польза остаётся спорной, в нескольких рандомизированных исследованиях сообщалось о 65% отсутствии рецидивов при целенаправленном воздействии на идентифицированные роторы у пациентов с персистирующей формой ФП [16][17]. К текущим ограничениям относят чувствительность к ошибкам аннотации и вычислительным артефактам в областях со сниженным потенциалом.
Картирование областей поздних потенциалов (Late Potential) и локальной аномальной желудочковой активности (Local Abnormal Ventricular Activity) является укрепившейся тактикой в лечении желудочковых нарушений ритма сердца. Существуют программные алгоритмы для сканирования полученных электрограмм и автоматической маркировки сигналов, возникающих значительно позже комплекса QRS поверхностной электрокардиограммы (например, >40-100 мс после окончания QRS) [18][19].
Отказ от рентгена — роль навигационных систем. Не менее важным аспектом при проведении интервенционных процедур является снижение лучевой нагрузки на фоне появления систем навигационного картирования. Применение подхода в сочетании с внутрисердечной эхокардиографией позволило полностью отказаться от рентгена на фоне сохраняющихся параметров эффективности процедуры аблации. Так, в регистре REAL-AF среди 2470 аблаций ФП 71,5% процедур были выполнены без использования флюороскопии под контролем внутрисердечной эхокардиографии и высокоплотного картирования. Свобода от аритмии по результатам 12 мес. наблюдения составила 81,6% [20].
В метаанализе Debreceni D, et al. сравнивалась эффективность «безрентгеновского» подхода с классической методикой катетерной аблации ФП. По результатам исследования не было получено статистически значимой разницы в отдаленной эффективности процедуры (относительный риск: 0,96, 95% доверительный интервал: 0,90-1,03; p=0,56), при этом время оперативного вмешательства оказалось ниже при нефлюороскопическом подходе в аблации ФП (p<0,01) [21].
Клинические возможности высокоплотного картирования по результатам исследований
ФП: аблация дополнительного субстрата. На сегодняшний день катетерная аблация является одним из ведущих методов лечения ФП, окончательно укрепив свои позиции за последние десятилетия. В актуальных отечественных и зарубежных клинических рекомендациях по лечению ФП катетерная аблация имеет высокий класс, в т.ч. рекомендована в качестве терапии первой линии у молодых пациентов без коморбидности при симптомной пароксизмальной форме аритмии [22]. По-прежнему не утихают споры об оптимальной стратегии аблации у пациентов с персистирующей формой ФП: достаточно ли антральной изоляции ЛВ? Результаты исследований противоречивы, единого мнения относительно данной формы аритмии нет [23-25]. Не менее дискутабельной является техника повторной аблации ФП (рис. 2).
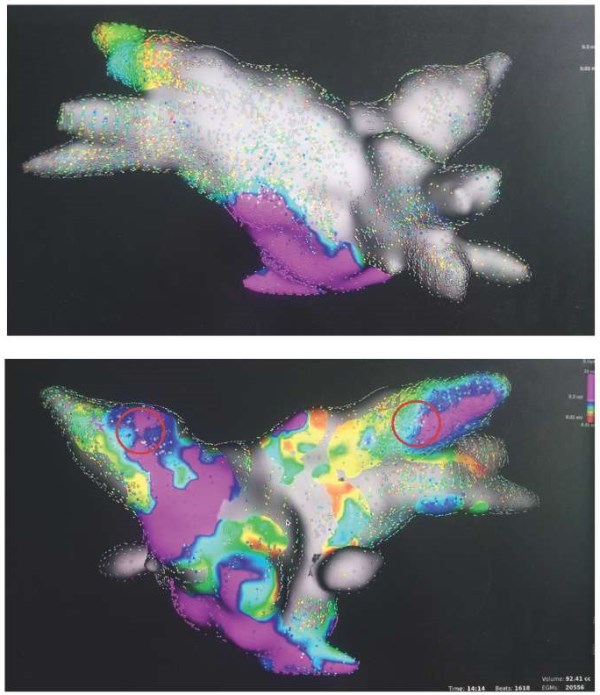
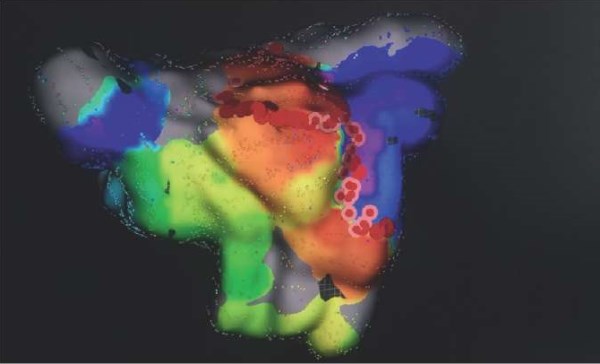
Рис. 2. Высокоплотное картирование после торакоскопической аблации ФП по технологии Cardioblate® Gemini® и повторной РЧА областей прорывов.
Примечание: воздействия в выделенных зонах привели к купированию и неиндуцируемости ФП (материалы архива лаборатории хирургических и рентгенхирургических методов лечения нарушений ритма сердца отдела сердечно-сосудистой хирургии института клинической кардиологии ФГБУ «НМИЦК им. акад. Е. И. Чазова» Минздрава России).
В регистре CHARISMA изучалось влияние дополнительной аблации низковольтных потенциалов (сниженной вольтажной активности), выявленных при помощи высокоплотного картирования, на эффективность катетерной изоляции ЛВ при ФП. Среди 58 проанализированных пациентов было обнаружено 86 прорывов в ЛВ у 34 (58,6%) больных и 44 низковольтных потенциала у 34 пациентов (58,6%). В 16 (27,6%) случаях выявлялся хотя бы один потенциал сниженной вольтажной активности у пациентов с полным отсутствием проведения по ЛВ. В раннем послеоперационном периоде успех процедуры составил 100%, все ЛВ были успешно изолированы. В течение среднего периода наблюдения (453±133 дней) у 6 пациентов (10,3%) наблюдался рецидив ФП [26].
В исследовании DECAAF II сравнивалась эффективность классической изоляции ЛВ с изоляцией ЛВ, дополненной гомогенизацией фиброзных очагов, выявленных перед операцией с помощью магнитно-резонансной томографии. При последующем наблюдении статистически значимой разницы в отсутствии рецидивов между двумя группами не наблюдалось [27].
В исследовании STABLE-SR-II (SubsTrate ABlation in the LEft Atrium during Sinus Rhythm) сравнивалась группа классической изоляции ЛВ с группой, в которой после изоляции ЛВ на синусовом ритме выполнялось высокоплотное вольтажное картирование ЛП. Зоны со сниженными вольтажными потенциалами (<0,5 мВ) обрабатывались либо «методом гомогенизации» (при неравномерном рубце), либо «методом изоляции» (при непрерывном рубце). Через 18 мес. наблюдения процент рецидивов достоверно не различался в группах STABLE-SR и CPVI (67,2% vs 67,4%; p=0,52). Лишь у половины пациентов (50,2%) в ЛП был выявлен аномальный субстрат со средним объемом в 4,6% (2,1-9,5%). Однако эффективность процедуры существенно различалась у пациентов с нормальным и аномальным субстратом ЛП (84,8% vs 60,9%; р<0,001) [28].
В исследовании Fiedler L, et al. изучалась эффективность применения электроанатомического картирования AdvisorTM HD Grid у пациентов с персистирующей формой ФП. В проспективное нерандомизированное исследование включались 344 пациента с персистирующей формой ФП. Несколько типов карт были созданы для различных ритмов с использованием HD Grid. Стратегия изолированной аблации ЛВ использовалась у 59% больных, 34,1% пациентам проводилась дополнительная аблация сниженных вольтажных потенциалов. Из них у 82% не регистрировалось рецидива предсердных аритмий в течение 12 мес. [29].
Работа Huang Y-S, et al. была посвящена эффективности аблации ФП с применением высокоплотного картирования у пациентов Азиатско-Тихоокеанского региона. 200 пациентам (n=164 — пароксизмальная форма ФП, n=36 — персистирующая форма) проводилась радиочастотная аблация (РЧА) с использованием картирующих катетеров AdvisorTM HD Grid, Sensor EnabledTM, Abbott (n=186) и InquiryTM AFocus IITM Double Loop, Abbott (n=14). Фокальные импульсы, роторы, сложные фракционированные электрограммы были найдены у <3% испытуемых. Стратегия аблации включала изоляцию ЛВ и дополнительных триггеров у 37,5% пациентов. По результатам 12 мес. наблюдения у 87,4% пациентов отсутствовали рецидивы аритмии [30].
Одним из наиболее перспективных и многообещающих методов лечения ФП на сегодняшний день признана электропорация — уникальный подход, позволяющий с высокой точностью и скоростью элиминировать аритмогенный субстрат аритмии. В современной литературе отмечается экспоненциальный рост публикаций по теме и обсуждаются концепции лечения.
Работа Mills M, et al. была посвящена изучению достижения полной изоляции ЛВ при проведении электропорации. 535 пациентам с ФП (из них n=375 — с пароксизмальной формой) после процедуры электропорации осуществлялось электроанатомическое картирование для оценки прорывов ЛВ. По результатам работы наличие прорыва как минимум одной ЛВ наблюдалось у четверти пациентов после стандартной процедуры электропорации (полная изоляция 1834 из 1978 ЛВ). Наиболее часто прорывы были выявлены в области верхних ЛВ [31].
ЖТ: прецизионная модификация субстрата. До появления высокоплотного картирования ключевым подходом к лечению ЖТ считалась антиаритмическая терапия, катетерная аблация же не являлась ведущим методом лечения аритмии. Ключевым прорывом стала концепция картирования субстрата при стабильном ритме (синусовом или стимулированном). Поскольку катетерная аблация становится терапией первой линии, основной задачей является разработка системного подхода к клинической оценке, картированию и аблации ЖТ. Принципиальными «мишенями» аблации ЖТ являются: устранение или снижение «бремени» аритмии, обеспечение безопасности пациента и ограничение сопутствующего повреждения для улучшения долгосрочных результатов [32][33].
В исследовании VISTA (Ablation of Stable VTs Versus Substrate Ablation in Ischemic Cardiomyopathy) сравнивались эффективность аблации ЖТ у пациентов с ишемической кардиомиопатией и гемодинамически переносимой ЖТ в группе картирования и аблации «клинической» тахикардии и в группе субстратной аблации, нацеленной на все «аномальные» электрограммы в рубцовой области. После периода наблюдения в 12 мес. рецидив ЖТ наблюдался у 9 (15,5%) и 29 (48,3%) пациентов в группах РЧА субстрата и РЧА клинической ЖТ, соответственно (p<0,001) [34].
Работа Schleberger R, et al. была посвящена сравнению аблации ЖТ с применением катетеров высокоплотного картирования и стандартной методики «point by point» при помощи 3D навигации. Проведение процедуры с использованием высокоплотного картирования сопровождалось статистически значимым снижением частоты развития рецидивов аритмии и смертности (р=0,048) [35].
В исследовании Balt JC, et al. изучалась эффективность РЧА ЖТ с использованием высокоплотного электроанатомического картирования у пациентов с ишемической кардиомиопатией. Безрецидивная выживаемость через 1 год, 2 года и 5 лет составила 65%, 49% и 40%, соответственно. При этом отсутствие шоковой терапии кардиовертера-дефибриллятора наблюдалось среди 90% через 1 год, 81% через 2 года и 70% через 5 лет [36].
Результаты исследований демонстрируют несколько эффективных методик аблации субстрата с разными мишенями и конечными точками, в т.ч. применяются линейные воздействия внутри рубцовой зоны под контролем стимуляционного картирования, аблация областей поздних потенциалов или локальной аномальной желудочковой активности, гомогенизация рубца, а также изоляция аритмогенного субстрата ЖТ. Следует отметить, что объективное определение конечной точки операции представляет собой серьезную проблему при аблации ЖТ. Невоспроизводимость аритмии в ответ на программную стимуляцию — классическая процедурная конечная точка, и несмотря на ряд ограничений, она остается золотым стандартом (рис. 3).

Рис. 3. Трехмерная электроанатомическая и вольтажная карты левого желудочка.
Примечание: красным выделена зона сниженного потенциала. Черными точками отмечены области фракционированных потенциалов. Выполнены РЧА-воздействия (розовые шарики), в дальнейшем тахикардия не воспроизводима (материалы архива лаборатории хирургических и рентгенхирургических методов лечения нарушений ритма сердца отдела сердечно-сосудистой хирургии института клинической кардиологии ФГБУ «НМИЦК им. акад. Е. И. Чазова» Минздрава России).
Сложные предсердные тахикардии: подход, основанный на механизме конкретной аритмии
Многочисленные сравнительные когортные исследования и перспективные регистры последовательно продемонстрировали, что системы высокоплотного электроанатомического картирования значительно повышают показатели успеха, сокращают время процедуры и использование рентгеноскопии, а также снижают риск рецидивов в долгосрочной перспективе по сравнению с традиционными подходами, требующими длительной рентгеноскопии и использования маневра «entrainment» для аблации сложных предсердных тахикардий (рис. 4).
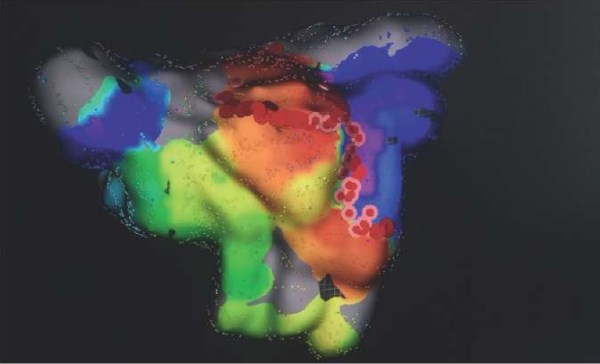
Рис. 4. Высокоплотное картирование после криоаблации ФП и изоляции каво-трикуспидального перешейка.
Примечание: наблюдается перимитральное АТП. Линейная изоляция переднего истмуса привела к купированию и неиндуцируемости тахикардии (материалы архива лаборатории хирургических и рентгенхирургических методов лечения нарушений ритма сердца отдела сердечно-сосудистой хирургии института клинической кардиологии ФГБУ «НМИЦК им. акад. Е. И. Чазова» Минздрава России).
В исследовании Raymond-Paquin A, et al. 62 пациента перенесли высокоплотное картирование и аблацию атипичного трепетания предсердий (АТП). У 53 (85%) пациентов ранее была проведена аблация ФП/АТП. 44 (46%) фронта распространения АТП были классифицированы как «обычные», а 51 (54%) — как «оригинальные». «Обычные» АТП имели более длинные критические перешейки (19,0±9,0 vs 10,8±6,3 мм, p<0,001), более редкую распространенность замедленного проведения в критическом перешейке (59% vs 86%, p=0,005) и более длительное время аблации до купирования тахикардии (117±119 vs 51±66 с, p=0,002). Попытки проведения манёвра «entrainment» были предприняты в 19 случаях (20%) в основном в начальном периоде исследования и никак не влияли на эффективность процедуры. Отсутствие рецидивов предсердной тахикардии составило 65% за период наблюдения 13,8±9,0 мес. [37].
Заключение
Высокоплотное электроанатомическое картирование на сегодняшний день является одной из ведущих технологий при проведении катетерной аблации, позволяя сократить общую продолжительность процедуры, использование флюороскопии и, что наиболее важно, снизить риск рецидива аритмии на 25-40% при различных сложных субстратах.
Эта технология способствовала принципиальному переходу от анатомически опосредованных подходов к аблации к персонализированным стратегиям модификации субстрата, что позволило изменить стратегию в лечении сложных наджелудочковых и ЖТ. Возможность точного анализа аритмогенного субстрата привела к созданию новых терапевтических парадигм, направленных на устранение специфических патологических свойств тканей, а не на создание анатомических линий блока.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Bench testing performed by Biosense Webster, Inc. CARTO® 3 V7 CARTOFINDER Algorithm POD. 2019.
2. Santangeli P. Ensite™ X EP System Technology Overview — Understanding the Market. JAFIB EP Abbott special issue. 2023; 16(5).
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Сапельников О.В., Ардус Д.Ф., Куликов А.А., Черкашин Д.И., Ширяев А.А. Высокоплотное электроанатомическое картирование при катетерной аблации нарушений ритма сердца (обзор). Российский кардиологический журнал. 2025;30(4S):6735. https://doi.org/10.15829/1560-4071-2025-6735. EDN: KLLTKT
Скопировать