Тромболитическая терапия в сравнении с нефракционированным гепарином в лечении гемодинамически стабильных пациентов с тромбоэмболией легочной артерии: систематический обзор и метаанализ
Аннотация
В настоящее время проведение тромболитической терапии (ТЛТ) при тромбоэмболии легочной артерии (ТЭЛА) рекомендуется только пациентам высокого риска. Вместе с тем в реальной практике врачи часто проводят ТЛТ у гемодинамически стабильных пациентов. При этом основное противоречие возникает из-за различных соотношений риска и пользы проведения ТЛТ в сравнении с монотерапией антикоагулянтами.
Цель. Оценить преимущества проведения ТЛТ по сравнению с монотерапией нефракционированным гепарином (НФГ) у гемодинамически стабильных пациентов с ТЭЛА в снижении смертности, рецидивов и риска кровотечений.
Материал и методы. Поиск рандомизированных контролируемых исследований проводился в базах данных PubMed, Embase, Cochrane Library. Из найденных 3050 публикаций для детального исследования было отобрано 100 статей, в результате проведения их подробного анализа в итоге по установленным первоначально критериям осталось 7 рандомизированных клинических исследований, в которых принимало участие 1611 пациентов.
Результаты. Проведение ТЛТ у пациентов с ТЭЛА и стабильной гемодинамикой, в сравнении с НФГ, показало тенденцию к снижению частоты госпитальной смерти: 2,39% vs 3,68% (отношение шансов (ОШ): 0,73; 95% доверительный интервал (ДИ): 0,34-1,57) и снижению комбинированной конечной точки — смерть и/или рецидив ТЭЛА: 3,14% vs 5,15% (ОШ: 0,61; ДИ: 0,37-1,01). При этом отмечалось статистически значимое увеличение количества больших кровотечений: 8,81% vs 2,70% (ОШ: 3,35; 95% ДИ: 2,06-5,45). Введение тромболитического препарата у пациентов с ТЭЛА и стабильной гемодинамикой позволяет снизить уровень давления в легочной артерии, уменьшить дефекты перфузии по данным сцинтиграфии легких, потребность в эскалации терапии в большей степени, чем монотерапия НФГ. Однако неоднородность исследований и небольшое число участников требуют осторожности при интерпретации результатов подобных публикаций.
Заключение. Проведение ТЛТ у пациентов с ТЭЛА и стабильной гемодинамикой имеет тенденцию к снижению смертности и/или частоты рецидивов ТЭЛА, но увеличивает частоту больших кровотечений. В дальнейших исследованиях необходимо определить фенотипы пациентов с ТЭЛА со стабильной гемодинамикой, которые выиграют от проведения ТЛТ.
В настоящее время проведение тромболитической терапии (ТЛТ) при тромбоэмболии легочной артерии (ТЭЛА) рекомендуется только пациентам с ТЭЛА высокого риска (уровень доказанности IA), т.к. госпитальная летальность у этой категории пациентов может превышать 40% [1]. Целесообразность ТЛТ у пациентов с ТЭЛА, имеющих стабильную гемодинамику при поступлении в стационар, обсуждается в течение последних трех десятилетий. Пациенты данной группы имеют существенно меньший риск смерти в стационаре [2]. При этом основное противоречие возникает из-за различных соотношений риска и пользы проведения тромболизиса в сравнении с монотерапией антикоагулянтами в рандомизированных контролируемых исследованиях (РКИ) [1].
Цель проведения метаанализа — оценка преимуществ в снижении смертности, рецидивов ТЭЛА и риска кровотечений, связанных с проведением ТЛТ, по сравнению с монотерапией антикоагулянтами у гемодинамически стабильных пациентов с ТЭЛА.
Материал и методы
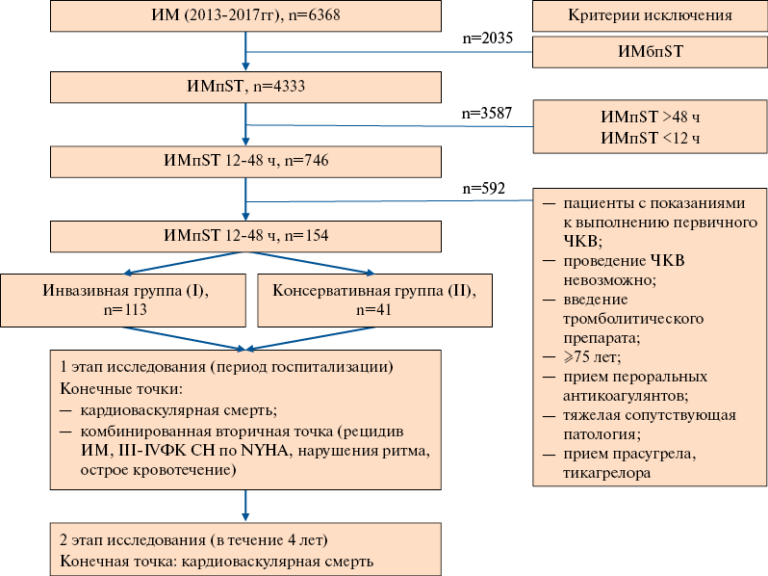
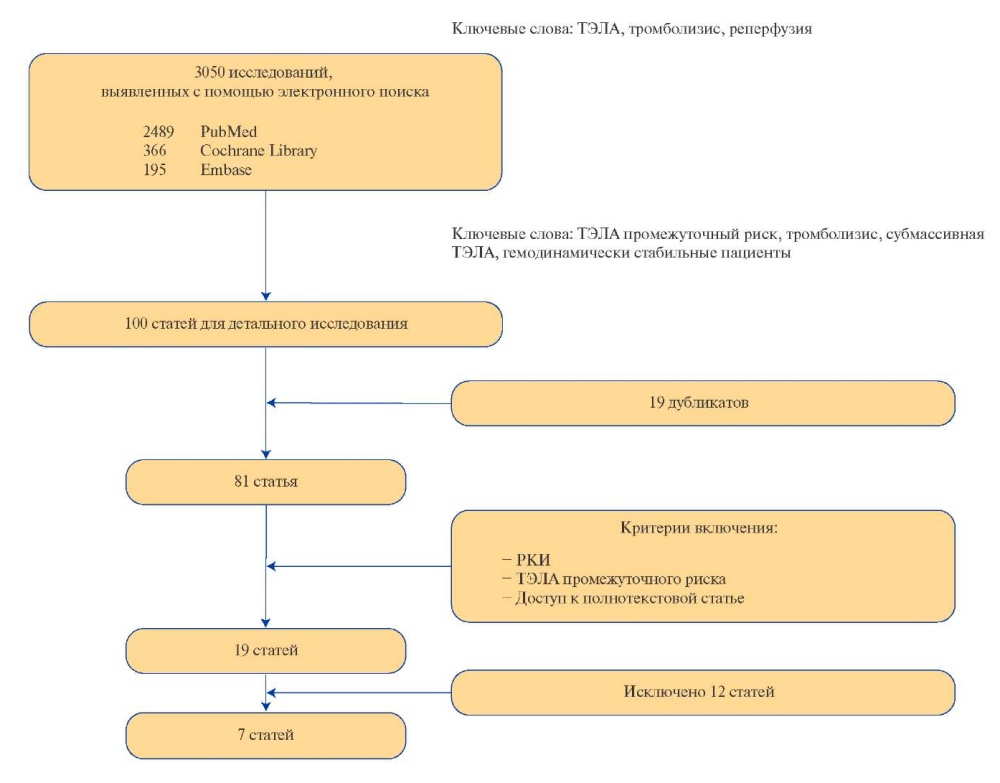
Поиск публикаций и отбор исследований. На первом этапе работы был выполнен поиск релевантных источников в нескольких электронных базах данных, включая PubMed, Embase, Cochrane Library за период с 01.01.1970 по 31.12.2021 (последнее обращение). Поисковыми терминами служили — thrombolysis, thrombolytic therapy, pulmonary embolism, reperfusion, PE intermediate risk, hemodynamically stable РЕ, submassive PE. Язык публикаций — английский. Алгоритм поиска информации был разработан в соответствии с требованиями и положениями отчетности для систематических обзоров и метаанализов (PRISMA) [3]. Тезисы докладов, протоколы заседаний, монографии, клинические случаи и серии случаев в анализ не включались. Процесс отбора исследований представлен на рисунке 1.

Рис. 1. Процесс отбора исследований, включенных в метаанализ.
Сокращения: РКИ — рандомизированное контролируемое исследование, ТЭЛА — тромбоэмболия легочной артерии.
Критерии включения/исключения. В анализ включались РКИ, если они отвечали следующим критериям: а) ТЭЛА со стабильной гемодинамикой/промежуточным риском при поступлении; б) проведение системного тромболизиса; в) использование нефракционированного гепарина (НФГ) в качестве антикоагулянта сравнения; г) возраст 18 лет и старше.
При первичном отборе с использованием вышеописанных поисковых запросов было получено 2489 публикаций c помощью PubMed, 366 публикаций — Сochrane Library, 195 публикаций из Embase.
Из анализа исключались исследования, в которых участвовали пациенты с ТЭЛА высокого риска/гемодинамически нестабильные, или использовались катетерные методики введения тромболитических препаратов, или сравнивались два различных тромболитических агента, или оценивались разные дозы одного и того же препарата, или использовались низкомолекулярные гепарины.
Из найденных 3050 публикаций для детального исследования было отобрано 100 статей. Следует подчеркнуть, что количество включенных в исследования пациентов не являлось определяющим фактором отбора. Также необходим был доступ к полнотекстовой версии статьи.
После анализа заголовков и их аннотаций было определено, что поставленной цели отвечала 81 статья, затем были исключены 19 повторяющихся публикаций. После оценки полнотекстовых копий для анализа осталось 19 публикаций, посвященных РКИ с использованием системной ТЛТ при ТЭЛА. В дальнейшем из их числа было исключено 8 публикаций, включающих пациентов с ТЭЛА высокого риска [4-11], два исследования с использованием 50% дозы ТЛТ [12][13], одно, где в качестве антикоагулянта использовались низкомолекулярные гепарины [14], одно, где сравнивались разные способы введения тромболитического препарата [15]. В итоге для анализа по установленным первоначально критериям осталось 7 публикаций.
Сбор и анализ данных. В работе использовался адаптированный и валидизированный вопросник для оценки риска систематических ошибок в РКИ [16]. Риск систематических ошибок оценивался как низкий (1 балл), высокий (2 балла) и неопределенный (0 баллов). Мы оценивали эффективность и безопасность вмешательства (ТЛТ по сравнению терапией НФГ), используя отношение шансов (ОШ) с 95% доверительным интервалом (ДИ). Расчеты были основаны на модели случайных эффектов при I2 >40%, P<0,10 и на модели фиксированных эффектов при I2 ?40%, Р?0,10. Основными исходами, представляющими интерес, были смерть в течение госпитализации, крупные кровотечения, комбинированная конечная точка (смерть в течение госпитализации от всех причин и/или рецидив ТЭЛА). Анализ был выполнен с использованием Review Manager (RevMan) версии 5.4.
Результаты
Основные характеристики РКИ, отвечающие критериям включения, представлены в таблице 1, риск предвзятости исследований, включенных в метаанализ, приведен в таблице 2.
Таблица 1
Характеристика исследований, включенных в систематический обзор

Сокращения: нд — нет данных, НФГ — нефракционированный гепарин, ПЖ — правых желудочек, рТАП — рекомбинантный тканевой активатор плазминогена, ТЭЛА — тромбоэмболия легочной артерии, ЭхоКГ — эхокардиография.
Таблица 2
Домены возникновения систематических ошибок

Последнее РКИ, выполненное у данной группы пациентов, датируется 2014г, а проведенные позже РКИ либо включали половинную дозу тромболитического препарата [13], либо низкомолекулярные гепарины в качестве антикоагулянта сравнения [14], либо анализировали катетерное введение тромболитических препаратов непосредственно в легочную артерию [17-20].
Общее количество пациентов, включенных в наш метаанализ, составило 1611 человек. Количество центров в РКИ варьировало от 3 до 76. В качестве тромболитического препарата в 4 исследованиях использовался рекомбинантный тканевой активатор плазминогена (рТАП), в 3 — тенектеплаза. Все РКИ, кроме исследования Meyer G, et al. [21], включали небольшое количество пациентов, поэтому смертность входила в состав комбинированной конечной точки.
В результате выполненного метаанализа оказалось, что проведение ТЛТ у пациентов с ТЭЛА и стабильной гемодинамикой имело тенденцию к снижению частоты госпитальной смерти (рис. 2): 2,39% vs 3,68% (ОШ: 0,73; 95% ДИ: 0,34-1,57) и снижению комбинированной конечной точки — смерть и/или рецидив ТЭЛА (рис. 3): 3,14% vs 5,15% (ОШ: 0,61; ДИ: 0,37-1,01). При этом отмечалось статистически значимое увеличение количества больших кровотечений (рис. 4): 8,81% vs 2,70% (ОШ: 3,35; 95% ДИ: 2,06-5,45).

Рис. 2. Госпитальная летальность.

Рис. 3. Госпитальная летальность и/или рецидив ТЭЛА.

Рис. 4. Большие кровотечения.
Ранее было показано, что введение тромболитического препарата позволяет снизить уровень давления в легочной артерии по данным эхокардиографии [22-24] и ангиопульмонографии [25], уменьшить дефекты перфузии по данным сцинтиграфии легких [22] и ангиопульмонографии [25], потребность в эскалации терапии [21][26] в большей степени, чем монотерапия НФГ. Однако неоднородность исследований и небольшое число участников требуют осторожности при интерпретации результатов подобных публикаций.
Так, в исследовании Dalla-Volta С, et al. [25] степень легочной обструкции по шкале Миллера по данным ангиографии легочной артерии значительно снизилась у пациентов, получавших рТАП с 28,3±2,9 мм рт.ст. до 24,8±5,2 мм рт.ст. (p<0,01), тогда как в группе НФГ достоверной динамики выявлено не было. Среднее легочное давление снизилось с 30,2±7,8 мм рт.ст. до 21,4±6,7 мм рт.ст. в группе рТАП и даже увеличилось в группе НФГ: с 22,3±10,5 до 24,8±11,2 мм рт.ст. (p<0,01).
В исследовании Goldhaber SZ, et al. [22] в группе ТЛТ отмечалось улучшение экскурсии стенки правого желудочка (ПЖ) через 24 ч по сравнению с исходным уровнем у 39% пациентов (16 пациентов), ухудшение — у 2% (1 пациент). Аналогичные показатели в группе НФГ составили — 17% (8 человек) и 17% (8 человек), соответственно (р=0,005). У пациентов, получивших рТАП, зафиксировано значительное улучшение легочной перфузии. Объем неперфузируемых участков легких снизился на 14,6% (с 42,9% до 28,3%) по сравнении со снижением на 1,5% с группе пациентов, получавших НФГ (с 36,0% до 34,5%, p<0,0001).
Частота первичной конечной точки (госпитальная смерть или эскалация лечения) в исследовании Konstantinides S, et al. [26] была значительно выше в группе НФГ плюс плацебо, чем в группе НФГ плюс альтеплаза (24,6% (34 пациента) vs 11,0% пациентов (13 пациентов), р=0,006). Под эскалацией лечения подразумевали необходимость инфузии инотропных препаратов из-за стойкой артериальной гипотензии или шока; повторный или «спасительный» тромболизис; эндотрахеальная интубация; сердечно-легочная реанимация; и экстренная хирургическая эмболэктомия или катетерная тромбэктомия. Вероятность 30-дневной выживаемости (согласно анализу КапланМейера) была выше в группе НФГ+альтеплаза (р=0,005). Это различие было связано с более высокой частотой эскалации лечения в группе НФГ+плацебо (24,6% vs 10,2%, р=0,004), поскольку госпитальная смертность была низкой в обеих группах (3,4% в группе ТЛТ и 2,2% в группе НФГ+плацебо, р=0,71).
В исследовании, выполненном Becattini C, et al. [23], было показано, что уменьшение соотношения конечно-диастолического размера ПЖ к левому желудочку через 24 ч в группе ТЛТ составило 0,31±0,08, а в группе плацебо 0,10±0,07 (p=0,04).
Применение ТЛТ в исследовании Fasullo MD, et al. [24] сопровождалось ранним уменьшением размера ПЖ (через 48 ч в группе НФГ с 48±2,3 мм до 39±1,2 мм, в группе ТЛТ — с 49±2,4 мм до 35±1,2 мм, р=0,0001; через 3 мес. в группе НФГ — 27±1,3 мм, в группе ТЛТ — 23±0,6 мм, р=0,001) и более благоприятной тенденцей в клинических исходах. Также в группе ТЛТ наблюдалось более выраженное снижение систолического давления в легочной артерии (с 57±18 мм до 38±7 мм через 48 ч и 12±3 мм через 6 мес., р<0,001), чем в группе НФГ (с 58±19 мм до 47±11 мм через 48 ч и 18±2 через 6 мес.).
Нарушения гемодинамики или острая сердечная недостаточность развилась у 1,6% пациентов при применении ТЛТ и у 5% в группе НФГ (p=0,002) по данным, полученным Meyer G, et al. [21].
В исследовании Klinе JA, et al. [27] в течение 90 дней наблюдения у 37% пациентов, получавших плацебо+НФГ, и у 15% пациентов с проведенным ТЛТ+НФГ наблюдался как минимум один неблагоприятный исход: смерть, интубация, смертельное внутричерепное кровоизлияние (р=0,017).
Обсуждение
В результате проведенного метаанализа оказалось, что выполнение ТЛТ у пациентов с ТЭЛА со стабильной гемодинамикой недостоверно снижает смертность и/или частоту рецидивов ТЭЛА, но статистически значимо увеличивает частоту развития кровотечений. Следует отдельно отметить, что эти данные были получены на исследованиях, включавших небольшое количество пациентов, и авторам требовалось прибегать к созданию комбинированных конечных точек, чтобы оценить пользу/риск вмешательств в обеих группах [22-27].
Фактически единственным РКИ, включившем >1 тыс. пациентов промежуточного-высокого риска ТЭЛА, было Pulmonary Embolism Thrombolysis (PEITHO) [21]. В исследовании PEITHO преимущества ТЛТ препаратом тенектеплаза (ОШ 0,44; 95% ДИ 0,23-0,87) были нивелированы значительным ростом числа крупных кровотечений (6,3% в группе ТЛТ vs 1,5% в группе без ТЛТ). Это исследование явилось знаковым, после которого в рекомендациях Европейского общества кардиологов 2019г [1] место реперфузионной терапии при ТЭЛА промежуточного риска было определено только как «спасительной» процедуры для пациентов с ухудшением гемодинамики на фоне антикоагулянтной терапии. Проведенные РКИ [22-25] подтвердили важную роль ТЛТ в способности уменьшать дисфункцию ПЖ при ТЭЛА промежуточного риска.
Очевидно, что ТЛТ — это не метод лечения всех пациентов с ТЭЛА промежуточного риска. И необходимо сосредоточиться на поиске предикторов ухудшения гемодинамики, не дожидаясь развития у пациента обструктивного шока, используя способность ТЛТ быстро уменьшать нагрузку на ПЖ. Так, в рекомендациях Американского колледжа торакальных врачей 2021г [28] изложена позиция о начале применения системной ТЛТ у пациентов с ТЭЛА с приемлемым риском кровотечения, состояние которых ухудшается после начала антикоагулянтной терапии, не дожидаясь развития шока или гипотензии (слабая рекомендация, доказательства с низкой степенью достоверности). Предлагается таким пациентам проводить антикоагулянтную терапию и контролировать признаки клинического ухудшения (снижение систолического артериального давления, увеличение частоты сердечных сокращений, ухудшение газообмена, признаки недостаточной перфузии, ухудшение функции ПЖ или повышение сердечных биомаркеров).
Аналогичные выводы были получены в ранее выполненных метаанализах [29-34]. Так, в 2009г Tardy B, et al. в метаанализе, включившем 5 РКИ [29], сравнили применение рТАП vs монотерапии НФГ у 464 гемодинамически стабильных пациентов с острой ТЭЛА. Объединенная оценка всех событий выявила статистически незначимое снижение смертности, связанной с ТЭЛА или рецидивом ТЭЛА при рТАП, по сравнению с НФГ (3,5% vs 4,6%, p=0,73). Также в группе рТАП в сравнении с НФГ не наблюдалось значительного увеличения крупных кровотечений (4,9% vs 4,6%, отношение рисков (ОР): 0,94; 95% ДИ: 0,39-2,27). Аналогичные результаты были получены, когда рассматривались только исследования, включавшие пациентов с эхокардиографическими признаками дисфункции ПЖ. Не отмечалось снижения ни смертности вследствие ТЭЛА, ни частоты рецидивов ТЭЛА на фоне введения рТАП по сравнению с НФГ у пациентов со стабильной гемодинамикой.
В 2014г было выполнено сразу 4 метаанализа по оценке эффективности ТЛТ в терапии гемодинамически стабильных пациентов с ТЭЛА [30-33].
Chen H, et al. [30] включили в метаанализ 15 РКИ (всего 1247 пациентов), где НФГ сравнивался с различными тромболитическими препаратами (урокиназа/альтеплаза/тенектеплаза). Проведение ТЛТ было связано со значительным снижением частоты рецидивов ТЭЛА или смерти (1,94% vs 5,87%, ОШ: 0,37; 95% ДИ: 0,21-0,66; без статистически значимой гетерогенности между исследованиями, P=0,49), при недостоверном увеличении количества больших кровотечений (3,57% vs 2,67%, ОШ: 1,34; 95% ДИ: 0,70-2,58), но значительным небольших кровотечений (12,78% vs 3,65%, ОШ: 4,12; 95% ДИ: 2,37-7,17). Однако, в отличие от нашего исследования, в данный метаанализ были также включены исследования с ТЭЛА высокого риска и 50% дозой тромболитического препарата. Liu Y, et al. [31] в метаанализе на основе 7 РКИ сравнивали рТАП с монотерапией НФГ (n=594 пациента). Применение рТАП ассоциировалось с незначительным снижением смертности (2,75% vs 3,96%, р=0,520); рецидивов ТЭЛА (2,13% vs 3,34%, ОР: 0,70; 95% ДИ: 0,28-1,73); незначительным (недостоверным) увеличением больших кровотечений (5,15% vs 4,29%, ОР: 1,06; 95% ДИ: 0,520-2,150). Аналогичные результаты были получены при анализе подгруппы пациентов с эхокардиографическими признаками дисфункции ПЖ. Напротив, использование рТАП по сравнению с НФГ было связано со значительным снижением в необходимости эскалации терапии в исследованиях, в которые также включались пациенты с дисфункцией ПЖ (6,56% vs 19,7%; ОР: 0,34; 95% ДИ: 0,20-0,65). В метаанализе был сделан вывод о том, что нет данных, свидетельствующих о преимуществе применения рТАП по сравнению с НФГ для стартового лечения абсолютно всех гемодинамически стабильных пациентов, перенесших острую ТЭЛА, но рТАП может быть полезен в лечении пациентов с дисфункцией ПЖ.
В метаанализе Marti К, et al. [32] (2057 пациентов, 15 РКИ) был сделан вывод, что по сравнению с НФГ проведение ТЛТ было связано с достоверным снижением общей смертности (OШ: 0,59; 95% ДИ: 0,360,96). Однако это снижение оказалось статистически незначимым после исключения из пула исследований пациентов с ТЭЛА высокого риска (OШ: 0,64; 95% ДИ: 0,35-1,17). Тромболизис был связан со значительным снижением комбинированной конечной точки смерти и/или эскалации терапии (OШ: 0,34, 95% ДИ: 0,22-0,53), смертностью, связанной с ТЭЛА (OШ: 0,29; 95% ДИ: 0,14-0,60) и рецидивом ТЭЛА (OШ: 0,50; 95% ДИ: 0,27-0,94). Большое кровотечение (OШ: 2,91; 95% ДИ: 1,95-4,36) и летальное или внутричерепное кровотечение (OШ: 3,18; 95% ДИ: 1,25-8,11) были значительно более частыми среди пациентов, получавших ТЛТ.
В метаанализе Nakamura S, et al. [33] было включено 1510 пациентов. Не было выявлено существенных различий в комбинированной конечной точке смерти от всех причин и/или рецидива ТЭЛА между группой ТЛТ и группой, получавшей только НФГ (3,1% vs 5,4%; ОР: 0,64; ДИ: 0,32-1,28). ТЛТ значительно снизила частоту комбинированной конечной точки смерти от всех причин или клинического ухудшения (3,9% vs 9,4%; ОР: 0,44; ДИ: 0,29-0,67). Не было статистически значимых различий в возникновении больших кровотечений при сравнении ТЛТ с монотерапией НФГ (6,6% vs 1,9%; ОР: 0,44; 95% ДИ: 0,58-7,35). Этот метаанализ также показал, что реперфузионная терапия существенно не снижает риск смертности или рецидива ТЭЛА у пациентов с острой субмассивной ТЭЛА, но ТЛТ предотвращает клиническое ухудшение, требующее эскалации лечения у пациентов с острой субмассивной ТЭЛА. Оценка риска кровотечения может быть наиболее успешным подходом для улучшения клинических результатов и пользы для конкретного пациента от применения ТЛТ.
Последний, наиболее крупный метаанализ Zuo Z, et al. [34], опубликованный в 2021г, включает 21 исследование, совокупно 2401 пациент, в т.ч. лица с массивной ТЭЛА и хирургическими вмешательствами. Авторами были сделаны выводы, что ТЛТ может снизить риск смерти после острой ТЭЛА по сравнению с НФГ (ОШ: 0,58; 95% ДИ: 0,38-0,88), однако эффективность её была в основном обусловлена исследованиями, проведенными у пациентов ТЭЛА высокого риска. Показано, что ТЛТ может быть полезна для уменьшения рецидива легочной эмболии (ОШ: 0,54; 95% ДИ: 0,32-0,91), но может вызвать большие (OШ: 2,84; 95% ДИ: 1,92-4,20) и малые геморрагические события (OШ: 2,97; 95% ДИ: 1,665,30), включая геморрагический инсульт (OШ: 7,59; 95% ДИ: 1,38-41,72). Авторы делают в статье акцент на том, что эти доказательства характеризуются низкой степенью достоверности из-за высокого риска предвзятости РКИ, включенных в анализ.
Таким образом, в настоящее время доказаны преимущества ТЛТ в снижении госпитальной летальности и рецидивов ТЭЛА в сравнении с риском кровотечений у пациентов с ТЭЛА высокого риска, и эту закономерность четко видно даже на исследованиях с небольшим количеством пациентов [4-11]. У пациентов с ТЭЛА со стабильной гемодинамикой не все так однозначно. На наш взгляд, применение ТЛТ оправдано у узкого круга пациентов с невысоким риском кровотечений и критериями начинающего ухудшения гемодинамики с целью своевременной разгрузки малого круга кровообращения, не дожидаясь развития обструктивного шока. Целесообразно проведение спланированного РКИ с четким дизайном и узкими критериями включения у пациентов с ТЭЛА промежуточно-высокого риска для подтверждения этой гипотезы.
Ограничения исследования. В данный метаанализ не были включены исследования, где в качестве антикоагулянтной терапии использовались низкомолекулярные гепарины или прямые оральные антикоагулянты.
Заключение
Выполненный нами метаанализ показал, что проведение ТЛТ у пациентов с ТЭЛА и стабильной гемодинамикой имеет тенденцию к снижению смертности и/или частоты рецидивов ТЭЛА, но увеличивает частоту больших кровотечений. Системное введение тромболитических препаратов приводит к более быстрому лизису тромба, чем монотерапия НФГ, тем самым снижая давление в легочной артерии, улучшая функцию ПЖ и легочную гемодинамику. В дальнейших исследованиях необходимо определить фенотипы пациентов с ТЭЛА со стабильной гемодинамикой, которые выиграют от проведения ТЛТ.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Черепанова Н.А., Подлипаева А.А., Андреева Е.С., Умярова Э.Н., Муллова И.С., Павлова Т.В., Дупляков Д.В. Тромболитическая терапия в сравнении с нефракционированным гепарином в лечении гемодинамически стабильных пациентов с тромбоэмболией легочной артерии: систематический обзор и метаанализ. Российский кардиологический журнал. 2022;27(3S):5120. https://doi.org/10.15829/1560-4071-2022-5120
Скопировать