Тактика кардиоверсии при фибрилляции и трепетании предсердий
Аннотация
В лечении пациентов с фибрилляцией (ФП) и трепетанием предсердий (ТП) наилучшие результаты достигаются при использовании комплексного подхода, способствующего выбору оптимальной для каждого конкретного пациента тактики ведения на основании действующих клинических рекомендаций. Кардиоверсия является важнейшей составной частью стратегии «контроля ритма», нацеленной как на обеспечение контроля над симптомами заболевания, так и на улучшение прогноза пациентов. Выбор оптимального способа восстановления синусового ритма, правильная подготовка пациента, в т.ч. применение антикоагулянтной терапии и правильное проведение всех этапов процедуры имеют принципиальное значение для эффективного и безопасного достижения результата. В статье рассмотрены способы купирования ФП и ТП, представлены рекомендации по тактике восстановления синусового ритма и антикоагулянтному сопровождению кардиоверсии в различных клинических ситуациях.
В лечении пациентов с фибрилляцией предсердий (ФП) наилучшие результаты достигаются при использовании комплексного подхода, способствующего выбору оптимальной для каждого конкретного пациента тактики ведения на основании действующих клинических рекомендаций. Ключевое звено при данном подходе занимает контроль симптомов заболевания. При ФП для достижения контроля над клиническими проявлениями аритмии применяют две основные стратегии: «контроль частоты сердечных сокращений (ЧСС)» или «контроль ритма». Стратегия контроля ритма направлена не только на восстановление синусового ритма (СР), но и на его длительное удержание.
Восстановление СР посредством электрической (ЭКВ) или медикаментозной кардиоверсии (МКВ) показано при выраженных клинических симптомах и субъективно плохой переносимости аритмии, в случаях недостижения целевых значений ЧСС (при выборе «стратегии контроля ЧСС»), а также в ситуациях, когда достигнутый целевой уровень частоты желудочковых сокращений не приводит к улучшению общего состояния пациента [1].
Экстренная ЭКВ проводится по жизненным показаниям в случаях неконтролируемой тахисистолии с развитием сердечной (СН) и/или коронарной недостаточности, а также при сохранении этих проявлений, несмотря на достижение адекватного снижения частоты желудочковых сокращений [2].
У больных с пароксизмальной формой ФП всегда присутствует вероятность спонтанного купирования аритмии, поэтому пациентам с недавно возникшими пароксизмами, при отсутствии гемодинамической нестабильности, применение урежающих ЧСС препаратов способствует улучшению состояния и нередко позволяет избежать необходимости МКВ или ЭКВ [3]. Нарушение электролитного баланса является фактором провоцирующим развитие ФП, поэтому на данном этапе может быть целесообразным внутривенное введение препаратов калия при отсутствии противопоказаний. Эпизоды трепетания предсердий (ТП) менее склонны к самостоятельному купированию и, как правило, имеют более выраженные клинические проявления. По этим причинам «выжидательная тактика» при ТП обычно не целесообразна [1].
Наличие ФП и ТП сопровождается риском образования тромбов в полостях предсердий и развитием системных тромбоэмболий. Этот риск возрастает пропорционально длительности аритмии, и дополнительно возрастает при нормализации сердечного ритма (нормализационные эмболии). Поэтому длительность текущего пароксизма определяет тактику оказания помощи пациенту. Купирование затяжных пароксизмов ФП/ТП и восстановление СР при персистирующей форме аритмии должно проводиться на фоне предшествующей адекватной антикоагулянтной терапии (АКТ) (длительность приёма не менее 3-х нед.) либо необходимо проведение чреспищеводного эхокардиографического исследования (ЧП-ЭхоКГ) с целью исключения образования тромбов в ушках и полостях предсердий. После успешно проведенной кардиоверсии существует риск формирования тромбов de novo на фоне временного нарушения функции предсердий (феномен «оглушенного предсердия»), в связи с чем все пациенты должны получать АКТ не менее 4-х нед. после восстановления СР, независимо от риска кардиоэмболических осложнений по шкале CHA2DS2-VASc [4-6]. Более подробно тактика антикоагулянтного сопровождения кардиоверсии рассмотрена ниже.
Нередко пациенты с затяжными эпизодами аритмии предъявляют неспецифические жалобы, такие как слабость, одышка, повышенная утомляемость, снижение работоспособности, потливость. Восстановление СР у данной категории больных может привести к улучшению самочувствия и повлиять на прогноз заболевания [7].
Очень редким (истинная распространённость не известна), но опасным для жизни осложнением кардиоверсии является отёк лёгких, случаи развития которого описаны при любых способах восстановления СР, как при ФП, так и при ТП. Осложняющие процедуру кардиоверсии отёки лёгких, как правило, быстро купируются относительно небольшими дозами внутривенно вводимых петлевых диуретиков и не требуют инвазивной вентиляции лёгких. Вероятность возникновения отёка лёгких выше при купировании персистирующей и длительно персистирующей формы ФП/ТП у пациентов, имеющих структурные заболевания сердца (пороки клапанов и СН со сниженной фракции выброса (ФВ) левого желудочка (ЛЖ)). Обычно это осложнение развивается в первые сутки после купирования аритмии (незамедлительно развивающийся отёк лёгких может быть следствием электрической травмы сердца или резкого снижения ЧСС), однако описаны и отсроченные случаи развития отёка лёгких (до 96 ч от момента восстановления СР), развивающиеся у пациентов с сохранной или быстро восстанавливающейся ФВ ЛЖ. В качестве патогенетического механизма, ответственного за развитие такого отсроченного отёка лёгких, предполагается перераспределение кровотока, связанное с преждевременной избыточной физической активностью пациента на фоне более раннего восстановления сократительной функции правого предсердия при отсутствии сократимости левого предсердия. По этим причинам при проведении кардиоверсии пациентам с персистирующей формой ФП/ТП целесообразно давать рекомендации об ограничении физической активности в первые несколько суток после восстановления СР [8].
Существуют два основных способа купирования аритмии — ЭКВ и МКВ. Для купирования ТП (но не ФП) может быть эффективно применена сверхчастая стимуляция предсердий. Для больных с редкими пароксизмами ФП, не получающих медикаментозной антиаритмической терапии, может быть рекомендован самостоятельный пероральный приём препаратов для купирования аритмии (подход «таблетка в кармане«), однако перед этим необходима тщательная оценка переносимости такого лечения.
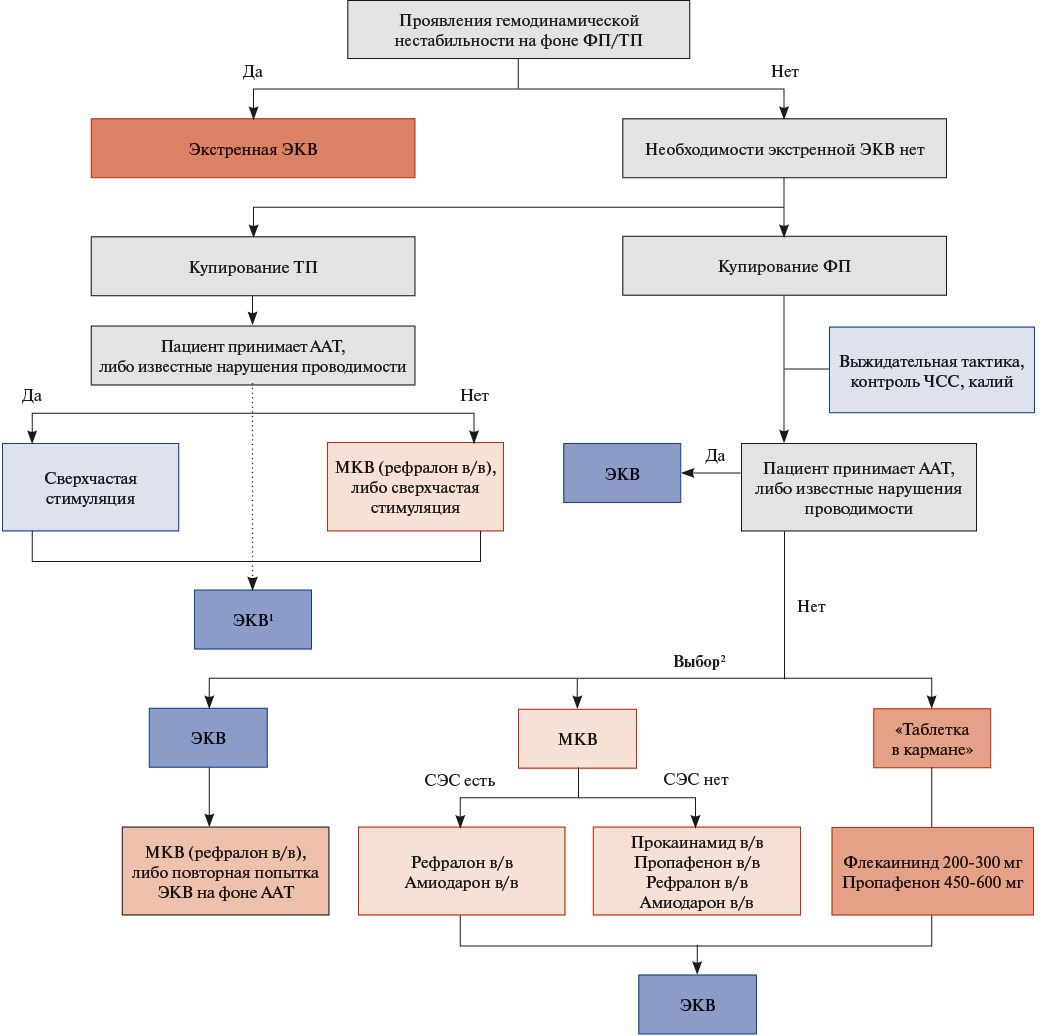
Выбор метода восстановления СР осуществляют с учётом клинических проявлений аритмии, её формы, длительности текущего эпизода, сопутствующих нарушений проводимости, постоянного приёма антиаритмических препаратов, наличия/отсутствия структурного заболевания сердца, а также анамнестических данных о предшествующем опыте купирования аритмии. Тактика кардиоверсии обобщена на рисунке 1.
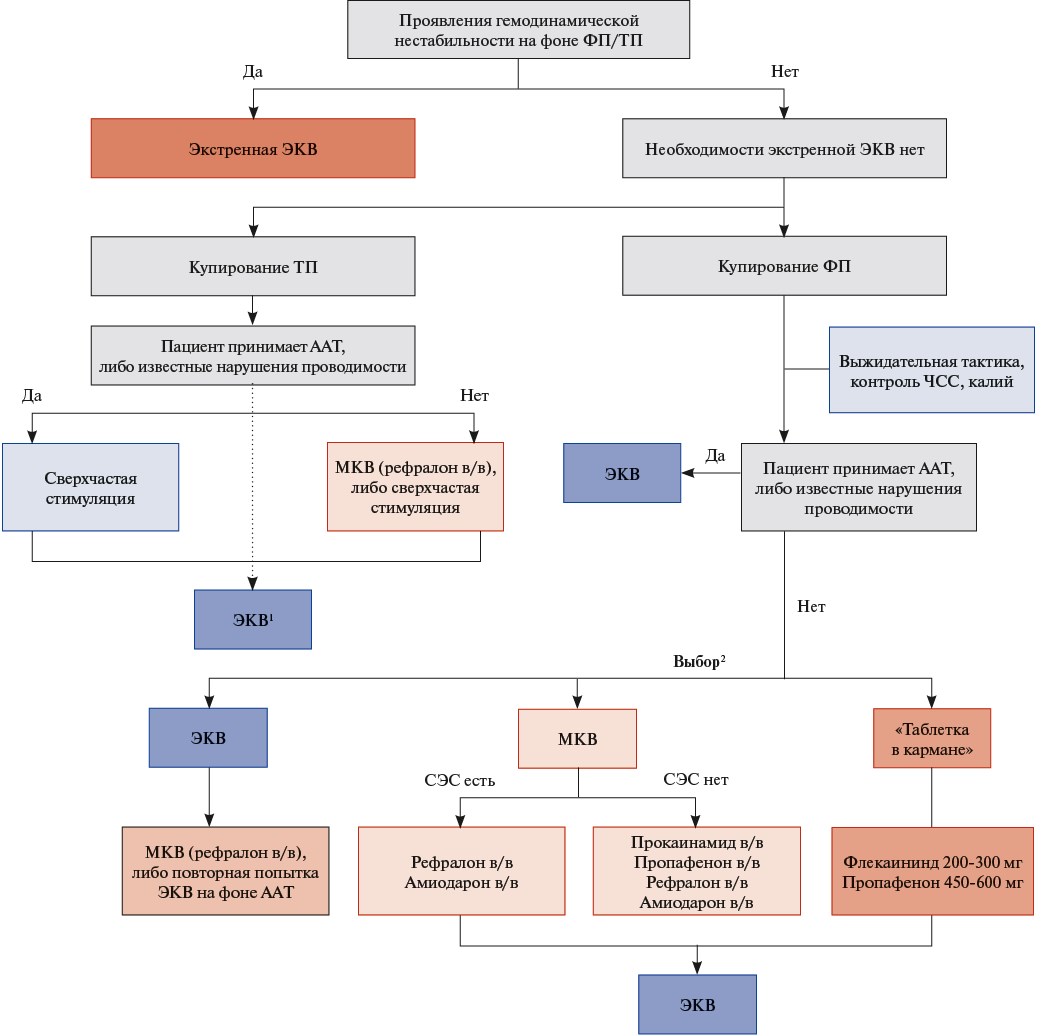
Рис. 1. Тактика кардиоверсии при ФП и ТП.
Примечание: ¹ — ЭКВ при ТП может быть проведена не только при неэффективности сверхчастой стимуляции и МКВ рефралоном, но и в качестве альтернативы этим методам купирования. ² — выбор осуществляется в соответствии с формой ФП (при персистирующей ФП большинство антиаритмических препаратов, за исключением рефралона, неэффективны), анамнезом заболевания (предшествующий опыт купирования аритмии, сведения о переносимости антиаритмических препаратов).
Сокращения: ААТ — антиаритмическая терапия, в/в — внутривенное введение, МКВ — медикаментозная кардиоверсия, СЗС — структурное заболевание сердца, ТП — трепетание предсердий, ФП — фибрилляция предсердий, ЧСС — частота сердечных сокращений, ЭКВ — электрическая кардиоверсия.
Цель обзора — рассмотрение способов восстановления СР при ФП и ТП, определение приоритетного метода кардиоверсии в различных клинических ситуациях, описание правил подготовки и возможных осложнений процедуры.
Методология исследования
Представлен описательный обзор методики кардиоверсии, рассмотрены действующие клинические рекомендации по диагностике и лечению ФП и ТП, а также актуальные научные работы по данной тематике. Поиск литературных источников проводился по базам данных Elibrary.ru, PubMed, Embase и Cochrane Library.
Результаты
ЭКВ
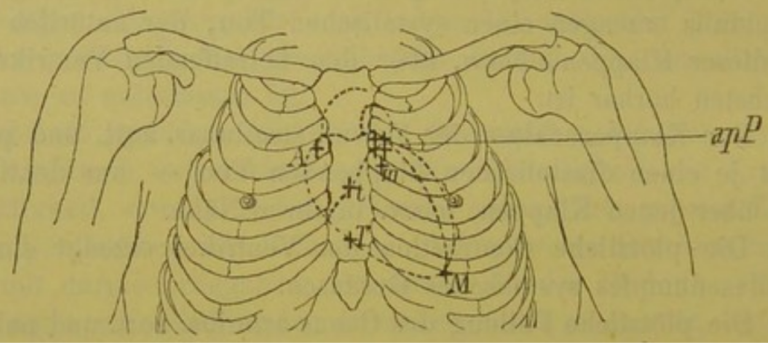
Серийное производство первого в мире импульсного дефибриллятора было начато в СССР в 1952г. Активное применение ЭКВ в клинической практике для купирования ФП началось с 1960-х годов [9]. При нанесении электрического разряда на переднюю грудную стенку происходит одномоментная деполяризация практически всех возбудимых клеток в предсердиях, вследствие чего кардиомиоциты переходят в состояние рефрактерности и циркуляция волн фибрилляции прекращается [10]. Проведение процедуры требует кратковременного наркоза, в связи с чем её выполняют натощак.
В случаях, когда эпизод ФП протекает с гемодинамической нестабильностью и требует незамедлительного купирования, ЭКВ является методом выбора в связи с быстротой купирования аритмии.
Эффективность данного метода достигает 90% [11]. Обычно используют энергию разряда 120-200 Дж. Согласно данным систематического обзора и метаанализа, проведенного Vinter N, et al. (2023), более высокий уровень электрической энергии при ЭКВ связан с более высокой частотой купирования ФП с помощью двухфазной ударной волны, при этом расположение электродов может быть выбрано исходя из удобства [12]. Следует отметить, что некоторые клинические ситуации, такие как высокий трансторакальный импеданс (характерно для пациентов с избыточной массой тела), большая длительность текущего эпизода ФП на момент планирования кардиоверсии или тяжёлые сопутствующие заболевания, такие как хроническая обструктивная болезнь легких или СН, могут снизить вероятность успеха ЭКВ на 10-50% [10][13-19].
Проведение ЭКВ на фоне заранее назначенной противорецидивной антиаритмической терапии (антиаритмическими препаратами III класса, реже IC класса) повышает эффективность процедуры, а также снижает риск развития ранних рецидивов ФП после успешного восстановления СР, частота которых может достигать 80% [14][15].
Осложнения при ЭКВ встречаются относительно редко. Ввиду того, что процедура проводится под наркозом, существует риск развития таких осложнений, как гипоксия и гиповентиляция, артериальная гипотензия, аспирация и отек легких. Нанесение разряда может приводить к электрической травме сердца, что проявляется артериальной гипотензией, острой СН и транзиторной элевацией сегмента ST в большинстве отведений электрокардиографии (ЭКГ). Описаны клинические случаи синдрома такоцубо при проведении ЭКВ. Изредка при ЭКВ могут наблюдаться ожоги кожи. При нарушении синхронизации наносимого разряда возможна индукция желудочковой тахикардии (ЖТ) и фибрилляции желудочков, которые являются угрожающими жизни состояниями. По этим причинам процедура ЭКВ должна осуществляться в условиях реанимационного отделения или палаты интенсивной терапии и проводиться опытным медицинским персоналом [16][20].
Сверхчастая стимуляция предсердий
Для купирования ТП может быть эффективно использована сверхчастая стимуляция предсердий, которая осуществляется при помощи системы чреспищеводной электрической стимуляции сердца, временной трансвенозной стимуляции (при наличии центрального венозного доступа), а также посредством программирования имплантированного электрокардиостимулятора, имплантированного кардиовертера-дефибриллятора или устройства сердечной ресинхронизирующей терапии [1]. Эффективность сверхчастой стимуляции при ТП достигает 80%. В некоторых случаях высокочастотная стимуляция сердца способна преобразовать ТП в ФП. Это может улучшить гемодинамические показатели и переносимость аритмии, т.к. ЧСС при ФП обычно ниже, чем при ТП. Однако высокочастотная стимуляция не является эффективным методом лечения уже существующей ФП [21].
МКВ
История МКВ берёт своё начало с публикации клинических случаев применения противомалярийного препарата хинидина для устранения мерцания предсердий в 1918г. [22]. С тех времен было создано и исследовано немало антиаритмических средств. В настоящее время для восстановления СР широко используются антиаритмические препараты I (прокаинамид, флекаинид, пропафенон) и III классов (амиодарон, рефралон). МКВ лишена недостатков, присущих ЭКВ, а преимуществом ее является способность используемого антиаритмического препарата предотвращать развитие ранних рецидивов аритмии после успешной кардиоверсии [14]. Согласно различным исследованиям, эффективность МКВ у пациентов с недавними пароксизмами аритмии варьирует от 50% до 95% [23-26].
В связи с отсутствием необходимости проведения натощак, данная процедура может быть выполнена у госпитализированных пациентов с недавно возникшим пароксизмом ФП/ТП в течение первых часов после поступления. В отдельных случаях возможно проведение процедуры в амбулаторном режиме. Следствием этого является сокращение сроков госпитализации (или даже отсутствие необходимости в госпитализации) и более быстрое восстановление трудоспособности больных. Однако восстановление СР путем МКВ требует более длительного времени по сравнению с ЭКВ, что является недостатком фармакологического метода кардиоверсии. Особенно важно, что антиаритмические средства обладают аритмогенным действием и могут приводить к развитию жизнеугрожающих осложнений и гемодинамической нестабильности, поэтому их применение должно производиться под контролем показателей гемодинамики и электрокардиографических параметров.
Как правило, МКВ не используют при купировании ТП, поскольку эффективность антиаритмических препаратов (за исключением рефралона, см. ниже) при этой форме аритмии меньше, чем при ФП. Фармакодинамического действия препаратов оказывается не достаточно для достижения блокады проведения электрических импульсов в миокарде предсердий и размыкания цикла macro reentry, лежащего в основе ТП. В то же время лекарственные препараты могут увеличить длительность цикла ТП, снижая частоту предсердной активации и увеличивая количество проводимых через атриовентрикулярный (АВ) узел волн трепетания, вплоть до проведения 1:1, что нередко сопровождается нестабильностью гемодинамики.
Процедуру МКВ не рекомендовано проводить у пациентов с нарушениями проводимости сердца (дисфункцией синусового узла, нарушениями АВ и внутрижелудочковой проводимости), брадисистолической формой ФП с частотой желудочковых сокращений <50 уд./мин, а также у пациентов с удлинением интервалов QT/QTc >500 мс. Также МКВ не должна проводиться больным, у которых пароксизм ФП/ТП развился на фоне предшествующего длительного приёма противорецидивной антиаритмической терапии, в связи с вероятностью неблагоприятного межлекарственного взаимодействия и повышенным в связи с этим риском развития нежелательных эффектов лекарственных средств [1].
Проведение МКВ с использованием антиаритмических средств, имеющих отрицательное инотропное действие (ꞵ-адреноблокаторы, антиаритмические средства Ia класса и блокаторы кальциевых каналов), сопровождается снижением артериального давления (АД). Дополнительное снижение АД на фоне высокой частоты желудочковых сокращений при пароксизмах ФП может сопровождаться клиническими проявлениями гемодинамической нестабильности. В связи с этим при наличии у пациентов артериальной гипотензии на фоне пароксизма ФП использовать данные лекарственные препараты для процедуры МКВ не следует [27][28].
Наиболее часто встречающимися нежелательными явлениями антиаритмических средств являются различного рода брадиаритмии. Брадиаритмии могут возникать по двум основным причинам: непосредственное влияние и фармакодинамические эффекты самих препаратов (угнетение функции синоатриального (СА) узла, нарушение АВ проводимости, замедление проведения по ножкам пучка Гиса) и/или уже имеющиеся скрытые нарушения проводимости сердца (дисфункция СА и АВ узлов, угнетение автоматизма СА узла вследствие длительного сохранения ФП и др.) [29][30]. Следует отметить, что замедление АВ проводимости под действием препаратов еще до восстановления СР нередко сопровождается снижением ЧСС и лучшей переносимостью пароксизма ФП.
Аритмогенное действие может проявляться трансформацией ФП в ТП, а также провоцированием опасных желудочковых аритмий. К ним относят частые желудочковые экстрасистолы, короткие эпизоды ЖТ, а также устойчивые формы ЖТ и фибрилляции желудочков.
Антиаритмические средства любых классов могут вызвать преобразование ФП в ТП. Так как ТП имеет более регулярную форму и протекает с более низкой частотой предсердной импульсации, большее количество волн F проводится на желудочки, по сравнению с ФП, что приводит к нарастанию ЧСС. Антиаритмические лекарственные препараты I класса замедляют циркуляцию волн трепетания по предсердию, но не увеличивают длительность рефрактерного периода АВ соединения, по этой причине при их применении для МКВ ФП риск развития ТП с проведением 1:1 возрастает. При ТП применение антиаритмических средств I класса не только неэффективно, но и потенциально опасно [31][32].
Основным электрофизиологическим эффектом антиаритмических средств III класса является удлинение трансмембранного потенциала действия и, следовательно, рефрактерного периода возбудимых тканей сердца. Реализация данного эффекта отражается на ЭКГ в виде удлинения интервала QT. При чрезмерном удлинении QT повышается риск возникновения жизнеугрожающих желудочковых аритмий, прежде всего полиморфной ЖТ типа пируэт (torsade de pointes) (TdP). Необходимо избегать применения препаратов III класса у пациентов, имеющих исходное удлинение интервала QT (например, на фоне гипокалиемии), а также у получающих лечение другими классами лекарственных средств, увеличивающими длительность интервала QT [33].
Выбор антиаритмического препарата для МКВ зависит от формы клинического течения, или типа ФП/ТП, наличия и тяжести сопутствующей сердечно-сосудистой и иной патологии, противопоказаний к применению и потенциальных побочных эффектов лекарственных средств, сведений об эффективности антиаритмической терапии в анамнезе, информации о сопутствующем лекарственном лечении [1][31].
Следует также отметить, что подавляющее большинство антиаритмических препаратов эффективны только при недавно возникших пароксизмах ФП. По мере увеличения сроков сохранения аритмии, вероятность восстановления СР при их использовании снижается.
При персистирующей форме ФП/ТП единственным антиаритмическим препаратом, позволяющим добиться быстрого восстановления СР с эффективностью, сопоставимой с ЭКВ, является рефралон. При персистирующем течении ФП/ТП восстановление СР может быть достигнуто и применением амиодарона, но не при внутривенном его введении, а при назначении пероральной лекарственной формы на длительный приём. Такой эффект достигается при насыщении препаратом, обычно спустя 2-3 нед. его приёма [1][31].
В настоящее время на территории Российской Федерации для восстановления СР рекомендованы и доступны антиаритмические препараты I класса (прокаинамид, флекаинил, пропафенон) и III класса (амиодарон, рефралон).
Прокаинамид (новокаинамид), препарат IA класса, блокируя быстрые натриевые каналы, приводит к замедлению скорости проведения импульса по тканям сердца. Также блокирует калиевые каналы, что приводит к удлинению трансмембранного потенциала действия и рефрактерного периода. Прокаинамид наиболее эффективен в купировании пароксизмов ФП длительностью <48 ч — 53-83%. При ТП эффективность препарата существенно ниже и составляет 33%. Препарат вводят внутривенно в дозе 500-1000 мг медленно (20-30 мг/мин), при этом антиаритмический эффект проявляется в течение 10-30 мин [23][24].
Наиболее серьёзными и часто встречающимися побочными эффектами препарата являются артериальная гипотензия (отмечается примерно в 10% случаев), нарушения проводимости сердца (остановка синусового узла, АВ блокады I и II степеней, иногда в сочетании с блокадами ножек пучка Гиса), трансформация ФП в ТП с увеличением ЧСС, желудочковое аритмогенное действие. Препарат противопоказан пациентам при наличии структурного заболевания сердца, нарушениях проводимости, СН со сниженной ФВ ЛЖ (<40%) и гипертрофии ЛЖ ≥14 мм [1][23][24].
Пропафенон, препарат относится к IC классу антиаритмических средств, вызывает выраженную блокаду быстрых натриевых каналов и замедляет скорость проведения импульса по тканям сердца, обладает свойствами неселективного бета-блокатора и блокатора кальциевых каналов. При внутривенном введении пропафенона в дозе 2 мг/кг массы тела больного антиаритмический эффект развивается достаточно быстро в течение 30 мин — 2 ч, при этом эффективность купирования пароксизмов ФП составляет 40-80%. При ТП препарат менее эффективен — 30% [32][33].
Пропафенон противопоказан больным с ишемической болезнью сердца и пациентам со структурным заболеванием сердца. Учитывая наличие β-блокирующих свойств, препарат может провоцировать приступы бронхоспазма у пациентов с тяжёлой бронхиальной астмой. Также может способствовать трансформации ФП в ТП, что может сопровождаться увеличением частоты желудочковых сокращений и ухудшением состояния больного [33].
Амиодарон, препарат III класса, при этом обладает механизмами действия всех четырех классов антиаритмических средств по классификации E. M. Vаughan Williams. Основным электрофизиологическим эффектом препарата является удлинение трансмембранного потенциала действия путем блокады калиевых каналов. Однако при внутривенном введении амиодарон первоначально проявляет свою β-блокирующую активность, а также вызывает блокаду натриевых и кальциевых каналов. Клинически это выражается в снижении ЧСС на фоне сохраняющейся аритмии, что является положительным эффектом, поскольку приводит к улучшению состояния больного.
В клинической практике для МКВ пароксизмальной ФП амиодарон используется наиболее часто. Препарат обладает широким спектром безопасности и может быть использован у пациентов с СН с низкой ФВ ЛЖ, а также у больных со структурным поражением сердца.
С целью купирования пароксизмов ФП и ТП амиодарон вводят внутривенно в стандартной дозе 5 мг/кг массы тела (медленная внутривенная инфузия), и его эффективность при этом составляет 34-69%, достигая максимума в относительно поздние сроки, спустя 3-12 ч от начала введения [34].
Наиболее частыми осложнениями МКВ с использованием амиодарона являются артериальная гипотензия (10-30%) и брадикардия (3-20%) [31]. Внутривенные инфузии препарата могут сопровождаться развитием периферического флебита, частота развития которого довольно высока и колеблется от 8 до 50% случаев [35]. Несмотря на способность амиодарона увеличивать длительность интервала QT, желудочковые нарушения ритма сердца при внутривенном введении отмечаются редко. Риск развития опасной ЖТ типа TdP не превышает 1,5% [36].
Рефралон (кавутилид) — отечественный антиаритмический препарат III класса. Основным электрофизиологическим механизмом действия рефралона является ингибирование выходящего калиевого тока задержанного выпрямления, приводящее к увеличению фазы реполяризации трансмембранного потенциала действия и, следовательно, удлинению рефракторного периода тканей сердца. Рефралон вводят внутривенно согласно следующей схеме: 10 мкг/кг — 10 мкг/кг — 10 мкг/кг с интервалами между введениями по 15 мин. В целях повышения безопасности МКВ рекомендуется разделение первой вводимой дозы на 2 введения (схема: 5 мкг/кг — 5 мкг/кг — 10 мкг/кг — 10 мкг/кг). Введение препарата должно быть прекращено на любом из этапов в случае: восстановления СР; снижения ЧСС <50 уд./мин; увеличения длительности интервала QT ≥500 мс; развития проаритмических эффектов. В отличие от других антиаритмических препаратов, рефралон рекомендован для восстановления СР при ФП/ТП любой продолжительности (пароксизмальная и персистирующая формы аритмии). Эффективность рефралона при персистирующей форме аритмии достигает 90%, что сопоставимо с максимально достижимыми результатами ЭКВ. В клинических исследованиях препарат продемонстрировал возможность успешного восстановления СР при ранее неэффективных попытках ЭКВ.
При пароксизмальной форме ФП эффективность рефралона ещё выше и приближается к 95%, при этом восстановления СР чаще достигается применением наименьших доз препарата (5 мкг/кг и 10 мкг/кг), что позволяет снизить вероятность нежелательных эффектов. Эффективность восстановления СР при ТП, как типичном, так и атипичном, превышает 95%. Поскольку рефралон повышает рефрактерность АВ узла и системы Гиса-Пуркинье, риск уменьшения кратности проведения на желудочки волн F до величины 1:1 и соответствующего нарастания ЧСС, практически отсутствует. Это принципиально важно отличает рефралон от других антиаритмических препаратов. В подавляющем большинстве случаев для восстановления СР требуется от нескольких минут до 1 ч, но длительность терапевтического действия составляет 24 ч [37][38].
К преимуществам рефралона, помимо высокой эффективности и скорости купирования аритмии, относится отсутствие влияния на сократимость миокарда и показатели АД. Как и остальные представители III класса антиаритмических средств, препарат вызывает увеличение продолжительности интервала QT, что потенциально влечет за собой возрастание риска развития жизнеугрожающих желудочковых аритмий. Согласно проведенным исследованиям частота возникновения тахикардии типа TdP не высока и составляет ~1,5%, но требует того, чтобы процедура МКВ с использованием рефралона проводилась в условиях палаты интенсивной терапии, с телеметрическим контролем ЭКГ до 24 ч [37-40].
Самостоятельный приём антиаритмических препаратов для купирования пароксизмов ФП (подход «таблетка в кармане»)
Больным с редкими пароксизмами ФП (но не ТП), не принимающим постоянной противорецидивной антиаритмической терапии, может быть рекомендован самостоятельный прием антиаритмических средств внутрь для восстановления СР. С этой целью используют антиаритмические препараты IC класса флекаинид (в дозе 200-300 мг), а также пропафенон (в дозе 450-600 мг). Восстановление СР при пероральном приеме препаратов регистрируется в более поздние сроки (по сравнению с внутривенным применением), спустя 2-6 ч, о чём следует информировать пациента, однако эффективность не уступает таковой при внутривенном введении. Для предотвращения чрезмерного повышения ЧСС вследствие возможной трансформации ФП в ТП рекомендуется одномоментный прием β-адреноблокаторов короткого действия (пропранолол 10-20 мг) [41-43].
Данный лечебный подход может быть использован только при отсутствии противопоказаний к использованию этих препаратов, таких как структурные заболевания сердца и нарушения проводимости. Кроме того, данный подход не должен использоваться у пациентов с документированными эпизодами ТП. И наконец, индивидуальная безопасность применения такой схемы лечения должна быть предварительно подтверждена путем проведения соответствующих лекарственных проб, выполненных в условиях стационара под контролем ЭКГ и ХМ ЭКГ [44].
Антикоагулянтное сопровождение кардиоверсии
Требования по антикоагулянтному сопровождению кардиоверсии универсальны и не зависят от способа ее проведения (ЭКВ, МКВ, сверхчастая стимуляция).
Назначение адекватной АКТ во время кардиоверсии способствовало снижению частоты нормализационных тромбоэмболических осложнений (ТЭО) с 5-8% до 0,5-0,8% [45-47]. Несмотря на то, что риск подобных ТЭО максимален в первые 72 ч, он сохраняется до 10 сут. после кардиоверсии по причине возможности изгнания тромба не только, собственно, в момент купирования аритмии, но и на фоне восстановления механической систолы предсердий. При этом даже исходное отсутствие тромбоза ушка левого предсердия по данным ЧП-ЭхоКГ не исключает последующего его формирования после восстановления СР на фоне оглушения миокарда [47][48].
Даже экстренная кардиоверсия должна проводится на фоне АКТ. Для больных, не получавших АКТ, с этой целью используют гепаринотерапию (в дозах, рекомендованных для лечения венозного тромбоза). А для больных, получавших пероральные антикоагулянты, в такой ситуации главное убедиться, что достигнута целевая антикоагуляция и терапия не прерывалась [1][49].
В случае принятия решения о плановой кардиоверсии, тактика зависит от длительности текущего пароксизма ФП и получал или не получал больной АКТ [1][49].
В том случае, если пациент, которому требуется проведение плановой кардиоверсии, принимал АКТ ≥3 нед., то при целевых значениях международного нормализованного отношения при терапии варфарином или отсутствии сомнений в комплаентности при приеме прямых оральных антикоагулянтов (ПОАК), восстановление СР может быть проведено без ЧП-ЭхоКГ. Однако многие клиники, следуя локальному протоколу, предпочитают быть уверенными в отсутствии тромбоза ушка левого предсердия, особенно если нет полной уверенности в приверженности больного лечению.
В том случае, если плановая кардиоверсия показана больному, не получавшему ранее АКТ, тактику определяет длительность текущего пароксизма.
Если целью является восстановление СР в ближайшее время (так называемая ранняя кардиоверсия), а длительность текущего эпизода ФП <48 ч, рекомендовано незамедлительно начать АКТ, используя для этого гепаринотерапию (в дозах, одобренных для лечения венозного тромбоза) или ПОАК. Все препараты из группы ПОАК рекомендованы в качестве антикоагулянтного сопровождения кардиоверсии с такой же эффективностью и безопасностью, как и варфарин [1][49-52]. В соответствии с действующими рекомендациями ПОАК следует назначать не менее чем за 2-4 ч до попытки восстановления СР. Если препаратом выбора является апиксабан, то кардиоверсии проводится спустя 5 приемов стандартных доз апиксабана. При необходимости проведения более ранней кардиоверсии (через 2-4 ч) первая доза апиксабана должна составлять 10 мг (5 мг при наличии принятых критериев для снижения дозы) [52]. При терапии дабигатраном и ривароксабаном такого режима дозирования не требуется.
В соответствии с современными клиническими рекомендациями у пациентов с длительностью эпизода ФП <48 ч можно рассмотреть возможность выполнения ранней кардиоверсии без проведения ЧП-ЭхоКГ. Однако в последнее время накопилось достаточно данных о повышении риска ТЭО уже начиная с первых 12 ч пароксизма. Поэтому при наличии технической возможности целесообразно выполнять ЧП-ЭхоКГ даже в случае пароксизма <48 ч у пациентов с высоким риском ТЭО (CHA2DS2-VASc ≥2 баллов у мужчин, ≥3 баллов у женщин и/или длительность эпизода ФП >12 ч) [4][49]. В Европейских рекомендациях по ФП 2024г длительность пароксизма, не требующая проведения ЧП-ЭхоКГ у пациентов без предшествующей АКТ в течение 3 и более недель, уменьшена с 48 до 24 ч [50]. Рекомендации Американской ассоциации сердца и российские эксперты пока сохранили свою позицию неизменной (длительность пароксизма должна быть <48 ч) [49][51].
В том случае, если раннее восстановление СР не является целью, возможно назначить АКТ больному на 3 нед. и вернуться к вопросу о проведении кардиоверсии через 3 нед.
В том случае, если вопрос о плановом восстановлении СР стоит для больного с длительным пароксизмом ≥48 ч или истинная длительность неизвестна, показано назначение АКТ на 3 нед., после чего может быть выполнена кардиоверсия. Альтернативой трёхнедельной АКТ перед кардиоверсией может быть исключение тромба в полости/ушке левого предсердия с помощью ЧП-ЭхоКГ. Но даже в случае отсутствия тромбов по данным ЧП-ЭхоКГ, кардиоверсия проводится на фоне адекватной АКТ. В настоящее время в качестве альтернативы ЧП-ЭхоКГ допустимой опцией является проведение мультиспиральной компьютерной томографии сердца с контрастированием.
При обнаружении тромба следует проводить АКТ и повторить ЧП-ЭхоКГ через 3-4 нед. Если тромб сохраняется, можно провести повторные ЧП-ЭхоКГ либо отказаться от восстановления ритма сердца в пользу контроля частоты желудочковых сокращений [1][49-51].
После проведения кардиоверсии необходимая минимальная длительность АКТ составляет 4 нед. Если исходно назначались гепарин и его производные, рекомендовано перевести пациента на пероральные антикоагулянты, предпочтительно ПОАК. Продолжение приёма препаратов по истечении 4 нед. определяется в соответствии с факторами риска по шкале CHA2DS2-VASc [49].
В настоящей статье приведен алгоритм антикоагулянтного сопровождения кардиоверсии (рис. 2), представленный в Евразийских рекомендациях по лечению ФП, как наиболее удобный для практического врача [1].

Рис. 2. Алгоритм антитромботической терапии у пациентов с ФП, подвергаемых кардиоверсии [6].
Сокращения: АВК — антагонисты витамина К, АКГ — антикоагулянтная терапия, жен. — женщины, КВ — кардиоверсия, МНО — международное нормализованное отношение, муж. — мужчины, НМГ/НФГ — низкомолекулярный/нефракционированный гепарин, ПОАК — прямые оральные антикоагулянты, УЛП/ЛП — ушко левого предсердия/левое предсердие, ЧП-ЭхоКГ — чреспищеводная эхокардиография, ФП — фибрилляция предсердий.
Заключение
В статье рассмотрены способы купирования ФП и ТП, представлены рекомендации по тактике восстановления СР и антикоагулянтному сопровождению кардиоверсии в различных клинических ситуациях.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Гаглоева Д.А., Кропачева Е.С., Миронов Н.Ю., Голицын С.П. Тактика кардиоверсии при фибрилляции и трепетании предсердий (обзор). Российский кардиологический журнал. 2025;30(4S):6708. https://doi.org/10.15829/1560-4071-2025-6708. EDN: FSVJMQ
Скопировать