Радионуклидные методы диагностики при фибрилляции предсердий
Аннотация
Проведен анализ отечественной и зарубежной литературы для определения диагностической эффективности радиоизотопных методов с различными радиофармацевтическими лекарственными препаратами (РФЛП) у пациентов с фибрилляцией предсердий (ФП).
Проведен поиск научных публикаций в базах данных PubMed, Elibrary, за период 2000-2025гг, посвященных применению радиоизотопных методов с различными РФЛП.
В обзоре освещены возможности методов радиоизотопной диагностики однофотонной эмиссионной компьютерной томографии и позитронной эмиссионной томографии с различными РФЛП у пациентов с ФП. Обсуждаются диагностические и прогностические аспекты радиоизотопных технологий при постоянной и пароксизмальной формах мерцательной аритмии. Отмечен вклад сцинтиграфического исследования с [123I]-МИБГ планирования интервенционного лечения ФП. Радиоизотопные методы исследования вносят существенный вклад в диагностику причин нарушения ритма и обладают прогностическим значением в прогнозировании неблагоприятных событий и эффективности лечения.
Совершенствование аппаратуры для лучевой визуализации и значительный прогресс в радиофармацевтике привели к появлению целого ряда принципиально новых неинвазивных способов исследования сердечно-сосудистой системы, которые существенно повысили эффективность обследования пациентов, в т.ч. с фибрилляцией предсердий (ФП)1 [1].
Особое место занимают методы радиоизотопной диагностики. Радиофармацевтические лекарственные препараты (РФЛП), используемые при выполнении радиоизотопной визуализации, аккумулируются в сердечной мышце пропорционально миокардиальному кровотоку или являются естественными метаболитами или их аналогами. Включение в их состав радионуклидов не меняет их биохимических свойств, что дает возможность корректно оценивать физиологические и метаболические процессы в кардиомиоцитах.
Таким образом, цель исследования — провести анализ отечественной и зарубежной литературы для определения диагностической эффективности радиоизотопных методов с различными РФЛП у пациентов с ФП, а также сравнить диагностические и прогностические аспекты радиоизотопных технологий при постоянной и пароксизмальной формах мерцательной аритмии.
Материал и методы
Поиск публикаций на русском и английском языках производился по базам данных научной литературы PubMed и elibrary, посвященных применению радиоизотопных методов с различными РФЛП у пациентов с ФП, по ключевым словам «фибрилляция предсердий», «однофотонная эмиссионная компьютерная томография компьютерная томография» (ОФЭКТ/КТ), «ОФЭКТ», «сцинтиграфия» «позитронная эмиссионная томография» (ПЭТ/КТ), «перфузия миокарда», «[ 18F]-фтордезоксиглюкоза» ([ 18F]-ФДГ), «68Ga-FAPI», «метайодбензилгуанидин, меченный йодом-123» ([ 123I]-МИБГ). Временной диапазон охватывал период 2000-2025гг. В анализ были включены 35 обзоров, метаанализов и клинических исследований, изучающих тему радиоизотопных методов с различными РФЛП у пациентов с ФП.
Результаты
К радионуклидным методам исследования сердечно-сосудистой системы относятся ОФЭКТ или ПЭТ с различными РФП. По сравнению с радиоизотопами, применяемыми для ОФЭКТ-⁹⁹мТс, ¹²³I, ¹¹¹In и ⁶⁷Ga, нуклиды, используемые для ПЭТ, такие как ⁸²Rb, ¹⁵О, ¹³N, ⁶⁸Ga, ¹⁸F и ¹¹С, обладают ультракороткими периодами физического распада и биологического полувыведения, что позволяет на порядок снизить лучевую нагрузку на пациента и сократить время сканирования. Это дает возможность проведения повторных исследований в сжатые сроки.
Внедрение в клиническую практику совмещенных систем медицинской визуализации, таких как ОФЭКТ/КТ, ПЭТ/КТ и ПЭТ/магнитно-резонансная томография, разработка программных пакетов постпроцессинговой обработки способствовали появлению новых возможностей изучения структурно-функциональной патологии сердца.
Визуализация в популяции пациентов с ФП играет решающую роль не только в оценке размера левого предсердия (ЛП), но и в определении основных структурных и функциональных особенностей сердца. ОФЭКТ/КТ миокарда может быть полезна для диагностики ишемической болезни сердца (ИБС) у пациентов с ФП [2].
Радиоизотопная оценка перфузии миокарда осуществляется посредством радиодиагностических приборов, предназначенных для регистрации гамма-излучения от изотопов, входящих в состав РФЛП, — ОФЭКТ или ПЭТ.
Перфузионная ОФЭКТ миокарда является доступным и информативным методом визуализации микроциркуляции сердечной мышцы. Для оценки перфузии миокарда методом ОФЭКТ используются РФЛП на основе катионных комплексов, меченных ⁹⁹мТс (МИБИ, sestamibi, тетрафосмин, технетрил). ПЭТ с перфузионными РФЛП имеет меньшую доступность, тем не менее существенное преимущество, а именно возможность оценки быстропротекающих физиологических процессов в миокарде. По сравнению со сцинтиграфией ПЭТ дает возможность оценить перфузию в более широком диапазоне объемов коронарного кровотока, что в сочетании с фармакологическими пробами позволяет использовать метод для определения как глобального, так и регионарного коронарного резерва. Основными РФЛП для оценки миокардиального кровотока являются ¹⁵О-вода, ¹³N-аммоний, ¹⁸F-флурпиридаз и ⁸²Rb-хлорид. Эти РФЛП имеют общее свойство аккумуляции в кардиомиоцитах пропорционально миокардиальному кровотоку.
Перфузионная ОФЭКТ миокарда и перфузионная ПЭТ миокарда в покое малоинформативны. При уменьшении просвета коронарных артерий вследствие атеросклероза происходит компенсаторная вазодилатация пораженных сосудов, кроме того, образуется сеть коллатерального кровообращения, благодаря чему в состоянии покоя кровоснабжение миокарда длительное время может оставаться практически нормальным, а нарушение миокардиальной перфузии возможно установить в условиях физической или фармакологической нагрузки.
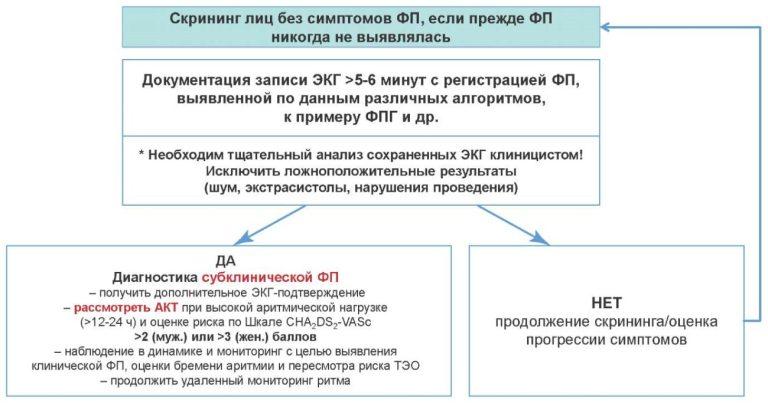
Согласно рекомендациям ACC/AHA/Американского общества ядерной кардиологии (ASNC) по клиническому применению радионуклидной визуализации сердца перфузионная ОФЭКТ или ПЭТ миокарда пациентам с ФП не показана [3]. Однако в консенсусном письме ACC (ACCF)/ASNC «Критерии целесообразности использования SPECT MPI» рассматривается использование перфузионной ОФЭКТ в рамках обследования асимптомных пациентов с впервые выявленной ФП с целью выявления ИБС. Для пациентов с низким риском ИБС по шкале Фрамингема в настоящем документе применение ОФЭКТ оценивается как неопределенное. Для пациентов с высоким риском ИБС по шкале Фрамингема применение ОФЭКТ оценивается как целесообразное. Перфузионная ОФЭКТ на фоне нагрузочной пробы хорошо зарекомендовала себя как метод диагностики и стратификации риска у пациентов с ИБС. Учитывая, что ФП может быть проявлением ИБС, было проведено ограниченное количество исследований, оценивающих диагностическое и прогностическое применение перфузионной ОФЭКТ, в частности, у пациентов с ФП. Так, Askew JW, et al. (2007) проанализировали результаты перфузионной ОФЭКТ у 374 бессимптомных пациентов с мерцательной аритмией без анамнеза ИБС [4]. Исследуемая группа пациентов сравнивалась с контрольной популяцией без ФП соответствующего возраста и пола. В результате этой работы достоверные различия в частоте встречаемости нарушений перфузии миокарда по данным ОФЭКТ у пациентов с мерцательной аритмией и лиц контрольной группы обнаружено не было (51,6% vs 48,4%; p=0,38). При этом, по данным многофакторного анализа после поправки на клинические переменные и результаты перфузионной ОФЭКТ, ФП оставалась независимым предиктором неблагоприятных событий (p=0,01).
В исследовании Abidov A, et al. (2004) изучалось прогностическое значение перфузионной ОФЭКТ у пациентов с ФП [5]. В отличие от исследования Askew JW, et al. (2007), в эту работу были включены пациенты с клиническими симптомами и/или ИБС в анамнезе. По результатам многофакторного анализа ФП также оказалась независимым предиктором внезапной смерти (p=0,001).
Интересный вопрос, связанный с применением радиоизотопных исследований перфузии миокарда у пациентов с мерцательной аритмией, заключается в том, сама по себе ФП может нарушать коронарную микроциркуляцию. Этот вопрос изучался в исследовании Range FT, et al. (2007), в котором выполняли расчет миокардиального кровотока с помощью ПЭТ с ¹⁵O-водой в покое, на фоне холодовой стимуляции и фармакологической пробы с вазодилататором (аденозином) у 25 пациентов мужского пола с ФП без ИБС, но с как минимум одним фактором риска, и 13 добровольцами мужского пола контрольной группы, сопоставимыми по возрасту и факторам риска [6]. Авторы показали, что миокардиальный кровоток был значительно снижен в покое (0,95±0,19 vs 1,14±0,22 мл/мин/мл; p=0,009), на фоне фармакологической пробы (2,07±0,80 vs 3,33±0,78 мл/мин/мл; p<0,001) и холодовой стимуляции (0,90±0,25 vs 1,14±0,25 мл/мин/мл; p<0,014) у пациентов с мерцательной аритмией по сравнению с контрольной группой. Десяти пациентам основной группы была проведена кардиоверсия, и повторное исследование миокардиального кровотока с помощью ПЭТ было выполнено в условиях синусового ритма. При этом отмечено улучшение миокардиального кровотока в покое и на фоне холодовой пробы, который стал сопоставим со значениями контрольной группы. Эти результаты свидетельствуют о том, что у пациентов с мерцательной аритмией снижение перфузии может быть обусловлено нарушением ритма предсердий, а результаты радиоизотопного исследования оказаться ложноположительными т.е. не коррелировать со степенью стеноза коронарных артерий.
Cremer PC, et al. (2015) изучали перфузию миокарда в покое и на фоне нагрузочной пробы у 1700 пациентов с ФП без клинических симптомов ИБС [7]. Авторы установили, что у пациентов с мерцательной аритмией и отсутствием симптомов ИБС сцинтиграфические признаки ишемии миокарда диагностировались редко и их появление статистически не увеличивалась с повышением клинического риска. Более того, после поправки на исходный клинический риск, сцинтиграфические признаки стресс-индуцированной гипоперфузии не давали дополнительной информации для прогнозирования общей смертности. Хотя ограничением исследования являлась недооценка нефатального инфаркта миокарда, и информация о летальных исходах была доступна не для всех пациентов.
Smit MD, et al. (2010) изучали диагностическую ценность перфузионной ОФЭКТ миокарда для оценки риска развития ИБС у пациентов с ФП в анамнезе [8]. Исследование не выявило достоверного различия в отношении положительного результата ОФЭКТ между пациентами с ФП и пациентов с синусовым ритмом. Коронарная ангиография, выполненная после ОФЭКТ, продемонстрировала большее число стенозированных коронарных артерий в контрольной группе с положительными результатами ОФЭКТ, чем у пациентов с ФП, что еще раз свидетельствует о том, что нарушения предсердного ритма могут приводить к появлению участков гипоперфузии миокарда.
Аналогичные результаты были получены Bechlioulis A, et al. (2025), в своем исследовании они изучали вклад ФП в ишемию миокарда с помощью перфузионной ОФЭКТ миокарда с ⁹⁹mTc-тетрофосмином у 259 пациентов с подозрением на стабильную ИБС [9]. В исследовании была обнаружена взаимосвязь ФП с большими по площади дефектами перфузии у пациентов с клиническими признаками ИБС независимо от количества факторов риска сердечно-сосудистых заболеваний.
В недавних исследованиях продемонстрировано, что идиопатическая ФП связана со снижением перфузии миокарда и коронарного резерва, которые также определяются при различных формах неишемических кардиомиопатий. Byrne C, et al. (2019) на 114 пациентах с ФП изучали наличие дополнительного отрицательного влияния нарушений предсердного ритма на перфузию миокарда у пациентов с неишемической систолической сердечной недостаточностью (СН) с помощью ПЭТ с ⁸²Rb-хлоридом [10]. Авторы пришли к выводу, что у пациентов с систолической СН коронарный резерв кровотока был ниже, чем у здоровых лиц контрольной группы, особенно у пациентов с ФП в течение ПЭТ-сканирования.
В исследовании Range FT, et al. (2009) выполнялось сопоставление состояния перфузии миокарда у пациентов с неишемической дилатационной кардиомиопатией с ФП и синусовым ритмом [11]. По сравнению с контрольной группой здоровых лиц у пациентов с дилатационной кардиомиопатией и синусовым ритмом наблюдалось снижение миокардиального кровотока на фоне пробы с вазодилататором (2,52±1,29 vs 3,57±0,88 мл/мин/мл, P=0,014) и коронарного резерва (2,10±1,01 vs 3,37±0,97, P=0,003). Кроме того, у пациентов с дилатационной кардиомиопатией и ФП отмечены низкие значения миокардиального кровотока в состоянии покоя (0,82±0,31 мл/мин/мл, P=0,010) и на фоне фармакологической пробы с вазодилататором (1,32±0,93 мл/мин/мл, P=0,022), а по сравнению с контрольной группой у пациентов с дилатационной кардиомиопатией и ФП наблюдались самые низкие показатели коронарного резерва (1,68±0,94 vs 3,37±0,97, P<0,001), сопровождавшееся самым высоким коронарным сосудистым сопротивлением.
Gimelli A, et al. (2015) в своем исследовании поставили задачу оценить диагностическую точность перфузионной ОФЭКТ с помощью гамма-камеры нового поколения с кристаллами кадмием-цинком-теллуридом у пациентов с ФП [12]. В исследование включены 74 пациента, которым были выполнены перфузионная ОФЭКТ и коронарная ангиография. В группу контроля вошли 148 пациентов с синусовым ритмом, соответствующие по возрасту, полу и типу протокола стресс-теста, с известной анатомией коронарных артерий. Коронарный стеноз ≥70% считался значимым. При анализе результатов перфузионной ОФЭКТ обнаружена высокая диагностическая точность в выявлении значимой ИБС как у пациентов с ФП, так и у пациентов контрольной группы (площади под кривой 0,71 vs 0,80, P для разницы: 0,212).
Измерение фракции выброса левого желудочка с помощью ОФЭКТ в режиме кардиосинхронизации оказалась малоинформативной у пациентов с мерцательной аритмией, поэтому данная методика не нашла отражения в клинических рекомендациях. Поэтому пациентам с ФП следует выполнять перфузионную ОФЭКТ без режима кардиосинхронизации [2].
Следует отметить, что радиоизотопные методы являются наиболее апробированными технологиями визуализации перфузии и миокардиального кровотока, открывающие новые возможности в изучении патофизиологии коронарного кровообращения. Методы позволяют определить не только пространственное распределение, но и функциональную значимость нарушений внутрисердечной гемодинамики на уровне микроциркуляции. Определение объемного миокардиального кровотока в сочетании с нагрузочными пробами позволяет использовать ПЭТ для вычисления глобального и регионарного коронарного резерва при различных заболеваниях сердечно-сосудистой системы. Неинвазивная диагностика нарушений коронарной микроциркуляции также играет важную роль в стратификации риска кардиоваскулярных осложнений.
Хорошо известно, что ЛП играет ключевую роль в возникновении и поддержании ФП, при этом во многих исследованиях сообщается об электрическом и структурном ремоделировании, а также об изменениях метаболизма сердечной мышцы [13-15]. Совмещенная позитронная эмиссионная и рентгеновская компьютерная томография (ПЭТ/КТ) с [ 18F]-ФДГ нашла широкое клиническое применение для диагностики воспаления, в т.ч. сердца. Причинами гипераккумуляции [ 18F]-ФДГ в предсердиях у пациентов с ФП в первую очередь может быть «метаболический сдвиг» кардиомиоцитов в сторону повышенного потребления глюкозы вследствие нарушения ритма. Этому свидетельствует снижение интенсивности накопления РФЛП после интервенционного лечения. Также повышенное накопление [ 18F]-ФДГ в миокарде предсердий обусловлено воспалительным процессом — чаще кардиосаркоидозом с сочетанным или изолированным поражением миокарда предсердий, что может способствовать развитию ФП. Кроме того, гипераккумуляция РФЛП может наблюдаться при некоторых видах генетически обусловленных кардиомиопатий [14-16]. Изменение метаболизма ЛП в сторону интенсификации гликолиза отражает нарушения энергетического обмена, которые способствуют развитию и поддержанию ФП, поддержанию аномальной электрической активности, а также структурным изменениям, таким как фиброз стенки ЛП [17].
Nakamura O, et al. (2022) в своем исследовании продемонстрировали что у пациентов с постоянной формой ФП интенсивность гиперфиксации РФПЛ в ЛП и ушке ЛП была выше, чем у пациентов с синусовым ритмом, при этом после успешных интервенционных вмешательств, направленных на контроль ритма, отмечено значительное снижение уровня аккумуляции [ 18F]-ФДГ в миокарде предсердий [15]. Следует отметить, что гиперфиксация [ 18F]-ФДГ при мерцательной аритмии наблюдается не только в миокарде ЛП, но и правого предсердия (ПП), что, как сообщается в исследовании Wang Y, et al. (2023), ассоциировано с повышенным риском острого нарушения мозгового кровообращения [18].
В исследовании Sinigaglia M, et al. (2019) были проанализированы ПЭТ изображения сердца у 64 пациентов с мерцательной артерией и 64 больных с синусовым ритмом в качестве контрольной группы, сопоставимых по возрасту и полу [19]. Результаты ПЭТ/КТ с [ 18F]-ФДГ были сопоставлены с клиническими характеристиками, включая перенесенное острое нарушение мозгового кровообращения. Диффузная гипераккумуляция РФЛП в ПП наблюдалось у трети пациентов с ФП и только у 2 пациентов в контрольной группе. Риск возникновения инсульта был тесно связан с интенсивностью накопления [ 18F]-ФДГ в миокарде предсердий и, по-видимому, связан с повышенной частотой кардиоэмболических инсультов.
Различие в интенсивности накопления [ 18F]-ФДГ в миокарде предсердий в зависимости от формы ФП — пароксизмальной или постоянной, продемонстрировали в своем исследовании Wan P, et al. (2023) [20]. В исследовании было установлено, что у пациентов с постоянной формой мерцательной аритмии гиперфиксация [ 18F]-ФДГ в миокарде предсердий наблюдалась чаще и ее интенсивность была выше, чем у пациентов с пароксизмальной формой (91,4% vs 28,6%, P<0,001; SUVmax: 4,10 (3,20-4,90) против 2,60 (2,40-3,10), P<0,001). В группе пациентов с высоким клиническим риском инсульта наблюдалось более высокое накопление РФЛП в миокарде ПП (3,35 (2,70, 4,50) vs 2,8 (2,4, 3,1), P=0,01).
В публикации Kassar A, et al. (2025) представлен метаанализ исследований с участием пациентов с мерцательной аритмией, у которых при ПЭТ/КТ с [ 18F]-ФДГ была обнаружена гипераккумуляция РФЛП в миокарде предсердий, при этом в 6 из 8 статей повышенное накопление РФЛП не было обусловлено кардиосаркоидозом [21]. Авторами отмечено, что у пациентов без верифицированного кардиосаркоидоза интенсивное накопление [ 18F]-ФДГ в миокарде предсердий было обусловлено предсердным нарушением ритма, что указывает на «метаболический переход» в кардиомиоцитах в сторону гликолиза. В целом, метаболические изменения и воспалительные процессы играют важную роль в патофизиологии ФП и стратификации риска неблагоприятных кардиоваскулярных событий.
Таким образом, ПЭТ-визуализация с использованием [ 18F]-ФДГ предоставляет уникальную информацию о метаболических изменениях, происходящих в кардиомиоцитах при ФП, позволяет понять метаболические потребности кардиомиоцитов предсердий при различных типах сердечного ритма, а также диагностировать активный воспалительный процесс в сердечной мышце.
В последние годы повышенное внимание уделяется РФЛП для ПЭТ/КТ на основе ингибиторов белка активации фибробластов FAPI, меченного радиоизотопами [ 18F] или [ 68Ga], которой экспрессируется на мембранах активированных фибробластов. В доступной литературе обнаружена только одна публикация, в которой оценивалась возможность использования ПЭТ/КТ-визуализации с использованием [ 18F]-FAPI для оценки активированных фибробластов в предсердиях при ФП и выявления факторов, способствующих повышенной активности фибробластов в предсердиях [22]. У всех экспериментальных животных с моделью ФП и у 18 (64,3%) пациентов с мерцательной аритмией отмечалась гиперфиксация [ 18F]-FAPI в миокарде предсердий. В образцах ткани предсердий экспериментальных животных отмечен повышенный уровень мРНК FAP (r=0,98, P=0,002) и FAP (r=0,82, P=0,03), а также гиперэкспрессия мРНК коллагена I (r=0,85, P=0,02), которые находились в прямой корреляционной зависимости с интенсивностью накопления¹⁸F-FAPI в предсердиях [23].
Не уменьшается интерес к возможностям оценки симпатической иннервации сердца с помощью радиоизотопных методов при мерцательной аритмии. Экспериментальные и клинические исследования показали, что внутренняя автономная нервная система сердца играет важную роль в инициации и поддержании ФП. Оценку общей и региональной симпатической иннервации миокарда выполняют с помощью радиоизотопных технологий: сцинтиграфии и ОФЭКТ сердца с [ 123I]-МИБГ. Данный РФЛП является структурным аналогом медиатора норадреналина и отражает процессы его обратного захвата и ретенции в симпатических нервных окончаниях [24]
Накопленный мировой опыт использования ОФЭКТ сердца с [ 123I]-МИБГ демонстрирует высокую релевантность этой технологии в отношении оценки прогноза у пациентов с пароксизмальной формой ФП, определения исходов катетерной аблации, а также оценки денервации и реиннервации миокарда левого желудочка после интервенционного лечения2 [25-28].
У пациентов с пароксизмальной формой ФП и без структурных заболеваний сердца снижение отсроченного индекса «Сердце/Средостение» как маркера нарушения автономной иннервации сердца оказалось предиктором неблагоприятных сердечно-сосудистых событий: инфаркта миокарда, инсульта или СН, в течение среднего периода наблюдения 4,5 года [25]. Авторами сделан вывод о диагностической ценности сцинтиграфии сердца с [ 123I]-МИБГ в отношении клинической стратификации риска, тем не менее для включения этой стратегии в клинические рекомендации необходимы дополнительные данные многоцентровых исследований.
В исследовании Никитина Н. А. (2024) установлено, что индекс накопления [ 123I]-МИБГ в миокарде на отсроченной серии и скорость вымывания РФЛП являются значимыми независимыми предикторными показателями риска рецидива предсердных тахиаритмий после интервенционного лечения ФП2.
Учеными Томского НИМЦ кардиологии разработана медицинская технология «Способ прогнозирования эффективности катетерного лечения ФП на основе оценки динамики симпатического и парасимпатического тонуса вегетативной нервной системы миокарда», направленная на повышение эффективности катетерного лечения постоянной формы ФП путем оптимизации отбора пациентов для выполнения данной процедуры [29]. Отбор пациентов ФП перед выполнением радиочастотной аблации основан на результатах планарной сцинтиграфии сердца с [ 123I]-МИБГ, и при значении раннего индекса «Сердце/Средостение» <1,7, отсроченного индекса «Сердце/Средостение» <1,69 и скорости вымывания РФЛП >13,5% прогнозируется развитие рецидива ФП через год после радиочастотной аблации.
Известно, что в эпикардиальной жировой клетчатке предсердий локализованы ганглионарные сплетения, содержащие как симпатические, так и парасимпатические нервы. Ганглионарные сплетения сосредоточены в области задней стенки ЛП и вокруг устьев легочных вен, имеют вариабельные размеры — 5—10 мм [30][31].
Катетерная аблация ганглионарных сплетений в дополнение к аблации устьев легочных вен или даже изолированно у пациентов с ФП, по сообщениям ряда исследователей, улучшает клинические результаты [32][33]. А наличие остаточной активности ганглионарных сплетений после аблации устьев легочных вен может служить предиктором вероятности рецидива мерцательной аритмии [34].
Было высказано предположение, что неинвазивная оценка иннервации ЛП может идентифицировать ганглионарные сплетения как области фокального накопления [ 123I]-МИБГ на эпикардиальной поверхности ЛП, что потенциально может служить навигацией для процедур катетерной аблации.
В исследовании Stirrup J, et al. (2020) сообщается о первом опыте визуализации ганглионарных сплетений ЛП с помощью ОФЭКТ/КТ с [ 123I]-МИБГ [35]. Авторами подробно описаны методы получения и интерпретации сцинтиграфических изображений, а также результаты обследования пациентов с ФП, включая оценку внутриисследовательской и межисследовательской вариабельности данных. В этом пилотном исследований отмечено, что размер и распределение ганглионарных сплетений индивидуальны и поэтому для обеспечения эффективности катетерной аблации необходима анатомическая навигация с помощью ОФЭКТ/КТ с [ 123I]-МИБГ.
Заключение
В заключение следует отметить, что прогресс в области радионуклидной визуализации во многом обусловлен техническими достижениями в разработке современной диагностической аппаратуры — ОФЭКТ и ПЭТ сканеров, совмещенных с компьютерным и магнитно-резонансным томографами и развитием радиофармацевтики. Использование совмещенных диагностических систем позволяет в рамках одного исследования изучить анатомо-топографические особенности сердца, выявить нарушения коронарной микроциркуляции, оценить особенности метаболизма и иннервации сердечной мышцы, а также определить локализацию ганглионарных сплетений предсердий. Комплексное использование современного диагностического оборудования и новых радиофармацевтических препаратов открывает широкие перспективы для определения новых клинических показаний в области диагностики, патофизиологии, более точной оценки прогноза сердечно-сосудистых заболеваний.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Рыжкова Д. В. Позитронная эмиссионная томография в комплексной диагностике ишемической болезни сердца: дис… докт. мед. наук: 14.01.13. Томск, 2008: 342 с.
2. Никитин Н. А. Оценка состояния автономной нервной системы сердца и персонифицированный подход к катетерной аблации фибрилляции предсердий с помощью совмещенной 123I-МИБГ ОФЭКТ/КТ. Диссертация на соискание ученой степени кандидата медицинских наук. Новосибирск, 2024г. 96 С.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Рыжкова Д.В., Карпова О.В. Радионуклидные методы диагностики при фибрилляции предсердий (обзор). Российский кардиологический журнал. 2025;30(4S):6707. https://doi.org/10.15829/1560-4071-2025-6707. EDN: DQEYMG
Скопировать