Персональный мониторинг симптомов и приверженности к терапии при фибрилляции предсердий
Аннотация
В связи с высокой распространенностью фибрилляции предсердий (ФП), в т.ч. ее субклинических форм, все большее значение приобретает поиск новых подходов к скринингу данной аритмии, мониторингу симптомов, а также эффективных способов контроля приверженности к терапии. Наряду с имплантируемыми мониторами для диагностики ФП используются современные цифровые методы персонализированного контроля ритма: беспроводные регистраторы, смарт-устройства, мобильные помощники и другие технологии. В работе проведен сравнительный анализ наиболее распространенных методов персонального мониторинга при ФП, разработанных с целью оценки динамики заболевания, контроля симптомов и профилактики осложнений. Также рассматриваются современные технологии повышения приверженности к терапии в различных клинических группах пациентов. Представлены собственные результаты по разработке проекта мобильного приложения для пациентов с ФП.
На современном этапе развитие цифровых технологий открывает значительные возможности для оптимизации медицинской помощи пациентам, проведения научных исследований и накопления новых клинических данных, в т.ч. в области кардиологии. Безусловно, при внедрении новых персональных информационных технологий в клиническую практику, несмотря на их потенциал, следует серьезно отнестись к вопросам обеспечения надлежащего качества данных, конфиденциальности и соответствия действующим нормативным требованиям регулирующих органов. В широком смысле «смарт-технологии» в современном здравоохранении можно охарактеризовать как принципы использования цифровой информации, данных и технологий связи для сбора, обмена и анализа медицинской информации в целях улучшения здоровья пациентов и качества оказания медицинской помощи в различных сферах [1]. Отдельно выделяется «мобильное здравоохранение», представляющее собой медицинскую клиническую практику и практику общественного здравоохранения, основанную на данных мобильных устройств, включая мобильные телефоны, портативные мониторы, персональные цифровые помощники и другие беспроводные устройства [2].
В современной кардиологии существует несколько перспективных направлений применения технологий цифрового здравоохранения, прежде всего, в отношении повышения точности диагностики, улучшения комплаентности пациентов с нарушениями ритма, а также достижения эффективного контроля симптомов, оценки прогрессирования заболевания и своевременного выявления и профилактики возможных осложнений. Наиболее ярким примером является персональный мониторинг фибрилляции предсердий (ФП), который реализуется с помощью различных цифровых инструментов на популяционном и индивидуальном уровне. Важно подчеркнуть, что ФП, являющаяся наиболее распространенной патологической аритмией, остается одной из основных глобальных причин развития инсульта, сердечной недостаточности, деменции, а также способствует увеличению уровня инвалидизации и смертности вследствие сердечно-сосудистых причин [3]. Кроме того, в настоящее время эффективность контроля осложнений ФП может быть лимитирована низким уровнем выявления ее бессимптомных форм, а также несоблюдением врачебных рекомендаций и нерегулярным режимом приема терапии, особенно у пожилых пациентов [4-6]. Тем более актуальным представляется изучение возможных областей применения персонализированных цифровых подходов с целью повышения эффективности лечения пациентов с ФП за счет улучшения их комплаентности и более строго контроля симптомов аритмии.
Цифровые возможности скрининга ФП
Нужно отметить, что оценка реальной распространенности пароксизмальной ФП является сложной задачей, т.к. эпизоды аритмии могут быть кратковременными, абсолютно бессимптомными и трудно выявляемыми с помощью привычных методов диагностики. Помимо стандартной регистрации поверхностной электрокардиограммы (ЭКГ) в 12 отведениях в момент приступа аритмии (в случае ее сипмтомности), рекомендованные способы мониторинга будут различаться в зависимости от частоты возникновения клинических проявлений (табл. 1).
Таблица 1
Рекомендуемые методы скрининга ФП (адаптировано из [7])
|
Частота симптомов |
Рекомендуемая технология |
|
Ежедневно |
24-ч холтеровское мониторирование ЭКГ |
|
Несколько раз в неделю |
48-72-ч холтеровское мониторирование ЭКГ |
|
Еженедельно |
7-дневное холтеровское мониторирование ЭКГ или беспроводной регистратор ЭКГ (патч-монитор) |
|
Ежемесячно |
14-30-дневное мониторирование с помощью беспроводных регистраторов ЭКГ (патч-мониторов) |
|
Реже одного раза в месяц |
имплантируемый монитор ЭКГ (регистратор событий) |
Сокращение: ЭКГ — электрокардиограмма.
Недостаточная выявляемость ФП в реальной практике отражает серьезную клиническую проблему, т.к., по данным недавних исследований, асимптомная форма независимо ассоциируется с более высоким риском прогрессирования по сравнению с симптомной ФП (отношение рисков 1,6, 95% доверительный интервал: 1,1-2,2) [7-9]. Причем по мере увеличения периода наблюдения (от 5 до 10 лет) у значительной доли бессимптомных пациентов отмечается прогрессия в хроническую ФП с частотой 25% для пароксизмальной формы и 50% для персистирующей формы аритмии, соответственно [10][11]. Это особенно важно учитывать при анализе данных различных обсервационных обследований, где распространенность бессимптомной ФП широко варьирует и, главным образом, зависит от интенсивности наблюдения и используемых систем мониторинга. К примеру, методы низкой диагностической интенсивности включают регистрацию ЭКГ в покое, суточное мониторирование и неинвазивные регистраторы событий с расчетной частотой выявляемости асимптомных форм ФП около 10-40%. В свою очередь, к высокоинтенсивным методам выявления нарушений ритма относятся имплантируемые мониторы для регистрации событий, и именно они позволяют диагностировать бессимптомные эпизоды ФП более, чем у 50% пациентов [8][9]. Важным преимуществом имплантируемых регистраторов является возможность длительного мониторинга ЭКГ (до нескольких лет), высокая чувствительность к выявлению коротких или бессимптомных рецидивов ФП с их автоматической детекцией, хранение ЭКГ данных и опция дистанционного контроля, обеспечивающая обратную связь врача и пациента (рис. 1).
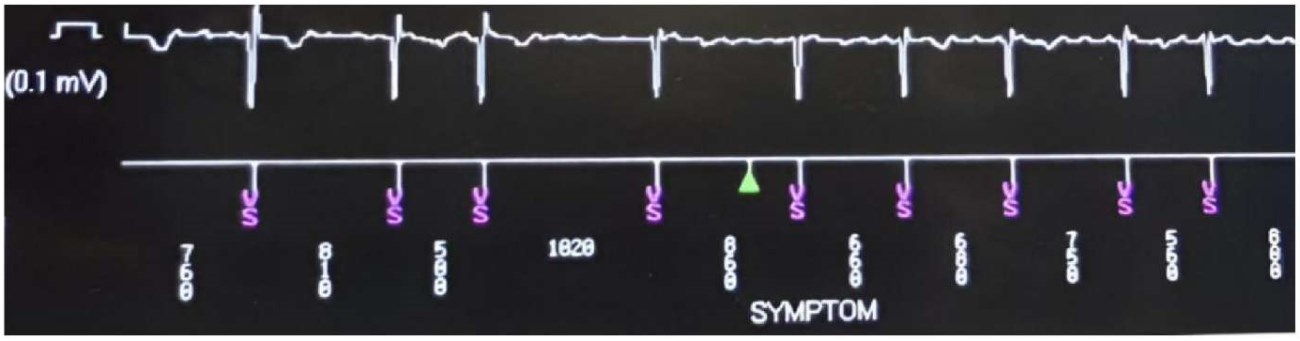
Рис. 1. Выявление ФП по данным имплантируемого монитора ЭКГ.
Примечание: маркер SYMPTOM отражает активацию записи пациентом во время возникновения симптомов аритмии (фото из личного архива авторов).
На современном этапе высока роль других имплантируемых внутрисердечных электронных устройств (кардиостимуляторы, дефибрилляторы и другие), которые могут достоверно выявлять асимптомные предсердные нарушения ритма, определяя их как эпизоды ускоренного ритма предсердий (УРП) с высокой частотой, когда частота сокращений предсердий за определенный промежуток времени превышает запрограммированную пороговую частоту обнаружения [12] (рис. 2).

Рис. 2. Регистрация УРП по данным имплантированного двухкамерного стимулятора.
Примечание: маркерный канал отражает интерпретацию внутрисердечных электрограмм устройством: А — регистрация предсердных событий (частота 307 в минуту), V — регистрация желудочковых событий (частота 105 в минуту), AS — детектируемое спонтанное предсердное событие, VS — детектируемое спонтанное желудочковое событие, VР — стимулируемое желудочковое событие (фото из личного архива авторов).
Выявление подобных эпизодов УРП в дальнейшем может повлиять на выбор оптимального алгоритма терапии и профилактики осложнений, т.к. наличие кратковременных периодов УРП (>5-6 мин) ассоциируется с более высоким риском инсульта и системных эмболий [13][14]. С другой стороны, у ряда пациентов с УРП и эмболическими событиями механизм инсульта может оставаться неясным, если осложнение возникает на фоне четкого синусового ритма, что требует дальнейшего изучения и поиска дополнительных диагностических предикторов. Но тем не менее эти эпизоды, по-видимому, являются постоянным маркером риска тромбоэмболических осложнений, каким бы ни был конечный механизм [15]. Таким образом, эпизоды УРП, выявляемые при помощи различного рода имплантируемых электронных устройств и мониторов, до настоящего времени представляют собой «серую зону», в которой отсутствуют рекомендации и четкие алгоритмы по управлению тактикой ведения пациентов, особенно в плане антикоагулянтной профилактики. В любом случае, во всех текущих клинических исследованиях было установлено, что чем дольше проводится мониторирование сердечного ритма с помощью мобильных или имплантированных цифровых регистраторов у пациентов с факторами риска, тем больше бессимптомных эпизодов ФП выявляется с течением времени, и эти эпизоды достоверно ассоциируются с более высоким риском эмболических событий. В будущем ожидается, что результаты регистров APTECиА (прием апиксабана для снижения риска тромбоэмболий у пациентов с субклинической ФП, обнаруженной с помощью цифровых устройств; NCT01938248) и NOAH (прием пероральных антикоагулянтов, не являющихся антагонистами витамина К, у пациентов с эпизодами УРП; NCT026185) предоставят доказательства по выбору оптимального алгоритма ведения пациентов с неустойчивой бессимптомной ФП. Но тем не менее до получения будущих достоверных доказательных данных на современном этапе практические подходы к лечению при наличии эпизодов УРП по результатам статистики цифровых устройств должны быть основаны на определении индивидуальных факторов риска пациентов с учетом расчетных показателей шкалы CHA2DS2-VASc [8][16][17].
На современном этапе, согласно действующим клиническим рекомендациям, для постановки диагноза ФП необходима регистрация эпизода аритмии с типичными ЭКГ критериями в 12 отведениях или записи длительностью ≥30 сек на устройствах ЭКГ с одним или несколькими отведениями [17]. Учитывая высокую актуальность использования инструментов цифрового здравоохранения в клинической практике, ФП все чаще выявляется при проведении мобильного скрининга. До настоящего времени рекомендуемая длительность регистрации аритмии на цифровых устройствах, необходимая для постановки диагноза ФП, не является четко определенной. Наиболее актуальными остаются границы длительности ФП ≥10 сек для стандартной записи ЭКГ в 12 отведениях и ≥30 сек для устройств ЭКГ с одним или несколькими отведениями.
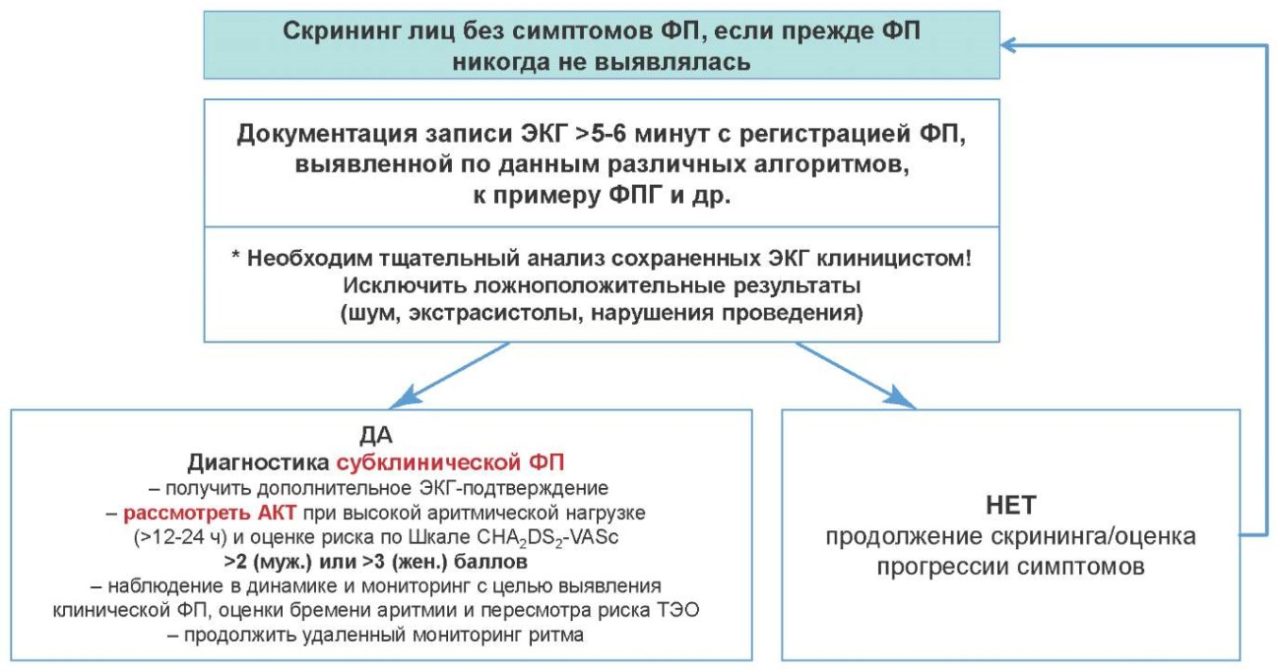
В течение последних нескольких лет широко обсуждается правомочность принятия клинических решений и, прежде всего, инициации антикоагулянтной терапии на основании записи ФП, полученной в одном ЭКГ-отведении. Еще в 2023г отдельными экспертными документами регламентировалась подобная возможность, но только после тщательной оценки ЭКГ клиницистом, верификации ФП по необходимым критериям и на основании расчета индивидуального тромбоэмболического риска пациентов (рис. 3) [18].
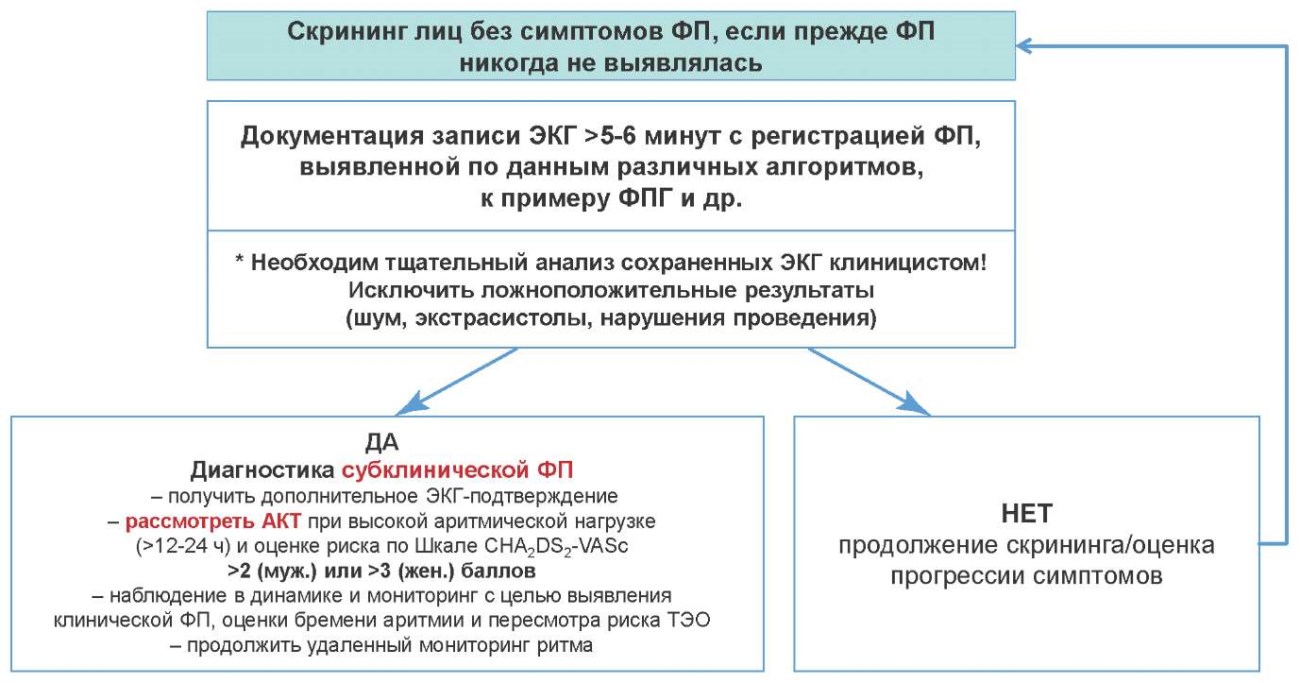
Рис. 3. Алгоритм ведения пациентов с ФП, выявленной по данным персональных цифровых устройств. Адаптировано из [18].
Сокращения: АКТ — антикоагулянтная терапия, ТЭО — тромбоэмболия легочной артерии, ФП — фибрилляция предсердий, ФПГ — фотоплетизмография, ЭКГ — электрокардиограмма.
В новых клинических рекомендациях вопрос рассматривается не так однозначно. С одной стороны, раннее обнаружение ФП позволяет своевременно начать антикоагулянтную терапию, существенно снизив вероятность инсульта и других сосудистых событий, что особенно актуально в группах высокого риска: пожилой возраст, сопутствующая артериальная гипертензия, хроническая сердечная недостаточность и т.д. Но в то же время до конца не изучены исходы при раннем начале приема антикоагулянтов в случаях, когда пароксизмы ФП являются недлительными, а пациенты имеют низкий риск по шкале CHA2DS2-VASc [17].
Важно отметить, что эффективность современных методов цифрового скрининга ФП является неодинаковой. Ниже будут описаны преимущества и недостатки каждого способа персонального мониторинга ритма. Но несмотря на потенциальные ограничения, оптимальную тактику скрининга (в т.ч. с комбинацией нескольких диагностических методов) следует выбирать исходя из целей мониторинга, характера и выраженности клинических симптомов, а также с учетом ресурсов пациента и врача в каждом случае индивидуально.
Устройства для персонального мониторинга ЭКГ на основе «умных часов»
В последние годы, помимо стандартных моделей применения диагностических мобильных приложений в кардиологии, развитие смарт-технологий позволило начать разработку цифровых аксессуаров для регистрации ритмограммы с помощью «умных часов». Исторически первым среди всех производителей стал проект Kardia Band — цифровой аксессуар, реализованный в последних моделях Apple Watch, получивший одобрение ассоциации FDA и позволяющий регистрировать запись, эквивалентную стандартному отведению ЭКГ в течение 30 сек с мгновенным анализом ритма при помощи автоматических алгоритмов (рис. 4). Зарегистрированные данные при необходимости могут быть немедленно переданы для удаленного анализа и контроля квалифицированному специалисту телемониторинга, что позволит своевременно вносить коррекции в тактику ведения пациентов. Данная технология была протестирована на примере достаточно большой выборки пациентов с ФП, которым предстояла плановая электрическая кардиоверсия [19]. В данной ситуации применение приложения Kardia Band позволило получать на регулярной основе актуальную информацию о состоянии ритма пациентов, что нередко помогало избежать ненужных госпитализаций в стационар и снизить незапланированные расходы на лечение за счет того, что спонтанная конверсия в синусовый ритм была четко и своевременно выявлена во всех случаях [19]. Расчетные статистические показатели чувствительности и специфичности метода в выявлении ФП составили 93% и 84%, соответственно.
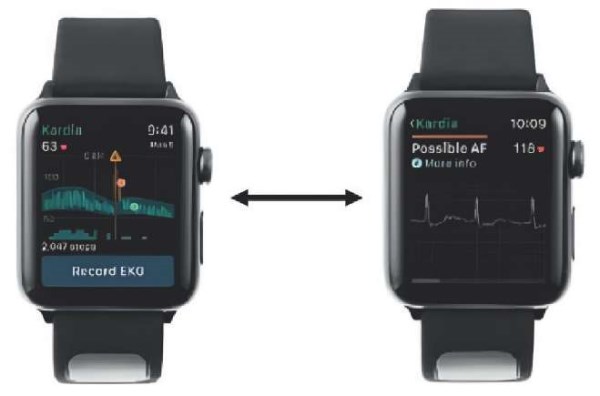
Рис. 4. Приложение Kardia Band для регистрации ЭКГ (Alivecor, Inc., США). Адаптировано из [19].
Регистрация частоты сердечных сокращений с помощью «умных часов», в которых реализована технология оптической фотоплетизмографии — это удобный и доступный способ мониторинга сердечного ритма в повседневных условиях. В большинстве подобных устройств есть встроенная функция определения ЭКГ в одном отведении (как правило, эквивалент I стандартного ЭКГ отведения) с активацией записи при прикосновении к металлическому датчику (например, к коронке или боковой поверхности часов). Время записи может варьировать от нескольких секунд до минуты. Полученные данные анализируются автоматически и отображаются на экране или в мобильном приложении. Несмотря на неоспоримые преимущества использования «умных часов» для регистрации ритма (удобство, портативность, доступность мгновенной записи ЭКГ, возможность сохранения результатов в личном кабинете для последующего анализа), есть и потенциальные ограничения. Прежде всего, это довольно высокая стоимость, т.к. только определенные модели часов из общей линейки, представленной на рынке, имеют подобный расширенный функционал с опцией ЭКГ-диагностики. Кроме того, при регистрации ЭКГ в одном отведении возможна гипердиагностика ФП за счет ошибок автоматического анализа и интерпретации сердечного ритма у пациентов с нерегулярными RR интервалами (на фоне экстрасистолии, транзиторных нарушений атриовентрикулярного проведения и т.д.) или при наличии шумов и помех на ЭКГ. Ниже приводится сравнение двух записей ЭКГ у одного и того же пациента, зарегистрированных на фоне пароксизма ФП (рис. 5 А) и на фоне синусового ритма с частой предсердной экстрасистолией (рис. 5 Б).
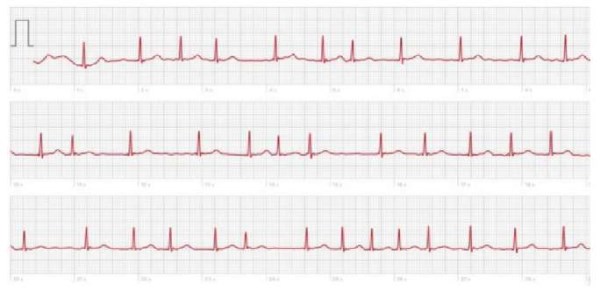
Рис. 5 А. Диагностика ФП по данным «умных часов» в одном отведении.
Примечание: регистрируются низкоамплитудные волны f, нерегулярные RR интервалы и отсутствуют волны Р (фото из личного архива авторов).
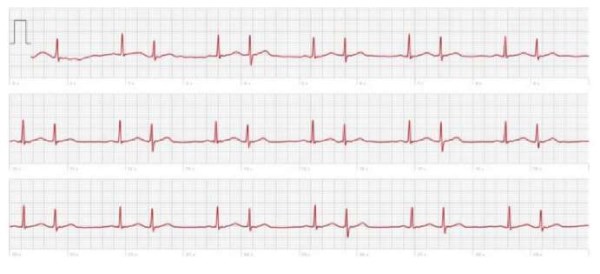
Рис. 5 Б. Ложноположительная диагностика ФП по данным «умных часов» в одном отведении.
Примечание: регистрируются нерегулярные RR интервалы за счет частой предсердной экстрасистолии на фоне нормального синусового ритма (фото из личного архива авторов).
На основании указанных ограничений можно сделать вывод, что во всех случаях при использовании смарт-часов для скрининга ФП окончательную интерпретацию ЭКГ необходимо доверять клиницисту, и принятие последующих тактических решений должно выполняться только после тщательного анализа данных с учетом индивидуальных характеристик пациента.
Портативные беспроводные регистраторы ЭКГ
Следующим этапом развития цифровых технологий, позволяющих проводить скрининг ФП и других нарушений ритма вне стен медицинского учреждения, стало внедрение портативных беспроводных ЭКГ-регистраторов. Основным преимуществом при их использовании является неинвазивность, простота применения, достаточно хорошая точность мониторинга, а также доступная стоимость. Данные компактные устройства популярны как для повседневного самоконтроля, так и для профессиональной диагностики, к примеру, после выполнения катетерной аблации ФП или в рамках поиска недиагностированных причин криптогенных ишемических инсультов [20-22]. Важным и перспективным направлением является применение одноканальных беспроводных регистраторов в кардиоонкологии, к примеру, для оценки кардиотоксичности или выявления субклинических признаков диастолической дисфункции левого желудочка у пациентов, получающих различные схемы полихимиотерапии [23][24]. Для беспроводной передачи данных используется технология Bluetooth или Wi-Fi, позволяющая осуществлять связь со смартфонами, планшетами или компьютерами (рис. 6).1

Рис. 6. Цифровой беспроводной регистратор ЭКГ КардиоКарта (из открытых источников)1.
Традиционно, для регистрации ЭКГ требуется ручная активация со стороны пациента во время жалоб на перебои в работе сердца, что почти полностью исключает вероятность регистрации асимптомных эпизодов аритмии. Кроме того, среди потенциальных недостатков можно выделить отсутствие возможности непрерывного длительного мониторинга ЭКГ, а также, по аналогии с другими портативными одноканальными регистраторами, вероятность «ложноположительных результатов» и гипердиагностики. Нужно отметить, что у большинства цифровых устройств для контроля ритма отсутствует классификация других нарушений ритма, помимо ФП, т.е. адекватная диагностика блокад синоатриального или атриовентрикулярного проведения, предсердной или желудочковой эктопии или оценка ритма электрокардиостимулятора на протяжении длительного периода времени была невозможной. Однако в последние годы производители разрабатывают новые алгоритмы, применяя в т.ч. методы машинного обучения и другие возможности, которые позволяют повысить точность диагностики и улучшить дискриминацию нарушений ритма даже в беспроводных приборах с одним ЭКГ отведением (рис. 7 А, Б).
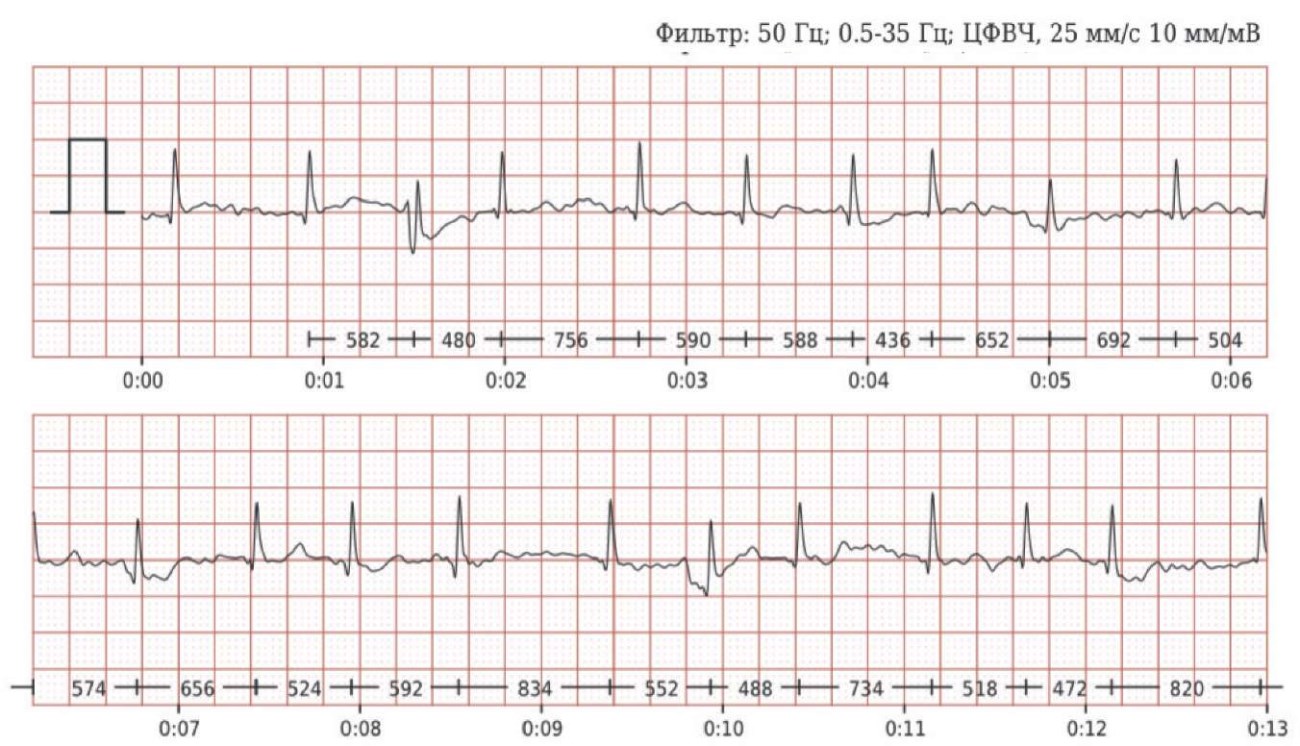
Рис. 7 А. Диагностика ФП по данным беспроводного регистратора КардиоКарта в одном отведении.
Примечание: регистрируются низкоамплитудные волны f, нерегулярные RR интервалы и отсутствуют волны Р (фото из личного архива авторов).

Рис. 7 Б. Работа алгоритмов дискриминации желудочковой эктопии у пациента с жалобами на нарушения ритма при использовании беспроводного регистратора КардиоКарта в одном отведении.
Примечание: несмотря на нерегулярность RR интервалов, ритм автоматически классифицируется как синусовый с частой желудочковой экстрасистолией (фото из личного архива авторов).
Проводные портативные регистраторы ЭКГ
Среди средств персонального мониторинга при ФП отдельно рассматривается использование проводных портативных регистраторов ЭКГ с возможностью хранения и передачи данных, которые сочетают в себе точность классических электродных измерений с мобильностью современных цифровых устройств (рис. 8).

Рис. 8. Цифровой проводной регистратор ЭКГ Кардиофлешка ECG Dongle (из открытых источников).2
За счет наличия дополнительных электродов подобные устройства регистрируют шесть стандартных отведений ЭКГ, что значительно повышает точность диагностики и позволяет проводить корректную дискриминацию выявленных нарушений ритма и проводимости. Основным ограничением является удлинение времени подготовки к регистрации ЭКГ (за счет необходимости наложения нескольких электродов на грудную клетку), особенно у пациентов с ограниченными возможностями, когнитивным дефицитом, в т.ч. после перенесенного инсульта, в пожилом возрасте, а также при коротких приступах аритмии (<5 мин). Из преимуществ можно отметить высокое качество записи и фильтрации ЭКГ сигнала за счет снижения уровня шумов и посторонних воздействий в сравнении с распространенными одноканальными портативными регистраторами. В ценовом сегменте подобные проводные устройства занимают среднюю нишу и являются значительно более доступными, чем смарт-часы последних моделей, но обычно превышают по стоимости одноканальные ЭКГ мониторы.
Носимые патч-мониторы ЭКГ
Неоспоримым преимуществом носимых беспроводных ЭКГ регистраторов является возможность их применения для длительного непрерывного мониторинга ритма, что особенно ценно при бессимптомной ФП, не сопровождающейся яркими клиническими проявлениями. Кроме того, подобные устройства мобильны, компактны и не требуют использования проводов и коннекторов, т.к. накожные электроды ЭКГ крепятся, как правило, непосредственно к корпусу регистратора (рис. 9).
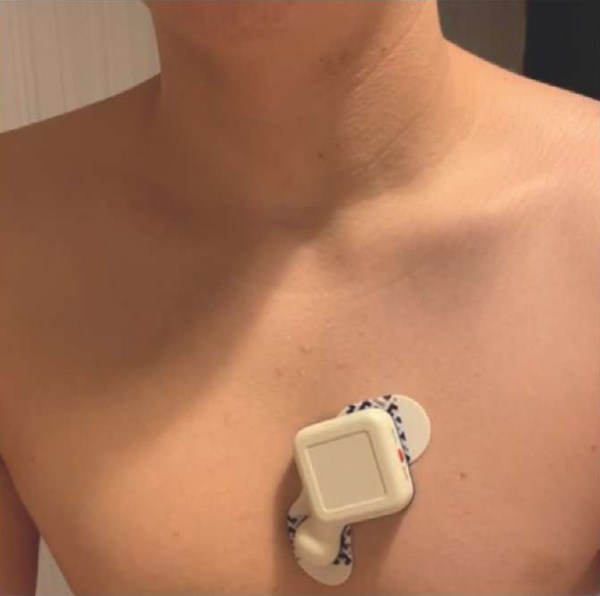
Рис. 9. Цифровой беспроводной патч-монитор «Светлячок» для регистрации ЭКГ (фото из личного архива авторов).
Помимо регистрации ЭКГ в течение заданного периода времени, большинство носимых мониторов имеют возможность онлайн-контроля и последующей передачи данных для хранения на компьютере или мобильном устройстве. Пример дистанционного мониторинга как наиболее эффективного решения у пациентки с персистирующей формой ФП для оценки ритма на фоне медикаментозной кардиоверсии представлен на рисунке 10.2

Рис. 10. Фрагмент записи данных беспроводной системы мониторирования ЭКГ Doctor Spyder — восстановление синусового ритма в ходе медикаментозной кардиоверсии у пациентки с ФП (фото из личного архива авторов).
Важно, что носимые регистраторы ЭКГ можно использовать для раннего выявления бессимптомных форм ФП у пациентов высокого риска, что позволяет вовремя начать профилактическое лечение, снизить риск инсульта и улучшить качество жизни пациентов. В условиях возрастания заболеваемости и социально-экономической нагрузки это направление приобретает все большую значимость в современной кардиологии.
Будущие перспективы персонального мониторинга ФП
В настоящее время область внедрения виртуальных медицинских технологий стремительно увеличивается. В недалеком будущем ожидается значительный прогресс в отношении методологии и практических подходов, реализуемых в условиях цифрового здравоохранения (включая применение новых беспроводных гаджетов, умного текстиля, систем для видеомониторинга, носимых регистраторов и средств удаленного контроля симптомов) с целью оценки состояния здоровья пациентов. Получает все большее развитие концепция создания «цифрового двойника», которая позволяет создать полностью идентичную реальным данным симуляционную модель пациента с целью прогнозирования вероятного ответа на предстоящее оперативное вмешательство, выбора оптимальной тактики и моделирования возможных клинических исходов при различных вариантах лечения [25][26].
Несомненно, со временем прогресс в области инновационных технологий будет только продолжаться, и создание различных цифровых инструментов будет иметь большое значение в развитии клинической медицины, значительно повышая точность диагностики, эффективность лечения и качество мониторинга пациентов с сердечно-сосудистыми заболеваниями.
Цифровые инструменты контроля приверженности к терапии у пациентов с ФП
Известно, что низкая приверженность к лечению является общемировой проблемой огромной значимости, что подтверждается в последних отчетах Всемирной организации здравоохранения на протяжении уже нескольких лет [27]. Это одна из основных причин прогрессирования и сохраняющегося высокого уровня смертности больных с сердечно-сосудистой патологией, и в т.ч. среди пациентов с нарушениями ритма. Установлено, что только 50% пациентов, имеющих хронические заболевания, привержены к лечебным рекомендациям, что значительно снижает эффективность терапии. Для пациентов с ФП строгий контроль соблюдения врачебных рекомендаций является критически важным, т.к. высокая приверженность положительно влияет на выживаемость, сопровождается снижением риска осложнений и позволяет прогнозировать успешное достижение основных целей лечения, регламентированных действующими клиническими рекомендациями [17].
С момента первого упоминания понятия «комплаентности» или «приверженности к терапии» определение перетерпело ряд изменений, но при этом сохранив основной смысл, характеризующий данный клинический термин. Как правило, под приверженностью к терапии понимают точное выполнение пациентом всех врачебных рекомендаций назначений в рамках профилактики, лечения заболевания и реабилитации. Другое определение характеризует приверженность к лечению как согласие пациента следовать рекомендациям врача. Официальное определение Всемирной организации здравоохранения описывает комплаентность или приверженность к терапии как степень соответствия поведения пациента в отношении применения лекарства, выполнения рекомендаций по питанию или изменению образа жизни назначениям и указаниям врача3. Высокая приверженность к лечению проявляется открытым сотрудничеством врача и пациента, свободным обсуждением всех возможных аспектов лечения (не только медикаментозного), а также индивидуальных особенностей и затруднений, возникающих в его процессе [28].
Для пациентов с ФП, получающих медикаментозную терапию, если принять комплайнс приема препарата (КПП) как отношение количества принятых доз к надлежащему количеству назначений, выраженное в процентах, хорошая приверженность будет характеризоваться показателями, близкими к 90-100%. Но, к сожалению, в клинической практике часто наблюдаются так называемые периоды «лекарственных каникул», когда показатель КПП значимо снижается, и, напротив, возможно встретить не менее опасное состояние передозировки препарата, если показатель КПП превышает 100%, что возможно только в случае ошибочного одновременного приема сразу нескольких дозировок. На современном этапе можно выделить основные категории факторов, которые будут оказывать наиболее значимое влияние на восприятие пациентом процесса лечения и согласие с рекомендованными врачебными предписаниями (табл. 2).
Таблица 2
Группы факторов, влияющих на комплайнс (Всемирная организация здравоохранения, 2003)3
|
Категории фактора |
Зоны влияния |
|
Социальные и экономические |
Финансовое положение |
|
Системные (связанные с системой здравоохранения) |
Отношения «Врач — Пациент» |
|
Связанные с болезнью |
Степень тяжести симптомов |
|
Обусловленные терапией |
Сложность режима |
|
Обусловленные особенностями пациента |
Страх перед нежелательными побочными эффектами |
Учитывая анализ основных причин снижения приверженности к терапии, очень часто встречающихся и среди кардиологических пациентов, имеющих нарушения ритма, можно предположить основные направления воздействия, которые помогут повысить комплаентность к соблюдению врачебных рекомендаций. Прежде всего, к ним относится развитие образовательных проектов, включающих адекватное и доступное обучение, информирование и консультирование пациентов, особенно групп риска недостаточной приверженности. Далее возможно воздействие на поведение пациента различными способами, имеющими общую направленность на коррекцию режима приема препаратов: специальные устройства, напоминающие о необходимости приема лекарств, индивидуальные упаковки с таймером на неделю или на курс лечения и прочие технологии.
Во всех случаях рекомендуется регулярный мониторинг комплаентности к терапии, основанный на анализе дневников по приему лекарств пациентами, содержащих также информацию по значимым показателям самочувствия и переносимости препаратов. Учитывая все большее внедрение цифровых технологий в кардиологии, подобные инструменты контроля приобретают в основном электронный формат, что делает еще более удобным анализ эффективности терапии. Завершающим фактором, влияющим на степень комплайнса на современном этапе, остается индивидуальная адаптация терапии в рамках персонализированного подхода для каждого пациента — прежде всего, упрощение сложных схем медикаментозного лечения, например перевод пациента на ретардные формы, комбинированные препараты и др. В подобных случаях имеет смысл упрощение режима терапии до максимально допустимого уровня с повторным мониторингом и обратной связью с пациентом для определения причины несоблюдения назначений и адекватного планирования последующего лечения.
Принципы оптимизации основных алгоритмов ведения пациентов с ФП во многом повторяют вышеизложенные рекомендации, где также реализуется структурированный комплексный пациент-ориентированный подход к терапии с учетом все большего внедрения цифровых технологий здравоохранения для достижения основных целей лечения: улучшения прогноза, снижения риска осложнений и повышения качества жизни пациентов [3][29][30].
На текущий момент методам технического воздействия на приверженность пациентов к терапии отводится особое внимание, наблюдается все большая их автоматизация и алгоритмирование с использованием современных компьютерных программ и мобильных приложений. Причем нужно отметить, что одновременное сочетание даже простых способов контроля приверженности к лечению позволяет добиться достоверного улучшения результата, в т.ч. за счет самоконтроля терапии [31].
Наиболее часто технические средства контроля комплаентности пациентов включают четыре основных типа смарт-устройств, имеющих различный функционал, но схожие цели и задачи применения (рис. 11).

Рис. 11. Методы технического воздействия на приверженность пациентов к терапии. Адаптировано из [32].
К относительно простым мероприятиям по улучшению комплаентности пациентов, нуждающихся в регулярном приеме антиаритмической медикаментозной терапии, можно отнести использование специальных электронных контейнеров для лекарств с микросчетчиком, расположенным на крыше используемого флакона (рис. 11 А). Это своеобразная технологическая крышка для стандартного пузырька, названная «GlowCap» (мигающий колпачок), выпускаемая вместе с беспроводным передатчиком, который включается в электрическую сеть. Когда наступает время принимать очередную дозу препарата, GlowCap мигает оранжевым светом; и при отсутствии реакции со стороны пациента спустя час начинает через каждые 5 минут подавать все более настойчивые звуковые сигналы. После этого, если пациент пропускает прием лекарства, устройство может отправить автоматическое сообщение на телефон или электронную почту. Оно также может генерировать электронные отчеты, сообщающие родственникам и членам семьи пациента или лечащему врачу, как пациент выполняет курс медикаментозного лечения. Для удобства слабовидящих пациентов и людей со снижением зрения на крышке может находиться шрифт Брайля, содержащий правила пользования счетчиком, при этом каждое открытие флакона также сопровождается голосовым сообщением или звуковым сигналом о необходимости принять лекарство, с информационным «окном» с указанием времени последнего открытия флакона. Подобные электронные микросчетчики показали свою эффективность не только в плане напоминания пациенту о приеме препарата, но и в плане оценки приверженности терапии, т.к. на приеме у врача представляется возможность анализа реального количества принятых таблеток из флакона с последующим принятием решения о необходимости коррекции режима лечения [32].
Следующим шагом по улучшению приверженности к длительной медикаментозной терапии является использование «умных» устройств для хранения и приема таблеток, которые представляют собой многосекционный электронный контейнер с отсеками для медикаментов разного типа (к примеру, антиаритмиков, препаратов неотложной помощи и антикоагулянтов) при условии указания периодичности их приема (рис. 11 Б). В установленное время устройство напоминает о необходимости принять лекарство, при этом после каждого приема одной дозы препарата счетчик обнуляется. Кроме этого, электронный контейнер «запоминает», когда пациент открывал крышку, чтобы взять таблетку, и может предоставлять все данные лечащему врачу, загружая их на удаленный сервер. Отдельные типы смарт-устройств для контроля комплаентности к терапии могут иметь установленное программное обеспечение, позволяющее подключаться к телефонной линии, контролировать время, дозировку и инструкции по приему до четырех различных видов медикаментов (с голосовыми и письменными напоминаниями для пациента) [33].
Свою нишу для применения имеют электронные боксы для таблеток с таймером приема лекарств (рис. 11 В). Часть из них одновременно сопровождается функцией регистрации пульсовой волны на специальном сенсоре, что облегчает задачу контроля симптомов параллельно с оценкой приверженности к терапии. Для оповещения о приеме таблеток необходимо положить их в электронный бокс для хранения и установить таймер на нужное время. Прибор имеет возможность установки до 5 «напоминаний» в день в виде звукового сигнала и/или вибрации, кроме того, предусмотрен повторный сигнал, если пациент не услышал или не отключил таймер. Имеется несколько отсеков для хранения различных медикаментов, функция блокировки кнопок, часы. Использование данного электронного прибора облегчает большой жидкокристаллический дисплей с крупными цифрами при относительно небольшом размере самого корпуса устройства, что может быть особенно важным для пожилых пациентов с нарушениями ритма [34].
Электронные аптечки с таймером позволяют, в свою очередь, обеспечить индивидуальное хранение лекарственных средств с постоянной функцией напоминания о своевременном приеме медикаментов, в то время как однократный цикл использования подобных устройств составляет, как правило, неделю без перерыва, а иногда более длительный период (рис. 11 Г). По истечении указанного периода цикл использования электронной аптечки повторяется с возможностью внесения изменений в режим дозирования препаратов. Прибор состоит из кассеты, в которую вкладываются семь контейнеров с четырьмя отделениями для таблеток, и блока цифрового таймера. С лицевой стороны на кассету нанесены названия дней недели, с обратной стороны расположены магниты для крепления к металлическим поверхностям. Пластиковые контейнеры имеют несколько отделений с маркировкой по времени суток. В необходимое время таймер подает оповещение в виде мигающего сигнала с подсветкой нужного номера отсека или отделения, из которого необходимо принять лекарство. Длительность сигнала составляет, как правило, одну минуту, но при отсутствии реакции со стороны пациента указанный цикл действий повторяется. Особенно актуально использование подобных электронных приборов у пациентов, получающих комплексные схемы терапии с включением антикоагулянтов, строго дозируемых по времени, контроль приема которых позволит снизить вероятность пропуска приема дозы или, напротив, передозировки препаратов, что соответственно повысит безопасность проводимой терапии [35].
Важным аспектом лечения пациентов с ФП и другими нарушениями ритма является обеспечение доступных технологий обратной связи пациента с лечащим врачом или специалистом телемедицинского отдела для получения подробных инструкций и алгоритмов действий в неотложных ситуациях или в случае ухудшения течения заболевания. Этот механизм может быть реализован путем телефонного консультирования, интернет-связи, электронных почтовых серверов, при использовании систем автоматизированного дозвона или с помощью функции отправляемых напоминаний, которые также могут представлять собой текстовые смс-сообщения или данные, передаваемые по электронной почте. В одном из крупных исследований было продемонстрировано, что уровень комплаентности к терапии значительно повышался, если существовала возможность еженедельного контакта пациентов с медицинским центром через компьютерную сеть. В ходе плановых сеансов связи пациенты через сайт сообщали лечащему врачу основные клинические и гемодинамические параметры, имеющиеся симптомы и побочные эффекты терапии, если они были. Далее на основании анализа полученной информации принималось решение о коррекции терапии либо необходимости очной консультации в тех случаях, когда это было целесообразно. После 6 мес. работы было зафиксировано достоверное повышение приверженности среди пациентов, включенных в программу, по сравнению с контрольной группой (р=0,03). Дальнейший анализ в пределах исследуемых подгрупп пациентов позволил сделать выводы, что наибольший прирост эффективности лечения наблюдался среди ранее не приверженных пациентов, что еще раз подчеркивает важность подобного комплексного подхода [36].
На современном этапе инструменты электронного здравоохранения продолжают изучаться в качестве вспомогательного средства для поддержки совместного принятия решений по многим режимам терапии у пациентов с ФП, включая параметры антикоагуляции, а также для обеспечения обратной связи на основе дистанционного мониторинга и, как следствие, повышения комплаентности и эффективности лечения [37].
Опыт создания мобильного приложения СМАРТ-ФП
В настоящее время на базе НИО аритмологии НМИЦ им В. А. Алмазова осуществляется разработка многофункционального мобильного приложения «СМАРТ-ФП», ориентированного на реализацию персонального подхода к лечению ФП4. Приложение предназначено для пользователей с ФП с целью контроля симптомов и динамики заболевания, прогнозирования и профилактики побочных эффектов и повышения эффективности лечения и улучшения прогноза пациентов (рис. 12).

Рис. 12. Содержание проекта мобильного приложения СМАРТ-ФП (фото из личного архива авторов).
Базовая версия мобильного приложения включает в себя следующие разделы:
— Приветствие от разработчиков;
— Согласие на обработку персональных данных;
— Аритмопедия: информация для пациентов по ФП, рискам эмболических осложнений и кровотечений, методам профилактики и лечения (антиаритмическая терапия, радиочастотная аблация, окклюдеры ушка левого предсердия, антикоагулянты, описания действия препаратов), рекомендации по видам лечения;
— Мои клинические данные (вес, рост, пол, частота сердечных сокращений, артериальное давление, фракция выброса левого желудочка, левое предсердие, частота пароксизмов/хроническая ФП, эпизоды транзиторной ишемической атаки и острого нарушения мозгового кровообращения, другие эмболии, ишемическая болезнь сердца, перенесенный инфаркт миокарда, кровотечения, алкоголь, нарушения функции почек, печени, сахарный диабет);
— Мои приложения:
- качество жизни (опросник EQ-5D), уровень физической активности, тест с шестиминутной ходьбой, шкала симптомов EHRA;
- дневник ритма (графики, хронокарты, бремя ФП, в зависимости от антиаритмической терапии, интервенции);
- оценка персональных рисков эмболических осложнений;
- оценка персональных рисков кровотечений;
- календарь событий;
- планировщик медикаментозной терапии с контролем выполнения (установка оповещения на смартфоне);
- контроль эффективности и безопасности терапии (лабораторные показатели –международное нормализованное отношение, оценка функции щитовидной железы (тиреотропный гормон), клинический анализ крови с подсчетом уровня гемоглобина и тромбоцитов, оценка функции почек (креатинин с расчетом скорости клубочковой фильтрации) в динамике);
- диагностика осложнений терапии (включая раздел самоконтроля признаков кровотечений (симптомы, лабораторные анализы) и непереносимости препаратов с описанием побочных явлений).
Приложение регулярно обновляется в соответствии с действующими рекомендациями и изменениями в клинических подходах к ведению пациентов с ФП.
Будущие перспективы развития проекта Смарт ФП включают возможность формирования «облачного хранилища» данных пациентов для хранения и дальнейшего применения в научных и практических целях, создание комплексного многоцелевого проспективного регистра пациентов с ФП и рабочей станции для врача-кардиолога (аритмолога) для динамического наблюдения за облачным хранилищем и ведения статистики. Среди общего пула пациентов с ФП возможно выделение групп, находящихся в зоне повышенного риска развития осложнений, с последующей разработкой клинических алгоритмов для их своевременного предотвращения. При выявлении лиц с низкой приверженностью к приему медикаментозных препаратов необходимо проведение мероприятий по ее улучшению, возможной коррекции терапии с контролем потенциальных побочных эффектов, а также своевременное направление на интервенционное лечение. Планируется потенциальная интеграция приложения с портативными беспроводными ЭКГ регистраторами, внедрение технологий активной «обратной связи» с пациентом, в т.ч. формирование чатов со специалистом и своевременное информирование о необходимости контрольного визита в клинику.
Заключение
Поскольку, согласно статистическим прогнозам, к 2030г распространенность ФП удвоится, необходимы четкие рекомендации и алгоритмы для ведения данной группы пациентов с возможностью своевременного персонализированного скрининга, самоконтроля симптомов и оценки безопасности и эффективности проводимой терапии. В рамках подобных алгоритмов цифровые приложения, мобильные устройства и другие инновационные инструменты представляются наиболее эффективным инструментом достижения намеченных результатов. Цифровые технологии трансформируют современную аритмологию, позволяя достичь более точной диагностики, делая лечение персонализированным, а последующее наблюдение — более удобным и доступным. В будущем ожидается дальнейшее развитие и интеграция технологий искусственного интеллекта, автоматизированных алгоритмов и персонализированных устройств для цифрового скрининга, что сделает управление аритмиями ещё более эффективным.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Цифровой беспроводной регистратор ЭКГ КардиоКарта. Медицинское изделие РУ МИ № РЗН 2024/22 855. https://www.cardioqvark.ru.
2. Цифровой проводной регистратор ЭКГ Кардиофлешка ECG Dongle. Медицинское изделие РУ МИ № РЗН 2019/8179. https://cardio-cloud.ru/good/kardiofleshka-ecg-dongle
3. Adherence to long-term therapies: evidence for action. World Health Organization 2003: 196р. https://iris.who.int/handle/10665/42682.
4. Лебедев А. Д., Лебедев Д. С., Гарькина С. В., Мухортова Т. З., Волков С. М., Щекутьева И. С. Самооптимизация антикоагулянтной терапии, динамики качества жизни и приверженности к терапии больных с фибрилляцией предсердий (СМАРТ-ФП). Свидетельство о регистрации программы для ЭВМ 2021660905, 05.07.2021. Заявка № 2021616632 от 30.04.2021.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Гарькина С.В., Оршанская В.С., Лебедев А.Д., Лебедев Д.С. Персональный мониторинг симптомов и приверженности к терапии при фибрилляции предсердий (обзор). Российский кардиологический журнал. 2025;30(4S):6772. https://doi.org/10.15829/1560-4071-2025-6772. EDN: FECJKJ
Скопировать