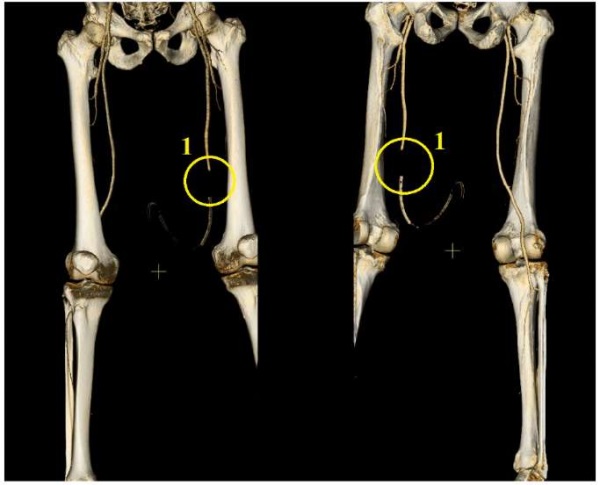
Морфологическое исследование сердца при фибрилляции предсердий. От патогенеза к лечению
Аннотация
Цель. Оценить влияние различных патологических процессов на патогенез фибрилляции предсердий (ФП).
Материал и методы. У 42 пациентов, умерших от различных заболеваний, измерялась толщина жировой клетчатки передней брюшной стенки, взвешивались сердца и предварительно удаленный эпикардиальный жир (ЭЖ), вычислялось отношение массы сердца к массе ЭЖ. Еще у 52 пациентов исследовался миокард из зон терминального гребня, пучка Бахмана, верхней и нижней части задней стенки левого предсердия между устьями легочных вен. У 17 из них была длительно персистирующая ФП, у 7 — пароксизмальная. Проводились иммуногистохимическое исследование (ИГХИ) с антителами к коллагенам I и III, к Isl1 и иммунофлуоресцентное — с коктейлем Isl1/desmin.
Результаты. Не было выявлено корреляции между массой ЭЖ, толщиной жировой клетчатки и ФП (соответственно, р=0,85, r=-0,029 и р=0,09, r=-0,29), средняя относительная площадь фиброзной ткани у пациентов без сердечнососудистой патологии в различных зонах предсердий составила от 6,0±4,1% до 9,9±6,3%, достоверно отличаясь во всех исследованных зонах предсердий в группе с длительно персистирующей ФП (р<0,05). Амилоидоз предсердий был выявлен только в 3 случаях. Определена сильная корреляция ФП с коллагеном III (r=0,869, p<0,01). ИГХИ выявило Isl1+стволовые клетки кардиомиоцитов. Заключение. Выявлена достоверная связь ФП со степенью фиброза предсердий, который обусловлен отложением коллагена III, а не коллагена I. Установлено отсутствие зависимости ФП от массы ЭЖ, ожирения и амилоидоза. Обнаружение стволовых клеток кардиомиоцитов в предсердии у пожилых пациентов открывает перспективы для клеточной терапии.
В настоящее время многие исследователи считают, что воспалительные процессы являются ключевыми факторами патофизиологии фибрилляции предсердий (ФП) [1]. Воспаление способствует как электрическому, так и структурному ремоделированию предсердий и тромбозу у пациентов с ФП, и терапия, направленная на определенные воспалительные каскады, может быть потенциальной стратегией профилактики и лечения ФП [2]. Исходом воспаления и некроза является фиброз, который также ведет к структурному ремоделированию предсердий. Коллаген — основной структурный белок внеклеточного матрикса сердца. Коллаген I типа и коллаген III типа составляют соответственно около 85% и 11% от общего содержания коллагена сердца. Эти два типа коллагена имеют значительно различающиеся механические свойства. Коллаген I типа обеспечивает прочность на разрыв и жесткость, тогда как коллаген III типа обеспечивает эластичность. Считается, что последний увеличивается на начальных стадиях ремоделирования сердца и позже заменяется коллагеном I, что изменяет биомеханику сердца, ухудшает сердечную функцию и приводит к хронической сердечной недостаточности (ХСН) [3]. На сегодняшний день активно изучается возможность лечения фиброза ингибиторами ангиотензинпревращающего фермента и лизилоксидазы [4].
Описывают также депозиты амилоида в операционном материале левого предсердия (ЛП) у пожилых больных [5], рассуждая о влиянии этого патологического процесса на ФП. Кроме того, в последние годы появились статьи о влиянии эпикардиального жира (ЭЖ) на ФП через структурное и электрическое ремоделирование предсердий как прямым (например, путем инфильтрации жировой ткани, приводящей к изменению электрофизиологических свойств предсердий), так и косвенными механизмами (например, выступая в качестве источника паракринных модуляторов воспаления миокарда и окислительного стресса). При этом увеличение объема ЭЖ у пациентов с ФП констатируется при компьютерной томографии [6].
Цель исследования: оценить влияние различных патологических процессов на патогенез ФП.
Материал и методы
Исследовались истории болезни и аутопсийный материал 42 пациентов от 34 до 86 лет (средний возраст 67,8±13,4 лет), 18 мужчин и 24 женщины. Основными заболеваниями у 18 пациентов были ишемическая болезнь сердца (ИБС) с гипертонической болезнью III стадии, у 9 — онкологические заболевания, у 8 — приобретенные пороки сердца различной этиологии, у 3 — дилатационная кардиомиопатия, у 3 — хроническая цереброваскулярная болезнь, у 1 — хронический тромбофлебит. 29 пациентов умерли от острой и/или ХСН, 9 — от раковой интоксикации, 2 — от инсульта с отеком головного мозга, 1 — от двусторонней пневмонии, 1 — от тромбоэмболии легочной артерии. У 5 из 42 больных была длительно персистирующая ФП, у 17 — пароксизмальная ФП. У всех пациентов измерялась толщина жировой клетчатки передней брюшной стенки, взвешивались сердца и предварительно удаленный ЭЖ, вычислялось отношение массы сердца (МС) к массе ЭЖ.
Материалом послужили 52 сердца, протоколы вскрытий и истории болезни пациентов возрастом от 33 до 96 лет (средний возраст — 68,2±14,3 года), из них 19 женщин и 33 мужчины. Основными заболеваниями у 21 пациента были ИБС с гипертонической болезнью III стадии, у 6 — онкологические заболевания, у 3 — приобретенные пороки сердца различной этиологии, у 5 — дилатационная кардиомиопатия, у 14 — хроническая цереброваскулярная болезнь, у 1 — первичная легочная гипертензия, у 1 — сепсис, у 1 — пневмония. 14 пациентов умерли от ХСН, 4 — от острой, 1 — от тампонады перикарда, 6 — от раковой интоксикации, 14 — от инсульта с отеком головного мозга, 4 — от двусторонней пневмонии, 4 — от тромбоэмболии легочной артерии, 5 — от сепсиса. У 17 больных была длительно персистирующая ФП, у 7 — пароксизмальная. Образцы миокарда по 1,5×0,5 см забирались из зон терминального гребня, пучка Бахмана, верхней и нижней части задней стенки ЛП между устьями легочных вен. Парафиновые срезы окрашивались гематоксилином с эозином, по ван Гизону и конго красным. В 10 случаях с персистирующей ФП, в 4 случаях — с пароксизмальной и в 10 случаях без ФП было проведено иммуногистохимическое исследование (ИГХИ) с антителами к коллагенам I и III фрагментов верхней части задней стенки ЛП. С целью поиска стволовых клеток миокарда в 1 случае с персистирующей ФП, в 1 случае без ФП и в 1 контрольном случае (ребенок с врожденным пороком сердца возрастом 7 мес.) было выполнено ИГХИ верхней части задней стенки ЛП с антителом к Isl1 (фактор транскрипции, кодируемый белок, играющий важную роль в эмбриогенезе островков Лангерганса поджелудочной железы; Isl1 также является маркером предшественников кардиомиоцитов) и проведено иммунофлуоресцентное исследование с коктейлем антител Isl1/desmin. В качестве первых вторичных антител использовали AlexaFluor 647® (Abcam, Великобритания), дававших красную флюоресценцию, а в качестве вторых вторичных антител — AlexaFluor 488® (Abcam, Великобритания), дававших зеленую флюоресценцию. После промывки образцы докрашивались DAPI (AppliChem, Германия) и заключались в среду DAKO. Полученные микропрепараты исследовались на флуоресцентном микроскопе Leica DM6000B. При микроскопическом исследовании с помощью анализатора изображения LeicaScope (Россия) в 20 полях зрения при ×200 высчитывалась относительная площадь фиброза и амилоидоза (отношение площади патологического процесса к площади препарата соответственно при окрасках по ван Гизону и конго красным) фрагментов стенок предсердий всех локализаций и средний диаметр кардиомиоцитов между устьями верхних легочных вен. Экспрессия коллагенов оценивалась в баллах: 1 балл — на единичных волокнах, 2 — мелкоочаговая экспрессия, 3 — крупные поля, 4 — на всех волокнах.
Статистическая обработка данных выполнялась в R 4.3.1 и IBM SPSS 29.0 с применением описательной статистики (средние значения ±SD, медианы (Me)) и сравнения групп по критерию Манна-Уитни (для непараметрических данных), t-теста (для нормального распределения). Выполнялся корреляционный анализ, использовался критерий Краскала-Уоллиса. Принят уровень значимости р<0,05.
Результаты
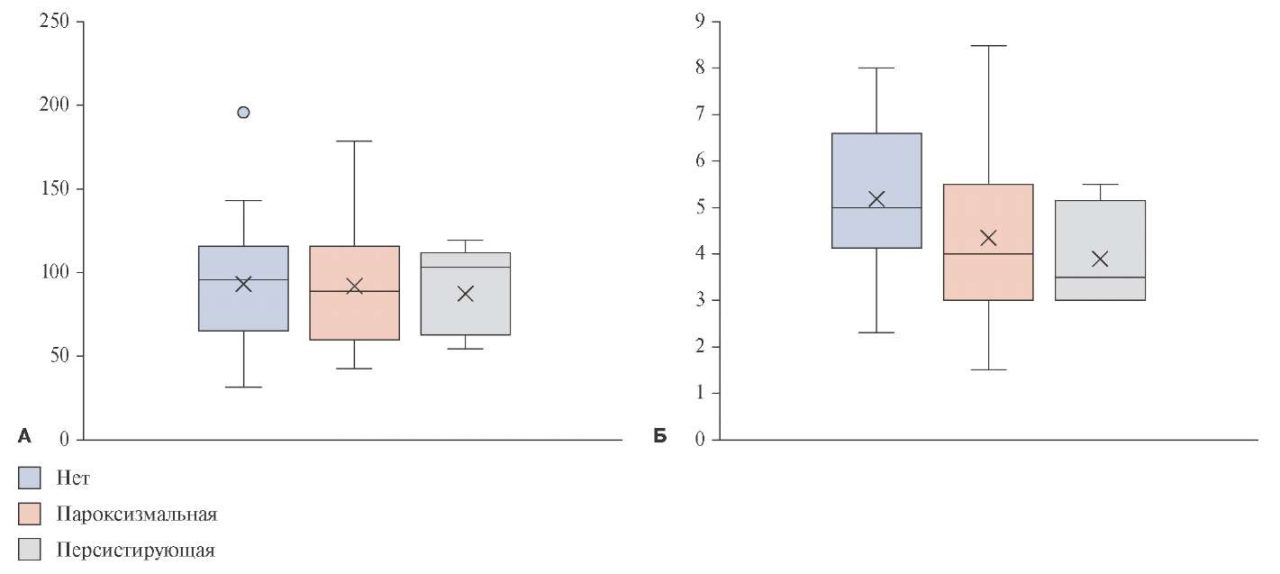
МС была от 200 г до 722 г, масса ЭЖ — от 18,6 до 193 г, отношение МС/ЭЖ — от 1,27 до -21,8, толщина жировой клетчатки передней брюшной стенки — от 1,5 до 8,5 см. Не было выявлено корреляции между массой ЭЖ и ФП (р=0,85, r=-0,029; рис. 1), между толщиной жировой клетчатки передней брюшной стенки и ФП (р=0,09, r=-0,29), между отношением МС к массе ЭЖ и ФП (р=0,19, r=0,2), но есть прямая корреляционная связь средней силы (р<0,001, r=0,6) между массой ЭЖ и толщиной жировой клетчатки передней брюшной стенки.
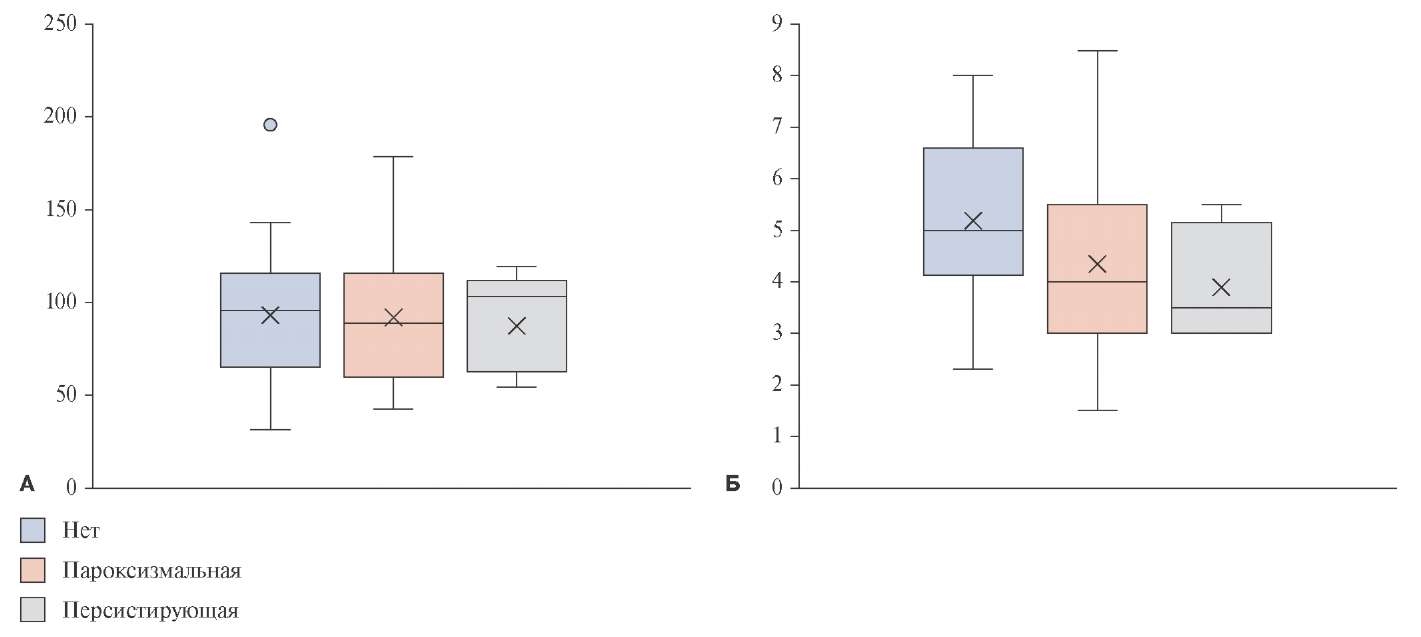
Рис. 1. Значения массы ЭЖ и толщины жировой клетчатки передней брюшной стенки у пациентов с ФП и без нее. По оси абсцисс — группы без ФП, пароксизмальная ФП и длительно персистирующая ФП; А — по оси ординат — масса эпикардиального жира в граммах; Б — толщина жировой клетчатки в см.
Средняя относительная площадь фиброзной ткани в crista terminalis у пациентов без сердечно-сосудистой патологии и ФП была 8,9±7,9%, в пучке Бахмана — 9,8±6,1%, в стенке ЛП между нижними легочными венами — 6,0±4,1%, между верхними легочными венами — 9,9±6,3% (рис. 2 А, Б). У больных с пароксизмальной ФП средняя относительная площадь фиброзной ткани в crista terminalis была 11,8±5,6%, в пучке Бахмана — 3,6±3,7%, в стенке ЛП между нижними легочными венами — 16,0±13,8%, между верхними легочными венами — 11,5±2,3%. У больных с длительно персистирующей ФП средняя относительная площадь фиброзной ткани в crista terminalis была 24,0±11,7%, в пучке Бахмана — 23,7±14,2%, в стенке ЛП между нижними легочными венами — 20,4±11,2%, между верхними легочными венами — 25,7±21,0%. Статистический анализ выявил достоверность различий относительной площади фиброзной ткани в терминальном гребне между группами без ФП и пароксизмальной ФП, между группами без ФП и персистирующей ФП, между группами ФП (р=0,004); между группой без ФП и пароксизмальной ФП (р=0,002), без ФП и персистирующей ФП (р=0,04) в пучке Бахмана, между верхними и нижними легочными венами (р=0,007). Корреляционный анализ по Пирсону выявил слабую корреляционную связь между площадью фиброзной ткани и возрастом: r=0,3, p=0,03. Амилоидоз был выявлен только в 3 случаях: 1) во всех локализациях предсердий при системном транстиретиновом амилоидозе (находка при аутопсии) у мужчины 96 лет с аортальным стенозом, относительная площадь — от 36 до 67% (рис. 2 В, Г); 2) у женщины 65 лет с хронической цереброваскулярной болезнью — в терминальном гребне относительная площадь белковых депозитов 20%, между нижними легочными венами — 19%; 3) у мужчины 72 лет с ИБС, площадь депозитов амилоида в пучке Бахмана — 9,1%. Статистический анализ показал слабую корреляционную связь между амилоидозом и возрастом: r=0,3, p=0,03.
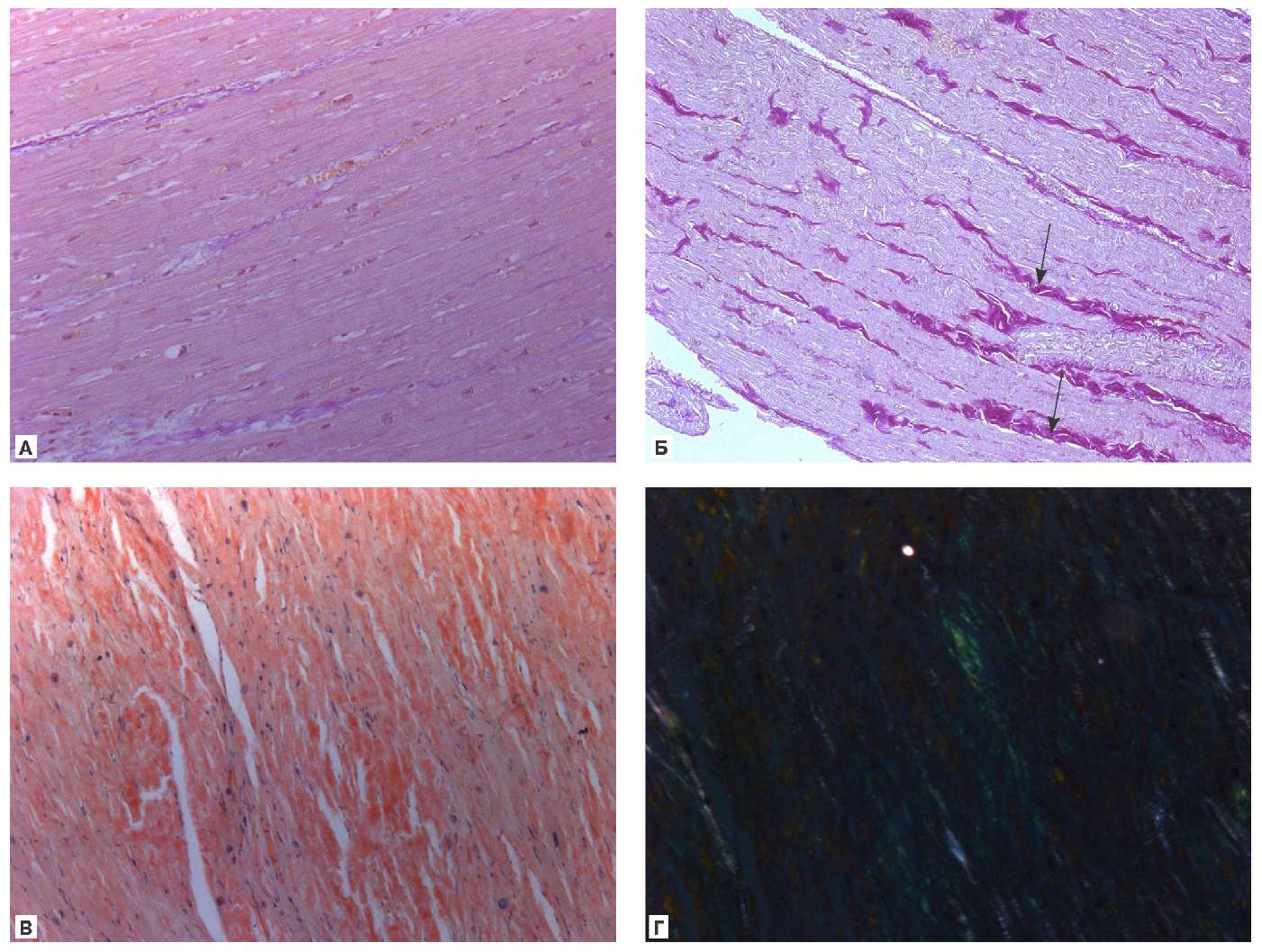
Рис. 2. Пучок Бахмана: А — у пациента без ФП, Б — с длительно персистирующей ФП и перимускулярным фуксинофильным фиброзом (указан стрелками); окраска по ван Гизону; В, Г — с длительно персистирующей ФП и транстиретиновым амилоидозом; В — кирпично-красное окрашивание амилоида; Г — яблочно-зеленое свечение амилоида в поляризованном свете; окраска конго красным, ×100.
ИГХИ с антителами к коллагенам I и III фрагментов верхней части задней стенки ЛП во всех изучаемых группах ФП и без нее с оценкой экспрессии в баллах (рис. 3, 4) выявило сильную положительную корреляционную связь ФП с коллагеном III (r=0,869, p<0,01) и отсутствие связи с коллагеном I.
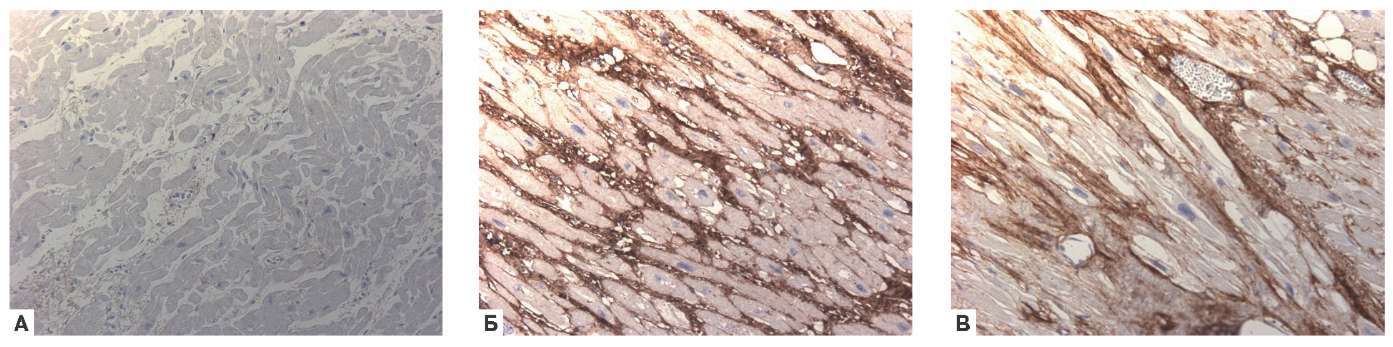
Рис. 3. ИГХИ ЛП с антителами к коллагенам. А — отсутствие экспрессии коллагена III в стенке предсердия у пациента без ФП. Б — экспрессия коллагена III (коричневое окрашивание; 4 балла), фиброз — оплетка при длительно персистирующей ФП; В — экспрессия коллагена I (коричневое окрашивание; 3 балла) вокруг мышечных волокон у пациента с пароксизмальной ФП; х200.

Рис. 4. Распространенность экспрессии коллагенов в баллах (1-4) в различных группах с ФП и без нее. А — экспрессия коллагена I, Б — коллагена III.
Определение среднего диаметра кардиомиоцитов в различных группах с ФП и без нее между верхними легочными венами не выявило какой-либо зависимости этого показателя от ФП, равно как и не было установлено связи объема ЛП и площади правого предсердия с ФП по данным эхокардиографии (рис. 5).

Рис. 5. Значения объемов ЛП и площади правого предсердия по данным эхокардиографического исследования в различных группах ФП и без нее. По оси абсцисс: группа пациентов без ФП (синий цвет), с пароксизмальной ФП (оранжевый цвет), с длительно персистирующей ФП (серый цвет). А — по оси ординат — объем ЛП в см³. Б — по оси ординат — площадь правого предсердия в см².
ИГХИ с антителом к Isl1 и иммунофлуоресцентное исследование с коктейлем Isl1/desmin выявило стволовые клетки кардиомиоцитов в ЛП у ребенка 7 мес. и у мужчин 65 и 73 лет с ФП и без нее (рис. 6).

Рис. 6. Стволовые клетки кардиомиоцитов: А — в ЛП ребенка 7 мес. Яркое коричневое окрашивание ядер Isl1 при иммуногистохимическом исследовании; Б, В, Г — стволовые клетки кардиомиоцитов в стенке ЛП между верхними легочными венами при флуоресцентной микроскопии. А — у мужчины 65 лет без ФП; В, Г — у мужчины 73 лет с персистирующей ФП. Красная флуоресценция — десмин, зеленая — Isl1, синяя — DAPI (окрашивание ядер), оранжевая — коэкспрессия десмина с Isl1; ×400.
Таким образом, наше исследование установило отсутствие зависимости ФП от массы ЭЖ и ожирения в целом, были установлены нормативы средней относительной площади фиброзной ткани в предсердиях (в среднем от 6 до 9,9%). Различия между этим показателем в группах без ФП и с ФП были статистически достоверны во всех локализациях предсердий с выраженным фиброзом при данном нарушении ритма, площадь которого достигала 1/4-1/5 стенок предсердий при длительно персистирующей ФП. Причем фиброз был обусловлен в основном отложением коллагена III, а не коллагена I. Депозиты амилоида были выявлены всего в 3 случаях (5,7%), причем в одном из них амилоидоз был системным. Не было установлено достоверной связи между увеличением предсердий и ФП, равно как и увеличением диаметра кардиомиоцитов (гипертрофии). Удивительным фактом для нас стало обнаружение стволовых клеток кардиомиоцитов в предсердии у пациентов 65 и 73 лет с ФП и без нее.
Обсуждение
В целом, патогенез ФП имеет много уровней: электрофизиологический, анатомический, гистологический, клеточный, ультраструктурный и молекулярный. Электрофизиологические изменения способствуют возникновению и прогрессированию ФП. Клинические исследования показали, что ФП может быть вызвана автономной стимуляцией, брадикардией, предсердной экстрасистолией, тахикардией, дополнительными путями проведения и острым растяжением предсердий [7]. Электрические или очаговые механизмы ФП включают аномальный автоматизм, триггерную активность и множественные вариабельные реципрокные паттерны [8][9]. При ФП наблюдались снижение тока Ca²⁺ L-типа (ICaL), перегрузка Ca⁺, изменения тока K⁺ (IKACh, IK1), тока Na⁺ (INa) и транзиторного внешнего тока (Ito) [10]. В свою очередь, ионные токи могут напрямую влиять на функцию митохондрий кардиомиоцитов, поскольку ранее было показано, что высокое содержание Ca²⁺ ингибирует митохондриальное дыхание, рассеивает мембранный потенциал и подавляет продукцию АТФ [11][12]. Ремоделирование кальциевого цикла может способствовать прогрессированию ФП до персистирующей и активировать профибротические пути [13].
Помимо электрофизиологических аспектов, большое значение имеет сложная анатомическая структура предсердий [14]. Известно, что проведение электрического импульса осуществляется через широкие мышечные пучки с параллельным расположением мышечных волокон [15][16]. Анатомия легочных вен способствует re-entry благодаря сочетанию резких изменений ориентации волокон и сниженной электрической связности между мышечными пучками, что создает области гетерогенной скорости проведения и локализованного блока [17-19].
Сегодня известно, что не только кардиомиоциты обладают электрической активностью в сердце. Недавние исследования показали, что фибробласты экспрессируют потенциалзависимые натриевые каналы, которые обеспечивают входящий ток (INa) [20-22]. Хотя они не являются электрически возбудимыми, они могут влиять на электрофизиологические свойства миоцитов [23]. Было обнаружено, что фибробласты электрически реагируют с миоцитами через щелевые контакты [24]. Фибробласты активируются при воспалительной реакции, а затем дифференцируются в миофибробласты [25] различными путями [26]. Миофибробласты отличаются от фибробластов тем, что вырабатывают сократительные белки и демонстрируют более деполяризованный мембранный потенциал покоя [27] и большую мембранную ёмкость [28].
В настоящее время известно, что миокард содержит трёхмерную сеть телоцитов, которые плотно покрывают кардиомиоциты и контактируют со всеми типами клеток и структур [29-31]. Помимо щелевых контактов, телоциты имеют точечные, наноконтакты и планарные контакты с клетками. Они могут проникать через базальную мембрану, которая одновременно окружает две P-клетки проводящей системы сердца [32]. Sheng J, et al. [33] продемонстрировали, что телоциты предсердий и желудочков экспрессируют активируемый Ca²⁺ высокопроводящий (быстрый) калиевый ток (BK(Ca)) и внутренний выпрямляющий калиевый ток (IK(ir)), но не экспрессируют транзиторный внешний калиевый ток (Ito)) и АТФ-чувствительный калиевый ток (K(ATP)). В нескольких исследованиях были показаны специфические макрофагально-зависимые механизмы, регулирующие электрическое, структурное или автономное ремоделирование, приводящее к аритмиям [34-39]. Взаимодействие между макрофагами и сердечными фибробластами регулирует баланс сердечного фиброза [40].
Результаты настоящего исследования еще раз подтвердили на большей и более разнообразной выборке по составу заболеваний наши выводы о том, что степень фиброза не связана с возрастом, но достоверно коррелирует с наличием, тяжестью и продолжительностью ФП [41][42]. Важную роль в этом процессе, несомненно, играет хроническое воспаление, которое было также доказано нами в предыдущих работах [43][44]. Мы не подтвердили достоверной связи ФП с ожирением и увеличением массы ЭЖ, в отличие от других авторов, которые оценивали увеличение жировой клетчатки в эпикарде с помощью компьютерной томографии [45][46]. Возможно, разница в результатах обусловлена методами исследования, и следует провести сравнительный анализ выявления объема/массы ЭЖ при КТ и у секционного стола. Наше исследование также не показало должной распространенности амилоидоза у пожилых больных как причины ФП. Считается, что предсердный натрийуретический пептид высвобождается в ответ на растяжение или расширение объема предсердий, вызывая диурез, натрийурез и расширение сосудов. Белок ингибирует ренин-ангиотензин-альдостероновую систему и регулирует клеточные токи [47]. Именно с этим белком связывают изолированный амилоидоз предсердий, приводящий к ФП. Но достоверно выявляют его только в ушках предсердий [48][49]. Мы же исследовали другие локализации, патологический процесс в которых может напрямую, а не косвенно приводить к ФП. Кроме того, мы не выявили достоверной связи увеличения площади/объема предсердий с ФП. По-видимому, больший вклад в этот процесс вносит основное заболевание сердца.
Несмотря на успехи малоинвазивной хирургии ФП, эффективность однократной катетерной аблации в течение 5-летнего периода составляет 20% [50], идет непрерывный поиск гибридных операций и новых хирургических технологий [51]. Параллельно развиваются и новые терапевтические подходы, основанные на патогенезе заболевания. В частности, идет поиск эффективных препаратов — ингибиторов фиброза [52]. Хотя этиология сердечно-сосудистой дисфункции неоднородна, общей чертой прогрессирования практически всех форм является развитие фиброза сердца. Патологическое фиброзное ремоделирование включает пролиферацию и активацию резидентных сердечных фибробластов и изменение состава внеклеточного матрикса. Несмотря на существенный вклад фиброзного ремоделирования в сердечную дисфункцию, новые методы лечения сердечного фиброза не появились в клинической практике. Одним из основных ограничений в изучении и внедрении антифиброзной терапии является проблема точной количественной оценки фиброзной нагрузки [53]. Магнитно-резонансная томография сердца стала предпочтительным неинвазивным методом визуализации для безопасной диагностики фиброза миокарда. Магнитно-резонансная томография с использованием нетаргетных гадолиниевых зондов может обнаружить заместительный фиброз в виде макроскопических областей с поздним усилением гадолиния и интерстициальный фиброз путем измерения увеличения внеклеточного объема с использованием картирования T1 до и после введения гадолиния [54]. Несмотря на свою клиническую ценность, этот метод не позволяет напрямую оценить фиброз и различать подтипы коллагена. Поэтому для выявления фиброза и мониторинга эффективности терапии необходимы разработка и оптимизация молекулярных зондов для специфической визуализации типов коллагена [55]. В этой связи нормативы относительной площади фиброзной ткани в разных зонах предсердий, описанные нами, нацелены служить точкой отсчета.
ИГХИ предсердий позволило нам выявить, что у пациентов с ФП достоверно преобладает коллаген III, который способствует эластичности миокарда [56]. Более того, экспериментальное исследование Uchinaka A, et al. [57] демонстрирует снижение дисфункции левого желудочка при сверхэкспрессии этого типа коллагена. Этот факт наталкивает на мысль, а нужно ли лечить пациентов с ФП антифибротическими препаратами, тем более, что на сегодняшний день этот вид консервативной терапии находится на стадии разработки и обоснованности применения? Более того, нельзя исключить, что дополнительным эффектом аблации со стороны эндокарда или эпикарда является постнекротический фиброз, представленный коллагеном I типа, который способствует жесткости стенок предсердий, укрепляя и фиксируя их. Более обещающей, на наш взгляд, является стратегия лечения основного патологического процесса, приведшего к фиброзу, в частности, воспаления. И наконец, обнаружение стволовых клеток кардиомиоцитов даже у пациентов в пожилом возрасте открывает перспективы клеточной терапии.
Признание того, что митоз миоцитов происходит в плодном, неонатальном, взрослом и гипертрофированном сердце, и что в миокарде присутствует пул примитивных, недифференцированных клеток, позволило по-новому взглянуть на биологию сердца. Новая парадигма предполагает, что формирование миоцитов сохраняется в постнатальном периоде, во взрослом или старческом возрасте, указывая на значительный резерв роста сердца на протяжении всей жизни организма [58]. Было продемонстрировано, что сердце млекопитающих содержит органоспецифическую прогениторную клетку, экспрессирующую Isl1, которую можно локализовать, очистить, размножить и дифференцировать в зрелые кардиомиоциты [59]. Наше исследование подтвердило наличие Isl1+клеток даже у пожилых людей, а значит, и возможность осуществления этой идеи.
Заключение
Наше исследование установило отсутствие зависимости ФП от массы ЭЖ и ожирения, амилоидоза, гипертрофии мышечных волокон, увеличения объема и площади предсердий по данным эхокардиографии, но выявило достоверную связь этого нарушения ритма со степенью фиброза предсердий, который был обусловлен отложением коллагена III, а не коллагена I. Обнаружение стволовых клеток кардиомиоцитов в предсердии у пожилых пациентов открывает перспективы для клеточной терапии. В целом, результаты нашего исследования в очередной раз подчеркивают многоуровневость и сложность патогенеза ФП и открывают новые перспективы для лечения.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Митрофанова Л.Б., Силкин M.С., Зубарев С.В. Морфологическое исследование сердца при фибрилляции предсердий. От патогенеза к лечению. Российский кардиологический журнал. 2025;30(4S):6706. https://doi.org/10.15829/1560-4071-2025-6706. EDN: MCCTDC
Скопировать