Профилактика инсульта при фибрилляции предсердий: ключевые аспекты
Аннотация
Острые нарушения мозгового кровообращения и другие тромбоэмболические осложнения представляют собой серьезную проблему в лечении пациентов с фибрилляцией предсердий (ФП). Как известно, наличие нарушений ритма сердца является независимым предиктором увеличения риска инсульта и других системных осложнений по сравнению с общей популяцией. В то же время именно ФП сопровождается значимым повышением риска системных тромбоэмболий, независимо от клинической формы и выраженности симптомов. Эффективная профилактика инсультов требует комплексного подхода, включающего своевременную диагностику, лечение и контроль факторов риска, а также разработку новых интервенционных методов, направленных на снижение риска тромбоэмболических событий при различных формах ФП.
Фибрилляция предсердий (ФП) является наиболее часто встречаемой патологической аритмией и сопровождается значимым повышением риска системных тромбоэмболических событий, независимо от клинической формы и выраженности симптомов. Нередко при отсутствии своевременной тромбопрофилактики (особенно при бессимптомной форме аритмии) первым проявлением заболевания являются кардиоэмболические инсульты (КЭИ), которые характеризуются обширным инфарктом мозга, приводящим к выраженному неврологическому дефициту, что влечет за собой стойкую инвалидизацию и ухудшение прогноза пациентов. По данным различных источников, в современной популяции пациентов с ФП вероятность развития инсульта оценивается в пределах 1-20% в год [1-3]. По прогнозам Всемирной организации здравоохранения, в ближайшие десятилетия ожидается увеличение числа пациентов с тромбоэмболическими осложнениями (ТЭО) ФП, несмотря на значительный прогресс в лечении большинства сердечно-сосудистых заболеваний [4][5]. Во многом данные результаты можно объяснить недостаточной выявляемостью малосимптомных форм ФП на популяционном уровне, в т.ч. у пациентов с криптогенными ишемическими инсультами и другими тромбоэмболическими событиями.
Следует отметить, что высокий риск ТЭО у пациентов с нарушениями ритма сердца может наблюдаться не только на фоне ФП или трепетания предсердий, а также при отдельных формах врожденных пороков сердца и сопутствующих предсердных тахиаритмиях (за счет значимых нарушений гемодинамики, к примеру, при циркуляции Фонтена и т.д.) [6]. Данный фактор необходимо принимать во внимание при назначении схем тромбопрофилактики в указанных группах пациентов, в то время как стандартные подходы к стратификации риска ТЭО (в т.ч. с использованием шкалы CHA2DS2-VASc) в подобных обстоятельствах могут оказаться недостаточными, т.к. не учитывают индивидуальные дополнительные предикторы тромботических осложнений [7].
Установлено, что при ФП формирование тромба происходит преимущественно в предсердиях (в 90-95% — в ушке левого предсердия (ЛП) (УЛП), в остальных случаях — в полости предсердия) с последующей эмболией церебральных артерий и развитием клиники ишемического инсульта. Реже могут наблюдаться периферические тромбоэмболии с поражением артерий конечностей, сосудов глазного дна и других локализаций [4][5].
Учитывая, что риск инсульта значимо возрастает независимо от клинического течения ФП, в данной группе пациентов представляется актуальным поиск новых подходов и совершенствование существующих режимов тромбопрофилактики, в т.ч. с помощью нефармакологических методов.
Основные причины тромбообразования при ФП
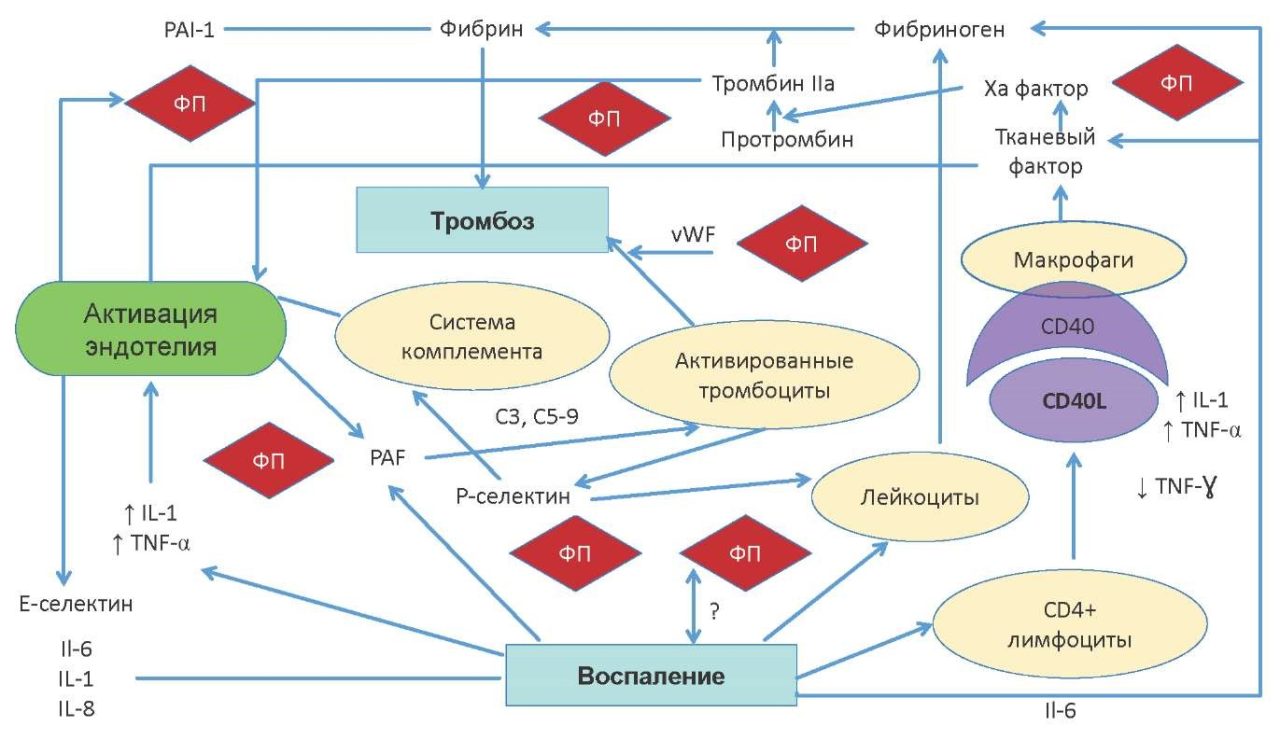
Наличие любых форм ФП ассоциировано со значительным увеличением вероятности ТЭО и прежде всего развитием острых КЭИ на фоне тромбообразования в УЛП или полостях сердца. В патогенезе тромбоза на фоне ФП ключевую роль имеет реализация стандартной триады Вирхова (рис. 1).

Рис. 1. Реализация триады Вирхова на фоне ФП. Адаптировано из Kaski JC, et al., 2011 [8].
Сокращения: ФП — фибрилляция предсердий, IL — интерлейкин, TNF — фактор некроза опухоли.
Традиционно три звена тромбообразования включают:
1) Замедление кровотока (стаз крови)
Данный компонент триады Вирхова наиболее вероятно наблюдается за счет потери эффективной сократительной функции предсердий на фоне частой хаотичной фибрилляторной активности кардиомиоцитов. Особенно выражен стаз кровотока в полости УЛП, но нельзя исключать и вероятность формирования внутриполостного тромбоза других локализаций.
2) Повреждение эндотелия (эндокарда ЛП)
Вследствие сохраняющейся ФП возникает и прогрессирует электрическое и структурное ремоделирование ЛП, что сопровождается не только ухудшением электрических свойств кардиомиоцитов, активацией провоспалительных и профибротических факторов, но и нарушением высвобождения регуляторных цитокинов и других гуморальных факторов, влияющих на регуляцию свертывания крови.
3) Повышенная свертываемость крови (гиперкоагуляционный статус)
На фоне ФП запускается каскад коагуляции за счет провоспалительных факторов, активации системы свертывания крови в условиях нестабильной предсердной гемодинамики и повреждения эндокарда. Кроме того, наблюдается нарушение баланса противосвертывающих и фибринолитических механизмов, что способствует формированию тромбов.
Стратификация риска ТЭО на фоне ФП
Как уже было указано, основным источником тромбообразования на фоне ФП принято считать полость УЛП [4][5][8]. Для оценки риска ТЭО в клинической практике традиционно используется чреспищеводная эхокардиография (ЧП-ЭхоКГ) и компьютерная томография (КТ) с внутривенным контрастированием. Данные методики не взаимоисключают, а дополняют друг друга, и выбор оптимальной техники визуализации зависит от индивидуальной клинической ситуации.
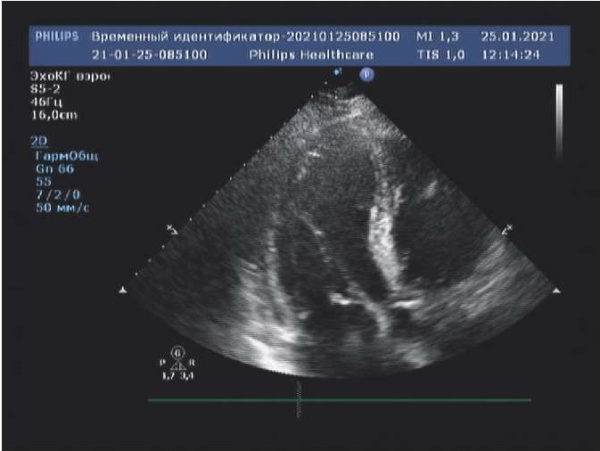
Основными показателями, которые можно оценить в ходе кардиовизуализации у пациентов с ФП, являются: размеры и локализация тромба (рис. 2), выявление флотирующих фрагментов при их наличии, анатомические особенности, в т.ч. форма УЛП. Отдельно следует сказать о гемодинамических параметрах, которые являются очень важными в плане дополнительной оценки риска ТЭО, но при этом не относятся к официальным предикторам инсульта на современном этапе. Вышеперечисленные параметры включают максимальную скорость изгнания крови из УЛП, фракцию выброса УЛП, степень выраженности феномена спонтанного контрастирования и кровоток в легочных венах.

Рис. 2. Тромб в полости УЛП (визуализация по данным ЧП-ЭхоКГ). Адаптировано из Cresti A, et al., 2019 [9].
Сокращения: ЛП — левое предсердие, УЛП — ушко левого предсердия.
Отдельного внимания заслуживает феномен спонтанного контрастирования в УЛП и полости ЛП, который также не включен в современные шкалы оценки риска инсульта, но пока недостаточно изучен в плане риска тромботических осложнений и влияния на прогноз пациентов (табл. 1).
Таблица 1
Характеристика феномена спонтанного эхоконтрастирования (адаптировано из Fatkin D, et al. 1994 [10])
|
Степень |
Характеристика |
|
0 |
СК отсутствует |
|
1+ |
Легкое/минимальное СК (преимущественно в УЛП и реже в полости ЛП, может выявляться непостоянно в ходе сердечного цикла, не всегда заметно при рабочих настройках усиления для двумерного эхокардиографического анализа) |
|
2+ |
Легкое/умеренное СК (более четкий рисунок завихрений, чем у класса 1+, но с теми же особенностями распределения, обнаруживается без увеличения настроек усиления) |
|
3+ |
Умеренное СК (четко различимые завихрения потока в УЛП, обычно с меньшей интенсивностью в основной полости ЛП, интенсивность может колебаться, но СК обнаруживается постоянно на протяжении всего сердечного цикла) |
|
4+ |
Выраженное СК (высокая плотность потока с очень медленной скоростью, обычно одинаковые в УЛП и полости ЛП) |
Сокращения: ЛП — левое предсердие, СК — спонтанное контрастирование, УЛП — ушко левого предсердия.
Большинство исследователей сходятся во мнении, что эффект спонтанного контрастирования (ЭСК) является сильным независимым предиктором формирования тромба в УЛП и риска развития тромбоэмболий у пациентов с ФП [11][12]. Возникновение ЭСК объясняют образованием «монетных столбиков» (агрегацией эритроцитов) и взаимодействием их с белками плазмы (в основном с фибриногеном). Эхокардиографически феномен проявляется в виде подвижных, наподобие дыма, эхосигналов, формирующих потоковые вихри, что не рассматривается как истинный тромбоз ЛП, но может служить гемодинамической предпосылкой к его формированию. Постепенно прогрессирование сладжа форменных элементов крови приводит к «уплотнению» эхосигнала и слоистости, сигнал остается подвижным и сохраняется в течение всего сердечного цикла. В свою очередь, дальнейшее усиление сладжа может сопровождаться формированием тромбов, которые визуализируются как отграниченные эхоплотные структуры, четко дифференцирующиеся от прилежащего эндокарда ЛП или ушка и гребенчатых мышц, но менее гетерогенные и подвижные, чем сладж (рис. 3).

Рис. 3. Степени феномена спонтанного эхоконтрастирования (визуализация по данным ЧП-ЭхоКГ). Адаптировано из Ito T, et al., 2019 [13].
Сокращения: ЛЖ — левый желудочек, ЛП — левое предсердие, УЛП — ушко левого предсердия.
Учитывая, что в настоящее время четкие клинические рекомендации по ведению пациентов с ФП и высокой степенью ЭСК не разработаны, клиническое решение по тактике должно приниматься индивидуально, с учетом всех имеющихся факторов риска. Отдельно нужно принимать во внимание и анатомические характеристики УЛП, особенно увеличение размеров, неблагоприятную форму, наличие трабекулярных структур и гребенчатых мышц и другие потенциальные предикторы ТЭО (рис. 4).

Рис. 4. Варианты анатомии УЛП (визуализация по данным ЧП-ЭхоКГ). Адаптировано из Shiyu Gong, et al., 2021 [15].
Рядом исследователей было доказано, что при увеличении площади УЛП >6 см² риск ТЭО повышается в 5 раз, а снижение пиковой скорости кровотока <0,2 м/с сопровождается как минимум трехкратным увеличением риска ишемического инсульта [14].
В свою очередь, наиболее неблагоприятной, хотя и достаточно редко встречающейся анатомией УЛП считаются варианты «кактус» и «цветная капуста», когда тромбоэмболический риск увеличивается как минимум в 2 раза. [14][16] (рис. 5).
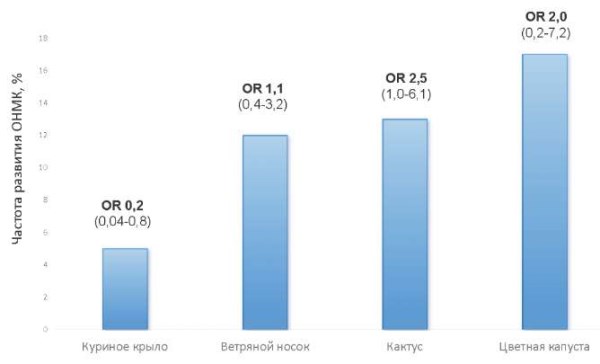
Рис. 5. Частота случаев острого нарушения мозгового кровообращения/транзиторной ишемической атаки (%) в зависимости от анатомического строения УЛП. Адаптировано из Di Biase L, et al., 2012 [16].
Сокращение: ОНМК — острое нарушение мозгового кровообращения, OR — отношение шансов.
Шкалы прогнозирования риска инсульта при ФП
Традиционным инструментом стратификации риска кардиоэмболических осложнений у пациентов с ФП на протяжении многих лет является шкала CHA2DS2-VASc (табл. 2). После оценки суммарного риска принимается решение о необходимости старта антикоагулянтной профилактики. Так, по современным рекомендациям, назначение оральных антикоагулянтов (ОАК) для профилактики ТЭО при ФП необходимо рассмотреть у мужчин с суммой баллов CHA2DS2-VASc ≥2, и у женщин с суммой баллов по CHA2DS2-VASc ≥3, принимая во внимание индивидуальные характеристики и предпочтения пациента [17].
Таблица 2
Клинические факторы риска инсульта, транзиторной ишемической атаки и системной эмболии по шкале CHA2DS2-VASc [17]
|
Факторы риска по CHA2DS2-VASc |
Баллы |
|
Застойная сердечная недостаточность Признаки/симптомы сердечной недостаточности или объективные доказательства снижения фракции выброса левого желудочка |
+1 |
|
Артериальная гипертензия Артериальное давление в состоянии покоя >140/90 мм рт.ст. по крайней мере при двух повторных измерениях или текущая антигипертензивная терапия |
+1 |
|
Возраст 75 лет или старше |
+2 |
|
Сахарный диабет Гликемия натощак >125 мг/дл (7 ммоль/л) или лечение пероральными сахароснижающими препаратами и/или инсулином |
+1 |
|
Перенесенный инсульт, транзиторная ишемическая атака или тромбоэмболия |
+2 |
|
Сосудистые заболевания Перенесенный инфаркт миокарда, заболевания периферических артерий или атеросклероз аорты |
+1 |
|
Возраст 65-74 года |
+1 |
|
Пол (женский) |
+1 |
В 2024г опубликована модифицированная версия шкалы оценки тромбоэмболического риска CHA2DS2-VA, где из процесса стратификации риска исключен женский пол как дополнительный предиктор инсульта (табл. 3). Кроме того, впервые в практику были введены дополнительные факторы, которые модифицируют индивидуальный риск инсульта и ТЭО, включая онкологию, хроническую патологию почек, этническую принадлежность, биомаркеры (уровень тропонина и мозгового натрийуретического пептида), а также увеличение ЛП, гиперлипидемию, курение и избыточный вес [4].
Таблица 3
Модифицированная версия шкалы CHA2DS2-VA [4]
|
Факторы риска по CHA2DS2-VA |
Баллы |
|
|
C |
Застойная сердечная недостаточность Признаки/симптомы сердечной недостаточности (независимо от уровня ФВ ЛЖ) или асимптомное снижение ФВ ЛЖ <40% |
+1 |
|
H |
Артериальная гипертензия Артериальное давление в состоянии покоя >140/90 мм рт.ст. по крайней мере при двух повторных измерениях или текущая антигипертензивная терапия. Оптимальное значение целевого артериального давления для снижения риска больших неблагоприятных сердечно-сосудистых событий — 120-129/70-79 мм рт.ст. или достижение минимально возможных значений |
+1 |
|
A |
Возраст 75 лет или старше Независимый предиктор высокого риска инсульта, представляет собой континуум, но для практических целей выделяется отдельно возраст старше 75 лет (2 балла) |
+2 |
|
D |
Сахарный диабет Наличие сахарного диабета 1 или 2 типа, диагностированного по общепринятым критериям, или лечение пероральными сахароснижающими препаратами и/или инсулином |
+1 |
|
S |
Перенесенный инсульт, транзиторная ишемическая атака или артериальные тромбоэмболии При наличии в анамнезе тромбоэмболического осложнения риск значительно возрастает (2 балла) |
+2 |
|
V |
Сосудистые заболевания Наличие ишемической болезни сердца, анамнез инфаркта миокарда, стенокардии, коронарной реваскуляризации (ЧКВ/АКШ) или гемодинамически значимое поражение коронарного русла по данным ангиографии и других методов визуализации. Заболевания периферических артерий (перемежающаяся хромота, анамнез реконструктивных операций на периферических артериях, эндоваскулярные или открытые вмешательства на аорте) или наличие атеросклеротического поражения аорты по данным визуализации (с признаками мобильности, нарушения поверхности, увеличением размера бляшки >4 мм) |
+1 |
|
A |
Возраст 65-74 года |
+1 |
Сокращения: АКШ — аортокоронарное шунтирование, ФВ ЛЖ — фракция выброса левого желудочка, ЧКВ — чрескожное коронарное вмешательство.
Таким образом, с учетом внесенных дополнений, проведение тромбопрофилактики у мужчин и женщин с ФП в настоящее время рекомендуется при значении показателя CHA2DS2-VA ≥2 баллов и может рассматриваться у пациентов, имеющих 1 балл, при наличии индивидуальных дополнительных факторов риска. При этом во всех случаях нужно переоценивать клиническую ситуацию в динамике с периодичностью не менее, чем 1 раз в 6 мес. или чаще, если происходит изменение функционального статуса пациента. Важно помнить, что клиническая форма документированной ФП (пароксизмальная, персистирующая или постоянная) не должна оказывать влияния на выбор способа тромбопрофилактики, т.к. тромбоэмболические риски одинаково высокие.
Медикаментозные способы профилактики ТЭО при ФП
Лечение ФП направлено на улучшение прогноза пациентов, главным образом за счет профилактики ТЭО с помощью антикоагулянтной терапии и нефармакологических методов, а также коррекции сопутствующей сердечно-сосудистой патологии, и кроме того, на уменьшение симптоматики посредством контроля ритма и частоты сердечных сокращений. В настоящее время актуальна концепция «AF-CARE», которая заключается в применении персонализированного подхода с учетом индивидуального профиля риска и многофакторной характеристики аритмии у каждого пациента в конкретный момент времени. Подобная стратегия позволяет проводить динамическую оценку клинического статуса пациента, контролировать прогрессию ФП, имеющихся факторов риска и сопутствующей патологии, что будет способствовать повышению эффективности лечения за счет своевременной реализации комплексных профилактических и лечебных мероприятий [4].
Возможности антикоагулянтной профилактики у пациентов с ФП включают использование прямых пероральных антикоагулянтов (апиксабан, дабигатран, эдоксабан или ривароксабан), которые являются более предпочтительными, чем антагонисты витамина K, если не имеется прямых противопоказаний. Важно помнить, что при назначении антагонистов витамина К необходимо достигать целевого времени в терапевтическом окне антикоагуляции (в целевом диапазоне должно находиться не менее 70% всех результатов измерений международного нормализованного отношения (МНО)).
Коррекция дозы антикоагулянтов всегда проводится индивидуально, исходя из конкретной клинической ситуации, при этом следует избегать необоснованного снижения дозировки препаратов (табл. 4).
Таблица 4
Коррекция доз пероральных ОАК в различных клинических ситуациях [18]
|
Дабигатран |
Ривароксабан |
Апиксабан |
Эдоксабан |
|
|
Стандартная доза |
150 мг 2 раза/сут. |
20 мг 1 раз/сут. |
5 мг 2 раза/сут. |
60 мг 1 раз/сут. |
|
Возможная минимальная доза |
110 мг 2 раза/сут. |
30 мг 1 раз/сут. |
||
|
Сниженная доза |
15 мг 1 раз/сут. |
2,5 мг 2 раза/сут. |
30 мг 1 раз/сут./15 мг 1 раз/сут. |
|
|
Критерии для уменьшения дозы |
– возраст ≥80 лет — совместное применение верапамила или — повышенный риск кровотечений |
клиренс креатинина 15-49 мл/мин |
как минимум 2 из 3 критериев: — возраст ≥80 лет — вес ≤60 кг или — креатинин сыворотки ≥1,5 мг/дл (133 мкмоль/л) |
хотя бы один критерий: — клиренс креатинина 30-50 мл/мин — вес ≤60 кг — совместное применение верапамила, хинидина или дронедарона |
При назначении антикоагулянтов у пациентов с ФП всегда следует учитывать геморрагические риски и проводить модификацию факторов кровотечения путем достижения адекватного контроля АД, минимизируя длительность и интенсивность сопутствующей терапии дезагрегантами и нестероидными противовоспалительными препаратами, корректируя анемию и возможные причины кровопотери, а также поддерживая стабильное МНО у пациентов на терапии антагонистами витамина K и корректируя диету и потребление алкоголя.
На протяжении довольно длительного времени основным инструментом оценки риска кровотечений оставалась шкала HAS-BLED (табл. 5).
Таблица 5
Шкала оценки риска кровотечений HAS-BLED [17]
|
Показатель |
Клиническая характеристика |
Число баллов |
|
H |
Артериальная гипертония (САД >160 мм рт.ст.) |
1 |
|
A |
Нарушение функции печени или почек (по 1 баллу) |
1 или 2 |
|
S |
Инсульт в анамнезе |
1 |
|
B |
Кровотечение или предрасположенность к нему |
1 |
|
L |
Лабильное МНО |
1 |
|
E |
Возраст старше 65 лет |
1 |
|
D |
Прием некоторых лекарств или алкоголя (по 1 баллу) |
1 или 2 |
Сокращения: МНО — международное нормализованное отношение, САД — систолическое артериальное давление.
Основным недостатком данной шкалы, на наш взгляд, является недооценка индивидуальных дополнительных предикторов и ассоциированных клинических состояний, которые могут оказывать значимое влияние на общий геморрагический риск у пациентов с ФП. Более удачным представляется выделение нескольких градаций факторов риска кровотечений в зависимости от их обратимости, на которые можно оказывать потенциальное воздействие и контролировать как с позиции врача, так и самого пациента [4][17].
Модифицируемые факторы риска кровотечений у пациентов с ФП, получающих антикоагулянты, включают следующие параметры:
- Артериальная гипертензия (особенно если систолическое артериальное давление >160 мм рт.ст.);
- Лабильное МНО или время нахождения в терапевтическом диапазоне <60% у пациентов, принимающих антагонисты витамина K;
- Прием лекарственных препаратов, предрасполагающих к развитию кровотечения, таких как антитромботические и нестероидные противовоспалительные препараты;
- Чрезмерное употребление алкоголя (≥8 доз в нед.).
К потенциально модифицируемым факторам риска кровотечений у пациентов с ФП, получающих антикоагулянты, относятся:
- Анемия;
- Нарушение функции почек;
- Нарушение функции печени;
- Снижение количества тромбоцитов или нарушение их функции;
- Отдельно выделяют биомаркеры риска кровотечений;
- Высокочувствительный тропонин;
- Креатинин сыворотки/оценка клиренса креатинина.
Немодифицируемые факторы риска кровотечений у пациентов с ФП, получающих антикоагулянты, включают:
- Возраст (>65 лет);
- Большое кровотечение в анамнезе;
- Перенесенный инсульт;
- Хронический диализ у пациентов с хронической болезнью почек или трансплантация почки;
- Цирроз печени;
- Злокачественное новообразование;
- Генетические факторы.
Важно помнить, что при высоком риске кровотечения риск инсульта у пациента с ФП будет всегда выше. Наиболее ярко данный факт демонстрируется на примере известного шведского когортного исследования с включением почти 160 тыс. пациентов с ФП на терапии ОАК [19]. Полученные результаты доказывают не только высокую эффективность прямых ОАК в снижении риска инсульта, но и преобладание ишемических рисков над геморрагическими во всех группах пациентов, даже с высоким количеством баллов по шкале HAS-BLED (рис. 6).

Рис. 6. Частота геморрагических и ТЭО у пациентов с ФП на терапии ОАК. Данные Шведского когортного исследования (n=159013). Адаптировано из Friberg L, et al., 2012 [19].
Абсолютные противопоказания к приему антикоагулянтов для пациентов с ФП встречаются редко и в основном представляют собой экстренные хирургические ситуации, сопровождающиеся активным тяжелым кровотечением (в этой ситуации следует как можно раньше найти и устранить потенциальный источник). Также к возможным причинам временного отказа от антикоагулянтной терапии относятся сопутствующая декомпенсированная патология гемостаза (уровень тромбоцитов <50×10⁹/л, тяжелая анемия неясного генеза), либо недавнее сосудистое событие высокого риска (внутричерепное кровоизлияние, тяжелый геморрагический инсульт и т.д.).
Важно помнить, что выявление повышенного риска или наличие часто встречающихся «досаждающих кровотечений» не должно приводить к полной отмене терапии антикоагулянтами, т.к. абсолютных противопоказаний к антикоагуляции крайне мало. После того, как указанные причины будут устранены или компенсированы, следует повторно вернуться к оценке риска и возможности реинициации антикоагулянтной терапии. При наличии сохраняющегося высокого риска кровотечений следует рассмотреть немедикаментозные методы профилактики ТЭО.
Нефармакологические способы профилактики инсульта при ФП
На протяжении последних десятилетий в клинической практике применяются нефармакологические подходы к предотвращению ТЭО у пациентов с ФП, включающие эндоваскулярную окклюзию и хирургические техники исключения из кровотока УЛП, т.к. более чем в 90% случаев именно данная зона является источником тромбообразования (рис. 7) [14][16]. Данные хирургические методы могут использоваться в качестве дополнения к другим кардиохирургическим вмешательствам или как самостоятельная процедура.

Рис. 7. Примеры устройств для эндоваскулярного закрытия УЛП. Адаптировано из Cruz-Gonzalez I, et al., 2015 [23].
Примечание: A — устройство PLAATO, B — устройство WATCHMAN, C — устройство AMPLATZER TM Cardiac Plug 1, D — устройство Amulet.
Эндоваскулярная окклюзия УЛП рассматривается, как правило, у пациентов умеренного или высокого тромбоэмболического риска с сопутствующими ограничениями или противопоказаниями к длительной пероральной антикоагулянтной терапии. При этом в рандомизированных исследованиях доказано, что окклюзия УЛП не уступает варфарину и прямым ОАК по эффективности и безопасности [20-22].
Основные показания к имплантации окклюдера УЛП перечислены ниже:
- Риск ТЭО по шкале CHA2DS2-VASc ≥2 баллов;
- Высокий риск геморрагических осложнений;
- Состоявшееся большое кровотечение на фоне приема антикоагулянтов;
- Непереносимость или токсические эффекты варфарина;
- Наличие других ограничений в приеме антикоагулянтов;
- Деменция, отсутствие возможности частого лабораторного контроля и стабильного приема ОАК (терминальная болезнь почек, пациенты на хроническом гемодиализе, тяжелая патология печени и т.д.);
- Отказ пациента от приема антикоагулянтов, низкая приверженность лечению.
Процедура эндоваскулярной окклюзии УЛП проводится в рентгеноперационной в условиях общей анестезии или глубокой седации и включает несколько этапов:
Предоперационная подготовка
- Проведение диагностического клинического минимума;
- Проведение трансторакальной эхокардиографии;
- Проведение мультиспиральной КТ сердца (опционально) — оценка размеров, формы и исключение тромбоза;
- Проведение ЧП-ЭхоКГ — верификация отсутствия тромбов, оценка анатомии УЛП: размеры устья в 4-х проекциях (0°, 45°, 90°, 135°) и глубины УЛП от устья до верхушки.
Интраоперационный этап
- Доступ через бедренную вену.
- Доступ к ЛП осуществляется через правое предсердие посредством транссептальной пункции
- Выбор размера окклюдера и зоны имплантации осуществляется с помощью ЧП-ЭхоКГ, используются результаты КТ и рентгеноскопия (рис.8).

Рис. 8. Контроль позиции окклюдера УЛП в ходе имплантации (фото из личного архива авторов).
Потенциальные ограничения и противопоказания к эндоваскулярной окклюзии УЛП включают наличие тромба в УЛП на момент обследования, терминальную стадию сердечной недостаточности, а также перенесенные операции с проведением пластики, ушивания или имплантацией окклюдера межпредсердной перегородки. Однако при наличии технических ограничений у пациентов с анамнезом хирургической коррекции дефекта межпредсердной перегородки следует оценить возможности проведения системы доставки и имплантации окклюдера УЛП, либо рассмотреть возможность применения других способов тромбопрофилактики.
Послеоперационное ведение после выполнения эндоваскулярной окклюзии УЛП регламентировано действующими клиническими рекомендациями, однако некоторые позиции остаются противоречивыми. Так, антитромботическая терапия после имплантации окклюдера УЛП (при его оптимальной позиции) у пациентов с ФП предполагает прекращение антикоагуляции максимум через 45 дней от момента операции, но тем не менее всегда необходимо оценивать индивидуальный клинический профиль пациента с последующим выбором оптимального режима тромбопрофилактики.
В ряде случаев при наличии высокого риска ТЭО возможно рассмотреть сохранение редуцированных доз антикоагулянтов для лучшего контроля осложнений, особенно принимая во внимание тот факт, что причиной повторных инсультов у больных с ФП могут быть тромбы, локализованные не в УЛП, а в полостях сердца. В свою очередь, неполная окклюзия или неоптимальная позиция устройства могут быть ассоциированы с повышенным риском инсульта, что однозначно является основанием для продолжения антикоагулянтной терапии в подобных случаях.
Хирургические способы профилактики инсульта при ФП
В последние годы было предложено множество хирургических подходов к окклюзии УЛП, включая шовное выключение, удаление, клипирование и другие способы, направленные на полное выключение УЛП из кровотока для предотвращения тромбообразования у пациентов с ФП. Открытые хирургические методы окклюзии/иссечения УЛП обычно выполняются в ходе других кардиохирургических вмешательств на открытом сердце, а в последние годы и в сочетании с хирургической аблацией ФП или в качестве изолированной торакоскопической процедуры [24][25].
Спектр возможных хирургических подходов к изоляции УЛП включает использование разнообразных шовных техник или специально разработанных устройств (например, зажима или степлера для закрытия УЛП) в условиях эпикардиального или торакоскопического доступа (рис. 9).

Рис. 9. Спектр возможных хирургических техник окклюзии УЛП. Адаптировано из D’Abramo M, et al., 2023 [26].
Примечание: A — эндоскопическая петля, B — хирургический степлер, C — эпикардиальная резекция, D — кисетный шов.
По современным представлениям, пациентам с ФП, имеющим повышенный риск ТЭО (CHA2DS2-VASc ≥2 баллов), при проведении кардиохирургических вмешательств рекомендована хирургическая изоляция/ампутация УЛП в комбинации с продолжающейся антикоагулянтной терапией с целью снижения риска инсульта и системных эмболий. Также хирургическое закрытие УЛП следует рассматривать как дополнение к пероральной антикоагуляции у пациентов с ФП, перенесших торакоскопическую или гибридную аблацию ФП, для профилактики ишемического инсульта и ТЭО. Отдельное эндоскопическое хирургическое закрытие УЛП может быть рассмотрено у пациентов с ФП, имеющих противопоказания к длительному лечению антикоагулянтами [4][5][26].
Согласно современным данным, эффективность различных хирургических методов закрытия УЛП неодинакова и зависит от многих факторов, в т.ч. технических характеристик применяемых устройств и индивидуальных особенностей пациента (рис. 10).

Рис. 10. Статистика достижения эффективного закрытия УЛП при различных подходах, в %. Адаптировано из Petersen J, et al., 2024 [27].
Сокращение: УЛП — ушко левого предсердия.
По современным данным, наличие любых форм ФП ассоциировано со значительным увеличением вероятности тромбоэмболических событий и прежде всего развитием кардиоэмболического инсульта на фоне тромбообразования в УЛП или полостях сердца. В отдельной группе риска находятся лица с бессимптомным течением данной аритмии, т.к. отсутствие своевременной диагностики и, как следствие, неназначение антикоагулянтной терапии сопровождается высокой частотой развития системных тромбоэмболий.
В свою очередь, кардиоэмболический тип инсульта, реализующийся на фоне ФП, относится к наиболее неблагоприятным в структуре всех острых нарушений мозгового кровообращения, имеет тяжелые последствия и сопровождается значимым ухудшением прогноза пациентов.
Своевременная антикоагулянтная профилактика — главный доказанный способ снижения риска ишемических инсультов при ФП. Так как согласно современным данным, риск ТЭО является одинаково высоким при любой форме данной аритмии, в т.ч. и у асимптомных пациентов, специфическую профилактику КЭИ с применением антикоагулянтов при верификации диагноза ФП необходимо проводить подавляющему большинству больных. С целью объективизации показателей риска развития ТЭО у пациентов с ФП используется шкала CHA2DS2-VASc и другие инструменты индивидуальной оценки риска [4][5].
Заключение
Применение хирургических подходов к окклюзии УЛП — это современный, эффективный и безопасный способ дополнительной профилактики ТЭО у пациентов с ФП, особенно имеющих высокий риск кровотечений или серьезные геморрагические осложнения в анамнезе. Метод эндоваскулярной окклюзии УЛП широко внедрен в повседневную медицинскую практику и является оптимальной тактикой у данной категории пациентов, в т.ч. в ситуациях, когда длительный прием антикоагулянтов затруднен или невозможен.
При проведении кардиохирургических вмешательств у пациентов с ФП рекомендована хирургическая изоляция/ампутация УЛП в комбинации с продолжающейся антикоагулянтной терапией с целью снижения риска инсульта и системных эмболий. После вмешательства всегда необходимо оценивать индивидуальный клинический профиль пациента с последующим выбором оптимального режима тромбопрофилактики.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Гарькина С.В., Миллер Ю.В., Гуреев С.В., Лебедев Д.С. Профилактика инсульта при фибрилляции предсердий: ключевые аспекты (мнение по проблеме). Российский кардиологический журнал. 2025;30(4S):6724. https://doi.org/10.15829/1560-4071-2025-6724. EDN: EZHBGR
Скопировать