Контроль частоты сердечных сокращений при постоянной форме фибрилляции предсердий на основе данных непрерывной регистрации артериального давления методом разгруженной артерии
Аннотация
Цель. Оценить как изменение терапии контроля частоты сердечных сокращений (ЧСС) при постоянной фибрилляции предсердий (ФП) влияет на поударные показатели гемодинамики по данным непрерывного мониторирования артериального давления (АД).
Материал и методы. В исследование включено 32 пациента с постоянной неклапанной ФП (69,5±12,0 лет; 20 мужчин). Проводили две 15-минутные записи электрокардиограммы и АД на каждом сердечном сокращении: до и через 14-17 дней после назначения/коррекции терапии контроля ЧСС. Рассчитывали среднее гемодинамическое АД (СГАД), вариабельность СГАД (average real variability, ARV; root mean square of successive differences, RMSSD), долю недостаточно гемодинамически эффективных сокращений (НГЭСС) по трём порогам, ЧСС, нормированное RMSSD, коэффициент вариации RR (CVRR), долю пар соседних RR-интервалов с различием >10% от среднего RR (pNN10%) и «бремя коротких RR» (долю RR ниже индивидуального порога RRx).
Результаты. ЧСС снизилась с 106,6±12,1 до 85,4±10,5 уд./мин (p<0,001). Доля НГЭСС значимо уменьшилась по всем порогам ("заметные" отклонения 26,5±8,4 → 13,5±8,0%; "выраженные" 15,2±8,8→ 6,0±6,8%; "сильные" 6,8±5,4→ 2,4±3,6%; все p<0,001). Среднее СГАД оставалось стабильным (94,3±11,6→ 93,3±13,7 мм рт.ст.; p=0,67), тогда как вариабельность СГАД снижалась (ARV и RMSSD: обе p<0,001). Показатели вариабельности RR увеличились (нормированное RMSSD, CVRR, pNN10%; все p<0,001). "Бремя коротких RR" уменьшилось с 37,5±12,5 до 12,7±9,7% (p<0,001). При монотерапии β-блокатором более выраженно снижались "заметные" НГЭСС и бремя коротких RR; добавление дигоксина сопровождалось большим ростом pNN10%. При общих тенденциях выявлялись заметные индивидуальные различия. Заключение. Изменение терапии контроля ЧСС при постоянной ФП позволяет уменьшить долю НГЭСС, вариабельность СГАД и бремя коротких RR без снижения среднего СГАД, т.е. улучшить поударные показатели гемодинамики при сохранении системного АД. Выявленная выраженная межиндивидуальная гетерогенность этих эффектов при сходной ЧСС поддерживает целесообразность персонифицированной терапии, ориентированной не только на среднюю ЧСС, но и на поударные гемодинамические параметры, и требует подтверждения в более крупных проспективных исследованиях.
Фибрилляция предсердий (ФП) — самая распространённая устойчивая аритмия, ассоциированная со снижением качества жизни, повышением риска инсульта, сердечной недостаточности и смерти. При постоянной форме ключевой клинической стратегией остаётся контроль частоты сердечных сокращений (ЧСС). Поиск оптимальной целевой частоты предпринимался в ряде крупных исследований (RACE II, AFFIRM, AF-CHF) [1-3]. Несмотря на продолжающиеся дискуссии и опубликованные постанализы [4-6], данные именно этих исследований легли в основу актуальных российских и европейских рекомендаций, в которых выбор «мягкого» или «строгого» контроля ЧСС главным образом соотносится с выраженностью симптомов [7][8]. Вместе с тем только лишь средняя ЧСС в полной мере не учитывает структуру и гемодинамическую составляющую нерегулярного ритма. Модели и экспериментальные данные показывают, что ударный объём при ФП существенно зависит от длительностей нескольких предшествующих RR-интервалов и чередования коротких и длинных циклов [9][10]. В отечественных работах предпринимались попытки индивидуализировать целевую ЧСС с учётом внутрисердечной гемодинамики и реакции на β-адреноблокаторы при постоянной ФП [11][12].
По данным непрерывной регистрации артериального давления (АД) на каждом ударе сердца ранее было показано, что при близкой средней ЧСС гемодинамические характеристики ФП могут существенно различаться между пациентами, что ставит под сомнение универсальность стандартных целевых частот [13][14]. Однако имеется мало данных о том, как стандартная терапия контроля ЧСС отражается именно на поударных гемодинамических и ритмических показателях при постоянной ФП. В настоящем исследовании оценивалось как назначение терапии контроля ЧСС или её усиление влияет на поударные показатели гемодинамики и структуру ритма у пациентов с постоянной неклапанной ФП в парном сравнении до и после вмешательства.
Материал и методы
В итоговый анализ включены 32 пациента 69,5±12,0 лет (20 мужчин) с постоянной неклапанной ФП и классом симптомности по шкале mEHRA 1 (отсутствие симптомов) или 2A (слабо выраженные симптомы). Для каждого пациента выполнены две стандартные 15-минутные записи: до назначения или усиления терапии контроля ЧСС и после (через 14-17 дней). Критериями невключения были внутрижелудочковые нарушения проводимости (QRS ≥120 мс), частая желудочковая экстрасистолия, изменения сопутствующей терапии, способной повлиять на гемодинамику, и фракция выброса левого желудочка <50%. Исследование проводилось в соответствии с принципами GCP и Хельсинкской декларации, протокол одобрен локальным этическим комитетом, все пациенты подписали информированное согласие. Сводная таблица с клинической характеристикой пациентов представлена в таблице 1.
Таблица 1
Клинические характеристики и медикаментозная терапия пациентов
|
Параметр |
Число пациентов, n (%) |
|
Диагнозы |
|
|
Гипертоническая болезнь |
32 (100,0%) |
|
Ишемическая болезнь сердца |
5 (15,6%) |
|
Инфаркт миокарда в анамнезе |
1 (3,1%) |
|
Сахарный диабет 2 типа |
4 (12,5%) |
|
Медикаментозная терапия |
|
|
иАПФ/БРА |
30 (83,0%) |
|
Бета-блокаторы |
32 (100%) |
|
Дигоксин |
15 (46,9%) |
|
SGLT2-ингибиторы |
4 (12,5%) |
|
Статины |
32 (100%) |
|
Метформин |
4 (12,5%) |
|
Прямые оральные антикоагулянты |
32 (100%) |
Сокращения: БРА — блокаторы рецепторов ангиотензина II, иАПФ — ингибиторы ангиотензинпревращающего фермента, SGLT2 — натрий-глюкозный котранспортер 2 типа.
Регистрация сигналов. Синхронно с электрокардиограммой в 12 отведениях выполнялась непрерывная регистрация на каждом ударе сердца систолического, диастолического и пульсового АД (ПАД) методом «разгруженной артерии» пальцевой манжетой (система «Кардиотехника-САКР», НАО «Инкарт», Санкт-Петербург; патенты RU 2694737 C1, RU 2698447 C1). Для привязки периферических (пальцевых) значений к уровню сердца каждые 3 мин осуществлялось автоматическое измерение давления в плече на противоположной руке.
Переменные и вычисления. Для каждого сердечного цикла помимо основных характеристик АД рассчитывали среднее гемодинамическое АД (СГАД) как интеграл среднего во времени:
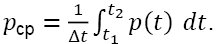
По 15-мин записи определяли долю «недостаточно гемодинамически эффективных» сердечных сокращений (НГЭСС), которые ранжировались относительно индивидуального среднего ПАД, принятого за 1: «заметные» — если ПАД <0,75 от индивидуального среднего; «выраженные» — <0,50; «сильные» — <0,25.
Вариабельность СГАД оценивали двумя независимыми показателями: ARV (средняя реальная вариабельность, мм рт.ст.) и RMSSD (корень из среднеквадратичных разностей последовательных значений СГАД, мм рт.ст.).
В контексте характеристик ритма рассчитывались: ЧСС за 15 мин, nRMSSD по RR-интервалам (RMSSD, нормированное на средний RR, в %), CVRR (коэффициент вариации RR, в %), pNN10% (доля пар соседних RR, различающихся более чем на 10% от среднего RR).
Бремя коротких RR определяли как долю RR-интервалов, ниже индивидуального порога RRx. Порог RRx задавали по исходной записи для каждого пациента по критерию Юдена на ROC-кривой для предсказания ударов с ПАД/среднее ПАД <0,75; далее этот же RRx неизменно применяли к записи, сделанной после коррекции терапии.
Терапия. У одной части пациентов (n=18) усиление терапии предусматривало только повышение дозы β-блокаторов; у другой части (n=14) — добавление дигоксина. Для сопоставления доз β-блокаторов использовали эквиваленты метопролола (мг/сут.) согласно принятым конверсиям (табл. 2).
Таблица 2
Терапия β-адреноблокаторами (в эквиваленте метопролола) и дигоксином до и после коррекции у 32 пациентов
|
Группа |
n |
MEQ до (M±SD), мг |
MEQ после (M±SD), мг |
Δ MEQ (после — до), M±SD |
Дигоксин до, % |
Дигоксин после, % |
|
Только β-блокатор |
18 |
70,1±65,5 |
141,0±102,0 |
70,8±47,2 |
0,0 |
0,0 |
|
β-блокатор + дигоксин |
14 |
82,1±45,4 |
107,1±54,1 |
25,0±40,4 |
0,0 |
100,0 |
Примечание: MEQ (metoprolol-equivalent dose) — суточная доза β-адреноблокатора, переведённая в эквивалент метопролола по ориентировочным эквипотентным дозам из официальных источников/рекомендаций. Пример эквипотентности: ≈100 мг метопролола ≈5 мг бисопролола ≈5 мг небиволола ≈25 мг карведилола.
Статистическая обработка. Нормальность распределения проверяли критерием Шапиро-Уилка. Для парных сравнений показателей до и после коррекции терапии применяли парный t-тест. Межгрупповые сравнения эффектов терапии (только β-блокаторы и β-блокаторы+дигоксин) выполняли по Δ-значениям с помощью критерия Манна-Уитни. Применялись двусторонние критерии: уровень значимости был принят как p<0,05.
Результаты
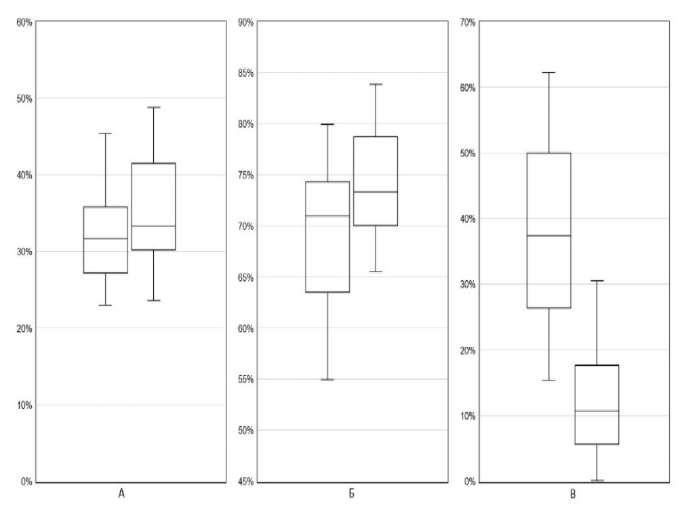
После коррекции терапии доля НГЭСС заметно снизилась по всем трём градациям. Доля «заметных» НГЭСС уменьшилась с 26,50±8,41 до 13,47±8,02% (Δ=-13,03 процентных пунктов (п.п.); 95% доверительный интервал (ДИ) [ -15,28;-10,79]; t(31)=11,84; p<0,001). Доля «выраженных» НГЭСС снизилась с 15,21±8,78 до 6,00±6,75% (Δ=-9,21 п.п.; 95% ДИ [ -11,71;-6,71]; t(31)=7,52; p<0,001). Наконец, доля «сильных» НГЭСС сократилась с 6,77±5,37 до 2,40±3,61% (Δ=-4,36 п.п.; 95% ДИ [ -6,27;-2,45]; t(31)=4,66; p<0,001) (рис. 1).

Рис. 1. Доля «заметных» (А), «выраженных» (Б) и «сильных» (В) НГЭСС до и после коррекции терапии. («Ящик»: медиана и межквартильный размах (Q1-Q3), «усы» до 1,5 межквартильного размаха; ось Y — %, n=32).
СГАД в целом оставалось стабильным: 94,25±11,62 по сравнению c 93,32±13,72 мм рт.ст. (Δ=0,93 мм рт.ст.; 95% ДИ [ -3,49;5,35]; t(31)=0,43; p=0,67). При этом вариабельность СГАД заметно уменьшилась: ARV снизилась с 6,08±1,73 до 4,61±1,96 мм рт.ст. (Δ=-1,47 мм рт.ст.; 95% ДИ [ -2,15;-0,79]; t(31)=4,41; p=0,00012), а RMSSD — с 7,61±2,04 до 6,03±2,44 мм рт.ст. (Δ=-1,59 мм рт.ст.; 95% ДИ [ -2,47;-0,71]; t(31)=3,68; p=0,00088) (рис. 2).
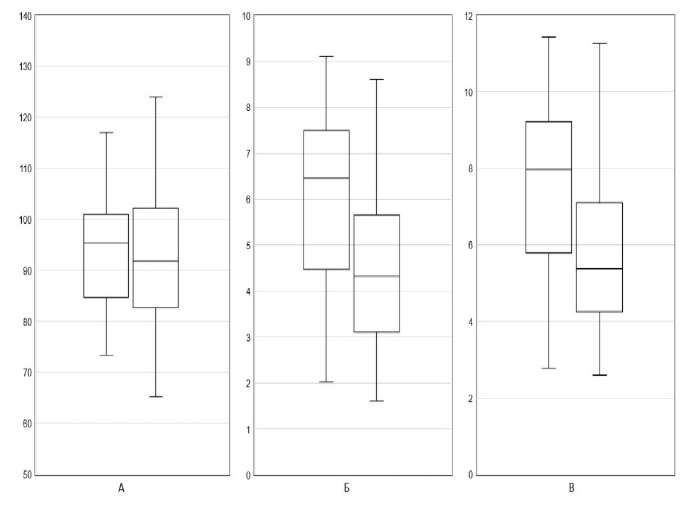
Рис. 2. СГАД среднее (А), ARV СГАД (Б) и RMSSD СГАД (В) до и после коррекции терапии. «Ящик» — медиана и межквартильный размах (Q1-Q3), «усы» — значения в пределах 1,5 межквартильного размаха; ось Y — мм рт.ст.
Ожидаемо снизилась ЧСС: с 106,63±12,12 до 85,41±10,51 уд./мин; Δ=-21,22 уд./мин (95% ДИ [ -25,10;-17,34]; t(31)=11,15; p<0,001).
Изменения структуры ритма носили разнонаправленный характер. Показатели вариабельности RR выросли: нормированное RMSSD — с 32,34±5,97 до 35,12±6,33%; Δ=2,78 п.п. (95% ДИ [ 1,32;4,24]; t(31)=3,89; p=0,00050), CVRR — с 22,88±3,92 до 24,72±4,38%; Δ=1,85 п.п. (95% ДИ [ 0,85;2,85]; t(31)=3,78; p=0,00067), pNN10% — с 69,42±6,78 до 74,02±4,85%; Δ=4,60 п.п. (95% ДИ [ 2,21;6,99]; t(31)=3,93; p=0,00045). При этом весьма существенно сократилось бремя коротких RR: с 37,47±12,45 до 12,65±9,70%; Δ=-24,82 п.п. (95% ДИ [ -29,48;-20,16]; t(31)=10,86; p<0,001). Таким образом, на фоне урежения ритма и снижения бремени коротких RR суммарная вариабельность RR могла расти за счёт появления более длинных и чередующихся интервалов без ухудшения гемодинамики (рис. 3).

Рис. 3. nRMSSD RR (A), pNN10% (Б) и бремя коротких RR (В) до и после коррекции терапии. «Ящик» — медиана и межквартильный размах (Q1-Q3), «усы» — значения в пределах 1,5 межквартильного размаха; ось Y — %.
При межгрупповом анализе изменений метрик более выраженным оказалось снижение «заметных» НГЭСС при монотерапии β-блокаторами (U=62; Z=2,27; p=0,023), тогда как для доли «выраженных» отмечался лишь недостоверный тренд (U=72; Z=1,88; p=0,060); различий по доле «сильных» не получено (U=98,5; p=0,41). Между группами не выявлено значимых различий по динамике среднего СГАД и его вариабельности (для ARV p=0,98; для RMSSD p=0,859; для среднего СГАД p=0,173). Снижение бремени коротких RR оказалось большим при монотерапии β-блокаторами (U=58,0; Z=2,43; p=0,015). Из метрик вариабельности RR значимо различалась только pNN10% (больше при добавлении дигоксина: U=51,0; Z=-2,71; p=0,0068), тогда как по метрикам nRMSSD и CVRR отличий не было выявлено (p=0,44 и p=0,42).
Индивидуальные случаи и гетерогенность ответа
В индивидуальном анализе было выделено 45 пар записей с сопоставимой средней ЧСС (различие ≤5 уд./мин), но с существенно различающимися профилями НГЭСС, что подчёркивает выраженную межиндивидуальную гетерогенность гемодинамического ответа даже при близкой ЧСС. Всего в эти пары вошли 28 пациентов. Это связывали с различиями в структуре последовательности RR-интервалов и наличием или отсутствием кластеров коротких RR относительно порога RRx.
У некоторых пациентов (n=2) после назначения/коррекции терапии увеличение доли крупных перепадов RR (рост показателя pNN10%) сопровождалось повышением вариабельности СГАД, что отражало сохранение выраженных колебаний СГАД на фоне укорочения части RR-интервалов. У части пациентов (n=3) рост крупных перепадов RR сочетался с уменьшением вариабельности СГАД и снижением НГЭСС на фоне более равномерной гемодинамики.
У некоторых пациентов (n=3) на фоне урежения ЧСС снижение доли НГЭСС было минимальным или отсутствовало, а часть показателей вариабельности СГАД и RR-интервалов изменялась незначительно, что свидетельствовало о неполном гемодинамическом ответе на проведённую коррекцию терапии.
Обсуждение
Полученные результаты указывают на общее статистическое улучшение как гемодинамических, так и ритмических характеристик на фоне скорректированной терапии в рамках данного исследования. Однако на фоне общего улучшения, подтвердились существенные индивидуальные различия при сходных значениях средней ЧСС, что поддерживает целесообразность персонификации контроля частоты на основе поударных показателей гемодинамики.
НГЭСС
Доля НГЭСС закономерно снижалась во всех трёх градациях после коррекции терапии. При сходной средней ЧСС у разных больных сохранялись существенно различающиеся доли НГЭСС, что отражает вклад структуры последовательности RR-интервалов и индивидуальных гемодинамических особенностей. Это согласуется с предыдущими наблюдениями [13][14] и подтверждает, что НГЭСС могут рассматриваться как удобный маркер гемодинамической несостоятельности ритма при ФП.
СГАД и его вариабельность
СГАД — интегральный показатель, косвенно отражающий уровень системного АД и периферического сосудистого тонуса, устойчивый к колебаниям систолического и диастолического давления. В нашей выборке средний уровень СГАД не изменился значимо после коррекции терапии (94,25±11,62 → 93,32±13,72 мм рт.ст.; p=0,67), что согласуется с представлением о барорефлекторном поддержании системного АД и периферическом тонусе при постоянной ФП. При этом краткосрочная вариабельность СГАД достоверно снизилась: ARV уменьшилась на 1,47 мм рт.ст. (p=0,00012), RMSSD — на 1,59 мм рт.ст. (p=0,00088). Таким образом, можно говорить об увеличении стабильности гемодинамики при её сохранном среднем уровне на фоне коррекции терапии и снижении ЧСС, что не противоречит результатам предыдущего исследования [14].
Несмотря на значимый групповой эффект, у части больных средний уровень СГАД оставался на верхней границе нормы или демонстрировал тенденцию к повышению, у других — незначительно снижался. Полученные данные указывают на целесообразность использования абсолютных значений СГАД как дополнительного ориентира при ФП, когда трудно получить точные цифры систолического и диастолического АД; этот интегральный показатель помогает удерживать безопасный индивидуальный уровень давления.
У части пациентов на фоне урежения ЧСС фиксировался рост ARV и/или RMSSD СГАД, что можно трактовать как ухудшение стабильности гемодинамики, даже если доля НГЭСС при этом снижалась. Подобная картина обычно была связана с неблагоприятной структурой ритма — сохранением/усилением чередований длинных и коротких RR, а также, как можно предположить, с колебаниями сосудистого тонуса.
nRMSSD, CVRR и pNN10%
Данные индексы оценивались, чтобы подтвердить или исключить их самостоятельный отрицательный вклад в гемодинамику. В группе пациентов после коррекции терапии, несмотря на рост nRMSSD, CVRR и pNN10%, наблюдалось снижение доли НГЭСС и вариабельности СГАД, что показывает: временные индексы RR отражают перестройку структуры ритма, а не ухудшение гемодинамики. Это согласуется с данными литературы [15], где при урежении частоты временные метрики RR нередко возрастают без ухудшения механики. Вместе с тем были индивидуальные исключения: у части пациентов существенный рост pNN10% сопровождался увеличением ARV СГАД — вероятно, на фоне выраженных чередований длинных и коротких RR. В таких случаях pNN10%, предположительно, может служить сигнальным маркером к пересмотру терапии, тогда как рост pNN10% на фоне снижения ARV СГАД и НГЭСС можно трактовать как безопасную перестройку ритма.
Роль бремени коротких RR
Введённый индивидуальный порог коротких RR, полученный на исходной записи (по критерию Юдена), позволяет рассматривать «бремя коротких RR» как удобный количественный терапевтический ориентир. Снижение доли коротких RR сопровождалось уменьшением ARV/RMSSD СГАД и доли НГЭСС на групповом уровне, даже если nRMSSD/CVRR/pNN10% растут, что подчёркивает клинически важное расхождение между выраженностью нерегулярности ритма и гемодинамической эффективностью сердечного цикла.
Групповой анализ терапии (группа β-блокаторы и группа β-блокатор+дигоксин)
При оценке характеристик по группам терапии наблюдалось более выраженное снижение доли «заметных» НГЭСС, больший спад бремени коротких RR и большее урежение ЧСС при монотерапии β-блокаторами. При добавлении дигоксина сильнее возрастал показатель pNN10%. Полученные результаты следует трактовать осторожно, как отражение разных профилей влияния на атриовентрикулярное проведение и «рисунок» ритма: β-блокаторы в большей степени уменьшают долю коротких RR и урежают ЧСС, тогда как дигоксин, за счет вагусного влияния на атриовентрикулярный узел, может усиливать чередования RR (рост pNN10%) без явных преимуществ по гемодинамическим характеристикам давления. Клинически это соответствует привычной практике: базовый инструмент — β-блокатор, а дигоксин — адъювант, когда есть ограничения по дозе β-блокатора (например, гипотензия). При этом в двух терапевтических группах средний СГАД не менялся, а характеристики краткосрочной гемодинамической стабильности (по вариабельности) улучшались при обеих тактиках.
Ограничения исследования. Ограничения исследования включают одноцентровый дизайн, небольшой объём выборки, гетерогенность терапии и исследовательский характер части анализируемых показателей. Не оценивались жёсткие клинические исходы и динамика симптомов, что требует дальнейших проспективных исследований. В работу не включались пациенты со сниженной фракцией выброса левого желудочка.
Заключение
Полученные данные демонстрируют, что назначение или усиление контроля ЧСС при постоянной ФП сопровождается снижением доли НГЭСС, вариабельности СГАД и бремени коротких RR при сохранении среднего СГАД. Выраженная межиндивидуальная гетерогенность этих метрик при сходной ЧСС поддерживает концепцию персонифицированного контроля частоты, ориентированного не только на среднюю ЧСС, но и на поударные показатели гемодинамики. Представленный подход требует подтверждения в более крупных проспективных исследованиях.
Благодарности. Выражаю благодарность НАО «Инкарт» за предоставление аппаратно-программного комплекса для синхронной регистрации электрокардиограммы и поударного АД, а также за техническую поддержку и помощь в организации исследования. Выражаю особую благодарность д.т.н. Пивоварову В. В. за методическую помощь при планировании исследования и критическое обсуждение полученных результатов.
Отношения и деятельность: автор заявляет об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Корнеев А.Б. Контроль частоты сердечных сокращений при постоянной форме фибрилляции предсердий на основе данных непрерывной регистрации артериального давления методом разгруженной артерии. Российский кардиологический журнал. 2025;30(4S):6732. https://doi.org/10.15829/1560-4071-2025-6732. EDN: YXNRDX
Скопировать