Железодефицитные состояния у пациентов с хронической тромбоэмболической легочной гипертензией: распространенность, патогенез и критерии диагностики
Аннотация
Цель. Оценить распространенность железодефицитных состояний у пациентов с хронической тромбоэмболической легочной гипертензией (ХТЭЛГ), их влияние на выживаемость и функциональный статус больных, а также поиск наиболее информативного показателя оценки дефицита железа (ДЖ) в данной группе.
Материал и методы. В исследование включено 283 пациента с впервые поставленным согласно текущим клиническим рекомендациям диагнозом ХТЭЛГ (средний возраст 56,0 [44,0; 67,0] лет, 47% мужчин). Всем пациентам исследовали показатели обмена железа: железо сыворотки, трансферрин, ферритин сыворотки (СФ), растворимые трансферриновые рецепторы; уровень провоспалительных цитокинов: интерлейкина (ИЛ)-6, -8, -10 и моноцитарный хемотаксический протеин (MCP-1), а также гепсидина и эндотелина-1. Группу контроля составили 24 здоровых донора (средний возраст 58 [39; 64] лет; 46% мужчин).
Результаты. Распространенность анемии составила 17% (n=48), а доля пациентов с железодефицитной анемией 78% (n=37). Не выявлено различий по показателям гемодинамики малого круга кровообращения и функционального статуса при сравнении пациентов с анемией и без таковой, а также влияния анемии на трехлетнюю выживаемость пациентов. Продемонстрировано повышение уровня С-реактивного белка, ИЛ-10 и МСР-1 у пациентов с ХТЭЛГ и их ассоциация с показателями обмена железа. В зависимости от используемых критериев распространенность ДЖ варьировала от 24,5% до 69,1%. Для показателя насыщения трансферрина железом (НТЖ) была установлена слабая прямая корреляционная связь с такими прогностическими показателями, как тест с 6-минутной ходьбой (r=0,21; p=0,032), пиковое потребление кислорода (r=0,26; p=0,044) и насыщение кислородом смешанной венозной крови (r=0,34; p=0,040), а также значимые различия по показателям тяжести ХТЭЛГ при делении на группы по значению НТЖ более/менее 20%. При анализе трехлетней выживаемости пациентов с ХТЭЛГ получены значимые отличия выживаемости для критериев ДЖ на основании уровня растворимых рецепторов трансферрина (ж >4,4; м >5,0 (Roche Diagnostics)) и предложенных нами критериев ДЖ (СФ <30 мкг/л или 30< СФ <299 мкг/л при НТЖ <20%).
Заключение. Получены данные в пользу диагностической значимости показателя НТЖ для диагностики дефицита железа у пациентов с ХТЭЛГ и предложены дополненные критерии ДЖ для данной подгруппы пациентов с легочной гипертензией.
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) характеризуется тромботической обструкцией легочной артерии и вторичной микроваскулопатией, приводящими к повышению легочного сосудистого сопротивления, давления в легочной артерии и постнагрузки на правый желудочек с последующей его дисфункцией и развитием клиники правожелудочковой сердечной недостаточности (СН) [1]. Распространенность дефицита железа (ДЖ) в данной группе колеблется от 20 до 30% [2][3], при этом в ряде работ подтверждено его отрицательное влияние на переносимость физических нагрузок и выживаемость независимо от наличия анемии [4]. Исключительная роль железа определяется биологическими функциями белков, в состав которых входит этот элемент, прежде всего гемоглобина и миоглобина, обеспечивающих доставку кислорода к тканям и непосредственно тканевое дыхание. Кроме того, в ряде работ продемонстрирована ключевая роль железа в механизмах сигнального ответа на гипоксию (гипоксическая вазоконстрикция сосудов малого круга кровообращения), реализуемого с участием экспортёра железа ферропортина в гладкомышечных (PASMC) и эндотелиальных клетках лёгочной артерии (PAEC) [5].
Исходя из высокой распространенности железодефицитных состояний у пациентов с ХТЭЛГ и потенциальной возможности их коррекции, ключевой задачей является своевременная и правильная диагностика, особенно латентного ДЖ без достижения критериев анемии. Текущие отечественные клинические рекомендации по ведению пациентов с легочной гипертензией (ЛГ) регламентируют проведение скрининга на ДЖ, который определяется как сывороточный ферритин (СФ) <100 нг/мл или 100-299 нг/мл с насыщением трансферрина железом (НТЖ) <20%. При этом отчетливо не прописан объем обследования, а критерии ДЖ взяты из согласительных документов, посвященных хронической СН, ассоциированной в основном с заболеваниями левых камер сердца [1]. В то же время несколько исследований, проведенных у пациентов с СН, поставили под сомнение это определение, т.к. более выраженный эффект от внутривенного введения карбоксимальтозата железа в виде снижения госпитализации и смертности от сердечно-сосудистых заболеваний был получен у пациентов с уровнем НТЖ ≤20% вне зависимости от значения СФ [6]. Важно отметить, что в немногочисленных клинических исследованиях по распространенности и оценке эффективности коррекции ДЖ у пациентов с прекапиллярной ЛГ использовались различные критерии его определения [7]. Во многом это связано с ключевой ролью низкоградиентного асептического воспаления в патогенезе легочной артериальной гипертензии и ХТЭЛГ [8][9], при котором затруднена интерпретация результатов уровня СФ как наиболее специфичного и доступного теста для отражения общих запасов железа в организме.
Ферритин в форме апоферритина является белком острой фазы, концентрация которого увеличивается в условиях воспаления. Кроме того, под влиянием интерлейкина (ИЛ)-6 и ИЛ-1 происходит повышение уровня гепсидина, приводящего к секвестрации железа в макрофагах. В итоге формируется так называемый функциональный ДЖ, когда при нормальном или даже высоком уровне СФ имеется снижение доступности железа. В ранее проведенном нами исследовании у пациентов с ХТЭЛГ была продемонстрирована прямая взаимосвязь уровня моноцитарного хемотаксического протеина-1 (MCP-1) и концентрации СФ, что может быть свидетельством влияния хронического воспаления на обмен железа и развитие функционального ДЖ [10]. Исходя из этого существует рекомендация использовать различные пороговые значения для СФ в зависимости от наличия (<100 мкг/л) или отсутствия (<30 мкг/л) хронического воспаления [11]. Отдельного внимания заслуживают критерии, определяющие наличие субклинического воспаления, которые на сегодня четко не сформулированы. Традиционно уровень С-реактивного белка (СРБ) в сыворотке крови считается наиболее доступным и релевантным маркером воспаления, однако данный подход зачастую не работает при низкоградиентном асептическом воспалении и предлагается использовать высокочувствительный СРБ, оценку уровня ИЛ-1 и ИЛ-6, а также показателей гемограммы (уровень лейкоцитов, тромбоцитов и соотношение нейтрофилов к лимфоцитам) [12][13]. В аспекте трактовки показателей обмена железа в условиях воспаления меньшую изменчивость имеет показатель НТЖ: <16% обычно используется для диагностики ДЖ в целом, а порог <20% предлагается при наличии воспаления [14]. В работе Martens P, et al. на основании анализа данных 1028 пациентов с разными вариантами прекапиллярной ЛГ предлагается определять ДЖ при уровне НТЖ ≤21%, независимо от наличия анемии в связи с ассоциацией данной отсечки по уровню НТЖ с клинико-функциональными показателями, характеризующими тяжесть состояния пациентов с ЛГ [15].
В контексте диагностической неопределенности маркеров обмена железа в условиях хронического воспаления, оценка растворимых рецепторов трансферрина (sTfR) и расчет отношения растворимых рецепторов трансферрина к логарифму СФ (sTfRF), отражающего клеточную потребность костного мозга в железе и активность эритропоэза, может способствовать выявлению истинного ДЖ. Так, в крупном метаанализе, обобщившем данные 2419 пациентов с различной патологией, включая ревматологические и онкологические заболевания, было показано, что уровень sTfR и sTfRF обладают хорошими диагностическими способностями в отношении ЖДА и анемии хронического заболевания (чувствительность 86%, специфичность 75%, AUC 0,912). При этом отсутствие стандартизации доступных методов анализа и пороговых значений этих показателей ограничивает их широкое использование в клинической практике [16].
Таким образом, определение ДЖ у пациентов с ХТЭЛГ на основании СФ <100 мкг/л или СФ 100-299 мкг/л при НТЖ <20% является единственной актуальной рекомендацией на текущий момент. Однако нужен ли такой дифференцированный подход и является ли СФ более специфичным, чем НТЖ, маркером ДЖ, остается открытым вопросом. В связи с этим целью данного исследования была оценка распространенности железодефицитных состояний у пациентов с ХТЭЛГ, их влияния на выживаемость и функциональный статус больных, а также поиск наиболее информативного показателя оценки ДЖ в данной группе.
Материал и методы
В исследование включено 283 пациента с впервые поставленным диагнозом ХТЭЛГ (47% мужчин, 53% женщин, возраст 56,0 [ 44,0; 67,0] лет), которые проходили обследование и лечение в ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России с 2014 по 2024гг. Диагноз ХТЭЛГ верифицировали согласно критериям Европейского общества кардиологов от 2022г и клиническим рекомендациям Минздрава России «Легочная гипертензия, в том числе хроническая тромбоэмболическая легочная гипертензия» от 2024г (среднее давление в легочной артерии >20 мм рт.ст., давление заклинивания легочной артерии <15 мм рт.ст. и легочное сосудистое сопротивление >2 ед. Вуда) [1]. Все включенные в исследование пациенты на момент взятия биоматериала получали антикоагулянтную терапию эноксапарином натрия в дозе 1 мг/кг подкожно дважды в день, находясь на стационарном этапе лечения. Исследования были выполнены до назначения специфической терапии легочной артериальной гипертензии и проведения хирургического лечения. Критерии невключения: терапия препаратами железа в течение 3 мес. перед включением в исследование.
Морфофункциональная оценка сердца выполнялась с помощью эхокардиографического исследования на аппарате VIVID 7 Dimension (General Electric, США) в соответствии с рекомендациями Американского общества эхокардиографии [17]. Для оценки гемодинамических показателей малого круга кровообращения выполнялась катетеризация правых камер сердца с использованием термодилюционного баллонного катетера 7F Свана-Ганца (B. Braun Melsungen AG, Германия). Для оценки толерантности к физической нагрузке выполнялся тест с 6-минутной ходьбой (ТШХ) согласно рекомендациям Американского торакального общества [18]. Диагноз анемии выставлялся в соответствии с рекомендациями Минздрава России 2024г «Железодефицитная анемия», согласующимися с рекомендациями Всемирной организации здравоохранения: у мужчин при уровне гемоглобина <130 г/л, у женщин — <120 г/л.
Всем включенным в исследование пациентам выполняли клинический анализ крови (Sysmex XNL-350, Sysmex, Япония), измеряли уровень N-концевого промозгового натрийуретического пептида (NT-proBNP) в качестве лабораторного маркера СН, исследовали показатели обмена железа: железо сыворотки, трансферрин, СФ, sTfR (Cobas 6000, Roche Diagnostics, Швейцария), а также СРБ (Cobas с311, Roche Diagnostics, Швейцария). Рассчитывали НТЖ по формуле: НТЖ, % = (железо сыворотки/(трансферрин×25,2))×100 и sTfRF. Также было выполнено исследование уровня провоспалительных цитокинов: ИЛ-6, 8, 10 и MCP-1, а также гепсидина, эндотелина-1 с целью оценки влияния воспаления на показатели обмена железа и уточнения патогенеза и варианта развития ДЖ. Исследование проводилось с помощью стандартных коммерческих наборов (Cloud-Clone Corp., США) для иммуноферментного анализа на микропланшетном фотометре MultiskanFC (ThermoFisher, США).
Для сравнения результатов цитокинового профиля дополнительно была набрана группа контроля: в нее вошло 24 донора, медиана возраста 58 [ 39; 64] лет; из них 13 женщин и 11 мужчин без ЛГ, ишемической болезни сердца, аутоиммунных, воспалительных заболеваний, эпизодов клинически значимых кровотечений и венозных тромбоэмболических событий в анамнезе.
Материалом для лабораторных исследований служила венозная кровь, которую получали путем пункции кубитальной вены: для гематологических исследований и иммуноферментного анализа в пробирку с дикал этилендиаминтетрауксусной кислоты (K2ЭДТА) в качестве антикоагулянта, для биохимических — в пробирку с активатором свертывания. Цельную кровь исследовали в течение 12 ч, сыворотку для исследования показателей обмена железа, NT-proBNP и СРБ, а также плазму с дикал этилендиаминтетрауксусной кислотой для исследования уровня цитокинов, гепсидина и эндотелина-1 получали путем центрифугирования цельной крови при 2500 g в течение 15 мин и банкировали при -80 C.
Исследование выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования одобрен локальным этическим комитетом (выписка № 12-20 от 21 декабря 2020г). До включения в исследование у всех участников было получено письменное информированное согласие. Авторы заявляют об отсутствии конфликта интересов. Работа выполнена без задействования грантов и финансовой поддержки от общественных, некоммерческих и коммерческих организаций.
Статистическая обработка данных проводилась в SPSS Statistic. Для проверки нормальности распределения применялся тест Шапиро-Уилка. Количественные данные представлены в виде медианы, 25-й и 75-й процентилей (Me [Q1; Q3]). Для сравнения двух независимых групп применялся тест Манна-Уитни. Анализ качественных данных проводился с использованием критерия Фишера. Для оценки взаимосвязи между количественными переменными использовался коэффициент ранговой корреляции Спирмена. Различия считали значимыми при p<0,05.
Результаты
Анемия
Распространенность анемии среди включенных в исследование пациентов составила 17% (n=48), при этом доля пациентов с ЖДА составила 78% (n=37), среднее значение гемоглобина в этой подгруппе составляло 110 [ 106; 116] г/л, таким образом, все больные относились к категории анемии легкой степени тяжести. У 6 пациентов была выявлена гемолитическая анемия: в 2 случаях на фоне гемоглобинопатии (малая бета-талассемия в обоих случаях), у 2 больных — на фоне микросфероцитарной анемии, у 2 пациентов диагностирована аутоиммунная гемолитическая анемия вследствие системной красной волчанки. У 2 пациентов анемия трактовалась как В12 и фолиеводефицитная, у 3 оставшихся — как анемия хронического заболевания.
Пациенты с анемией были младше (45,0 [ 39,0; 55,0] лет vs 57,0 [ 45,0; 67,8] лет, р=0,001), среди них чаще встречались женщины (72% vs 49%, р=0,007), а среди сопутствующих заболеваний чаще присутствовали ожирение (36% vs 18%, р=0,020) и воспалительные заболевания кишечника (7% vs 1%, р=0,041). Не выявлено различий по показателям гемодинамики малого круга кровообращения, эхокардиографии, а также функционального статуса при сравнении пациентов с анемией и без таковой (табл. 1). При этом продемонстрирована слабая положительная корреляционная связь уровня гемоглобина с дистанцией, пройденной в ТШХ: r=0,16; р=0,013.
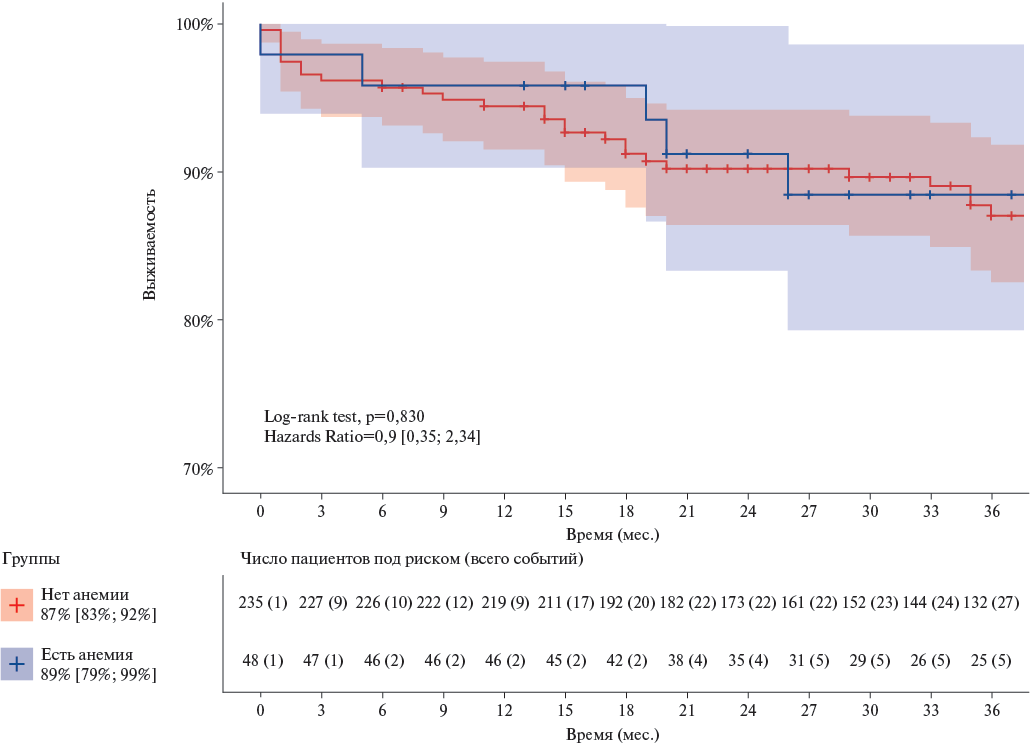
Общая трехлетняя выживаемость пациентов составила 87% [ 73%; 92%], при этом не подтверждено влияние анемии на выживаемость (рис. 1).
Дефицит железа
У 103 включенных в исследование пациентов были оценены показатели обмена железа. В зависимости от используемых критериев распространенность ДЖ среди пациентов с ХТЭЛГ варьировала от 24,5% до 69,1%, что дополнительно иллюстрирует сложность клинической трактовки предлагаемых критериев латентного ДЖ (рис. 2).
С целью поиска наиболее точных критериев ДЖ мы разбили пациентов по уровню СФ в соответствии с обсуждаемыми диагностическими значениями этого показателя на три группы и оценили частоту различных вариантов выполнения критериев ДЖ в этих группах (табл. 2) [11, 14, 19, 20]. Абсолютный ДЖ встречался у 23% пациентов (критерий ДЖ1, соответствующий значению СФ <30 мкг/л). Следует отметить, что с учетом текущих клинических рекомендаций по ведению пациентов с ЛГ, предлагающих в качестве критерия ДЖ уровень СФ <100 или <299 мкг/л при НТЖ <20%, (критерий ДЖ4 в нашем исследовании), наиболее сложной для дифференциального анализа является подгруппа больных с СФ от 30 до 100 мкг/мл — она в нашем исследовании составила 39% (n=40). При наложении на данную подгруппу критерия ДЖ3 (НТЖ <20%) группа с ДЖ уменьшалась до 21 пациента (уменьшалась на 48%, что представляется весьма существенным). Кроме того, при делении подгруппы пациентов с критериями ДЖ4 по значению показателя НТЖ более/менее 20% и сопоставлению полученных подгрупп по более специфичным для обмена железа показателям sTfR, мы получили значимые различия между группами, что косвенно свидетельствует о диагностической значимости показателя НТЖ и важности его применения в группе больных с СФ от 30 до 100 мкг/мл (табл. 3).
Взаимосвязь маркеров субклинического асептического воспаления с показателями обмена железа
У 51 пациента с ХТЭЛГ было также выполнено исследование уровня провоспалительных цитокинов с целью оценки влияния воспаления на показатели обмена железа и уточнения патогенеза и варианта развития ДЖ. Уровень эндотелина-1 был ожидаемо выше у пациентов с ХТЭЛГ при сравнении с донорами, однако различия не достигали статистической значимости, вероятно в силу небольшой численности группы. При исследовании уровня цитокинов в плазме крови в группе ХТЭЛГ по сравнению с группой контроля отмечалось значимое повышение ИЛ-8 (69,5 [ 45,0; 93,8] пг/мл и 40,3 [ 18,5; 45,8] пг/мл, соответственно; р=0,035) и MCP-1 (34,9 [ 30,7; 42,3] и 26,1 [ 20,1; 31,6], соответственно; p=0,002). По другим проанализированным маркерам (СРБ, ИЛ-6 и ИЛ-10) значимых различий получено не было (табл. 4). Не было получено ассоциации уровня СРБ и гепсидина как у пациентов с ХТЭЛГ, так и у доноров. При этом отмечалась сильная отрицательная корреляционная связь показателя СРБ с уровнем сывороточного железа (r=-0,35; p<0,001) и НТЖ (r=-0,32; p<0,001), а также умеренная прямая взаимосвязь MCP-1 с ферритином (r=0,46; p=0,01).
Ассоциация показателей обмена железа и критериев ДЖ с тяжестью ХТЭЛГ и прогнозом больных
При анализе корреляционных связей показателей обмена железа с клинико-инструментальными данными, характеризующими тяжесть больных на момент постановки диагноза ХТЭЛГ, была установлена слабая прямая взаимосвязь уровня гемоглобина с дистанцией в ТШХ (r=0,16; p=0,013) и такими показателями кардио-респираторного нагрузочного тестирования, как кислородный пульс (VO2/HRpeak) (r=0,17; p=0,042) и VO2peakАТ (r=0,21; p=0,033). Среди остальных показателей обмена железа только для параметра НТЖ была установлена слабая прямая корреляционная связь с такими прогностическими показателями, как ТШХ (r=0,21; p=0,032), VO2peakАТ (r=0,26; p=0,044) и SvO2 (r=0,34; p=0,040).
При разделении пациентов на подгруппы по наличию ДЖ, определяемого различными критериями, и его отсутствию, наибольшие различия по показателям тяжести течения ХТЭЛГ получены для критериев ДЖ3 (НТЖ <20%), ДЖ5 (sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics)), ДЖ6 (sTfRF >3,2 (Roche Diagnostics)) и предложенных нами ДЖ8 (СФ <30 мкг/л или 30< СФ <299 мкг/л при НТЖ <20%). Так, пациенты с НТЖ <20% (ДЖ3) имели меньшую дистанцию в ТШХ, более выраженное ремоделирование правого предсердия, а также более высокие вентиляторные эквиваленты по углекислому газу в кардио-респираторном нагрузочном тестировании при сравнении с больными со значением НТЖ >20%: 308 [ 215; 356] метров vs 352 [ 235; 405] метров, p<0,05; 30,0 [ 23,2; 36,4] см2 vs 26,0 [ 21,5; 30,5] см2, p<0,05; 59,6 [ 54,4; 69,1] vs 44,0 [ 41,5; 47,5], p<0,05, соответственно.
При анализе трехлетней выживаемости пациентов с ХТЭЛГ в зависимости от наличия критериев ДЖ получены значимые отличия выживаемости для критериев ДЖ5 (sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics)) и предложенных нами критериев ДЖ8 (виде СФ <30 мкг/л или 30< СФ <299 мкг/л при НТЖ <20%) (рис. 3).
Таблица 1
Клиническая характеристика включенных в исследование пациентов в зависимости от наличия анемии
| Показатель | ХТЭЛГ без анемии (n=235), Ме [Q1; Q3]# | ХТЭЛГ с анемией (n=48), Ме [Q1; Q3]# | Р |
| Возраст на момент включения, годы | 57,0 [ 45,0; 67,8] | 45,0 [ 39,0; 55,0] | 0,001* |
| Женский пол, % | 49% (n=115) | 72% (n=35) | 0,007* |
| I/II/III/IV, % ФК | 3/26/63/9 | 2/17/64/17 | 0,380 |
| Дистанция в ТШХ, м | 320,0 [ 207,0; 407,0] | 271,0 [ 216,0; 339,0] | 0,066 |
| NT-proBNP, пг/мл | 1364,0 [ 290,5; 2798,0] | 1066,5 [ 383,0; 2326,5] | 0,696 |
| Данные эхокардиографического исследования | |||
| Площадь ПП, см2 | 27,0 [ 22,5; 33,5] | 28,0 [ 21,5; 34,0] | 0,887 |
| ПЖ базальный размер, мм | 50,0 [ 44,0; 56,0] | 32,0 [ 31,0; 34,0] | 0,567 |
| ПЖ/ЛЖ | 1,2 [ 1,0; 1,4] | 1,2 [ 1,0; 1,3] | 0,131 |
| TAPSE, мм | 16,0 [ 13,0; 18,0] | 17,0 [ 14,0; 19,0] | 0,408 |
| TAV’S, см/сек | 10,0 [ 8,0; 11,0] | 10,0 [ 8,0; 11,0] | 0,630 |
| FAC, % | 28,0 [ 22,0; 32,0] | 30,0 [ 27,0; 34,0] | 0,158 |
| РСДЛА, мм рт.ст. | 90,0 [ 71,0; 101,0] | 85,0 [ 75,0; 105,0] | 0,875 |
| Наличие выпота в перикарде, % | 18% (n=42) | 17% (n=9) | 0,991 |
| Данные катетеризации правых камер сердца | |||
| срДЛА, мм рт.ст. | 54,0 [ 44,0; 61,0] | 50,0 [ 41,5; 58,2] | 0,133 |
| ДЗЛК, мм рт.ст. | 13,0 [ 11,0; 15,0] | 13,0 [ 10,0; 15,0] | 0,700 |
| ЦВД, мм рт.ст. | 14,0 [ 10,0; 18,0] | 11,0 [ 10,0; 16,0] | 0,148 |
| СИ, л/мин*м2 | 2,0 [ 1,7; 2,4] | 2,0 [ 1,8; 2,5] | 0,467 |
| ЛСС, дин*с*см-5 | 883,0 [ 547,5; 1160,0] | 791,5 [ 517,5; 1139,5] | 0,278 |
| SvO2, % | 92,0 [ 89,0; 95,0] | 93,5 [ 89,0; 96,0] | 0,551 |
| SatO2, % | 60,0 [ 54,0; 66,0] | 58,0 [ 50,0; 62,2] | 0,103 |
| Данные кардио-респираторного нагрузочного тестирования | |||
| VO2peak, %Д (норма >85%) | 54,0 [ 39,0; 68,0] | 52,0 [ 41,2; 61,5] | 0,549 |
| VO2/HRpeak, %Д (норма >85%) | 60,0 [ 48,0; 75,0] | 64,5 [ 57,5; 70,0] | 0,418 |
| VE/VCO2 (норма <34) | 56,0 [ 46,0; 67,1] | 55,0 [ 49,3; 59,3] | 0,844 |
| SpO2peak, % | 91,0 [ 87,5; 93,0] | 93,0 [ 89,0; 95,0] | 0,110 |
Примечание: # — данные представлены в виде медианы и интерквартильного размаха, * — статистически значимый уровень р<0,05.
Сокращения: ДЗЛК — давление заклинивания в легочных капиллярах, ЛЖ — левый желудочек, ЛСС — легочное сосудистое сопротивление, ПЖ — правый желудочек, ПП — правое предсердие, ПЖ/ЛЖ — отношение базальных размеров правого и левого желудочков, РСДЛА — расчетное систолическое давление в легочной артерии, СВ — сердечный выброс, СИ — сердечный индекс, срДЛА — среднее давление в легочной артерии, ТШХ — тест с шестиминутной ходьбой, ЦВД — центральное венозное давление, ФК — функциональный класс, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, FAC — процент изменения площади правого желудочка в одном сердечном цикле, NT-proBNP — N-концевой промозговой натрийуретический пептид, SatO2 — сатурация артериальной крови, SpO2peak — сатурация кислорода на пике ФН, SvO2 — насыщение кислородом смешанной венозной крови, TAPSE — амплитуда движения латеральной части фиброзного кольца трикуспидального клапана, TAV’S — скорость движения латеральной части фиброзного кольца трикуспидального клапана, VE/VCO2 — вентиляторный эквивалент по CO2, VO2peak — пиковое потребление кислорода, выраженное в процентах от должной, VO2/HRpeak — кислородный пульс.

Рис. 1. Кривые трехлетней выживаемости пациентов с ХТЭЛГ в зависимости от наличия анемии.

Рис. 2. Распространенность анемии и ДЖ среди пациентов с ХТЭЛГ в соответствии с различными критериями.
Примечание: анемия — соответствие критериям ВОЗ; ДЖ1 — СФ <30 мкг/л [14]; ДЖ2 — СФ <100 мкг/л [11]; ДЖ3 — НТЖ <20% [19]; ДЖ4 — СФ <100 или <299 мкг/л при НТЖ <20% [20]; ДЖ5 — sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics); ДЖ6 — sTfRF >3,2 (Roche Diagnostics); ДЖ7 — sTfRF >2,0 (Roche Diagnostics); ДЖ8 — СФ <30 или СФ <299 мкг/л при НТЖ <20% (предложен авторами).
Сокращения: ДЖ — дефицит железа, НТЖ — насыщение трансферрина железом, СФ — сывороточный ферритин, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, sTfR — растворимые рецепторы трансферрина, sTfRF — отношение растворимых рецепторов трансферрина к логарифму ферритина сыворотки.
Таблица 2
Частота наличия критериев ДЖ в трех подгруппах больных в зависимости от уровня СФ крови
| Критерии дефицита железа | СФ <30 мкг/л, n=24 (23%) | 30< СФ <100 мкг/л, n=40 (39%) | СФ >100 мкг/л, n=39 (38%) |
| ДЖ1 (СФ <30 мкг/л) | 24 (100%) | 0 (0%) | 0 (0%) |
| ДЖ2 (СФ <100 мкг/л) | 24 (100%) | 40 (100%) | 0 (0%) |
| ДЖ3 (НТЖ <20%) | 21 (95%) | 21 (55%) | 7 (18%) |
| ДЖ4 (СФ <100 или <299 мкг/л при НТЖ <20%) | 24 (100%) | 40 (100%) | 7 (18%) |
| ДЖ5 (sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics)) | 17 (89%) | 12 (35%) | 4 (11%) |
| ДЖ6 (sTfRF >3,2 (Roche Diagnostics)) | 17 (89%) | 9 (26%) | 1 (3%) |
| ДЖ7 (sTfRF >2 0 (Roche Diagnostics)) | 18 (95%) | 20 (59%) | 6 (16%) |
| ДЖ8 (СФ <30 мкг/л или 30< СФ <299 мкг/л при НТЖ <20%) | 24 (100%) | 21 (55%) | 7 (18%) |
Сокращения: ДЖ — дефицит железа, НТЖ — насыщение трансферрина железом, СФ — сывороточный ферритин, sTfR — растворимые рецепторы трансферрина, sTfRF — отношение растворимых рецепторов трансферрина к логарифму ферритина сыворотки.
Таблица 3
Частота наличия критериев ДЖ на основе растворимых рецепторов трансферрина и индекса sTfRF в особой подгруппе больных с пограничным значением ферритина и разным уровнем НТЖ
| Критерии дефицита железа | 30< СФ <100 мкг/л, n=40 (39%) | р | |
| НТЖ <20% (n=21) | НТЖ >20% (n=19) | ||
| ДЖ5 (sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics)), % | 61 (n=13) | 0 | <0,001 |
| ДЖ6 (sTfRF >3,2 (Roche Diagnostics)), % | 44 (n=9) | 0 | 0,004 |
| ДЖ7 (sTfRF >2,0 (Roche Diagnostics)), % | 89 (n=17) | 20 (n=4) | <0,001 |
Сокращения: ДЖ — дефицит железа, НТЖ — насыщение трансферрина железом, СФ — сывороточный ферритин, sTfR — растворимые рецепторы трансферрина, sTfRF — отношение растворимых рецепторов трансферрина к логарифму ферритина сыворотки.
Таблица 4
Уровни маркеров воспаления у пациентов с ХТЭЛГ и группы контроля
| ХТЭЛГ (n=51), Ме [Q1; Q3]# | Доноры (n=24), Ме [Q1; Q3]# | р | |
| СРБ, мг/л | 2,13 [ 1,28; 5,08] | 1,28 [ 0,38; 3,43] | 0,039* |
| Гепсидин, пг/мл | 1126 [ 936; 1545] | 658 [ 614; 1544] | 0,210 |
| ИЛ-6, пг/мл | 2,01 [ 1,46; 2,73] | 2,07 [ 1,49; 2,75] | 0,964 |
| ИЛ-8, пг/мл | 74,9 [ 41,9; 108,5] | 39,8 [ 18,3; 68,2] | 0,035* |
| ИЛ-10, пг/мл | 2,87 [ 2,16; 4,22] | 2,93 [ 2,16; 3,13] | 0,529 |
| MCP-1, пг/мл | 62,8 [ 32,7; 118,0] | 27,6 [ 22,1; 35,0] | 0,002* |
| ET-1, пг/мл | 63,6 [ 73,2; 82,7] | 65,8 [ 59,1; 73,7] | 0,096 |
Примечание: # — данные представлены в виде медианы и интерквартильного размаха, * — статистически значимый уровень р<0,05.
Сокращения: ИЛ — интерлейкин, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, СРБ — С-реактивный белок, ЕТ-1 — эндотелин-1, МСР-1 — моноцитарный хемотаксический протеин-1.

Рис. 3. Кривые трехлетней выживаемости пациентов с ХТЭЛГ в зависимости от критериев ДЖ.
Примечание: ДЖ1 — СФ <30 мкг/л [14]; ДЖ2 — СФ <100 мкг/л [11]; ДЖ3 — НТЖ <20% [19]; ДЖ4 — СФ <100 или <299 мкг/л при НТЖ <20% [20]; ДЖ5 — sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics); ДЖ6 — sTfRF >3,2 (Roche Diagnostics); ДЖ7 — sTfRF >2,0 (Roche Diagnostics); ДЖ8 — СФ <30 или СФ <299 мкг/л при НТЖ <20% (предложен авторами).
Сокращения: ДЖ — дефицит железа, НТЖ — насыщение трансферрина железом, СФ — сывороточный ферритин, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, sTfR — растворимые рецепторы трансферрина, sTfRF — отношение растворимых рецепторов трансферрина к логарифму ферритина сыворотки.
Обсуждение
С целью уточнения оптимальных критериев ДЖ у пациентов с ХТЭЛГ нами выполнено последовательное применение различных критериев с использованием принципиально разных показателей обмена железа. Критерии абсолютного ДЖ по значению СФ <30 мкг/л (ДЖ1) были выявлены только у 24,5% пациентов, а средний уровень СФ в обследованной группе был достаточно высок и составлял 73,8 [ 27,6; 123,2] мкг/л. Согласно результатам нашей предыдущей работы, согласующимся с международным опытом, для пациентов с ХТЭЛГ характерны более высокие значения СФ при сравнении с другим вариантом прекапиллярной ЛГ — идиопатической артериальной гипертензии [21][22], что делает данный показатель сложным для трактовки и исключает его изолированное использование для диагностики ДЖ. Эта особенность связана с влиянием хронического воспаления, которое является важнейшим звеном патогенеза ХТЭЛГ: в условиях воспаления СФ ведет себя как белок острой фазы и, вследствие этого, может давать повышение уровня в отсутствии каких-либо изменений в общих запасах железа в организме [23][24]. Помимо этого, при хронических воспалительных состояниях повышение уровня гепсидина приводит к секвестрации железа в макрофагах. Это реализуется в нормальном или даже высоком уровне СФ, несмотря на снижение доступности железа для эритропоэза, так называемом функциональном ДЖ. В нашем исследовании в пользу наличия низкоградиентного асептического воспаления свидетельствует повышение уровня СРБ, ИЛ-8 и МСР-1 у пациентов с ХТЭЛГ при сравнении с контролем. Следует отметить, что в рамках концепции анемии хронического заболевания хорошо известно об относительном ДЖ вследствие его секвестрации в клетках ретикуло-эндотелиальной системы при хроническом воспалении различной этиологии, сопровождающимся умеренной гиперцитокинемией [25]. О вероятном влиянии воспаления на обмен железа в нашем исследовании свидетельствует сильная отрицательная корреляционная связь показателя СРБ с уровнем сывороточного железа (r=-0,35; p<0,001) и НТЖ (r=-0,32; p<0,001). МСP-1 (или CCL2) относится к группе СС-хемокинов, являясь при этом мощным фактором хемотаксиса моноцитов и, таким образом, одним из ключевых цитокинов, ответственных за регуляцию макрофагального компонента в процессе воспаления. MCP-1 синтезируется различными типами клеток, в т.ч. эндотелиоцитами, фибробластами, моноцитами и макрофагами [26]. Повышение уровня MCP-1 в плазме крови у пациентов с ХТЭЛГ отмечалось во многих исследованиях, в которых авторами в т.ч. была установлена корреляционная связь уровня ИЛ-8 и МСР-1 с характером клеточного состава воспалительного инфильтрата стенки легочной артерии по результатам гистологического исследования материала, полученного при легочной тромбэндартерэктомии, в котором основными клетками были фагоциты [24]. При анализе связи провоспалительных цитокинов с показателями эритропоэза и обмена железа была установлена прямая корреляционная связь MCP-1 с ферритином. Ключевой молекулой, определяющей взаимосвязь метаболизма железа и воспаления, считается пептид — гепсидин, продуцируемый в первую очередь печенью, а также клетками иммунной системы (например, макрофагами и нейтрофилами) в процессе врожденного иммунного ответа посредством активации толл-подобного рецептора-4 (TLR-4). Гепсидин является регулирующим обмен железа белком: он подавляет абсорбцию железа в кишечнике и выход железа из депо, что снижает системную биодоступность железа и приводит к его перераспределению в условиях воспаления, в т.ч. к повышению уровня СФ. Продукция гепсидина напрямую связана с уровнем провоспалительных цитокинов, в частности ИЛ-6, ИЛ-1β [27][28]. Показано, что при ЛГ системное или локальное воспаление индуцирует экспрессию гепсидина, нарушая гомеостаз железа в гладкомышечных клетках легочной артерии [29]. Кроме того, в работе Valenti L, et al. продемонстрирована прямая взаимосвязь уровня MCP-1 c уровнем гепсидина в плазме крови у пациентов с атеросклерозом на фоне метаболического синдрома [30]. Эти данные объясняют выявленную нами прямую корреляцию уровня МСP-1 и СФ в настоящем исследовании. При этом нами не было получено отличий по значению уровня гепсидина и ИЛ-6, как одного из ключевых стимуляторов синтеза гепсидина, у пациентов и доноров, а также ассоциации уровня СРБ и гепсидина как у больных с ХТЭЛГ, так и у доноров.
Чтобы учесть влияние воспаления в литературе предлагается использовать иные, чем для пациентов без хронического воспаления, пороговые значения СФ для выявления ДЖ, однако здесь существует значительная вариабельность рекомендаций (<50, <100 или <200 мкг/л). Наиболее распространенным является использование уровней СФ <100 мкг/л для диагностики ДЖ при хронических воспалительных состояниях [11]. В нашем исследовании уровень СФ <100 мкг/л (ДЖ2) отмечался у 61,7% пациентов ХТЭЛГ (среди женщин 100% и 85%, соответственно), т.е. использование данного критерия приводило к расширению группы с констатацией ДЖ. При дальнейшем расширении критериев по значению СФ (ДЖ4) — использовании наиболее часто предлагаемого сочетания параметров обмена железа для пациентов с хронической СН — СФ <100 мкг/л или 100-299 мкг/л при НТЖ <20%, отмечалось дополнительное увеличение числа больных с ДЖ до 69,1%. В данном подходе показатель НТЖ, рассчитанный в нашей работе исходя из значения трансферрина сыворотки, отражающего истинную потребность в железе и в меньшей степени зависящего от воспаления показателя, накладывал ограничения только в подгруппе с СФ >100 мкг/л. Использование же только показателя НТЖ <20% (ДЖ3), без учета СФ, сокращало долю пациентов с ДЖ до 50%, что по данным ряда работ представляется патогенетически более целесообразно, т.к. значение НТЖ отражает как абсолютный, так и функциональный ДЖ. Кроме того, важна доступность теста в условиях Российской Федерации, а именно возможность расчета НТЖ с использованием сывороточного железа и показателя общей железосвязывающей способности сыворотки. Важным аргументов в пользу клинической значимости показателя НТЖ являются полученные нами данные о том, что пациенты с НТЖ <20% (ДЖ3) имели меньшую дистанцию в ТШХ, более выраженное ремоделирование правых камер сердца, а также более высокие вентиляторные эквиваленты по углекислому газу по результатам кардио-респираторного нагрузочного тестирования при сравнении с больными со значением НТЖ >20%.
В контексте неопределенности трактовки уровня маркеров обмена железа в условиях хронического воспаления нами также оценивался sTfR (ДЖ5) и индекс sTfRF (ДЖ6) с пороговым значением «3,2», что дополнительно снижало частоту детекции ДЖ в группе ХТЭЛГ до 32,9%. При этом важно понимать, что уровень sTfR отражает не только ДЖ, но и активацию эритропоэза в качестве компенсаторного механизма на фоне хронической системной гипоксии при тяжелом варианте течения ХТЭЛГ. В пользу этого могут свидетельствовать значимая положительная корреляционная связь между sTfR и NT-proBNP (r=0,450, p<0,001), а также отрицательная с ТШХ (r=-0,352, р=0,006), а также значимые отличия в трехлетней выживаемости больных с ХТЭЛГ в зависимости от наличия критерия ДЖ5 (sTfR, мг/л: ж >4,4; м >5,0 (Roche Diagnostics)): 100% vs 89% (long-rank test, р=0,017). Подобные результаты были получены в исследовании Sonnweber T, et al., которые с помощью индекса sTfRF выявили ДЖ у 33-48% пациентов с ЛГ и отметили более высокую смертность у пациентов с ДЖ (11%) в сравнении с группой без ДЖ (1,4%) при его определении на основе уровня sTfR, вне зависимости от наличия анемии. Подобных связей не наблюдалось при использовании других критериев, на основе СФ и НТЖ [2]. При анализе подгрупп больных со значением НТЖ более/менее 20% были получены значимые различия в показателе sTfR и индексе sTfRF, что косвенно, на наш взгляд, подтверждает диагностическую значимость показателя НТЖ у пациентов с ХТЭЛГ.
На основании полученных результатов нами предлагается дополненное текущее определению ДЖ для пациентов с ХТЭЛГ, где критерий НТЖ <20% распространяется и на подгруппу больных с пограничным значением СФ от 30 до 100 мкг/л, сокращая число больных с ДЖ с 69,1% до 44,6%, что представляется клинически значимым (рис. 1). Дополнительным свидетельством целесообразности данного подхода в определении ДЖ может служить значимое различие в трехлетней выживаемости, отмеченное в подгруппах с наличием и отсутствием предлагаемого нами определения ДЖ8 (СФ <30 или СФ <299 мкг/л при НТЖ <20%): 100% vs 89% (long-rank test, р=0,021) (рис. 3).
Заключение
На основании проведенного исследования получены данные в пользу диагностической значимости показателя НТЖ для диагностики ДЖ у пациентов с ХТЭЛГ и предложены дополненные критерии ДЖ в виде СФ <30 мкг/л или 30< СФ <299 мкг/л при НТЖ <20%, требующие дальнейшей апробации и валидации у пациентов с различными вариантами прекапиллярной ЛГ.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Симакова М.А., Карпова Ю.И., Золотова Е.А., Вавилова Т.В., Моисеева О.М. Железодефицитные состояния у пациентов с хронической тромбоэмболической легочной гипертензией: распространенность, патогенез и критерии диагностики. Российский кардиологический журнал. 2025;30(2S):6475. https://doi.org/10.15829/1560-4071-2025-6475. EDN: DPVQVZ
Скопировать