Клиническое течение легочной гипертензии в зависимости от гемодинамического типа и гистологической картины микрососудистого русла легких у пациентов после коррекции митральных пороков сердца
Аннотация
Цель. Выделить основные различия пациентов, подвергающихся хирургической коррекции приобретенного порока (ППС) митрального клапана (МК), в зависимости от типа легочной гипертензии (ЛГ) до операции; идентифицировать факторы, ассоциирующиеся с сохранением ЛГ и ее типом спустя год после хирургической коррекции порока МК.
Материал и методы. В рамках открытого одноцентрового проспективного исследования проведен анализ 40 пациентов с ППС МК неинфекционного генеза, подвергающихся коррекции порока, с верифицированной ЛГ согласно данным катетеризации правых камер (КПОС) сердца: 15 пациентов с изолированной посткапиллярной ЛГ и 25 пациентов с комбинированной пост-/прекапиллярной формой ЛГ. Интраоперационно 26 пациентам с ЛГ была проведена пункционная биопсия ткани правого лёгкого c дальнейшей микроскопией готовых гистологических препаратов. Спустя год после операции выполнялась КПОС для оценки динамики ЛГ. В качестве показателя вклада комплекса факторов в характер динамики ЛГ после операции использовались значения рангов значимости предикторов.
Результаты. Для пациентов с ППС и комбинированной пост-/прекапиллярной ЛГ было характерно более выраженное нарушение сердечно-сосудистого сопряжения правого желудочка–легочной артерии и повышение уровня маркеров миокардиального напряжения, более тяжелые изменения гемодинамики малого круга кровообращения, артериализация венул и более частое наличие пандемического тромбоза артериол (53,3%) по сравнению с пациентами с изолированной посткапиллярной ЛГ (9%). По данным КПОС спустя год после операции (n=21) у 28,5% наблюдался регресс ЛГ, у 42,85% сохранялась изолированная посткапиллярная ЛГ, а у 28,5% комбинированная пост-/прекапиллярная ЛГ. Факторами, оказывающими наиболее значимый вклад в регресс ЛГ спустя год после операции, являются: поражение МК по типу стеноза — 100 у.е., наличие фибрилляции предсердий — 73 у.е., наличие сахарного диабета 2 типа — 72 у.е., сочетанное вмешательство на МК и аортальном клапане — 61 у.е., степень ожирения — 56 у.е., мужской пол — 48 у.е. Характер морфологических изменений легких не оказал значимый вклад в периоперационную динамику ЛГ.
Заключение. Пациентов с ППС и комбинированной пост-/прекапиллярной ЛГ характеризует более выраженное нарушение сердечно-сосудистого сопряжения правого желудочка–легочной артерии, повышение уровня маркеров миокардиального напряжения, тяжелые изменения гемодинамики малого круга кровообращения с артериализацией венул и более частым наличием пандемического тромбоза артериол. Впервые выявлены факторы, в т.ч. потенциально модифицируемые, оказывающие наиболее значимый вклад в характер динамики ЛГ спустя год после операции.
Среди причин легочной гипертензией (ЛГ) на фоне патологии левых камер сердца (группа 2) значительную долю составляют пациенты с митральными пороками. ЛГ с уровнем расчетного систолического давления (рСДЛА) >50 мм рт.ст. по данным трансторакальной эхокардиографии (ЭхоКГ) наблюдается более, чем у 38% пациентов с митральным стенозом и более, чем у 23% больных с митральной недостаточностью [1][2]. Предоперационная ЛГ является фактором риска как раннего, так и долгосрочного неблагоприятного исхода у пациентов с приобретенными пороками сердца (ППС). У пациентов с пороком митрального клапана (МК) по типу стеноза присутствие ЛГ с рСДЛА =58,1 мм рт.ст. отражается в 5,5% риске интраоперационной смерти. Значение рСДЛА, превышающее системное давление, ассоциируется с 5-кратным увеличением риска интраоперационного летального исхода [3].
Согласно гемодинамической классификации ЛГ на фоне патологии левых камер сердца выделяют два принципиально разных типа: изолированная посткапиллярная и комбинированная пост-/прекапиллярная ЛГ. Данные типы ЛГ характеризуются различиями как в гемодинамике, где определяющим выступает уровень легочного сосудистого сопротивления (ЛСС), так и в характере ремоделирования сердца, как следствие отличается тяжесть симптомов, качество жизни и прогноз пациентов с ЛГ.
Критериями для верификации изолированной посткапиллярной ЛГ согласно данным катетеризации правых камер сердца (КПОС) являются: уровень среднего давления в легочной артерии (срДЛА) >20 мм рт.ст., значение давления заклинивания легочной артерии (ЛА) >15 мм рт.ст. и не повышенный уровень ЛСС (≤ 2 ед. Вуда). В свою очередь, отличительной чертой комбинированной пост-/прекапиллярной формы ЛГ является повышение уровня ЛСС >2 ед. Вуда при вышеуказанных уровнях срДЛА и давления заклинивания ЛА [4].
Именно при комбинированной пост-/прекапиллярной ЛГ хроническое повышение давление в левом предсердии у пациентов с заболеваниями левых отделов сердца вызывает более выраженное необратимое ремоделирование легочного микрососудистого русла и повышение ЛСС, что обычно не наблюдается при изолированной посткапиллярной форме ЛГ. Пациенты с комбинированной пост-/прекапиллярной ЛГ, по-видимому, находятся в середине спектра прекапиллярной и изолированной посткапиллярной ЛГ с точки зрения их клинической характеристики и выраженности ремоделирования правых камер сердца [2][5].
Современные исследования показывают, что регресса ЛГ и нормализации ЛСС не происходит примерно у 40% симптоматических пациентов с тяжелым митральным стенозом, несмотря на успешные вмешательства на клапане и сохранную функцию левого желудочка (ЛЖ) [6-9].
Представляется актуальным выделить основные различия пациентов, подвергающихся хирургической коррекции приобретенного порока МК, в зависимости от типа ЛГ до операции, на основании изучения характера ремоделирования правых камер сердца и уровня маркеров миокардиального напряжения, параметров гемодинамики малого круга кровообращения, а также особенностей морфологической картины легочной ткани и сосудов легких; идентифицировать факторы, ассоциирующиеся с сохранением ЛГ и ее типом спустя год после хирургической коррекции порока МК, что и явилось целью нашего исследования.
Материал и методы
Исследование является открытым одноцентровым проспективным с включением 64 пациентов с пороком МК неинфекционного генеза в возрасте с 35 до 75 лет (медиана возраста 61,0 [ 50,0; 67,0], 53,1% мужского пола) и высокой вероятностью ЛГ по данным ЭхоКГ. На момент включения в исследование все пациенты имели показания к кардиохирургической коррекции порока, которой были подвержены в дальнейшем в период с 2024г января по март 2025г. До хирургической коррекции порока всеми пациентами собственноручно были подписаны информированные согласия на возможность использования их истории заболевания, данных проведенных обследований, выполнение интраоперационной биопсии легкого. Исследование проведено на базе Научно-исследовательского института комплексных проблем сердечно-сосудистых заболеваний при поддержке гранта Российского научного фонда № 24-75-10031. Исследование проведено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practiсe) и принципами Хельсинкской Декларации. Протокол исследования одобрен локальным этическим комитетом НИИ КПССЗ (заседание локального этического комитета № 7 от 16.09.2024)
Критериями включения в исследование являлись:
— планируемое кардиохирургическое вмешательство в условиях искусственного кровообращения в виде изолированной коррекции порока МК или в сочетании с коррекцией порока аортального клапана/трикуспидального клапана (ТК) у пациентов с ППС, ассоциированным с ревматической болезнью сердца или соединительно-тканной дисплазией или дегенеративным поражением,
— возраст от 35 до 75 лет,
— согласие пациента на участие в исследовании.
Критерии исключения были следующими:
— ППС вследствие инфекционного эндокардита,
— наличие ишемической болезни сердца, требующей реваскуляризации миокарда,
— наличие сниженной фракции выброса ЛЖ,
— тяжелые сопутствующие заболевания, существенно затрудняющие проведение комплексного обследования (онкология, острое нарушение мозгового кровообращения с грубым неврологическим дефицитом, психические заболевания и пр.),
— острые состояния в течение предшествующих 6 мес. (инфаркт миокарда, острое нарушение мозгового кровообращения, тромбоэмболия ЛА),
— тяжелые послеоперационные осложнения (полиорганная недостаточность),
— наличие тяжелой патологии легких (бронхиальная астма, хроническая обструктивная болезнь легких; паренхиматозное заболевание легких).
Из 64 пациентов у 32,8% имело место поражение МК по типу стеноза, у 42,2% присутствовала недостаточность МК, а у 25% было сочетание стеноза и недостаточности. Комбинированный порок сердца имел место у 64,1% пациентов и был представлен в 14,1% случаях недостаточностью или стенозом аортального клапана, а в 50% случаев сопутствующей недостаточ- ностью ТК. Из включенных пациентов у 56,3% имел место ревматический генез, у 25% синдром соединительно-тканной дисплазии, у 10,9% дегенеративный генез порока и у 7,8% частичный отрыв хорд МК.
В качестве наиболее распространенной сопутствующей кардиологической патологии первое место занимала артериальная гипертензия, диагностируемая у 76,5% пациентов, в то время как у 60,9% имела место избыточная масса тела или ожирение. Наличие фибрилляции предсердий (ФП) до операции характеризовало 59,4% пациентов преимущественно за счет персистирующей формы (57,9%). У 35,9% имело место курение в анамнезе.
Критериями, определяющими высокую вероятность ЛГ согласно данным ЭхоКГ, являлись скорость трикуспидальной регургитации 2,9 м/с и выше (уровень рСДЛА ≥38 мм рт.ст.), и наличие дополнительных признаков ЛГ. Помимо стандартного протокола ЭхоКГ пациентам также выполнялся расширенный протокол с оценкой функции правого желудочка (ПЖ) и сердечно-сосудистого сопряжения ПЖ-ЛА (отношение систолической экскурсии кольца ТК (TAPSE) к рСДЛА).
У 45 пациентов из 64 пациентов, имеющих высокую вероятность ЛГ по данным ЭхоКГ до операции, для подтверждения ЛГ выполнялась КПОС. У 5 пациентов проведение КПОС не подтвердило наличие ЛГ, ранее подозреваемой по ЭхоК Г. Из 40 пациентов изолированная посткапиллярная форма ЛГ диагностирована у 15 больных с ППС МК (37,5%), комбинированная пост-/прекапиллярная — у 25 пациентов (62,5%) до операции. Помимо оценки манометрических показателей в течение КПОС пациентам выполнялся вазореактивный тест с ингаляцией 20 мкг/2 мл (1 ампула) илопроста в течение 5 мин, с последующей повторной оценкой динамики срДЛА, сердечного выброса (СВ) и ЛСС.
КПОС проводилась повторно спустя год после операции с целью идентификации регресса ЛГ или сохранения ЛГ с верификацией ее типа.
Выполнялся забор крови натощак с помощью вакуумных пробирок с активатором свертывания крови. Кровь центрифугировали, сыворотка крови хранилась в морозильной камере при температуре -70 C. Были определены концентрации биомаркеров миокардиального напряжения: N-концевого промозгового натрийуретического пептида (NT-proBNP) (референсные значения: 0-125 пг/мл) и стимулирующего фактора роста, экспрессируемого геном 2 (референсные значения: 0-35 нг/мл) в сыворотке крови с помощью метода твердофазового иммуноферментного анализа, используя коммерческие наборы. С помощью тест-систем определяли количественно уровень в сыворотке крови: NT-proBNP (Biomedical, Slovakia) и presage ST2 assay (Critical Diagnostics, USA).
Интраоперационно 26 пациентам с ЛГ (подтвержденной по данным КПОС) была проведена пункционная биопсия ткани правого лёгкого из переднего (S3) или медиального сегмента (SV) c дальнейшей микроскопией готовых гистологических препаратов для оценки изменения паренхимы легкого и микрососудистого русла, состояния бронхов; проведением морфометрического исследования сосудов с оценкой: площади сосудистой стенки, просвета сосуда, площади сосудистых оболочек (интимы, медии, адвентиции).
Химическую фиксацию тканей осуществляли в двух сменах 10% нейтрального забуференного формалина (ЭргоПродакшн) в течение 24 ч при комнатной температуре с заменой через первые 2 ч. Далее ткани промывали проточной водопроводной водой в течение 2 ч и подвергали дегидратации в этаноле возрастающей концентрации (50, 60, 70, 80 и 95%, по 1 ч на каждую смену этанола). На следующем этапе дегидратированные биоптаты пропитывали в трех сменах расплавленного парафина «Гистомикс Экстра» (по 1 ч в каждой при 60 C, температура плавления парафина 54-56 C, ЭргоПродакшн) и далее заливали в парафин «Мистер Вакс Экстра» (температура плавления парафина 56-58 C, ЭргоПродакшн). Полученные парафиновые блоки охлаждали при 4 C. Гистологическую резку выполняли на ротационном микротоме Microm HM 325 (Thermo Scientific). На каждое стекло помещали 3 гистологических среза толщиной 3 мкм.
Прогрессивное окрашивание гематоксилином и эозином выполняли с использованием гематоксилина Гариса (ЭргоПродакшн) и водно-спиртового эозина (ЭргоПродакшн), согласно стандартному протоколу производителя: депарафинизация в ксилоле (3 смены по 5 мин, ЭКОС-1), отмывка в бидистиллированной воде, инкубация в гематоксилине Гариса 10 мин, подсинение в водопроводной воде, инкубация в эозине 2 мин, обезвоживание в 95% этаноле (3 смены по 5 мин), просветление срезов в ксилоле (3 мин). После чего срезы заключали в монтирующую среду на основе заменителя ксилола (DiaPath) под покровное стекло (ЭргоПродакшн).
С готовых микропрепаратов получали цифровые копии путем сканирования на слайд сканере Leica Aperio AT2 (Leica Biosystems, Германия) с использованием стандартных настроек. Полученные слайды анализировали с помощью программного обеспечения SlideViewer.
Измерения площади гиперплазии интимы, площади и толщины сосудистых оболочек, наибольшей толщины интимы в месте гиперплазии, периметра и просвета сосудов выполняли с использованием программы ImageJ (National Institutes of Health).
Статистическая обработка данных. Статистический анализ проводился с использованием программы StatTech v. 4.8.0 (разработчик — ООО «Статтех», Россия). Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Колмогорова-Смирнова. В связи с отсутствием нормального распределения количественные данные описывались с помощью медианы (Me) и 25 и 75 квартилей (Q1-Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Оценка различий количественных показателей для двух независимых групп проводилась с помощью критерия Манна-Уитни; качественных показателей — с применением критерия Хи-квадрат Пирсона. Для оценки связи между количественными и качественными переменными использовался коэффициент ранговой корреляции Kendall-Tau. Прогностическая связь развития неблагоприятных исходов с факторами риска оценена посредствам бинарной логистической регрессии. Различия считались статистически значимыми при p<0,05.
В качестве показателя вклада комплекса факторов в характер динамики ЛГ по данным КПОС спустя год после операции использовались значения рангов значимости предикторов (при использовании деревьев классификации было выбрано дискриминантное одномерное ветвление и оценивалась значимость предикторов в процессе классификации). Для каждой из анализируемых независимых переменных устанавливался ранг ее значимости по 100-балльной шкале (0 соответствовал низкой значимости, а 100 — высокой).
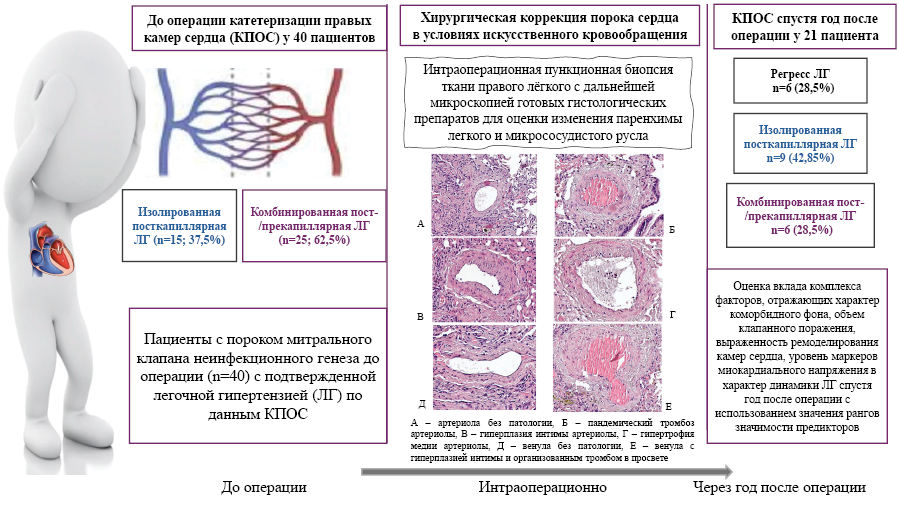
Дизайн исследования представлен на рисунке 1.
Результаты
Представлены основные различия пациентов с ППС МК в зависимости от типа ЛГ. Для пациентов с ППС и дооперационной комбинированной пост-/прекапиллярной ЛГ было характерно более выраженное повышение рСДЛА по данным ЭхоКГ, более выраженное нарушение сердечно-сосудистого сопряжения ПЖ-ЛА и повышение уровня маркеров миокардиального напряжения, более тяжелые изменения гемодинамики малого круга кровообращения с характерным ответом на вазореактивный тест илопростом именно для данной группы пациентов в виде снижения срДЛА и СВ с повышением ЛСС до коррекции порока. Данная когорта больных также характеризовалось проведением вмешательства на большем количестве клапанов (табл. 1).
При анализе морфологической картины паренхимы легких и сосудистого русла в зависимости от типа ЛГ у 26 пациентов с ППС МК, отмечено значимо более частое наличие пандемического тромбоза артериол, характеризующее именно пациентов с комбинированной пост-/прекапиллярной ЛГ (рис. 2, табл. 2).
При проведении микроскопии артериол и венул у пациентов с ППС МК и комбинированной пост-/прекапиллярной ЛГ отмечено большее значение площади венулы и ее просвета, также как интимы венулы, площади сочетания интимы, медии и просвета венулы, как и отношения адвентиции венулы к площади венулы по сравнению с пациентами с изолированной посткапиллярной ЛГ (табл. 3).
Выявлено, что поражение МК по типу стеноза характеризуется более частым присутствием тромбированных капилляров, отношение шансов (ОШ) 8,75 (95% доверительный интервал (ДИ): 1,1-69,5, р=0,029), а также очаговым интерстициальным фиброзом, ОШ 10,66 (95% ДИ: 0,89-126,78, р=0,046) (рис. 3). Наличие митрального стеноза имеет умеренную корреляцию с периваскулярным фиброзом (коэффициент ранговой корреляции Kendall-Tau =0,41; p=0,005).
Через год после операции у 21 пациента из группы дооперационной ЛГ была выполнена КПОС в динамике. Несмотря на успешную хирургическую коррекцию порока МК, через 1 год после вмешательства регресс ЛГ наблюдался только у 6 человек (28,5%), с сохранением спустя год после вмешательства у 6 пациентов комбинированной пост-/прекапиллярной ЛГ (28,5%) и у 9 пациентов изолированной посткапиллярной ЛГ (42,85%).
В качестве показателя вклада комплекса факторов, отражающих характер коморбидного фона, тип и объем клапанного поражения, выраженность ремоделирования камер сердца, уровень маркеров миокардиального напряжения в характер динамики ЛГ спустя год после операции использовались значения рангов значимости предикторов. Ранг значимости переменной по 100-балльной шкале: 0 соответствовал низкой значимости, а 100 — высокой.
Факторами, оказывающими наиболее значимый вклад в регресс ЛГ по данным КПОС спустя год после операции, являются: поражение МК по типу стеноза — 100 у.е., наличие ФП/трепетания предсердий (ТП) — 73 у.е., наличие сахарного диабета (СД) 2 типа — 72 у.е., сочетанное вмешательство на МК и аортальном клапане — 61 у.е., степень ожирения — 56 у.е., мужской пол — 48 у.е. (табл. 4).
Факторами, оказывающими наиболее значимый вклад в сохранение изолированной посткапиллярной ЛГ спустя год после операции, являются: поражение МК по типу стеноза — 100 у.е., наличие СД 2 типа — 90 у.е. (табл. 5).
Наиболее значимым фактором, оказывающим вклад в сохранение комбинированной пост-/прекапиллярной формы ЛГ спустя год после операции, является количество корригированных клапанов — 100 у.е. (табл. 6).
Характер морфологических изменений легких не оказал значимый вклад в особенности периоперационной динамики ЛГ спустя год после операции.

Рис. 1. Графический абстракт статьи.
Сокращения: КПОС — катетеризация правых отделов сердца, ЛГ — легочная гипертензия.
Таблица 1
Основные различия между изолированной посткапиллярной ЛГ и комбинированной пост-/прекапиллярной у пациентов с ППС МК до операции
|
Параметры |
Изолированная посткапиллярная ЛГ (n=15) |
Комбинированная пост-/прекапиллярная ЛГ (n=25) |
p |
|
Пол мужской, n (%) |
6 (40,0%) |
12 (48,0%) |
0,69 |
|
Возраст на момент операции, годы |
64,5 (59,0; 69,5) |
63,0 (43,0; 68,0) |
0,708 |
|
Стеноз МК, n (%) |
9 (60,0%) |
12 (48,0%) |
0,416 |
|
Стеноз+недостаточность МК, n (%) |
5 (33,33%) |
5 (20,0%) |
0,312 |
|
Количество корригированных клапанов, n |
1,0 (1,0; 1,0) |
2,0 (1,0; 2,0) |
0,026 |
|
Сопутствующие состояния |
|||
|
Фибрилляция/трепетание предсердий, n (%) |
7 (46,66%) |
13 (52,0%) |
0,992 |
|
Индекс массы тела, кг/м2 |
26,6 (23,8; 32,2) |
28,4 (22,4; 31,2) |
0,888 |
|
Ожирение, n (%) |
5 (33,3%) |
8 (32,0%) |
0,554 |
|
Сахарный диабет 2 типа, n (%) |
3 (20,0%) |
3 (12,0%) |
0,374 |
|
Хроническая болезнь почек 3а-5 стадия, n (%) |
6 (40,0%) |
14 (56,0%) |
0,420 |
|
Анамнез курения, n (%) |
6 (40,0%) |
7 (28,0%) |
0,828 |
|
Различия в данных ремоделирования правых камер сердца и уровне рСДЛА |
|||
|
TAPSE/рСДЛА, см/мм рт.ст. |
0,031 (0,028; 0,040) |
0,022 (0,016; 0,029) |
0,047 |
|
рСДЛА до операции по ЭхоКГ |
53,0 (45,5; 62,5) |
71,0 (55,0; 85,0) |
0,023 |
|
Уровень рСДЛА 38-50 мм рт.ст. по ЭхоКГ до операции |
11 (73,3%) |
6 (24,0%) |
0,025 |
|
Уровень рСДЛА >50 мм рт.ст. по ЭхоКГ до операции |
4 (26,6%) |
20 (80%) |
0,04 |
|
Данные катетеризации правых камер сердца до операции |
|||
|
срДЛА, мм рт.ст. |
31,5 (26,0; 35,5) |
38,5 (31,0; 44,0) |
0,047 |
|
Сердечный индекс, л/мин/м2 |
2,29 (2,1; 2,6) |
2,1 (1,6; 2,3) |
0,06 |
|
Сердечный выброс, л/мин |
4,4 (3,3; 4,9) |
3,7 (3,1; 4,3) |
0,49 |
|
ЛСС, ед. Вуда |
1,7 (1,7; 2) |
4,5 (3,6; 6,1) |
0,00007 |
|
Реакция острой фармакологической пробы* |
100% |
0 |
0,04 |
|
Маркеры миокардиального напряжения |
|||
|
sST-2, нг/мл |
20,1 (18,1; 24,0) |
26,8 (21,6; 41,1) |
0,048 |
|
NТ-proBNP, пг/мл |
26,5 (15,7; 33,0) |
52,7 (29,9; 102,9) |
0,032 |
Примечание: * — реакция острой фармакологической пробы с ингаляцией оксида азота в виде cнижения только ДЛА, но повышения ЛСС и снижения сердечного выброса.
Сокращения: ЛГ — легочная гипертензия, ЛСС — легочное сосудистое сопротивление, МК — митральный клапан, рСДЛА — расчетное давление в легочной артерии, срДЛА — среднее давление в легочной артерии, ЭхоКГ — эхокардиография, TAPSE — систолическая экскурсия кольца трикуспидального клапана, sST2 — стимулирующий фактор роста, экспрессируемый геном 2, NT-proBNP — N-концевой промозговой натрийуретический пептид.
Таблица 2
Сравнение морфологической картины паренхимы легких, сосудистого русла в зависимости от наличия изолированной посткапиллярной или комбинированной пост-/прекапиллярной формы ЛГ
|
Показатели |
Изолированная посткапиллярная ЛГ, Ме (%) (n=11) |
Комбинированная пост-/прекапиллярная ЛГ (%) (n=15) |
p* |
|
Плевра утолщена, n (%) |
9 (82,0%) |
13 (86,6%) |
0,860 |
|
Плевра фиброзирована, n (%) |
10 (90,9%) |
8 (53,3%) |
0,203 |
|
Капилляры полнокровны, n (%) |
4 (36,4%) |
3 (20,0%) |
0,818 |
|
Капилляры все тромбированы, n (%) |
5 (45,4%) |
8 (53,3%) |
0,729 |
|
Капилляры частично тромбированы, n (%) |
2 (18,2%) |
0 |
0,906 |
|
Артериолы преимущественно тромбированы, единичные полнокровны, n (%) |
2 (18,2%) |
0 |
0,622 |
|
Артериолы полнокровны, n (%) |
2 (18,2%) |
5 (33,3%) |
0,435 |
|
Пандемический тромбоз артериол, n (%) |
1 (9,1%) |
8 (53,3%) |
0,045 |
|
Частичный тромбоз артериол, n (%) |
3 (27,3%) |
3 (20,0%) |
0,622 |
|
Интерстиций без признаков фиброза, n (%) |
0 |
5 (33,3%) |
0,126 |
|
Очаговый интерстициальный фиброз, n (%) |
5 (45,4%) |
8 (53,3%) |
0,944 |
|
Диффузный интерстициальный фиброз, n (%) |
5 (45,4%) |
0 |
0,124 |
|
Периваскулярный фиброз, n (%) |
3 (27,3%) |
3 (20,0%) |
0,660 |
Примечание: * — Хи-квадрат с поправкой Йетса.
Сокращение: ЛГ — легочная гипертензия.
Таблица 3
Сравнение данных микроскопии артериол и венул в зависимости от наличия изолированной посткапиллярной или комбинированной пост-/прекапиллярной формы ЛГ у пациентов с ППС МК
|
Параметры* |
Изолированная посткапиллярная ЛГ, Ме (25; 75%) (n=11) |
Комбинированная пост-/прекапиллярная ЛГ, Ме (25; 75%) (n=15) |
р (Манна-Уитни) |
|
Артериола S сосудистой стенки, мкм2 |
19353,09 (12574,77; 32032,46) |
31410,97 (18722,46; 40645,85) |
0,386 |
|
Артериола S интимы, мкм2 |
1845,79 (1457,29; 3734,28) |
2125,57 (1066,63; 4822,86) |
0,901 |
|
Наибольшая толщина в месте гиперплазии артериолы, мкм |
15,23 (5,32; 28,91) |
21,49 (4,07; 43,87) |
0,832 |
|
Артериола S адвентиции, мкм2 |
8084,04 (5893,60; 16110,49) |
10459,47 (7918,50; 15851,28) |
0,772 |
|
Артериола S медии, мкм2 |
7312,76 (5691,73; 13167,51) |
13440,86 (9624,69; 17954,67) |
0,342 |
|
Артериола S сосуда + просвет, мкм2 |
28941,34 (19148,11; 34523,00) |
39623,11 (22952,85; 54646,39) |
0,536 |
|
Артериола S медии + интима + просвет, мкм2 |
17534,55 (13625,88; 23093,59) |
25172,74 (14921,72; 34409,78) |
0,433 |
|
Венула S сосудистой стенки, мкм2 |
23962,32 (21004,83; 41938,74) |
42175,47 (41938,74; 79860,54) |
0,130 |
|
Венула S интимы, мкм2 |
2769,73 (2416,96; 6302,28) |
6529,20 (6302,28; 8404,88) |
0,037 |
|
Наибольшая толщина в месте гиперплазии интимы венулы, мкм |
4,65 (0,00; 23,93) |
28,18 (0,00; 47,66) |
0,595 |
|
Венула S адвентиции, мкм2 |
8196,00 (6310,26; 20492,30) |
11017,14 (7837,72; 37973,48) |
0,591 |
|
Венула S медии, мкм2 |
12400,55 (5039,25; 27798,74) |
27798,74 (21810,44; 28671,71) |
0,157 |
|
Венула S сосуда + просвет, мкм2 |
33027,25 (28512,90; 91537,78) |
91537,78 (77577,91; 104708,5) |
0,037 |
|
Венула S медии + интима + просвет, мкм2 |
22705,91 (13133,77; 64736,25) |
77040,34 (60405,84; 83700,05) |
0,044 |
|
Венула отношение адвентиции к сосуду, % |
55,63 (45,72; 72,23) |
36,34 (24,54; 49,15) |
0,042 |
Примечание: * — толщина эндотелиоцита составила 5 мкм, S — площадь.
Сокращение: ЛГ — легочная гипертензия.

Рис. 2. Состояние артериол и венул по данным проведенного морфологического исследования сосудов легких у пациентов с ППС МК.
Примечание: А — артериола без патологии, Б — пандемический тромбоз артериолы, В — гиперплазия интимы артериолы, Г — гипертрофия медии артериолы, Д — венула без патологии, Е — венула с гиперплазией интимы и организованным тромбом в просвете.

Рис. 3. А — тромбированный капилляр, Б — интерстициальный фиброз.
Таблица 6
Вклад различных факторов в сохранение комбинированной пост-/прекапиллярной формы ЛГ
|
Ранги значимости |
|
|
Возраст на момент коррекции порока |
23 |
|
Фракционное изменение площади ПЖ, до % |
17 |
|
Индекс массы тела, кг/м2 |
4 |
|
Количество корригированных клапанов |
100 |
|
TAPSE/рСДЛА см/мм рт.ст. |
21 |
|
Время пережатия аорты, мин |
8 |
|
Искусственное кровообращение, мин |
19 |
|
рСДЛА мм рт.ст. до операции |
25 |
Сокращения: ПЖ — правый желудочек, TAPSE/рСДЛА — сердечно-сосудистое сопряжения (отношение систолической экскурсии кольца трикуспидального клапана к расчетному систолическому давлению в легочной артерии).
Таблица 4
Вклад различных факторов в факт регресса ЛГ спустя год после операции
|
Ранги значимости |
|
|
Мужской пол |
48 |
|
Сахарный диабет 2 типа |
72 |
|
Стеноз МК |
100 |
|
Сочетанное вмешательство на аортальном и МК |
61 |
|
Курение |
19 |
|
Перенесенная коронавирусная инфекция |
27 |
|
Степень ожирения |
56 |
|
ФП/ТП |
73 |
|
Хроническая болезнь почек 3а-5 стадия |
16 |
|
рСДЛА ≥38 мм рт.ст. до операции |
38 |
|
Возраст на момент коррекции порока |
23 |
|
рСДЛА мм рт.ст. до операции |
25 |
Сокращения: МК — митральный клапан, рСДЛА — расчетное давление в легочной артерии, ТП — трепетание предсердий, ФП — фибрилляция предсердий.
Таблица 5
Вклад различных факторов в сохранение изолированной посткапиллярной ЛГ
|
Ранги значимости |
|
|
Пол мужской |
23 |
|
Сахарный диабет 2 тип |
90 |
|
Стеноз МК |
100 |
|
Сочетанное вмешательство на аортальном и МК |
31 |
|
Курение |
23 |
|
Перенесенная коронавирусная инфекция |
16 |
|
Степень ожирения |
6 |
|
Наличие ФП/ТП |
8 |
|
Наличие хронической болезни почек 3а-5 стадия |
31 |
|
рСДЛА ≥38 мм рт.ст. до операции |
16 |
|
Объем пораженных клапанов |
11 |
|
Индекс массы тела, кг/м2 |
25 |
|
Количество корригированных клапанов |
8 |
Сокращения: МК — митральный клапан, рСДЛА — расчетное давление в легочной артерии, ТП — трепетание предсердий, ФП — фибрилляция предсердий.
Обсуждение
Помимо выраженности ЛГ при пороке МК, характера поражения клапанного аппарата, коморбидного статуса, еще очень важную роль в определении тяжести состояния пациента с ППС МК играет присутствие прекапиллярного компонента ЛГ до коррекции порока дополнительно к посткапиллярному.
В нашем исследовании из 40 пациентов, у которых до коррекции порока МК проведенная инвазивная оценка параметров гемодинамики малого круга подтвердила наличие ЛГ, изолированная посткапиллярная форма ЛГ диагностирована у 15 больных с ППС МК (37,5%), тогда как у большинства до операции имела место комбинированная пост-/прекапиллярная (n=25 (62,5%)).
Выполнение хирургической коррекции клапанной патологии сердца эффективно снимает посткапиллярный компонент ЛГ. Однако у ряда пациентов может сохраняться повышенное сопротивление малого круга (прекапиллярный компонент) в послеоперационном периоде, неблагоприятно влияя на гемодинамические параметры, вплоть до развития дисфункции ПЖ [10]. Присутствие и идентификация прекапиллярного компонента дополнительно к посткапиллярной ЛГ после операции имеет решающее значение, поскольку это может влиять на прогноз и принципы лечения пациентов [6].
Тяжесть нарушений гемодинамики малого круга и дезадаптивное ремоделирование правых камер сердца повышают периоперационные риски осложнений, в связи с чем решение о пользе/риске хирургического вмешательства у таких пациентов с ППС и ЛГ должно быть тщательно взвешено и обсуждено мультидисциплинарной командой [10]. Вазореактивность легочного артериального сосудистого русла и «обратимость» ЛГ, оцененная с помощью острой фармакологической пробы во время КПОС (с использованием оксид азота/кислорода), играет важную роль в определении дальнейшей тактики. Отсутствие положительной динамики срДЛА и ЛСС, снижение СВ отражает «необратимость» ЛГ и может быть ассоциировано с неблагоприятным исходом кардиохирургического вмешательства.
В нашем исследовании для пациентов с ППС и комбинированной пост-/прекапиллярной ЛГ до операции характерно вмешательство на большем количестве клапанов, более выраженное повышение рСДЛА по данным ЭхоКГ до вмешательства, более выраженное дооперационное нарушение сердечно-сосудистого сопряжения ПЖ-ЛА и повышение уровня маркеров миокардиального напряжения. Также пациенты с данным типом ЛГ характеризовались более тяжелыми изменениями гемодинамики малого круга кровообращения с характерным ответом на вазореактивный тест илопростом в виде снижения срДЛА и СВ, но с повышением ЛСС до коррекции порока.
При проведении микроскопии артериол и венул в нашем исследовании отмечено большее значение площади венулы и ее просвета, также как интимы венулы, площади сочетания интимы, медии и просвета венулы, как и отношения адвентиции венулы к площади венулы именно у пациентов с комбинированной пост-/прекапиллярной ЛГ и ППС МК по сравнению с пациентами с изолированной посткапиллярной ЛГ. Более того, для пациентов с комбинированной ЛГ было характерно более часто наличие пандемического тромбоза артериол.
Действительно, при гистологическом исследовании сосудов малого круга кровообращения у пациентов с ЛГ вследствие патологии левых отделов сердца имеет место утолщение альвеолярно-капиллярных мембран и их фиброзные изменения, гипертрофия и фиброз интимы венул. При присоединении прекапиллярного компонента у больных ЛГ 2 группы обнаруживаются утолщение интимы и гипертрофия медии ЛА, а также микротромбозы [11]. Ранее в работе Fayyaz AU, et al. на примере пациентов с сердечной недостаточностью (СН) было продемонстрировано, что тяжесть ЛГ и выраженность ухудшения диффузионной способности легких коррелирует с утолщением интимы и венул [12].
Впервые в работе Чазовой И. Е. были продемонстрированы основные характеристики ремоделирования легочного сосудистого русла при посмертной биопсии у 6 пациентов с ЛГ и митральным стенозом[13]. У данных пациентов отмечено утолщение интимы ЛА за счет концентрического фиброза, определяющегося лишь в 3,3% артерий и затрагивавшего сосуды диаметром 25-50 мкм. Однако накопленные данные по морфологической характеристике легочной ткани и легочного сосудистого русла ограничиваются небольшой выборкой пациентов и посмертной биопсией легких [13]. Более того, до сих пор не разработана классификация морфологических изменений сосудов легких при посткапиллярной ЛГ.
В нашем исследовании у пациентов с ППС МК интраоперационная биопсия ткани легкого с последующей морфологической оценкой паренхимы легких и сосудов в совокупности с неинвазивными и инвазивными параметрами выступила в роли дополнительного параметра, позволяющего отразить характер ремоделирования легочного сосудистого русла и тяжесть изменений для пациентов с ЛГ различного гемодинамического типа.
В нашем исследовании также проводилось изучение факторов, влияющих на достижение регресса ЛГ спустя год после эффективной коррекции порока, или на сохранение ЛГ различного типа.
Выявленный вклад типа поражения МК по типу стеноза в характер периоперационной динамики ЛГ и в принципе регресс ЛГ спустя год после операции можно объяснить более выраженным поражением сосудов легочного артериального русла, представленным в виде более частого присутствия тромбированных капилляров, связи стеноза МК с периваскулярным фиброзом и наличием интерстициального фиброза легких.
В то время как объем вмешательства на клапанах сердца выступил единственным фактором, оказывающим значимый вклад в сохранение комбинированной пост-/прекапиллярной ЛГ. Это, вероятно, можно объяснить более выраженным ремоделированием сердца и нарушением внутрисердечной гемодинамики, с большей длительностью течения порока и СН.
Помимо самого порока сердца, также и сопутствующая кардиологическая и коморбидная патология может оказывать вклад в периоперационное течение ЛГ.
Действительно, дополнительный вклад в нарушение внутрисердечной гемодинамики и гемодинамики малого круга кровообращения и, как следствие, в более тяжелое состояние пациентов с ППС МК оказывает ФП/ТП. До 80% с митральными пороками имеют ФП/ТП в раннем послеоперационном периоде коррекции порока, что ассоциируется с восьмикратным увеличением шансов сохранения ФП/ТП и в отдаленном послеоперационном периоде [14], а как следствие сохранении еще одного компонента, способствующего персистенции ЛГ.
Значимый вклад в наличие ЛГ у пациентов с патологией левых камер сердца при сохранной фракции выброса ЛЖ вносит характер нарушений метаболического фона, способствующего формированию хронически текущего воспалительного процесса. Предполагается, что воспалительное состояние активирует нейрогормональные медиаторы, адаптивный иммунитет и липидный ферментативный метаболизм, продуцируемый полиненасыщенными жирными кислотами, что приводит к ремоделированию легочных вен, легочной вазоконстрикции и диастолической дисфункции ПЖ у пациентов с СН и сохранной фракцией выброса ЛЖ [15].
В нашем исследовании одним из факторов коморбидного статуса пациентов, оказывающих значимый вклад в недостаточную динамику уровня рСДЛА в течение года после операции, является СД 2 типа.
СД 2 типа идентифицирован как независимый предиктор развития ЛГ, даже после поправки на другие факторы (например, ишемическая болезнь сердца, левожелудочковая СН, гипертония, курение) [16]. Результаты метаанализа, выполненного авторами Padte S, et al., указывают на повышенный уровень смертности среди больных ЛГ с СД по сравнению с лицами без СД (ОШ 1,40; 95% ДИ: 1,15-1,70), p=0,0006 [15].
Наличие СД 2 типа может влиять и на развитие ЛГ, поскольку может приводить к дисфункции и ремоделированию ПЖ [17]. Нарушение толерантности к глюкозе и инсулинорезистентность вовлечены в развитие и прогрессирование заболевания, влияя на ухудшение эндотелиальной функции в т.ч. и сосудов малого круга кровообращения, активируя продукция вазоконстрикторных агентов (таких как эндотелин 1) и снижения продукции агентов, ответственных за вазодилатацию (оксид азота) [16]. Другим важным фактором, который следует учитывать, является высокая распространенность скрытой диастолической дисфункции ЛЖ и ишемической микрососудистой патологии у пациентов с диабетом. Несмотря на интенсивные исследования по этому вопросу, точные клеточные и молекулярные эффекты СД 2 типа на легочное сосудистое русло до сих пор до конца не изучены.
В нашем исследовании наличие СД 2 типа явилось одним из факторов, оказывающих значимый вклад в факт регресса ЛГ спустя год после операции по данным КПОС (72 у.е.) и значимый вклад в сохранение изолированной посткапиллярной ЛГ спустя год после операции (90 у.е.) в совокупности с другими факторами.
Еще одним фактором, продемонстрировавшим свой умеренный вклад (56 у.е.) в характер динамики ЛГ спустя год после операции, является ожирение.
Такое состояние, как ожирение, все чаще встречается у пациентов с ППС различной этиологии до коррекции порока [18-20]. Ожирение может нарушать гомеостаз в малом круге кровообращения и усугублять уже исходно имеющееся ремоделирование легочного сосудистого русла за счет повышения уровня циркулирующих воспалительных маркеров, периваскулярной инфильтрации иммунных клеток, токсического действия пищевых насыщенных жирных кислот на эндотелий легочного сосудистого русла, вызывая прогрессирующую эндотелиальную дисфункцию, вазоспазм, гиперкоагуляционное состояние [21]. Увеличение массы тела также может усиливать системное сосудистое воспаление, что, в свою очередь, может способствовать ангиопролиферации легочного сосудистого русла и, таким образом, приводить к повышению давления в ЛА. Избыточная масса тела или ожирение ассоциируется с увеличением шансов наличия ЛГ в 1,34 раза (95% ДИ: 1,29-1,4; p<0,001 на каждые 5 единиц увеличения индекса массы тела) [22].
Проведенный в нашем исследовании комплексный анализ фенотипа пациентов с пороком МК в зависимости от типа ЛГ, а также поиск факторов, влияющих на неблагоприятную динамику ЛГ, спустя год после операции позволил идентифицировать модифицируемые состояния, коррекция или компенсация которых еще на этапе до операции, вероятно, способствует улучшению течения заболевания и характера нарушений гемодинамики малого круга кровообращения после эффективной хирургии порока сердца.
Заключение
В нашем исследовании пациентов с ППС и комбинированной пост-/прекапиллярной ЛГ характеризует более выраженное повышение рСДЛА по данным ЭхоКГ до вмешательства, более выраженное нарушение сердечно-сосудистого сопряжения ПЖ-ЛА и повышение уровня маркеров миокардиального напряжения (NT-proBNP и стимулирующего фактора роста, экспрессируемого геном 2), более тяжелые изменения гемодинамики малого круга кровообращения с характерным ответом на вазореактивный тест илопростом именно для данной группы пациентов в виде снижения срДЛА и СВ с повышением ЛСС до коррекции порока, а также вмешательство на большем количестве клапанов.
При морфометрии легочных артериол для пациентов с комбинированной пост-/прекапиллярной ЛГ и ППС МК характерна артериализация венул и более частое наличие пандемического тромбоза артериол (53,3%) по сравнению с пациентами с изолированной посткапиллярной ЛГ (9%).
Впервые выявлены факторы, оказывающие наиболее значимый вклад в регресс ЛГ спустя год после операции: поражение МК по типу стеноза — 100 у.е., наличие ФП/ТП — 73 у.е., наличие СД 2 типа — 72 у.е., сочетанное вмешательство на МК и аортальном клапане — 61 у.е., степень ожирения — 56 у.е., мужской пол — 48 у.е. Факторами, оказывающими наиболее значимый вклад в сохранение изолированной посткапиллярной ЛГ спустя год после операции, являются: поражение МК по типу стеноза — 100 у.е., наличие СД 2 типа — 90 у.е. Наиболее значимым фактором, оказывающим вклад в сохранение комбинированной пост-/прекапиллярной формы ЛГ спустя год после операции, является: количество корригированных клапанов — 100 у.е. Характер морфологических изменений легких не оказал значимый вклад в особенности периоперационной динамики ЛГ спустя год после операции.
Данное исследование позволило нам более детально изучить не только характер структурно-функционального нарушений камер сердца и гемодинамики малого круга кровообращения у пациентов с ППС МК и ЛГ, но и комплексно оценить фенотип пациента с комбинированной пост-/прекапиллярной ЛГ и изолированной посткапиллярной ЛГ на фоне митрального порока сердца до его коррекции, а также определить вклад факторов, в т.ч. потенциально модифицируемых, влияющих на неблагоприятную динамику ЛГ спустя год после коррекции порока сердца.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Ляпина И.Н., Богданов Л.А., Двадцатов И.В., Дрень Е.В., Горбатовская Е.Е., Маркова Ю.О., Хуторная М.В., Ляпин А.А., Сотников А.В., Стасев А.Н., Кутихин А.Г., Мартынюк Т.В., Барбараш О.Л. Клиническое течение легочной гипертензии в зависимости от гемодинамического типа и гистологической картины микрососудистого русла легких у пациентов после коррекции митральных пороков сердца. Российский кардиологический журнал. 2025;30(2S):6489. https://doi.org/10.15829/1560-4071-2025-6489. EDN: JVJYKF
Скопировать