Электрическая изоляция ушка левого предсердия в лечении пациентов с фибрилляцией предсердий
Аннотация
Катетерная изоляция легочных вен является методом выбора для лечения пациентов с симптомной фибрилляцией предсердий (ФП). Несмотря на технологический прогресс, появление все более совершенных методов изоляции — эффективность лечения по данным различных источников не превышает 60-80%. В преобладающем большинстве случаев это связано с наличием внелёгочных источников для аритмии. Одной из наиболее недооценённых структур для запуска и поддержания ФП является ушко левого предсердия (УЛП). В данном литературном обзоре дано современное представление о методах изоляции УЛП, эффективности и возможных осложнениях. Также отражен вопрос возможных тромбоэмболических событий после изоляции УЛП, который является наиболее частым и весомым ограничением для распространения данной процедуры.
Фибрилляция предсердий (ФП) является самым распространённым видом нарушения сердечного ритма среди взрослого населения во всём мире. С возрастом частота возникновения этой тахиаритмии значительно возрастает: если у людей 40-50 лет она встречается примерно у 1%, то к 80 годам — уже у 5-15% населения. За последние два десятилетия уровень заболеваемости ФП вырос на 13% [1][2].
Роль муфт легочных вен (ЛВ) в запуске ФП была описана еще в 2018г Hessaguere M, et al. [3]. Успешная радиочастотная аблация (РЧА) в данных участках приводила к устранению рецидивов ФП. Данное исследование являлось опорной точной в развитии различных технологий для достижения изоляции ЛВ. Выполнение антральной изоляции ЛВ с использованием катетеров с определением силы контакта или изменения локального сопротивления является наиболее современным методом РЧА при ФП [4].
Криобаллонная аблация (КБА) — на сегодняшний день это один из основных способов изоляции ЛВ, который, согласно исследованиям STOP-AF и CRYO-FIRST, показал лучшие результаты по сравнению с антиаритмической терапией как метод первой линии лечения ФП. При этом эффективность и безопасность КБА оказались сопоставимыми с РЧА, что подтверждено рядом исследований [5].
С точки зрения техники процедура выполняется с использованием специального баллонного катетера, который устанавливается в устье ЛВ. Внутренняя часть баллона охлаждается оксидом азота, что приводит к снижению температуры до низких температурных значений. Такое охлаждение вызывает образование кристаллов льда внутри клеток миокарда, в результате чего развивается воспалительная реакция, за которой следует формирование фиброза, который и обеспечивает электрическую изоляцию ЛВ [2][6-8].
Рецидив ФП может быть обусловлен не только восстановлением проведения импульсов в ЛВ, но и активацией внелегочных аритмогенных источников — триггеров или повторных кругов re-entry, что чаще всего связано с развитием фиброза предсердий. Наиболее распространёнными областями локализации таких триггеров являются верхняя полая вена, коронарный синус, ушко левого предсердия (УЛП), связка Маршалла, пограничный гребень, участки фрагментированной активности в зонах ганглионарных сплетений и задняя стенка левого предсердия (ЛП) [9]. В случае отсутствия эффекта от изоляции ЛВ криобаллон также применяется для изоляции задней стенки и УЛП [10][11].
Методика и результаты изоляции УЛП
УЛП является недооценённым эктопическим участком для запуска и поддержания ФП. Данная теория была описана в исследовании Di Biase L, et al. [9]. В проведенное в 2010г многоцентровое исследование было включено 987 пациентов, у которых ранее выполнялась катетерная аблация ФП. При повторном картировании оценивалась залповая активность УЛП, которая отмечалась только у 266 пациентов. Пациенты с залповой активностью были рандомизированы в три группы. Группа контроля (n=43) — которой аблация не выполнялась, группа точечной аблации в области УЛП (n=56) и группа изоляции УЛП (ИУЛП) (n=167). Для точечных воздействий картировалась наиболее ранняя зона эктопической активности из УЛП. При ИУЛП выполнялись радиочастотные воздействия, с позиционированием диагностического циркулярного электрода в УЛП. Первичной конечной точкой являлась свобода от аритмии после двухмесячного слепого периода. Рецидивы ФП оценивались при помощи 7-дневного суточного мониторирования электрокардиограммы на контрольных визитах и при помощи портативных регистраторов на этапе амбулаторного наблюдения. Рецидивы ФП наблюдались у 36% пациентов. В первой группе (контрольная группа) у 32 пациентов (74%) наблюдался рецидив, в группе точечной аблации — у 38 пациентов (68%), а в группе полноценной ИУЛП — у 25 пациентов (15%). Стоит отметить, что в 4 случаях вмешательство осложнилось развитием тампонады, однако все они разрешились без открытого хирургического вмешательства. Данное исследование продемонстрировало, что УЛП может являться потенциальным источником ФП. В связи с этим стала очевидной актуальность электрической ИУЛП, которое имеет залповую активность, у пациентов после перенесенной изоляции устья ЛВ.
Tohoku Sh, et al. уже ИУЛП при помощи РЧА сравнивали с аблацией при помощи криобаллона [12]. В исследование было включено 260 пациентов (РЧА =59, КБА =201). Острая ИУЛП была достигнута больше в группе КБА (КБА: 94,9% vs РЧА: 82,6%, p=0,02). Если говорить про осложнения, то в группе РЧА отмечались 4 случая острого нарушения мозгового кровообращения (ОНМК) и 1 случай кровотечения из желудка, в группе КБА большие осложнения не детектировались. Если же говорить про долгосрочную эффективность и свободу от аритмии, то статистически значимо меньше рецидивов случалось в группе РЧА (РЧА: 76,3% vs КБА 56,7%, p=0,0017). Проведенный в рамках исследования многофакторный анализ показал, что ИУЛП при помощи линейных радиочастотных воздействий является предиктором свободы от аритмии (отношение рисков (ОР): 0,478, 95% доверительный интервал (ДИ): 0,336 — -0,823, p=0,0017). Справедливости ради нужно сказать, что данный результат скорее всего был связан с тем, что помимо устранения эктопической активности в УЛП (группа КБА), у пациентов в группе РЧА также выполнялись дополнительные линейные воздействия в ЛП — тем самым изолируя не только УЛП, но и другие потенциальные источники ФП.
Говоря про методику КБ ИУЛП (рис. 1), стоит отметить работу Chen Sh, et al. [13]. На относительно ранних этапах развития данной технологии исследователи апробировали данный метод у 10 пациентов с не менее тремя неуспешными аблациями в анамнезе. Время до острой ИУЛП составило от 76 до 270 сек. Важно отметить, что во всех случаях при аппликации выполнялись маневры «pull-down или pull-away». Средняя температура при аппликациях составляла -50 (от -57 до -47) °C. Всем пациентам после успешной аппликации выполнялись бонусные воздействия длительностью 240 сек. Во избежание персистирующего пареза диафрагмы всем пациентам проводилась стимуляция диафрагмального нерва (ДН): для этого проводилась стимуляция с электрода, предварительно установленного в дистальную треть левой подключичной вены, либо через циркулярный диагностический электрод, расположенный дистальнее криобаллона. Острая ИУЛП была достигнута у всех пациентов. Изоляция сохранялась на этапе 6-нед. визита, во время которого всем пациентам выполнялось инвазивное картирование. Если говорить про клиническую эффективность, то свобода от аритмии в срок наблюдения 6 мес. наблюдалась у преобладающего большинства больных (80%).

Рис. 1. Окклюзированное УЛП при помощи криобаллона Medtronic AF pro 28 мм, диагностический 10-полюсный электрод установлен в левой подключичной вене для стимуляции ДН (архив ФГБУ НМИЦ ТПМ Минздрава России).
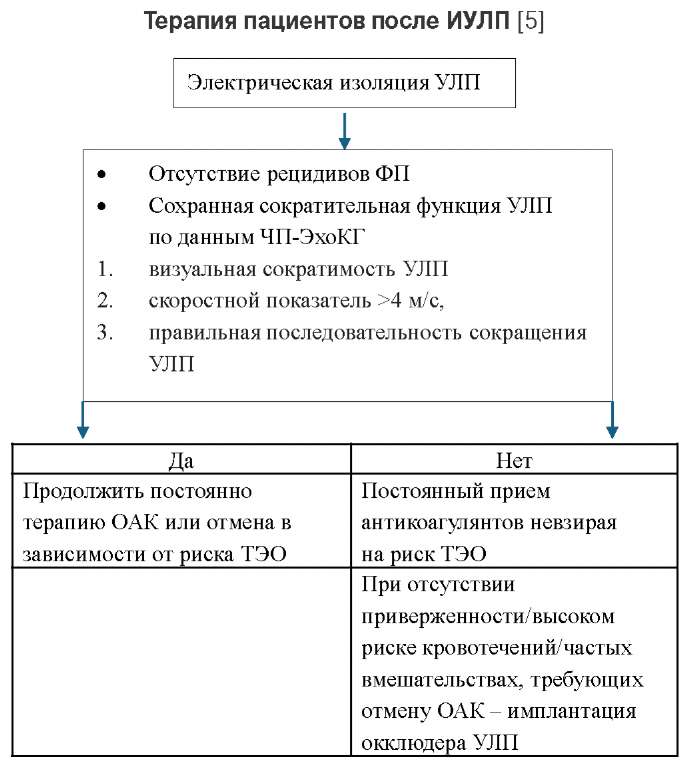
Сокращения: ОАК — оральные антикоагулянты, УЛП — ушко левого предсердия, ТЭО — тромбоэмболические осложнения, ФП — фибрилляция предсердий, ЧП-ЭхоКГ — чреспищеводная эхокардиография.
Идентичная техника КБА и бонусные аппликации применялись у Yorgun H, et al. [14]. Исследователи были одними из пионеров применения данной методики и также отмечали довольно продолжительный период с момента начала воздействия до достижения изоляции, который в среднем составил 115,5 (от 37 до 370) сек. На первых этапах при поздней изоляции Yorgun H, et al. применяли длительность аппликации 450 сек, однако после накопленного опыта начали использовать тактику бонусных аппликаций. Если ИУЛП до 150 сек — то ограничивались 1 аппликацией длительностью 300 сек. Если в более поздние сроки, то выполнялась еще одна бонусная аппликация длительностью 300 сек.
Эффективность и безопасность электрической ИУЛП явилась поводом для метаанализа, который был опубликован в журнале Europace в 2020г [15]. 9 исследований и 2336 пациентов были включены в данную работу. Стоит отметить, что все пациенты имели либо персистирующий, либо длительно-персистирующий характер ФП. Пациенты после электрической ИУЛП имели статистически значимую свободу от аритмии по сравнению с пациентами со стандартной аблацией (69,3% vs 46,4%; risk ratio 0,54; 95% ДИ: 0,42-0,69; P<0,0001).
Осложнения ИУЛП
Одним из ограничивающих факторов для распространения данного метода являются потенциальные осложнения. Одним из наиболее частых осложнений является парез ДН [12][14][16]. Постоянная стимуляция ДН с дистально расположенного циркулярного электрода от криобаллона, либо с левой подключичной вены снижают до минимума шансы развития данного осложнения [14]. Следующим более грозным интраоперационным осложнением, требующим своевременной реакции, является спазм коронарных сосудов, которые часто близко располагаются к устью УЛП (по передней полуокружности) [14][17]. В 98% случаев речь идет об огибающей артерии. При появлении ишемической динамики рекомендована незамедлительная остановка аппликации и введение нитратов. По сравнению с РЧА ИУЛП, при использовании КБА технологии данное осложнение встречается крайне редко [14].
Ключевой сдерживающий фактор для распространения ИУЛП — потенциальный риск ишемических событий у пациентов. Электрическая ИУЛП приводит к нарушению его механической функции, что вызывает застой крови и повышает риск образования тромбов [18][19]. Высокий риск тромбоэмболических явлений впервые был описан Fink T, et al. [18]. При детальной оценке данной работы стоит отметить факт достижения изоляции с использованием линейных воздействий в ЛП. Данные аппликации сами по себе могли скомпрометировать сократительную функцию ЛП и привести к повышенному тромбообразованию. Также обращает на себя внимание наличие в данной работе пациентов, которые не привержены к приему антикоагулянтной терапии. Идентичные выводы об высоких рисках тромбоэмболий были в работе Kim YG, et al. [20]. 9 из 39 пациентов после ИУЛП имели тромбоэмболические события после вмешательства. Такого рода высокий процент осложнений вероятнее всего был обусловлен отсутствием контроля международного нормализованного отношения у пациентов, которые находились на терапии варфарином и отмене оральных антикоагулянтов (ОАК) через 2 мес. после аблации у пациентов с низким риском CHA2DS2-VASc.
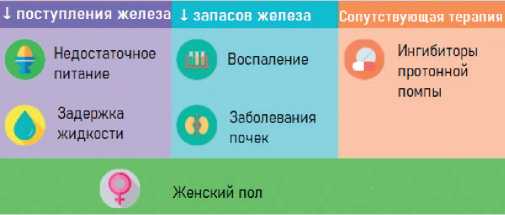
В 2024г опубликован согласительный документ по антикоагулянтному сопровождению пациентов, которые направлены на диагностические и лечебные электрофизиологические процедуры [5]. Ключевыми в выборе тактики антикоагулянтного сопровождения пациентов с ИУЛП являются клинические данные и параметры чреспищеводной эхокардиографии (ЧП-ЭхоКГ) на контрольном визите. Схематическое описание представлено в таблице 1. Основополагающей работой данного документа является исследование Di Biase L, et al. [19]. Целью исследования было определение наличия или отсутствия тромбозов/тромбоэмболический явлений у пациентов с ИУЛП, которые находится на постоянной терапии прямыми ОАК или на фоне отмены терапии. В исследование было включено 1854 пациента, которым выполнялась ИУЛП и которые имели свободу от аритмии в течение 6 мес. после процедуры. Для оценки скоростных показателей всем пациентам выполнялась контрольное ЧП-ЭхоКГ. Для определения гемодинамических показателей УЛП оценивались следующие параметры: визуальная сократимость УЛП, скоростной показатель >4 м/с, правильная последовательность сокращения УЛП. Пациентам, которые удерживали синусовый ритм и имели сохранную сократительную функцию УЛП (группа 1, n=336) — отменялась антикоагулянтная терапия. По данным контрольной ЧП-ЭхоКГ у 1518 пациентов (группа 2) из всех включенных (n=1854) имело место снижение сократительной функции. Данные пациенты после проведенной беседы с докторами (разъяснение рисков) были разделены на группу, которой дальнейшая антикоагулянтная терапия отменялась, и группу, которая продолжила терапию. Учитывая потенциально высокий риск тромбоэмболических осложнений (ТЭО), пациентам далее выполнялось контрольное ЧП-ЭхоКГ через 12 мес. При долгосрочном наблюдении >90% пациентов имели свободу от аритмии, что подчеркивает довольно значимую роль ИУЛП в эффективности лечения. Если же говорить про тромбоэмболические события, то стоит отметить, что в первой группе пациентов они не были отмечены. Во второй группе (n=1518) регистрировалось 92 случая тромбоэмболических событий (5,9%). Из них в 20 случаях пациенты находились на антикоагулянтной терапии, большинство случаев (n=72) отмечалось у пациентов, которым ранее отменялась терапия ОАК, невзирая на риск CHA2DS2-VASc. Преобладающее большинство больных (84 пациента из 92 с тромбоэмболическими событиями) — были направлены на имплантацию окклюзирующего устройства УЛП.
Таблица 1
Терапия пациентов после ИУЛП [5]
Роль КБА в ИУЛП
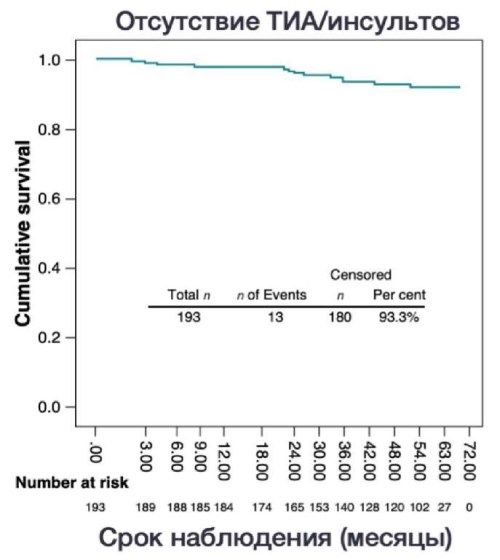
Наиболее актуальной на сегодняшний день работой по оценке КБ технологии в ИУЛП является исследование Yorgun H, et al., которое было опубликовано в издании Europace в 2023г [14]. Учитывая высокую выявляемость внелегочных триггеров у пациентов с персистирующей формой ФП помимо ЛВ, исследователи выполняли КБА ИУЛП. В многоцентровое ретроспективное исследование было включено 183 пациента. Для выполнения воздействия использовался криобаллон Medtronic разных поколений (Arctic Front Advance™, Arctic Front Advance ST, Arсtic Front Advance Pro, Medtronic, Minneapolis, MN, USA). После стандартного протокола изоляции ЛВ выполнялась ИУЛП. При поздней изоляции (>150 сек) выполнялось бонусное воздействие длительностью 300 сек. Парез левого ДН в ходе ИУЛП наблюдался в 2 случаях (1%), у 6 пациентов наблюдался транзиторный спазм ЛКА, который был восстановлен после внутривенного введения нитратов. В периоперационном периоде ТЭО у пациентов не отмечались. На 3 и 12 мес. для оценки гемодинамических показателей УЛП выполнялось контрольное ЧП-ЭхоКГ. В период наблюдения системные тромбоэмболические явления наблюдались у 14 пациентов (11 случаев инсульта, 1 случай транзиторной ишемической атаки, 1 случай тромбоэмболии почечной артерии) (рис. 2). Все пациенты с тромбоэмболическими ишемическими явлениями имели риск ТЭО >2 баллов и скоростной поток в УЛП <0,4 м/с (данные ЧП-ЭхоКГ на 12-мес. визите). Стоит также отметить, что средняя скорость потока в УЛП была значимо ниже у пациентов с ишемическими событиями, по сравнению с пациентами без такого рода осложнений (0,28±0,06 vs 0,44±0,15; P<0,001). Несмотря на рекомендации пожизненной антикоагулянтной терапии — 13 пациентов из 14 не имели приверженности к приему ОАК. Смерть, связанная с ОНМК, была в 1 случае из 14, 6 пациентов с ОНМК восстановились без какого-либо неврологического дефицита. Свобода от аритмии при наблюдении составила 67% (рис. 3). 34 пациента с клинически значимым рецидивом ФП были направлены на повторное катетерное лечение с использованием системы Biosense Webster Carto 3. При картировании возвратная активность в УЛП наблюдалась в 8 случаях (23,5%). При многофакторном регрессионном анализе объем ЛП (ОР 1,04, 95% ДИ: 0,53-1,32; P=0,023), мужской пол (ОР 0,53, 95% ДИ: 0,29-0,96; p=0,037) и хроническая сердечная недостаточность с низкой фракцией выброса (ОР 2,29, 95% ДИ: 1,04-5,02; P=0,038) являлись предикторами для возврата аритмии.

Рис. 2. График Каплана-Мейера, иллюстрирующий отсутствие транзиторных ишемических атак/инсультов за средний период наблюдения 55 (36,5-60,0) мес. после процедуры.
Сокращение: ТИА — транзиторная ишемическая атака.
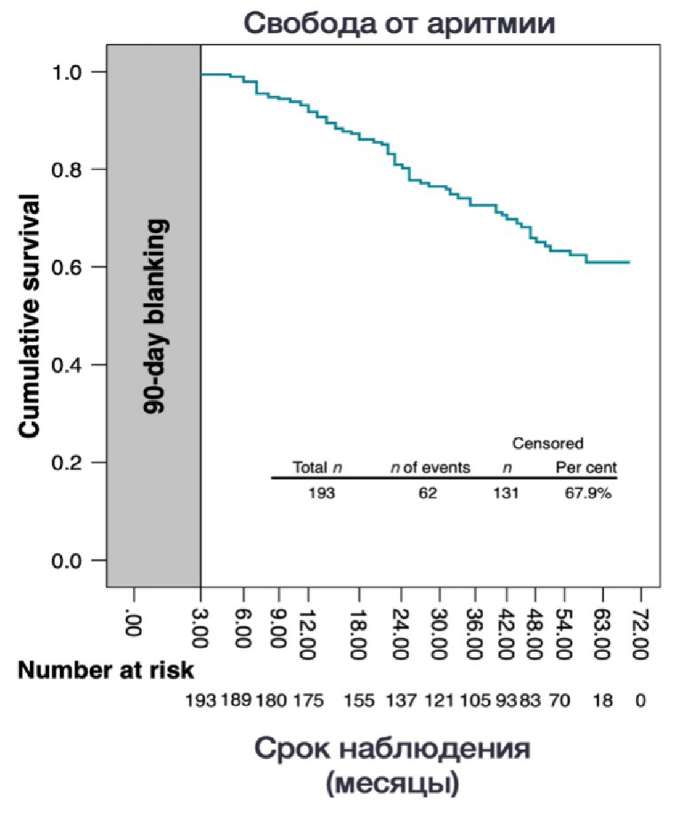
Рис. 3. График Каплана-Мейера, иллюстрирующий свободу от аритмии за средний период наблюдения 55 (36,5-60,0) мес. после процедуры (после слепого периода 90 дней).
На сегодняшний день нет единой тактики катетерного лечения пациентов с изолированными ЛВ. Несмотря на технологический прогресс, различные методы высокоплотного картирования — эффективность лечения пациентов с персистирующей ФП и изолированными ЛВ не превышает 60-70% при долгосрочном наблюдении. Применение КБА технологии в лечении пациентов с ФП по данным многочисленных исследований является высокоэффективным методом, а простота воздействия дает возможность для распространения среди клиник. Камнем преткновения является распространенная точка зрения о частых случаях ОНМК ввиду изменения гемодинамики в УЛП. При детальной оценке работ, описывающих данные осложнения, на первое место выходит отсутствие приверженности пациентов к приему ОАК [17][19][21][22]. Немаловажным фактором является отсутствие рандомизации и маленькая выборка больных [17][21][22]. Стоит отметить, что в вышеуказанных работах отсутствовал единый протокол аблации. В некоторых случаях выполнились локальные воздействия, в других — циркулярная аблация. Некоторые исследователи прибегали к линейным радиочастотным воздействиям по типу процедуры лабиринт [12]. Данная тактика сама по себе является довольно агрессивной, трудоемкой и может быть причиной последующих тромбоэмболических событий. С появлением технологии КБА ИУЛП с высокой вероятностью получит новый виток развития, ввиду простоты применения и низкого риска осложнений [14]. У пациентов с персистирующей ФП, высоким риском ТЭО ИУЛП при помощи КБА возможна как дополнение к стандартной изоляции ЛВ.
Заключение
Учитывая отсутствие стандартизированного протокола КБА УЛП и данных о долгосрочной ИУЛП — на сегодняшний день имеет место выполнение бонусных аппликаций (в случае поздней изоляции) для достижения долгосрочной изоляции. Контрольные исследования ЧП-ЭхоКГ также рекомендованы для дальнейшего изучения гемодинамических изменений и выбора оптимальной тактики ведения (имплантация окклюдера УЛП/постоянная терапия ОАК).
Декларация об использовании инструментов искусственного интеллекта: для коррекции перевода в статье использовался ИИ СhatGPT.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Брутян А.А., Давтян К.В., Чугунов И.А., Симонян Г.Ю. Электрическая изоляция ушка левого предсердия в лечении пациентов с фибрилляцией предсердий (обзор). Российский кардиологический журнал. 2025;30(4S):6651. https://doi.org/10.15829/1560-4071-2025-6651. EDN: XCROEB
Скопировать