Аутоиммунитет, аутовоспаление и сердечно-сосудистая система: иммунопатогенез и таргетная терапия
Аннотация
Клетки приобретенного звена иммунитета играют ключевую роль в патогенезе сердечно-сосудистых заболеваний, которые традиционно рассматриваются в контексте аутоиммунных процессов. Однако достижения последних десятилетий указывают на не менее важное значение аутовоспалительных механизмов при таких заболеваниях и синдромах, как перикардит, миокардит и атеросклероз. В обзоре рассматриваются точки пересечения аутоиммунитета и аутовоспаления при кардиоваскулярной патологии, с акцентом на то, как нарушение врождённого иммунитета и, в частности, активации инфламмасом, может способствовать развитию воспаления независимо от участия аутореактивных лимфоцитов. Особое внимание уделено идиопатическому рецидивирующему перикардиту как представителю спектра интерлейкин-1-зависимых заболеваний, наряду с синдромом Стилла взрослых, и классическими моногенными аутовоспалительными патологиями. Отдельно обсуждены возможности применения колхицина и блокаторов интерлейкина-1 при сердечно-сосудистых заболеваниях с учетом новых концепций их патогенеза. Интеграция иммунологических представлений в кардиологическую практику позволит по-новому взглянуть на воспалительные заболевания сердца и приблизиться к персонализированному подходу на основе дальнейшего изучения механизмов воспаления.
Аутоиммунные заболевания встречаются в общей популяции населения приблизительно в 3-10% случаев [1]. Частота кардиальных проявлений при системных аутоиммунных заболеваниях варьируется в зависимости от анализируемой выборки и лабораторных методов, используемых для их диагностики. Вместе с тем аутоиммунный компонент может присутствовать при широком спектре нозологических форм, которые традиционно не относятся к аутоиммунным заболеваниям, в т. ч. при таких традиционных для кардиологов заболеваниях, как атеросклероз, миокардиты и перикардиты.
Во время созревания иммунной системы Т-клетки, которые начинают реагировать против собственных антигенов, должны устраняться в процессе так называемой «негативной селекции», протекающей в тимусе. Этот защитный механизм является неполным и дополняется несколькими периферическими механизмами толерантности, включая преобразование аутореактивных T-клеток в T-регуляторные (Тreg) клетки, препятствующие развитию аутоиммунных реакций [2]. Характерным и диагностическим признаком аутоиммунных заболеваний служит появление клонов аутореактивных Т-лимфоцитов и аутоантител на фоне нарушения ингибирующего влияния Treg-клеток. В частности, в 2023г впервые в работах Wang Z, et al. и Depuydt MAC, et al. продемонстрировано нарушение периферической толерантности Т-клеток при атеросклерозе [3][4]. В качестве причин нарушения периферической толерантности Т-клеток авторы называют дефекты экспрессии иммунных контрольных точек, клональное расширение популяций CD4+— и CD8+-клеток, а также нестабильность Treg-клеток и их возможное превращение в Th17-клетки. Последним отводится важная роль в развитии аутоиммунных и воспалительных заболеваний.
Как большинство аутоиммунных заболеваний, миокардит имеет многофакторную природу с участием нескольких иммунологических механизмов. В основе развития воспалительных заболеваний миокарда лежит нарушение аутотолерантности Т и/или В-лимфоцитов с формированием клона аутореактивных кардиоспецифических Т-лимфоцитов и/или аутоантител, а также феномен «мимикрии», возникающий вследствие молекулярного сходства между чужеродными (инфекционные агенты) и собственными эпитопами, что приводит к развитию перекрестных реакций [5]. В качестве ключевого фактора возникновения аутоиммунных реакций при миокардитах большинство авторов называют дисфункцию Th17- и Treg-клеток. Дополнительными детерминантами возникновения миокардита и его трансформации в дилатационную кардиомиопатию может быть генетическая предрасположенность, ассоциированная со специфическими гаплотипами системы тканевой совместимости человека HLA (HLA-DR4, HLA-DR12, DR15 и DRB*0601).
Среди частых проявлений системных аутоиммунных заболеваний, таких как ревматоидный артрит, системная красная волчанка и синдром Шегрена, встречается перикардит [6]. Например, у пациентов, страдающих ревматоидным артритом, перикардит выявляется в 30% случаев, тогда как у больных системной красной волчанкой его частота может достигать 50%. Напротив, у пациентов с системной склеродермией, особенно при развитии легочной гипертензии, выпот в полости перикарда может носить невоспалительный характер (транссудат). Триггером развития аутоиммунных реакций при перикардите могут быть инфекционные агенты и в первую очередь кардиотропные вирусы, действующие на основе феномена «молекулярной мимикрии» в сочетании с нарушениями аутотолерантности. В пользу аутоиммунной теории патогенеза постперикардиотомного синдрома при операциях на открытом сердце или чрескожных вмешательствах свидетельствует повышение титра специфический аутоантител к саркомерным белкам кардиомиоцитов при анализе перикардиальной жидкости [7][8].
На основе исторических постулатов E. Witebsky и с учетом современных представлений Ноэлем Роузом в 1993г сформулированы большие критерии аутоиммунного заболевания [9]:
— наличие инфильтрации мононуклеарных клеток и аномальная экспрессия HLA в органе-мишени или в различных органах,
— появление циркулирующих аутоантител и/или аутореактивных лимфоцитов,
— обнаружение аутоантител и/или аутореактивных лимфоцитов в пораженной ткани,
— идентификация и изоляция кандидатных аутоантигенов,
— возможность воспроизведения клинической картины заболевания посредством переноса аутореактивных аутоантител и/или Т-клеточных клонов,
— клинический ответ заболевания на иммуносупрессивную терапию.
На фоне активного изучение иммунных нарушений ко второй половине двадцатого века оставалась группа воспалительных заболеваний, развитие которых не имело очевидных провоцирующих факторов, повышения титров аутоантител или антиген-специфических Т-лимфоцитов, характерных для классических аутоиммунных заболеваний. В качестве примера приводили такие заболевания, как средиземноморская лихорадка и другие периодические синдромы, для которых свойственны не спровоцированные, повторяющиеся эпизоды лихорадки, серозитов, артрита и воспаления кожи. Для обозначения новой группы заболеваний с так называемым неспровоцированным системным или локальным воспалением, не имеющих критериальных признаков аутоиммунной патологии, был предложен термин «аутовоспаление» [10]. Активное внедрение в клиническую практику секвенирования нового поколения выявило широкий спектр моногенных аутовоспалительных заболеваний, к которым относятся семейная средиземноморская лихорадка, семейная ирландская лихорадка, гипериммуноглобулинемия D с синдромом периодической лихорадки, синдрома Макла-Уэллса, семейная холодовая крапивница и ряд других более редких заболеваний, развитие которых, как показали дальнейшие исследования, было связано с нарушениями врожденного иммунитета [11] (табл. 1). Проведение полногеномного поиска ассоциаций (GWAS) позволило выявить генетические факторы риска и отнести к группе полигенных аутовоспалительных заболеваний болезнь Крона, подагру, саркоидоз и синдром Стилла взрослых. В частности, показано, что болезнь Крона является результатом полиморфного варианта гена NOD2, мутации которого также описаны при синдроме Блау и раннем саркоидозе.
Возвращаясь к сердечно-сосудистой патологии, следует отметить, что перикардит может встречаться в спектре клинических проявлений при всех моногенных аутовоспалительных заболеваниях с частотой от 0,4 до 3,7% [12]. У пациентов с классическим вариантом средиземноморской лихорадки перикардит встречается в 2,4% случаев, тогда как у пациентов с поздним дебютом заболевания его частота может достигать 6-8%, нередко повторяя клинические проявления идиопатического рецидивирующего перикардита (ИРП). Более частая имитация ИРП с отсутствием ответа на терапию колхицином характерна для пациентов с периодической лихорадкой, имеющих патологический вариант R92Q (p.Arg121Gln) в гене TNFRSF1A [13].
Как известно, триггерами любой воспалительной реакции являются патоген-ассоциированные молекулярные паттерны бактерий и вирусов (PAMP) или молекулярные паттерны, которые образуются при повреждении или гибели клеток хозяина (DAMP). PAMP и DAMP действуют через специфические рецепторы распознавания образов (NOD, NLR, TLR), принадлежащих к семейству нуклеотид-связывающих рецепторов и относящихся к основным компонентам инфламмасом [14]. Под влиянием различных триггеров в цитоплазме клеток врожденного иммунитета, к которым относятся моноциты, макрофаги, нейтрофилы, начинается сборка макромолекулярных белковых комплексов, называемых инфламмасомами. Среди рецепторов распознавания образов наиболее изученным остается NLRP3 из семейства NLR белков, вероятно, потому что NLRP3 активируется широким спектром стимулов в отличии от других рецепторов. Инфламмасома NLRP3 состоит из сенсора (рецептора распознавания образов NLRP3), белка-каркаса (ASC) и эффекторной каспазы. При стимуляции NLRP3 олигомеризуется и рекрутирует белок-каркаса, вызывая образование спиральных филаментов ASC. Множественные филаменты ASC объединяются в один макромолекулярный фокус, приводя к активации каспазы-1 из белка-предшественника. Каспаза-1, в свою очередь, обеспечивает превращение про-интерлейкина (IL)-1 и про-IL-18 в активные формы, за счет которых реализуются основные провоспалительные эффекты [15]. Помимо продукции воспалительных цитокинов, активация инфламмасомы NLRP3 приводит к пироптозу, который является быстрой формой литической запрограммированной гибели клеток. IL-1β в качестве основной циркулирующей формы IL-1 стимулирует синтез других медиаторов воспаления, включая циклооксигеназу-2 и простагландины. Напротив, IL-1α изначально вырабатывается как предшественник и хранится в цитоплазме клеток мезенхимального происхождения, например, перикардиальных клеток, если речь идет о развитии перикардита [16]. Под влиянием триггеров происходит высвобождение IL-1α, который, в свою очередь, стимулирует транскрипцию IL-1β в моноцитах/макрофагах. Обе формы, IL-1α и IL-1β, связываются с рецепторами IL-1 в эндотелиальных клетках, что приводит к увеличению адгезии нейтрофилов и моноцитов, а также к усилению локального воспаления. Образование инфламмасомы регулируется двумя независимыми механизмами, которые осуществляют контроль за выраженностью воспалительных и пироптотических последствий активации NLRP3. С помощью первого механизма, «прайминга», происходит инициация транскрипции и трансляции компонентов и субстратов инфламмасомы (NLRP3, про-IL-1β и про-IL-18), которая управляется ядерным фактором-κB (NF-κB). Второй механизм, тесно связанный с увеличением в результате гибели клеток внеклеточного аденозинтрифосфата, оттоком ионов калия, дестабилизацией лизосом или дисфункцией митохондрий, запускает структурные изменения в доменах NLRP3, необходимые для сборки инфламмасомы. Дополнительный уровень регуляции активности NLRP3 — посттрансляционные изменения белков инфламмасомы, такие как фосфорилирование или присоединение одной или нескольких молекул убиквитина.
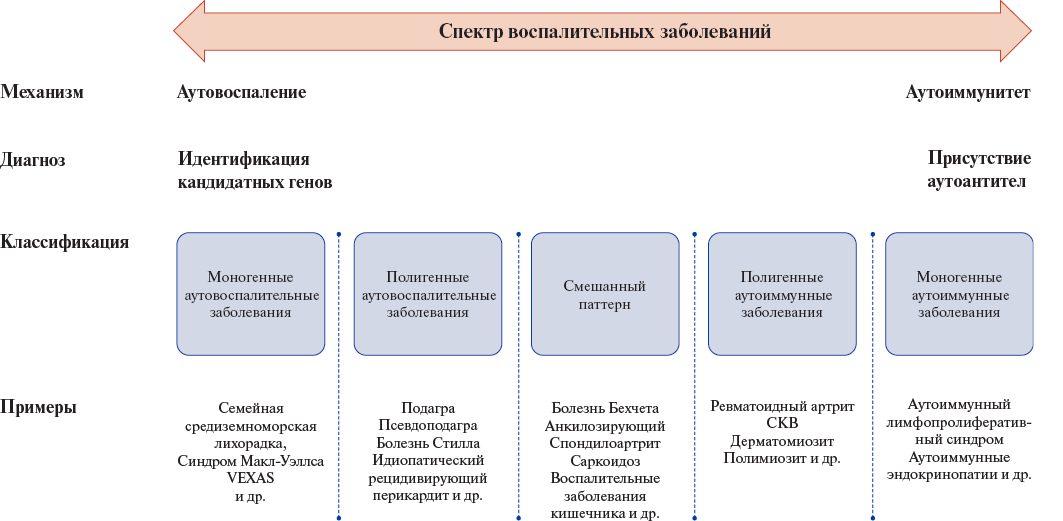
Аутоиммунные и аутовоспалительные состояния часто путают друг с другом, поскольку оба являются результатом ненадлежащей активации иммунной системы. Проблема усугубляется еще и тем, что границы между аутоиммунными и аутовоспалительными часто размыты (рис. 1). Известно, что активация инфламмасомы NLRP3 в ответ на инфекционные агенты — важнейший компонент внутриклеточного сигналлинга, участвующий в механизмах активации также и клеток приобретенного звена иммунитета. Связь между аутоиммунитетом и аутовоспалением реализуется за счет IL-1β, который жизненно важен для связывания врожденного иммунного ответа и адаптивных иммунных реакций Т- и В-клеток. IL-1 также имеет важное значение в активации интерферона-γ в Т-клетках памяти, пролиферации Т-клеток и В-клеток, а также в усилении синтеза антител [17]. Кроме того, патогенез целого ряда иммунозависимых заболеваний — многостадийный процесс, включающий в себя первоначально гиперактивацию врожденного звена иммунитета, так называемое «аутовоспалительное начало», с последующим вовлечением адаптивного иммунитета и развитием вторичных аутоиммунных реакций. Многочисленные двунаправленные связи врожденного и адаптивного иммунитета могут служить новыми перспективными мишенями для терапевтического воздействия. Чтобы разграничить аутовоспалительные и аутоиммунные механизмы развития заболеваний, приведем сравнительную характеристику их этиологических факторов, специфических клинико-демографических признаков и лабораторных маркеров, а также эффективности различных методов лечения (табл. 2).
Но вернемся к сердечно-сосудистой патологии, которую исходно мы рассмотрели с точки зрения нарушений адаптивного иммунитета. Известно, что активные формы кислорода, механические стимулы, такие как изменения кровотока, и активные метаболиты могут вызывать образование инфламмасомы NLRP3 в эндотелиальных клетках [18]. В ряде исследований при артериальной гипертензии выявлено не только повышение экспрессии белка NLRP3 и каспазы-1 в периферических Т-клетках, но и повышенные сывороточные уровни IL-1β и IL-18, связанные с чрезмерной активацией инфламмасомы [19]. Хроническое низкоградиентное воспаление, опосредованное развитием митохондриальной дисфункции, продукцией активных форм кислорода, активацией NLRP3 и гиперпродукцией IL-1β, наблюдается при ожирении, сахарном диабете 2 типа и его осложнениях [20][21].
Не менее важным фактором активации NLRP3 является холестерин липопротеинов низкой плотности (ЛНП). Как установлено ранее, окисленные ЛНП инициируют сборку инфламмасомы NLRP3 через лизосомальное повреждение. Кристаллы холестерина, фосфата кальция также участвуют в процессе активации NLRP3, но ключевым триггером этой активации является внеклеточный аденозинтрифосфат, выделяемый мертвыми клетками. Таким образом, низкоградиентное системное воспаление может способствовать не только развитию, но и прогрессированию атеросклероза. Согласно недавно опубликованному метаанализу трех рандомизированных клинических исследований с участием 31245 пациентов с атеросклерозом, находящихся на терапии статинами, уровень высокочувствительного С-реактивного белка (СРБ) был более сильным предиктором риска сердечно-сосудистых событий и смерти, чем холестерин ЛНП [22]. Подтверждением роли врожденного иммунитета в атерогенезе служат данные исследования LoDoCo, в котором назначение низких доз колхицина, блокирующего сборку инфламмасом, сопровождалось значительным снижением риска сердечно-сосудистых событий атеросклеротической природы (отношение рисков (ОР) 0,33; 95% доверительный интервал (ДИ): 0,18-0,59; p<0,001) [23]. В свою очередь, применение колхицина в качестве вторичной профилактики ассоциировалось с более низкой частотой сердечно-сосудистой смерти, инфаркта миокарда (ИМ), ишемического инсульта или потребности в реваскуляризации: 6,8% vs 9,6% в группе плацебо; ОР 0,69; 95% ДИ: 0,57-0,83; p<0,001 [24]. Обоснование клиническому эффекту колхицина находим в исследовании EKSTROM, где назначение препарата сдерживало прогрессирование атеросклеротических бляшек на 1,1% в течение года по сравнению с группой плацебо, а также вызывало регресс некальцинированной атеросклеротической бляшки и замедляло процесс кальцификации [25]. Однако применение колхицина в раннем периоде ИМ с пролонгацией терапии в течение 3 лет не снижало частоту комбинированной конечной точки, отношение рисков (ОР (9,1% vs 9,3% в группе плацебо; ОР 0,99; 95% ДИ: 0,85-1,16; p=0,93)) [26]. Отсутствие эффекта от колхицина при остром ИМ можно объяснить на примере экспериментальной модели заболевания. Реваскуляризация миокарда обеспечивает снижение риска повреждения кардиомиоцитов, но за счет дальнейшей активации инфламмасомы NLRP3 клетки остаются уязвимыми к программируемой гибели путем пироптоза [27]. Возможно, ингибирование других компонентов инфламмасомы будет ограничивать пироптоз и размер ИМ. В частности, на экспериментальных моделях и в клинических исследованиях пациентов с острым ИМ с подъемом сегмента ST блокатор рецептора IL-1 препарат анакинра показал, что ингибирование IL-1 улучшает заживление инфаркта, снижает уровни высокочувствительного СРБ и частоту развития сердечной недостаточности [28, 29]. Однако в аналогичном исследовании с применением отечественного блокатора IL-1 препарата гофликицепт на фоне значительного снижения уровня СРБ не выявлено статистически значимых различий по частоте развития и прогрессирования сердечной недостаточности, а также сердечно-сосудистой смертности, госпитализации и динамике уровня натрийуретического пептида [30]. Возможно, это связано с коротким периодом введения препарата, недостаточного для модификации атеросклеротического процесса. Напротив, в исследовании CANTOS (Canakinumab Antiinflammatory Thrombosis Outcome Study) длительное назначение канакинумаба в дозе 150 мг пациентам с постинфарктным кардиосклерозом приводило к снижению риска первичной конечной точки (нефатальный ИМ, нефатальный инсульт или сердечно-сосудистая смертность) на 15% (3,86 vs 4,50 событий на 100 человеко-лет в группе плацебо) и вторичной конечной точки на 17% (4,29 vs 5,13 событий на 100 человеко-лет, соответственно) [31]. Таким образом, подтверждено, что блокада IL-1 может быть перспективной в рамках вторичной профилактики сердечно-сосудистых осложнений после перенесенного ИМ.
Несмотря на очевидную роль приобретенного иммунитета в патогенезе миокардита, нельзя исключить в качестве стереотипного ответа на повреждение миокарда вклад активации инфламмасомы NLRP3 в дальнейшее повреждение и прогрессирование сердечной недостаточности. На экспериментальной модели энтеровирусного миокардита продемонстрировано, что введение блокаторов IL-1 может предотвращать хронизацию процесса за счет подавления процессов воспаления, интерстициального фиброза и патологического ремоделирования сердца миокарда [32]. Данный факт подтверждает гипотезу, что инфламмасома NLRP3 не только инициирует продукцию провоспалительных цитокинов, но и играет важную роль в модуляции хронического воспаления и прогрессировании сердечной недостаточности [33]. Однако назначение в клиническом исследовании блокатора IL-1 препарата анакинра пациентам с острым миокардитом (Anakinra vs. Placebo for the Treatment of Acute Myocarditis, ARAMIS, NCT03018834) не повлияло на частоту развития осложнений [34][35]. Вероятно, причиной подобного результата было включение в исследование пациентов с миокардитом без морфологического подтверждения диагноза, имеющих низкий риск по классификации клиники Mayo.
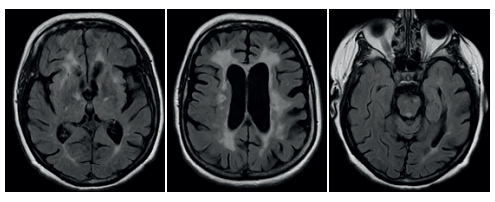
Повреждение мезотелиальных клеток перикарда чаще всего сопровождается развитием аутовоспалительных реакций, т. к. перикард инфильтрирован большим количеством клеток врожденного иммунитета (макрофагов, тучных клеток). Для аутовоспалительного фенотипа перикардитов характерны острое начало с появлением болевого синдрома в грудной клетке, лихорадки, высокой острофазовой активности, а в ряде клинических случаев полисерозитов (плеврита, асцита в дополнение к перикардиту), повышения печеночных трансаминаз и увеличения печени/селезенки. Подобные клинические проявления и их стереотипность при рецидивах в сочетании с классическими электрокардиографическими и эхокардиографическими феноменами, присущими всем вариантам перикардита, сближают ИРП с полигенными аутовоспалительными заболеваниями и в первую очередь с синдромом Стилла взрослых. Для проведения дифференциального диагноза с моногенными аутовоспалительными заболеваниями необходимо выполнить генетическое тестирование (табл. 1), а также оценить наличие критериальных признаков синдрома Стилла взрослых (табл. 3, 4). Дополнительным визуализирующим методом, указывающим на воспалительную природу перикардита, признана магнитно-резонансная томография сердца, при которой выявляется отек перикарда и отсроченное его контрастирование [16]. Терапия нестероидными противовоспалительными препаратами и колхицином, традиционно рассматриваемая в качестве первой линии терапии, может быть эффективна как у пациентов с ИРП, так и у пациентов с перикардитом без ярко выраженных воспалительных маркеров, что не позволяет исключить наличие у этой категории больных низкоградиентного воспаления, ассоциированного с активацией инфламмасом. Учитывая вклад нарушений врожденного иммунитета и ключевую роль IL-1, мы понимаем, что терапевтическое окно для воздействия на этот путь патогенеза может варьировать в зависимости от активности воспалительного процесса в перикарде. Однако на текущий момент эффективность применения блокаторов IL-1 (анакинра, рилонацепт, гофликицепт) доказана только для аутовоспалительного фенотипа рецидивирующего перикардита, к которым можно отнести прежде всего ИРП и редкие варианты стероид-зависимого колхицин-резистентного рецидивирующего постперикардиотомного синдрома [36-38]. Ключевые различия дизайна исследований AIRTRIP (анакинра), RHAPSODY (рилонацепт) и COURSE (гофликицепт) поднимают целый ряд важных вопросов: возможность более ранней инициации блокаторов IL-1 до назначения второй линии терапии глюкокортикостероидами, оптимальной ее продолжительности, подходов к оценке эффективности и профилактике осложнений.
Таблица 1
Моногенные аутовоспалительные заболевания [39]
|
Моногенные аутовоспалительные заболевания |
Тип наследования/ген (белок) |
Основные клинические признаки |
|
Семейная средиземноморская лихорадка (FMF) |
Аутосомно-рецессивный Ген MEFV (пирин) |
Рецидивы лихорадки, длительностью 12-72 ч, артрит и серозит (боль в животе и грудной клетке) |
|
Периодический синдром, связанный с рецептором фактора некроза опухоли (семейная ирландская лихорадка, TRAPS) |
Аутосомно-доминантный Ген TNFRSF1A (рецептор фактора некроза опухолей 1) |
Рецидивы лихорадки, длительностью 1-3 нед., артромиалгии, фасциит, сыпь, конъюнктивит периорбитальный отек и спленомегалия |
|
Гипериммуноглобулинемия с периодическим синдромом лихорадки |
Аутосомно-рецессивный Ген MVK (мевалонат киназа) |
Рецидивы лихорадки, длительностью 3-7 дней, боли в животе, диарея, гепато/спленомегалия и лимфаденопатия |
|
Семейный холодовой аутовоспалительный синдром (CAPS) |
Аутосомно-доминантный Ген NLRP3 (криопирин) |
Рецидивы лихорадки, вызванной простудой, длительностью 0,5-2 сут., крапивница, конъюнктивит и артралгия |
|
Синдром Макла-Уэллса |
Аутосомно-доминантный Ген NLRP3 (криопирин) |
Рецидивы лихорадки, длительностью 2-3 дня, крапивница, сыпь, сенсоневрональная глухота |
|
Пиогенный артрит, гангренозная пиодермия и синдром акне |
Аутосомно-доминантный Ген PSTPIP1 (PSTPIP1) |
Гангренозная пиодермия, кистозные угри и стерильный пиогенный олигоартрит |
|
Дефицит антагониста рецептора интерлейкина-1 |
Аутосомно-рецессивный Ген IL1RN (антагонист рецептора интерлейкина-1) |
Дебют в неонатальном периоде с мультифокального остеомиелита, периостита или пустулезной сыпи |
|
Синдром Маджида |
Аутосомно-рецессивный Ген LPIN2 (липин 2) |
Рецидивирующий мультифокальный остеомиелит, врожденная дизэритропоэтическая анемия и воспалительный дерматоз |
|
Синдром Блау |
Аутосомно-доминантный Ген NOD2/CARD15 (каспазоактивирующий белок 15, CARD15) |
Перемежающаяся лихорадка, гранулематозный дерматит, гранулематозный полиартрит, рецидивирующий панувеит |

Рис. 1. Континуум иммуноопосредованных воспалительных заболеваний [модифицировано из McGonagle D, Watad A. Autoinflammation and Autoimmunity. In P. J. Hashkes, et al. (eds.), Textbook of Autoinflammation, 2019:693-710. doi:10.1007/978-3-319-98605-0_38].
Сокращение: СКВ — системная красная волчанка.
Таблица 2
Сравнительная характеристика аутоиммунных и аутовоспалительных заболеваний [40]
|
Аутовоспаление |
Аутоиммунитет |
||
|
Этиология |
Генетика |
1) Герминативные мутации в элементах врожденной иммунной системы Моногенные > полигенные 2) Постзиготные мутации (соматический мозаицизм) |
Образование аутореактивных лимфоцитов путем соматической рекомбинации (дифференцировка лимфоцитов на ранних этапах) Полигенные > моногенные |
|
Иммунология |
Недостаточность аутоингибиторных механизмов ± конститутивный воспалительный сигналинг |
Нарушение иммунной толерантности ± повреждение тканей, вызванное аутореактивными лимфоцитами |
|
|
Демография |
Возраст дебюта |
Герминативные мутации: Детский > взрослый Соматические мутации: Взрослый > детский |
Взрослый > детский |
|
Семейный анамнез |
Герминативные мутации: +++ Соматические мутации: нет анамнеза |
+/- |
|
|
Клинические особенности |
Триггер |
Стресс, инфекции, простуда, физическое напряжение или травма, вакцинация, менструация, беременность |
Стресс, инфекции, беременность, вакцинация |
|
Рецидивы лихорадки |
+++ |
Редко |
|
|
Язвы полости рта/генитальные язвы |
+++ |
++ |
|
|
ЖКТ-симптомы |
Колит у детей, перитонит ВЗК-подобные симптомы |
Воспалительные заболевания кишечника у взрослых |
|
|
Асептический остеит/остеомиелит |
++ |
+/- |
|
|
Другие симптомы |
Сыпь, синовит, неврологические и почечные нарушения |
||
|
Лабораторные тесты |
Острофазовые биомаркеры |
Только во время рецидива |
В любой период времени в отсутствие контроля заболевания |
|
Аутоантитела |
– |
+++ |
|
|
Генетическое тестирование |
+++ |
– |
|
|
Ответ на терапию |
Колхицин, блокаторы IL-1 |
+++ |
+ |
|
Антиметаболиты (азатиоприн, метотрексат) гидроксихлорохин, циклоспорин |
– |
+++ |
|
|
Ингибиторы Янус-киназы, ингибиторы ФНО, ГКС |
+++ |
||
Сокращения: ВЗК — воспалительные заболевания кишечника, ГКС — глюкокортикостероиды, ЖКТ — желудочно-кишечный тракт, ФНО — фактор некроза опухолей, IL-1 — интерлейкин-1.
Таблица 3
Рекомендации по диагностике синдрома Стилла взрослых [41]
|
Уровень доказанности |
Согласие экспертов |
|
|
Клинические проявления |
2аВ |
94% |
|
Фебрильная лихорадка с температурой ≥39 0C в течение как минимум 7 дней |
||
|
Кожная сыпь носит транзиторный характер, часто совпадает с пиками лихорадки, преимущественно поражая туловище. Сыпь обычно эритематозная (лососево-розовая), но другие высыпания (например, крапивница) также могут соответствовать диагнозу |
||
|
Поражение опорно-двигательного аппарата обычно сопровождается артралгией/миалгией. Явный артрит не обязательный критерий для диагностики, он может появляться позднее |
||
|
Высокий уровень воспаления: нейтрофильный лейкоцитоз, повышение уровня СРБ и ферритина в сыворотке крови |
||
|
Значительное повышение уровня сывороточного уровня IL-18 и/или S100 (например, кальпротектина) убедительно подтверждает диагноз |
4С |
90% |
|
Исключить альтернативные диагнозы, такие как злокачественные новообразования, инфекционные заболевания, другие иммуноопосредованные воспалительные и моногенные аутовоспалительные заболевания |
5D |
85% |
Сокращения: СРБ — С-реактивный белок, IL-1 — интерлейкин-1.
Таблица 4
Критерии Ямагучи для диагностики болезни Стила у взрослых (1992) с адаптацией от PReS/EULAR [42][43]
|
Категория |
Критерий |
Описание |
|
Большие критерии |
1. Лихорадка ≥39 0C продолжительностью ≥1 нед. |
Ежедневная или рецидивирующая высокая температура |
|
2. Артралгия или артрит продолжительностью ≥2 нед. |
Часто поражает несколько суставов, может имитировать ревматоидный артрит. Не облигатный симптом в настоящее время (может отсутствовать) |
|
|
3. Бледно-розовая макуло-папулёзная сыпь |
Обычно мимолётная, возникает на фоне лихорадки, преимущественно на туловище и конечностях |
|
|
4. Лейкоцитоз ≥10000/мм3 с нейтрофилами ≥80% |
||
|
Малые критерии |
1. Боль в горле |
Часто наблюдается на раннем этапе заболевания |
|
2. Лимфоаденопатия и/или спленомегалия |
||
|
3. Нарушения функции печени |
Умеренное повышение трансаминаз (аспартатаминотрансфераза, аланинаминотрансфераза) либо лактатдегидрогеназы |
|
|
4. Отрицательные ревматоидный фактор и антинуклеарный фактор |
||
|
Для постановки диагноза необходимо наличие ≥5 критериев, включая не менее 2 основных |
||
|
Исключаемые состояния Инфекции, злокачественные новообразования, моногенные аутовоспалительные заболевания, другие иммуноопосредованные патологии |
||
Подводя итоги вышеизложенного, следует отметить, что инновационные исследования последнего десятилетия в области врожденного иммунитета и мультидисциплинарный подход позволили не только по-новому взглянуть на патогенез традиционных сердечно-сосудистых заболеваний, их развитие и прогрессирование, но и выявить новые мишени для терапевтического воздействия, связанные с активацией инфламмасом и образованием IL-1.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Моисеева О.М., Мячикова В.Ю., Маслянский А.Л. Аутоиммунитет, аутовоспаление и сердечно-сосудистая система: иммунопатогенез и таргетная терапия. Российский кардиологический журнал. 2025;30(3S):6437. https://doi.org/10.15829/1560-4071-2025-6437. EDN: SSDWDE
Скопировать