Клинический случай новой коронавирусной инфекции (COVID-19) у пациентки с CADASIL-синдромом
Церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией CADASIL-синдром (от англ. cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy) является редким генетическим заболеванием, обусловленным мутацией в гене NOTCH-3 на хромосоме 19q12, с аутосомно-доминантным наследованием. Данное заболевание характеризуется низкой распространенностью, в мире регистрируется 2-5 случаев на 100 тыс. человек, однако встречаемость этой патологии в различных популяциях может различаться [1].
Клинически CADASIL-синдром чаще всего проявляется рецидивирующими ишемическими эпизодами, приводящими к деменции, нарушениями ходьбы, недержанием мочи, бульбо-псевдобульбарным параличом, мигренью (с аурой и без) и эпилептическими припадками. Мигрень с аурой — ранняя характерная черта CADASIL-синдрома, встречается у 20-50% пациентов, средний возраст которых составляет 30 лет. Транзиторные ишемические атаки и лакунарные инфаркты головного мозга при CADASIL-синдроме встречаются у 60-85% больных в возрасте 50-60 лет. Когнитивные нарушения часто бывают ранним проявлением CADASIL-синдрома. Эпилептические припадки развиваются у 5-10% больных [2].
Новая коронавирусная инфекция 2019г (COVID-19) (от англ. coronavirus disease 2019), вызванная вирусом SARS-CoV-2 (от англ. severe acute respiratory syndrome-related coronavirus 2), представляет собой серьезную угрозу человечеству и связана с широким спектром клинических респираторных синдромов, варьирующих от легких симптомов поражения верхних дыхательных путей до представляющей опасность для жизни прогрессирующей вирусной пневмонии [3]. Пациенты с тяжелой формой COVID-19 характеризуются наличием дыхательной недостаточности и прогрессирующей гипоксемией, что нередко требует респираторной поддержки. На компьютерной томографии (КТ) грудной клетки у больных COVID-19 выявляются многочисленные уплотнения лёгочной ткани по типу “матового стекла” преимущественно округлой формы, различной протяженности с консолидацией или без, что соответствует берлинским критериям острого респираторного дистресс-синдрома [4]. К отличительным признакам COVID-19 относится сосудистая патология, обусловленная эндотелиальной дисфункцией и другими факторами. COVID-19 характеризуется также коагулопатией, вследствие которой формируются кожные изменения, свидетельствующие о тромботической микроангиопатии, а также диффузное альвеолярное повреждение за счет образования фибриновых тромбов; лабораторные изменения у этих пациентов характеризуются повышением уровней D-димера и ферритина [5].
Большая часть наших знаний в отношении инсультов, связанных с SARS-Cov-2 или усугубленных вирусной инфекцией, основана на данных, полученных в серии одноцентровых случаев, и отсутствуют четкие алгоритмы лечения данных пациентов. В настоящее время предпринимаются усилия для улучшения диагностики, определения факторов риска и подходов к терапии у пациентов с инсультами, ассоциированных с SARS-CoV-2.
Представляем описание клинического случая пациентки с церебральной аутосомно-доминантной артериопатией с субкортикальными инфарктами и лейкоэнцефалопатией (CADASIL-синдромом), перенесшей COVID-19 среднетяжелого течения — сочетание врожденной и инфекционно-обусловленной ангиопатий.
Клинический случай
В инфекционный стационар поступила пациентка Ш., 56 лет с выявленной ранее доминантной артериопатией с субкортикальными инфарктами и лейкоэнцефалопатией (CADASIL-синдром) и с COVID-19 (подтвержденной), двусторонней вирусной полисегментарной пневмонией. При поступлении жалобы на выраженную слабость, субфебрильную температуру.
Анамнез. Из анамнеза известно, что с 2010г (в возрасте 46 лет) появилось нарушение памяти и возникла неустойчивость при ходьбе. С 2010г диагностирована сенсорная афазия, моторная апраксия, нарушение право-левой ориентировки, пальцевая агнозия, хватательный феномен Бехтерева-Янишевского с 2-х сторон, псевдобульбарный синдром, двусторонняя пирамидная недостаточность, лёгкая двусторонняя мозжечковая атаксия. В 2015г в Медико генетическом научном центре г. Москвы обследована в лаборатории наследственных болезней обмена веществ — проведен анализ на мутации в гене NOTCH3 (Синдром CADASIL). Выявлена мутация с.548G>T (p.Cys183Phe) в гетерозиготном состоянии и установлен диагноз синдрома CADASIL. При последующих госпитализациях в неврологическую клинику отмечалась прогрессия неврологической симптоматики, нарастающие когнитивные нарушения (Монреальская шкала оценки когнитивных функций 21 балл, краткая шкала оценки психического статуса MMSE 17 баллов, батарея лобной дисфункции FAB 6), в 2020г диагностированы выраженные когнитивные нарушения (деменция лобно-подкоркового типа). При дуплексном сканировании брахио-цефальных артерий атеросклеротических бляшек и утолщения комплекса интима-медиа не выявлено (рис. 1). Электроэнцефалография от 2019г — изменения в пределах дезорганизованного типа. Эпилептиформной активности нет.

Рис. 1. Ультразвуковое исследование сонных артерий.
Примечание: общая сонная артерия, внутренняя сонная артерия, наружная сонная артерия проходимы на всем протяжении, диаметры достаточны, скоростные показатели в пределах нормы (в общей сонной артерии скорость кровотока 80,0 см/сек, наружной сонной артерии — 48,0 см/сек, внутренней сонной артерии — 42,0 см/сек). Толщина интима-медиа 0,08 см.
При исследовании методом ПЦР в ликворе и в крови ДНК вирусов Herpes и Borrelia не выявлено. Данных за наличие ревматологической патологии и антифосфолипидного синдрома не получено (антинуклеарный фактор, ревматоидный фактор, антитела к цитоплазме нейтрофилов, антитела к кардиолипину и к бета-2 гликопротеину не изменены. Олигоклональный иммуноглобулин G в сыворотке крови и в ликворе не был обнаружен, свободные лёгкие цепи каппа и лямбда в сыворотке крови и ликворе не повышены. Основной белок миелина и антитела к аквапорину 4 не повышены. Ф-50, HBsAg, HCVAb, RW в ликворе и крови отрицательные.
На фоне регулярных курсов нейрометаболической терапии, нерегулярного приёма блокатора глутаматных NMDA-рецепторов и ингибиторов ацетилхолинестеразы значимой положительной динамики не наблюдалось. С 2019г пациентка получала постоянную терапию: периндоприл 5 мг + индапамид 1,25 мг; аторвастатин — 10 мг; метформин — 850 мг; акатинол мемантин — 10 мг; леветирацетам — 500 мг.
Развитие COVID-19. За 7-8 дней до госпитализации у пациентки наросла слабость, снизился аппетит, снизились когнитивные функции, появилась субфебрильная лихорадка. При поступлении в инфекционный стационар при осмотре состояние средней тяжести. Температура 38,0o С. Пульс: 97 уд./мин, ритмичный, удовлетворительного наполнения, не напряжен, симметричный. Артериальное давление: 115/70 мм рт.ст. Дыхание: самостоятельное, эффективное, ритмичное. Частота дыхательных движений 21 в мин, SpO2 92%. Контакт с пациенткой существенно ограничен из-за деменции. Обоняние, движения глаз, поля зрения, чувствительность у пациентки оценить невозможно. Зрачки D=S. Фотореакция вялая, конвергенцию не оценить. Установочный нистагм при крайних отведениях
глазных яблок, корнеальные рефлексы сохранены, точки выхода ветвей тройничного нерва безболезненны, глотание не нарушено, глоточные рефлексы снижены, дизартрия. Язык в полости рта, по средней линии. Вызываются симптомы орального автоматизма, хватательный рефлекс справа. Мышечный тонус в руках повышен по пирамидному типу. Диффузная мышечная гипотрофия. Достоверно мышечную силу не оценить ввиду когнитивного дефицита. Бицепитальные, коленные рефлексы живые D>S, трицепитальные, карпорадиальные, ахилловы D=S. Брюшные рефлексы сохранены. Рефлексы Бабинского с двух сторон. Реакция на боль сохранена с обеих сторон. Координаторные пробы не оценить, оболочечных симптомов нет. Таким образом, выявлены следующие синдромы: когнитивные нарушения (деменция лобно-подкоркового типа), псевдобульбарный, сенсомоторная афазия, двусторонняя пирамидная недостаточность, нарушения функции тазовых органов по центральному типу, свидетельствующие о многоочаговом сосудистом процессе.
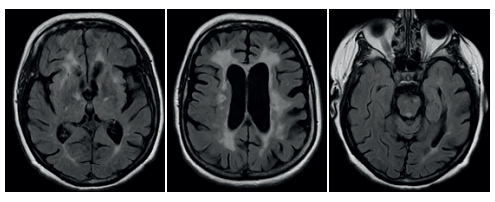
По данным магнитно-резонансной томографии (МРТ) картина множественных очаговых изменений в веществе головного мозга дисциркуляторного характера; многочисленные лакунарные кисты постишемического генеза, перивентрикулярные зоны лейкоареоза. Расширение ликворных пространств (рис. 2).

Рис. 2. Серия МРТ снимков головного мозга.
Примечание: МРТ картина множественных очаговых изменений в веществе головного мозга дисциркуляторного характера, многочисленных лакунарных кист постишемического генеза, перивентрикулярных зон лейкоареоза. Расширение ликворных пространств.
По данным КТ органов грудной клетки при поступлении — двухсторонняя вирусная пневмония, КТ-2. При оценке тяжести состояния пациента по шкале NEWS (от англ. National Early Warning Score) — 6 баллов. В газовом составе артериальной крови отмечался декомпенсированный алкалоз, Ph 7,600, а также снижение уровня порционного давления кислорода до 53,0 мм рт.ст. (табл. 1). Диагностирована дыхательная недостаточность 1 степени. В анализах крови отмечался высокий уровень С-реактивного белка (СРБ), небольшое повышение уровня фибриногена и D-димера, уровень лейкоцитов и прокальцитонина в пределах нормы (табл. 2, 3).
Таблица 1
Динамика гематологических показателей

Таблица 2
Динамика газового состава артериальной крови

Таблица 3
Динамика концентрации СРБ в сыворотке крови

На 11-й день болезни отмечен максимальный уровень СРБ (171,47 мг/л), на КТ органов грудной клетки на фоне неравномерной пневматизации легочной ткани в разных отделах обоих легких сохранялось сгущение легочного рисунка с формированием полей “матового стекла” с множественными очагами “консолидации” (как в периферических, так и в центральных отделах легких перибронхиально) и выраженными ретикулярными изменениями (с преимущественной локализацией в дорсальных и дорсо-базальных отделах). Поражение легочной ткани 65-70%. КТ-картина не противоречила проявлениям вирусной пневмонии (высокая вероятность COVID-19), протяженность изменений в легочной ткани соответствует степени КТ 2-3. При сравнении с предыдущими исследованиями отмечалась отрицательная динамика.
Согласно временным методическим рекомендациям по профилактике, диагностике и лечению COVID-19, существовавшим на тот период, пациентам показано назначение терапии препаратами гидроксихлорохина в сочетании с азитромицином по схеме (гидроксихлорохин 400 мг 2 раза/сут., затем 200 мг 2 раза/сут. в течение 6 дней + азитромицин 500 мг 1 раз/сут. в течение 7 дней). С учетом тяжелого неврологического дефицита, сохранения лихорадки и необходимости кислородной поддержки, нарастания уровня СРБ и отрицательной динамики по КТ органов грудной клетки было принято решение отказаться от данной схемы лечения в пользу назначения глюкокортикостероидов (ГКС). Через 10 дней терапии дексаметазоном (в дозе 12 мг/сут. длительностью 10 дней, 8 мг/сут. 11 дней, 4 мг/сут. 12 дней, далее отмена ГКС) отмечалось купирование лихорадки, нормализация уровня СРБ, положительная динамика в неврологическом статусе в виде легкого регресса когнитивных нарушений — улучшилось понимание обращённой речи (отмечалось увеличение скорости выполнения простых команд, рост интереса к выполнению простых заданий и появление положительных эмоций на обращённую речь персонала). Также отмечалось улучшение фиксации взгляда на молоточке в горизонтальном направлении. В газовом составе артериальной крови (при отмене кислородной поддержки) прирост лактата не отмечался, что свидетельствовало об отсутствии значимой тканевой гипоксии (табл. 2). По данным КТ органов грудной клетки в периферических и центральных отделах обоих легких сохранялись дольковые сливающиеся и мультидольковые участки снижения пневматизации легочной ткани по типу “матового стекла” с нечеткими контурами. Определялись аналогичные по структуре нодулярные уплотнения в верхней доле правого легкого. Преимущественно в дорзобазальных отделах обоих легких определялась трансформация некоторых интерстициальных инфильтратов в перилобулярные ретикулярные уплотнения, параплевральные и перибронховаскулярные зоны консолидации легочной паренхимы пластинчатой и звездчатой форм с тяжистыми контурами (закономерная динамика — формирование КТ-картины “криптогенной организующейся пневмонии”?). Протяженность инфильтративных изменений уменьшилась в сравнении с данными предыдущего КТ-исследования (рис. 3).
С учетом высокого риска внутрисосудистого тромбоза у пациентки с первого дня госпитализации была начата терапия низкомолекулярными гепаринами (эноксапарином натрия) в лечебной дозе из расчета 1 мг/кг (риск кровотечения устанавливался по шкале HAS-BLED). Эффективность антикоагулянтной терапии была оценена по данным КТангиографии головного мозга и органов грудной клетки на пике концентрации СРБ. По данным КТангиографии головы и шеи, КТ-данных за “наличие стенозов, тромбозов” в зоне исследования не получено (рис. 4). КТ-признаков тромбоэмболии средних и крупных ветвей лёгочной артерии не получено.

Рис. 3. Динамика КТ органов грудной клетки на 8, 14 и 21 день заболевания вирусной инфекцией.

Рис. 4. КТ-ангиография головы и шеи.
Примечание: диаметр сонных артерий не изменен, дефектов контрастирования не выявлено, ход без патологической извитости. Позвоночные артерии отходят типично, вступают в костно-фиброзный канал поперечных отростков на уровне С6, проходимы, не сужены, левая — доминантная. Интракраниальные сегменты внутренних сонных артерий, базилярная и мозговые артерии проходимы, не сужены. Передняя соединительная и правая задняя соединительная артерии хорошо развиты. Левая задняя соединительная артерия не развита. Отмечается диффузное расширение желудочков головного мозга, понижение плотностных показателей перивентрикулярного белого вещества головного мозга.
Обсуждение
COVID-19 — новое заболевание, вызываемое вирусом SARS-CoV-2, характеризующееся лихорадкой, кашлем, миалгией и, в конечном итоге, одышкой. Несмотря на характерное проявление COVID-19, часто отмечаются атипичные симптомы, такие как желудочно-кишечные расстройства и неврологические симптомы, включающие головную боль, изменение психического статуса, потерю обоняния и судороги. Часто у тяжелых пациентов с COVID-19 развиваются сердечно-сосудистые осложнения, такие как инфаркт миокарда, нарушения мозгового кровообращения, однако связь между инфекцией и данными осложнениями сложна и мало изучена. Было показано, что вирусы герпеса, такие как вирус ветряной оспы, могут проникать в стенку сосуда, вызывая церебральную васкулопатию. Для сравнения, цитомегаловирус, Chlamydia pneumonie и другие патогенные организмы тесно связаны с атерогенезом и нестабильностью атероматозных бляшек. Кроме того, известно, что недавние бактериальные или вирусные инфекции временно усугубляют уже существующие сосудистые факторы риска инсульта [6]. В различных обзорах литературы по COVID-19 было высказано предположение, что инфекции создают воспалительную среду, которая предрасполагает к инсульту, путем активации протромботических путей, влияющих на стабильность бляшек, вызывая эндотелиальную дисфункцию, утолщение интимы, приводя к ремоделированию артериальной стенки. У пациентов с вирусом SARS-CoV-2 инсульты, как правило, связаны с активацией ренин-ангиотензиновой системы, прокоагуляцией и массовым высвобождением воспалительных цитокинов (цитокиновый шторм) [7].
Инсульты у пациентов с CADASIL имеют склонность к подкорковым структурам. Поражение ствола мозга встречается значительно реже [8]. Интересно, что вскрытия и исследования на животных показали, что коронавирусы могут иметь особый тропизм к стволу мозга. В то же время ранее проведенные исследования с группой коронавирусов на доклинических моделях показали, что когда коронавирусы проникают в мозговой слой, у животных повышается частота смертности, и связано это, предположительно, с дисфункцией кардиореспираторного центра в стволе мозга [9]. У нашей пациентки были факторы риска сосудистых заболеваний: ожирение, гипертония и CADASIL.
У пациентки артериальная гипертензия контролировалась в пределах оптимальных значений, и связанные с синдромом CADASIL изменения головного мозга по данным МРТ оставались стабильными на протяжении многих лет, как и неврологическая симптоматика. Вполне возможно, что инфекция SARSCov-2 могла внести свой вклад в ухудшение течения CADASIL — усугубление неврологической симптоматики и когнитивных функций. Следует отметить, что на фоне своевременного лечения у пациентки был снижен риск возникновения спонтанных тромбозов — лабораторные показатели Д-димера были в пределах нормы, а концентрация С-реактивного белка в крови на фоне терапии ГКС достаточно быстро нормализовалась. Проводилось и лечение низкофракционными гепаринами в лечебных дозировках. Неврологические и когнитивные нарушения носили временный характер и, вероятнее всего, были связаны с вирусной интоксикацией.
Таким образом, у пациентов с сочетанием врожденной и инфекционно-обусловленной ангиопатий и COVID-19 необходимо выполнение нейровизуализации для исключения новых очагов нарушения мозгового кровообращения. Согласно рекомендациям, раннее начало терапии прямыми антикоагулянтами может быть полезным для уменьшения риска тромбоэмболии у данных пациентов. При наличие дыхательной недостаточности и в зависимости от тяжести пациентов с CADASIL-синдромом и COVID-19 рекомендована кислородотерапия для уменьшения гипоксии, которая также влияет на прогрессию неврологической симптоматики. Показана инвазивная и неинвазивная искусственная вентиляция легких, CPAP терапия (от англ. continuous positive airway pressure) и BiPAP-терапия (от англ. bilevel positive airway pressure), или использование высокопоточной подачи кислорода назальными канюлями у пациентов средней тяжести. Назначение специфического противовирусного лечения носит дискутабельный характер, назначение терапии должно выполняться в соответствии с методическими рекомендациями по лечению COVID-19 Минздрава России [10].
Отношения и деятельность: авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Заславская Е.Л., Заславский Л.Г., Баранова Е.И., Алексеева А.М., Марков Н.В., Загидуллин Н.Ш. Клинический случай новой коронавирусной инфекции (COVID-19) у пациентки с CADASIL-синдромом. Российский кардиологический журнал. 2020;25:4170. https://doi.org/10.15829/1560-4071-2020-4170
Скопировать