Кардиомиопатия, ассоциированная с аритмией: 12-летнее наблюдение пациентки после дебюта фибрилляции предсердий
Аннотация
Кардиомиопатия, ассоциированная с аритмией (КАА), — обратимое осложнение фибрилляции/трепетания предсердий, однако ее диагностика и выбор оптимальной тактики ведения остаются сложной клинической задачей. Длительное наблюдение за пациентами с КАА представляет особый интерес для оценки отдаленных результатов и совершенствования тактики ведения таких пациентов. В данной статье описан клинический случай пациентки 50 лет с агрессивным дебютом тахисистолической формы фибрилляции предсердий, приведшей к тяжелой дисфункции левого желудочка, аритмогенному шоку и жизнеугрожающим осложнениям, включая тромбоэмболию легочной артерии и ишемический инсульт, несмотря на оптимальную антитромботическую терапию. На начальном этапе, несмотря на медикаментозную терапию и множественные электрические кардиоверсии, достичь стабильного синусового ритма не удавалось. Была выполнена имплантация трехкамерного кардиовертера-дефибриллятора с предполагаемой дальнейшей деструкцией атриовентрикулярного соединения. Однако в дальнейшем тактика была изменена в сторону ритм-контролирующей стратегии: проведена серия катетерных аблаций (изоляция легочных вен и модификация субстрата в предсердиях), что позволило восстановить и поддерживать синусовый ритм. На фоне этого достигнута полная нормализация функции левого желудочка и компенсация сердечной недостаточности на протяжении 10 лет. Через 10 лет после последней аблации отмечен поздний рецидив аритмии, потребовавший повторного хирургического вмешательства. Представленный случай демонстрирует эффективность активной, в т.ч. многоэтапной, ритм-контролирующей стратегии при КАА, которая может приводить к полному и длительному восстановлению функции сердца. Ключевыми аспектами ведения являются раннее и агрессивное купирование аритмии, готовность к коррекции тактики, осознание риска поздних рецидивов, обусловленных прогрессирующим ремоделированием предсердий, и необходимость пожизненного динамического наблюдения.
Одним из осложнений наиболее распространенных нарушений ритма сердца –фибрилляции (ФП) и трепетания предсердий (ТП) [1] — является развитие кардиомиопатии. Кардиомиопатия, ассоциированная с аритмией (КАА), диагностируется примерно в 5% случаев у пациентов с ФП и/или ТП, при этом наблюдается снижение сократительной функции левого желудочка (ЛЖ), расширение камер сердца, формируется и/или нарастает сердечная недостаточность (СН). КАА может проявляться в виде усугубления имеющейся дисфункции ЛЖ или декомпенсации предсуществующей СН [2][3].
Лечение пациентов с СН и ФП включает как медикаментозную, так и немедикаментозную терапию. Кроме лечения антиаритмическими препаратами, обязательным является назначение в подобных случаях квадротерапии и антикоагулянтной терапии для профилактики ишемического инсульта [4]. Немедикаментозное лечение состоит из подходов к купированию и профилактике рецидивов ФП: катетерная или хирургическая аблация, создание атриовентрикулярной блокады с имплантацией устройства кардиоресинхронизирующей терапии или стимуляцией левой ножки пучка Гиса [5].
В практике кардиолога пациент с впервые выявленной ФП и кардиомиопатией представляет сложную диагностическую задачу, а успешность лечения таких пациентов зависит от патогенеза развития такого комбинированного состояния. Так, возникновение ФП у пациента с ранее имеющейся кардиомиопатией является неблагоприятным прогностическим фактором, однако лечение в первую очередь направлено на компенсацию СН с рассмотрением возможности и целесообразности купирования ФП и предупреждение рецидивов аритмии.
Напротив, манифестация ФП с развитием КАА чаще предполагает необходимость купирования ФП в первую очередь, а затем профилактику рецидивов ФП. Терапия СН в этом случае имеет крайне важное значение, но, по факту, компенсация состояния происходит довольно быстро после купирования аритмии.
Два гипотетических варианта КАА при ФП представлены на рисунке 1. Безусловно, между ними находится довольно широкий спектр промежуточных типов течения СН, однако упрощенная форма представления позволяет сформулировать основные акценты персонализированного лечения пациентов.
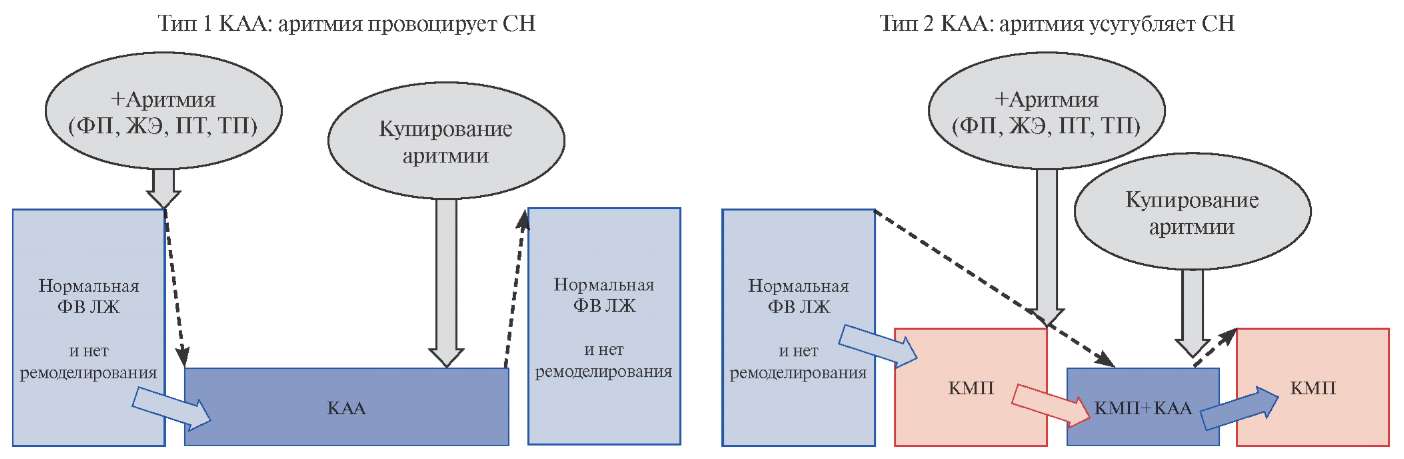
Рис. 1. Гипотетические варианты КАА.
Примечание: Панель 1: появление нарушения ритма сердца провоцирует развитие кардиомиопатии, а после купирования аритмии восстанавливается функция и размеры сердца, исчезают проявления СН. Панель 2: КАА манифестирует при возникновении аритмии на фоне имеющегося заболевания сердца с предсуществующей кардиомиопатией; состояние пациента и функция желудочков являются, по факту, сочетанием двух кардиомиопатий — исходной и КАА; после купирования КАА возможно улучшение функции желудочков и компенсация состояния вплоть до предсуществующего уровня. Часто данный тип относят к декомпенсации СН при нарушениях ритма.
Сокращения: КАА — кардиомиопатия, ассоциированная с аритмией, КМП — кардиомиопатия, ЖЭ — желудочковая экстрасистолия, ЛЖ — левый желудочек, ПТ — предсердная тахикардия, СН — сердечная недостаточность, ТП — трепетания предсердий, ФП — фибрилляция предсердий, ФВ — фракция выброса.
Целью данной публикации является представление результатов длительного наблюдения пациентки с КАА на фоне дебюта ФП, а также обсуждение сложности выбора оптимальной тактики ведения.
Клинический случай
Представлен клинический случай ведения пациентки с ФП и КАА с наблюдением в течение 12 лет (рис. 2).
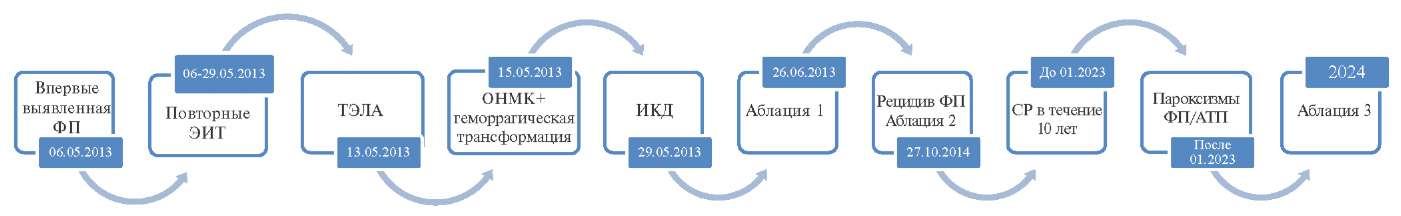
Рис. 2. Схема течения заболевания и подходов к лечению пациентки.
Сокращения: АТП — атипичное трепетание предсердий, ИКД — имплантируемый кардиовертер-дефибриллятор, ОНМК — острое нарушение мозгового кровообращения, СР — синусовый ритм, ТЭЛА — тромбоэмболия легочной артерии, ФП — фибрилляция предсердий, ЭИТ — электроимпульсная терапия.
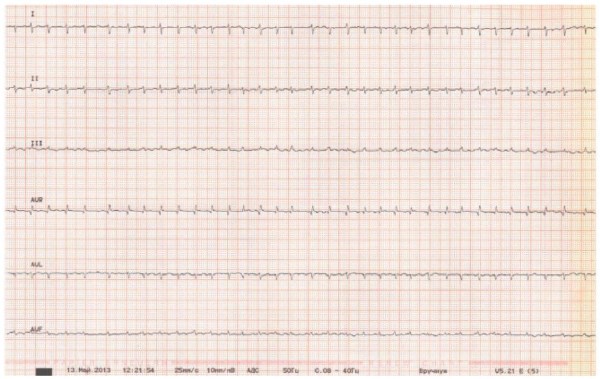
Пациентка 50 лет без анамнеза артериальной гипертензии, ишемической болезни сердца, острого нарушения мозгового кровообращения (ОНМК), без вредных привычек, с избыточной массой тела (индекс массы тела 29,1 кг/м²). Препараты, влияющие на систему гемостаза, в т.ч. гормональные контрацептивы, не принимала. Поступила в клинику 06.05.2013 с впервые выявленной персистирующей формой ФП, тахисистолией желудочков: средняя частота сокращения желудочков 170 в минуту (рис. 3). Обратимых причин ФП не было выявлено (электролитных нарушений, заболеваний щитовидной железы и др.). Клиническая картина аритмогенного шока потребовала проведения повторных электроимпульсных терапий. Терапия включала в себя внутривенную инфузию амиодарона (1200 мг в сут.) и гепарина (до достижения целевых цифр) с последующим переводом на низкомолекулярный гепарин — эноксапарин в дозировке 0,6 мг подкожно дважды в сутки, диуретики, проводилась антиагрегантная терапия ацетилсалициловой кислотой. Тем не менее 13.05.2013 симптомный эпизод тромбоэмболии мелких ветвей легочной артерии (с повышением Д-димера — до 8,8 мкг/мл и типичными признаками при компьютерной томографии), по данным эхокардиографии — выраженное снижение сократительной способности ЛЖ (фракция выброса (ФВ) ЛЖ по Симпсону 20%) с диффузной гипокинезией, дилатация всех камер сердца, давление в легочной артерии 45 мм рт.ст. Ультразвуковая диагностика вен нижних конечностей не выявила тромбоза. По данным выполненной чреспищеводной эхокардиографии наблюдалось спонтанное контрастирование левого предсердия 3 степени, без признаков наличия тромбов в камерах сердца, включая ушко левого предсердия. Через два дня выявлено ОНМК в бассейне левой средней мозговой артерии по ишемическому типу (с показаниями к выполнению внутрисосудистого тромболизиса и тромбэкстракции) и геморрагической трансформацией объемом 1 см³ на 7‑е сут. после операции с дальнейшей положительной динамикой по данным проведенной КТ головного мозга. В связи с возникшими на фоне адекватно проводимой антитромботической терапии тромбоэмболии легочной артерии (ТЭЛА) и ОНМК проведено обследование на коагулопатии и тромбофилии, системные воспалительные заболевания, в т.ч. васкулиты, системную красную волчанку, в результате которого данных за наличие заболеваний, влияющих на систему гемостаза, найдено не было.
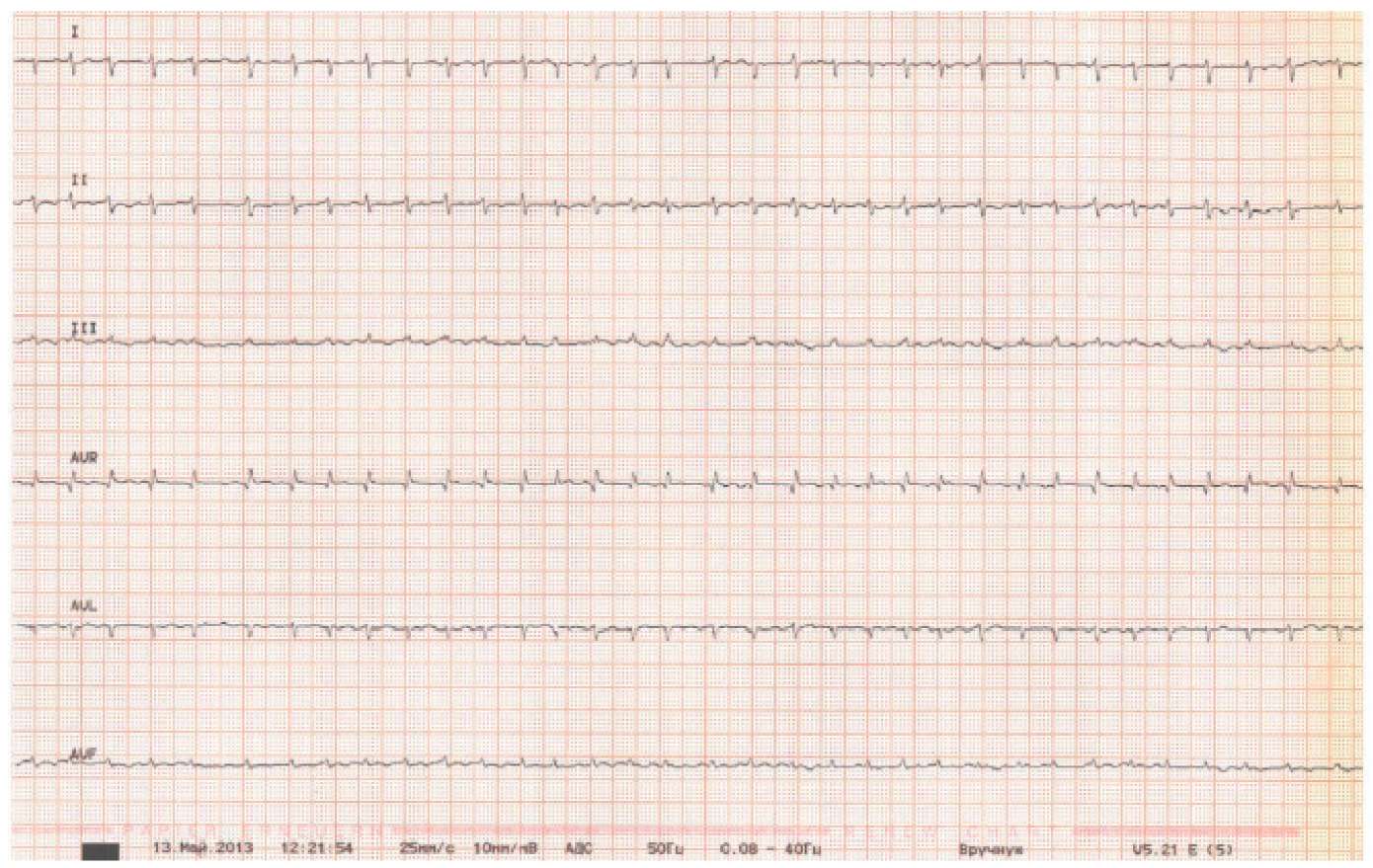
Рис. 3. Электрокардиография при поступлении в стационар.
В ходе наблюдения отмечались неоднократные пароксизмы ФП с частотой желудочковых сокращений до 240 ударов в минуту, выполнялись повторные электрические кардиоверсии с восстановлением синусового ритма. Однократно на фоне выраженной тахисистолии развился эпизод фибрилляции желудочков, купированный наружной дефибрилляцией. В рамках обследования на возможный миокардит выполнена эндомиокардиальная биопсия, однако был получен отрицательный результат. Магниторезонансная томография сердца на фоне значимой тахисистолии не могла быть выполнена. Для купирования тахисистолии и профилактики внезапной смерти предлагалось выполнение катетерной деструкции атриовентрикулярного узла с имплантацией трехкамерного кардиовертера-дефибриллятора (ИКД). В качестве антиаритмической терапии пациентка получала амиодарон в сочетании с бета-адреноблокаторами (бисопролол 7,5 мг). Имплантация ИКД была выполнена 29.05.2013. Установлены электроды — дефибриллирующий в правом желудочке, а также предсердный; левожелудочковый электрод не удалось установить ввиду особенностей анатомии венозной системы сердца. В ходе следующих дней наблюдения отмечались периоды спонтанного восстановления синусового ритма, и консилиумным решением была принята новая тактика лечения — катетерная изоляция легочных вен (ИЛВ) для подавления рецидивов ФП.
Во время катетерного вмешательства, после ИЛВ, выявлены несколько видов атипичного ТП, потребовавших создания дополнительных линейных аблаций по крыше и передней стенке левого предсердия. Течение раннего послеоперационного периода гладкое, наблюдалось быстрое нарастание ФВ ЛЖ до 50% на фоне синусового ритма. Через 2 мес. нарушения ритма рецидивировали в виде ТП с выраженной тахисистолией, однократным нанесением шока ИКД в ответ на тахисистолию с восстановлением синусового ритма (желудочковых тахикардий не зарегистрировано). В связи с этим 27.10.2014 пациентке выполнена повторная аблация субстрата аритмии в левом и правом предсердиях.
В дальнейшем в течение 10 лет (до 2023г) у пациентки не происходило каких-либо значимых сердечно-сосудистых событий, не было проявлений СН, ФВ ЛЖ сохранялась на уровне 55% (рис. 4, табл. 1). Терапия включала в себя постоянный прием ривароксабана 20 мг, периндоприла 5 мг и соталола 40*2 раза/сут. С января 2023г отмечены редкие рецидивы ФП и атипичного ТП на фоне физической нагрузки, купированные повторной медикаментозной и электрической кардиоверсией. Эпизоды аритмий сопровождались транзиторным снижением ФВ ЛЖ до 46% (рис. 5, табл. 1). В связи с симптомными пароксизмами аритмии, в октябре 2024г была выполнена третья катетерная аблация по поводу ФП и атипичного ТП, после которой у пациентки отсутствуют эпизоды аритмии в течение 1 года.
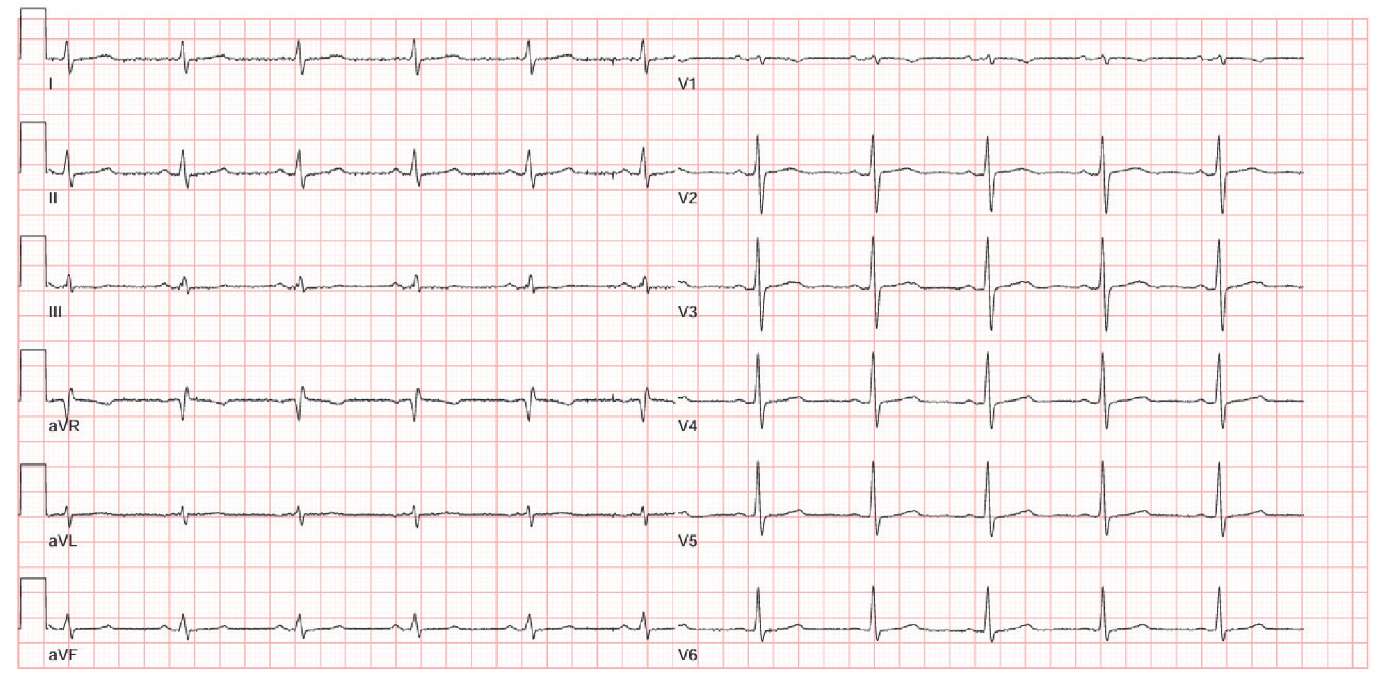
Рис. 4. Электрокардиография после выполнения второй катетерной аблации.

Рис. 5. Электрокардиография от 2024г на фоне атипичного ТП.
Таблица 1
Динамика принимаемой терапии и сократительной функции ЛЖ по данным эхокардиографии
|
Дата |
Терапия (мг в сутки) |
ФВ ЛЖ, % |
|
13.05.2013 |
Гепарин → НМГ Амиодарон (1200 в/в → 200 п/о) Бисопролол (2,5 → 7,5) Периндоприл (5) |
20 |
|
27.05.2013 |
25 |
|
|
07.06.2013 |
29 |
|
|
20.06.2013 |
28 |
|
|
Аблация 1 (от 26.06.2013) |
||
|
29.08.2013 |
Амиодарон (200 п/о) Бисопролол (7,5) Периндоприл (5) |
49 |
|
13.05.2014 |
53 |
|
|
Аблация 2 (от 27.10.2014) |
||
|
01.12.2016 |
Ривароксабан (20) Соталол (80-160) Периндоприл (5) |
59 |
|
19.10.2018 |
58 |
|
|
28.09.2020 |
59 |
|
|
На фоне пароксизма атипичного трепетания предсердий |
||
|
11.10.2024 |
Ривароксабан (20) Амиодарон (200) Метопролола сукцинат (25) Периндоприл (5) |
46 |
|
Аблация 3 (от 10.2025) |
||
|
10.2025 |
Ривароксабан (20) Соталол (80-160) Периндоприл (5) |
54 |
Сокращение: НМГ — низкомолекулярный гепарин, ФВ ЛЖ — фракция выброса левого желудочка.
Работа выполнена с использованием ресурсов Центра коллективного пользования «Центр доклинических и трансляционных исследований» на базе ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России.
Обсуждение
Данный клинический случай имеет несколько интересных аспектов. Впервые возникшая тахисистолическая ФП сочеталась с тяжелой СН, которая на момент первой госпитализации могла быть интерпретирована как по «первому», так и по «второму» варианту КАА (рис. 1). Впоследствии повышение ФВ ЛЖ и полная компенсация СН на фоне сохранения синусового ритма свидетельствуют о фенотипе КАА наиболее близком к «первому» варианту.
Другой особенностью клинического случая является наличие мультифокальных тромбоэмболий, причем как в легочном, так и системном круге кровообращения (ТЭЛА и ОНМК) на фоне лечебной дозы антикоагулянтной терапии при отсутствии критериев коагулопатии или тромбофилии (что, безусловно, не является абсолютным опровержением какого-либо редкого варианта, не имеющего диагностического теста на сегодняшний день). Теоретически допустимым может быть формирование внутрисердечных тромбов при тахисистолии, сопровождающейся турбулентным внутрисердечным кровотоком (особенно в предсердиях).
Первоначальный выбор тактики ведения в виде создания атриовентрикулярной блокады и имплантации трехкамерного дефибриллятора представляется приемлемым вариантом. Не исключено, что купирование тахисистолии после деструкции атриовентрикулярного соединения у пациентки с уже имеющимся кардиоресинхронизирующим устройством (при условии успешной имплантации левожелудочкового электрода) могло бы привести к подобному улучшению состояния и функции ЛЖ, что трактовалось бы как хороший ответ на кардиоресинхронизирующую терапию, однако изменение тактики на катетерную аблацию ФП также сопровождалось существенным улучшением состояния пациентки. Вопрос необходимости профилактики внезапной сердечной смерти в виде имплантации ИКД остается открытым, несмотря на документированный эпизод ФЖ в «горячую фазу» заболевания. Действительно, следующие 12 лет не наблюдалось желудочковых аритмий, не отмечалось срабатываний ИКД.
Еще следует обратить внимание на очень позднее возобновление нарушения ритма — через 10 лет после «успешной» аблации. Столь отсроченные рецидивы отражают прогрессирование изменений в миокарде предсердий. По данным литературы [6][7], катетерная аблация при поздних рецидивах аритмии имеет очень ограниченную эффективность, поскольку операторы сталкиваются с множественными механизмами новых аритмий на фоне уже имеющейся ИЛВ. Катетерная аблация не предотвращает прогрессирование заболевания, однако, как в случае данной пациентки, может на длительное время отсрочить рецидив клинических проявлений.
Ключевые аспекты ведения пациентов с КАА
Данный случай демонстрирует, что агрессивный дебют персистирующей тахисистолической ФП способен привести к выраженной кардиомиопатии и тяжелой СН. Сценарий КАА может развиваться как у пациента с исходно здоровым сердцем, так и при манифестации на фоне уже имеющейся кардиомиопатии, поэтому тактика ведения должна учитывать фенотип заболевания и индивидуальные риски пациента.
Эффективное купирование аритмии (кардиоверсия, катетерная аблация) способно значительно улучшить функцию ЛЖ и уменьшить симптомы СН, однако полный регресс кардиомиопатии не всегда возможен — вероятна персистенция фонового поражения миокарда.
Сложные и не всегда объяснимые эпизоды мультифокальных тромбоэмболий (ТЭЛА и ОНМК) на фоне адекватной антитромботической терапии требуют углубленного поиска редких причин гиперкоагуляции и пересмотра подходов к профилактике, особенно в условиях выраженной тахисистолии.
Имплантация ИКД оправдана при эпизодах угрожающих аритмий (фибрилляция желудочков), однако по прошествии долгого бессобытийного периода целесообразность устройства может быть пересмотрена.
Поздние рецидивы ФП и ТП после успешной аблации свидетельствуют о продолжающемся прогрессировании структурных изменений в миокарде предсердий, что ограничивает долгосрочную эффективность интервенционных методов и требует персонифицированного динамического наблюдения и возможной коррекции тактики.
Заключение
При ведении пациентов с КАА в дебюте ФП ранняя агрессивная ритм-контролирующая стратегия (катетерная аблация, кардиоверсия) крайне желательна, особенно при тяжелой СН, поскольку это может привести к улучшению функции ЛЖ. В каждом случае необходим индивидуализированный подход с учетом фенотипа КАА. Риск поздних рецидивов требует динамического наблюдения, возможно с периодической переоценкой тактики (повторные аблации, коррекция фармакотерапии, имплантация устройств).
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Немцов С.В., Гусев В.А., Самсонова И.В., Михайлова Е.В., Лебедев Д.С., Михайлов Е.Н. Кардиомиопатия, ассоциированная с аритмией: 12-летнее наблюдение пациентки после дебюта фибрилляции предсердий (клиническое наблюдение). Российский кардиологический журнал. 2025;30(4S):6667. https://doi.org/10.15829/1560-4071-2025-6667. EDN: RBQEZO
Скопировать