Стимуляционная кардиомиопатия: современные критерии диагностики и стратификация риска
Аннотация
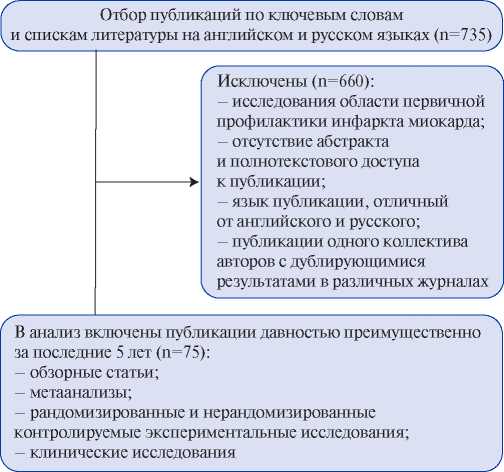
Стимуляционная кардиомиопатия (СКМП) представляет собой форму приобретённой дисфункции левого желудочка, развивающуюся у части пациентов с высокой долей правожелудочковой стимуляции. В основе патогенеза лежит диссинхронная активация миокарда, приводящая к нарушению координации сокращений, региональной перегрузке, фиброзогенезу и ремоделированию левого желудочка. Обзор посвящён современным представлениям о диагностике СКМП, факторах риска и подходах к стратификации пациентов. Описаны предимплантационные, интра- и постимплантационные предикторы СКМП. Отдельное внимание уделено новым неинвазивным методам визуализации и физиологическим стратегиям стимуляции, способным снизить риск развития СКМП. Подчёркивается важность мультифакторного подхода к диагностике, включая анализ клинико-инструментальных данных, динамики фракции выброса, биомаркеров и параметров кардиостимуляции. Обзор акцентирует необходимость раннего выявления СКМП и индивидуализации тактики имплантации и наблюдения, что может способствовать улучшению прогноза и снижению частоты осложнений, связанных с длительной правожелудочковой стимуляцией.
Стимуляционная кардиомиопатия (СКМП, англ. pacing-induced cardiomyopathy — PICMP) представляет собой форму приобретённой дисфункции левого желудочка (ЛЖ), возникающую у пациентов на фоне длительной стимуляции, преимущественно правого желудочка (ПЖ). Возникающая механическая диссинхрония нарушает нормальную последовательность активации и сокращения миокарда, приводя к региональной механической перегрузке и ремоделированию ЛЖ. Электрическая диссинхрония активирует фиброзогенез, способствует снижению перфузии миокарда и ухудшает внутрисердечную гемодинамику, создавая патофизиологические условия для снижения сократимости миокарда ЛЖ [1]. Несмотря на многолетнюю историю изучения, интерес к данной патологии остаётся не только актуальным, но и продолжает устойчиво расти. По мере старения населения и расширения показаний к имплантации устройств сердечной стимуляции доля пациентов, входящих в зону риска развития СКМП, неуклонно увеличивается.
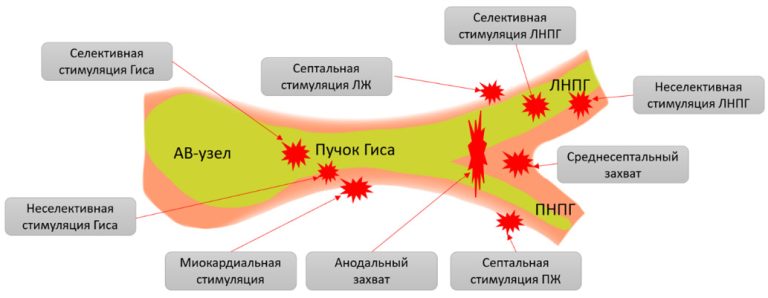
Современные исследования свидетельствуют о том, что СКМП развивается у 10-20% пациентов с высокой долей желудочковой стимуляции (>40-50%) в течение первых 2-3 лет после имплантации устройства. Снижение фракции выброса (ФВ) ЛЖ у этой категории больных ассоциируется с повышением риска госпитализации, развития клинически значимой сердечной недостаточности (СН) и увеличением общей смертности. Однако, несмотря на это, СКМП остаётся часто недооценённой патологией, особенно на ранних этапах, когда изменения в структуре и функции миокарда ещё обратимы. Потенциальная обратимость и выраженная зависимость от техники имплантации подчеркивают актуальность современной диагностики СКМП, особенно с учётом стремительного развития технологий физиологической стимуляции — таких как стимуляция пучка Гиса (His bundle pacing) и стимуляция области левой ножки пучка Гиса (left bundle brunch area pacing, LBBAP) [2]. Переход к этим методам позволяет существенно снизить частоту развития СКМП, демонстрируя потенциал для обратного ремоделирования ЛЖ и улучшения гемодинамических показателей даже у пациентов с уже развившейся дисфункцией [3].
Современные исследования также позволяют выделить группы пациентов с высоким риском развития СКМП ещё на этапе планирования имплантации антиаритмического устройства. К предикторам относят мужской пол, наличие в анамнезе инфаркта миокарда, хронической болезни почек (ХБП), фибрилляции предсердий (ФП), исходно сниженные значения ФВ ЛЖ, удлиненную продолжительность нативного и стимулированного QRS, а также высокий процент желудочковой стимуляции [4]. В то же время диагностика СКМП требует активного и регулярного наблюдения за функциональными изменениями ЛЖ, что актуализирует необходимость внедрения чувствительных неинвазивных методов визуализации и электрофизиологической оценки, таких как speckle-tracking-эхокардиография, трёхмерная эхокардиография, ультравысокочастотная электрокардиография и магнитно-резонансная томография с отслеживанием фиброзных изменений. Эти технологии позволяют выявлять субклинические формы СКМП на ранних этапах и своевременно корректировать терапевтическую стратегию, однако остаются малодоступными в рутинной практике [5].
Следует отметить, что СКМП представляет собой ценную модель изучения феномена диссинхронного ремоделирования миокарда, возникающего также при таких состояниях, как блокада левой ножки пучка Гиса, дилатационная кардиомиопатия и ишемическое повреждение миокарда. Таким образом, изучение механизмов развития СКМП способствует более глубокому пониманию универсальных закономерностей патологического и обратимого ремоделирования сердца, что делает данную патологию особенно значимой с точки зрения фундаментальной и прикладной кардиологии.
Кроме клинической и научно-экспериментальной значимости, изучение СКМП несёт в себе важность для организации здравоохранения и управления ресурсами, поскольку осложнения, связанные с поздней диагностикой, существенно увеличивают расходы на лечение, частоту госпитализаций и потребность в реимплантации или апгрейде устройств. Снижение доли стимуляционно-индуцированной СН за счёт раннего вмешательства и оптимального программирования антиаритмических устройств способно не только улучшить исходы, но и повысить эффективность кардиологической помощи.
Роль диссинхронной активации миокарда считается ведущим звеном в патогенезе СКМП. Однако остаётся неясным, почему при одинаковых параметрах стимуляции значимое снижение ФВ ЛЖ развивается лишь у части пациентов. Несмотря на накопленный значительный объём клинических данных, в настоящее время не существует надёжных инструментов, позволяющих с высокой точностью прогнозировать развитие СКМП или стратифицировать риск её возникновения у конкретного пациента.
Таким образом, углублённое изучение СКМП имеет важное значение для совершенствования подходов к отбору пациентов для различных видов стимуляции, разработки алгоритмов ранней диагностики и своевременной коррекции этого осложнения. Решение этих задач позволит не только улучшить непосредственные результаты лечения, но и существенно повлиять на отдалённый прогноз у пациентов, нуждающихся в постоянной электростимуляции сердца.
Целью обзора является анализ современных диагностических критериев СКМП и оценка существующих подходов к стратификации риска её развития с фокусом на выявление наиболее надёжных предикторов и факторов, потенциально поддающихся клинической модификации.
Определение СКМП
Формирование представлений о СКМП прошло сложный путь — от фрагментарных наблюдений клиницистов до признания этого состояния как самостоятельной клинической и патофизиологической единицы. На начальных этапах развития кардиостимуляции снижение сократительной функции сердца у пациентов с длительной желудочковой стимуляцией трактовалось как прогрессирование основного заболевания или возрастные изменения миокарда. Однако после ряда экспериментальных и клинических исследований стало очевидным, что хроническая стимуляция, особенно из апикальной области ПЖ, может сама по себе индуцировать ремоделирование миокарда, ведущее к дисфункции ЛЖ.
Одним из первых экспериментальных трудов, заложивших физиологические основы понимания дисфункции миокарда, индуцированной искусственной стимуляцией, стала работа Gilmore JP, et al., опубликованная в журнале Circulation Research в 1963г. Были исследованы гемодинамические различия между предсердной и желудочковой стимуляцией у собак, подвергнутых инвазивному мониторингу, авторы показали, что при одинаковой частоте стимуляции желудочковая активация вызывает менее эффективный сердечный выброс по сравнению с предсердной. Ключевое наблюдение заключалось в том, что желудочковая стимуляция нарушает физиологическую синхронность электрической активации и сокращения миокарда, это приводит к уменьшению ударного объёма и изменению перфузии миокарда [6].
Похожие результаты были получены и в исследованиях на пациентах спустя несколько десятков лет Tse HF и Lau CP, доказавшими, что апикальная стимуляция ПЖ, несмотря на сохранение атриовентрикулярной синхронизации и частотной адаптации, приводит к локальным нарушениям перфузии миокарда в зоне стимуляции, выявляемым при использовании сцинтиграфии с Tl-201. Было продемонстрировано, что эти изменения ассоциированы с нарушением региональной сократимости и, в последующем, снижением глобальной контрактильной функции ЛЖ [7].
Таким образом, ещё в 1960-х годах была экспериментально продемонстрирована гемодинамическая неполноценность желудочковой стимуляции, что, несмотря на отсутствие тогда самого термина «стимуляционная кардиомиопатия», фактически предвосхищало фундаментальные элементы её патогенеза — диссинхронию, нарушение наполнения ЛЖ и снижение его насосной функции. Эти концепции впоследствии легли в основу представлений о СКМП и послужили толчком к разработке альтернативных, более физиологических методов стимуляции.
Начиная с 1990-х годов термин СКМП постепенно вошёл в научный обиход, однако на начальном этапе он использовался преимущественно описательно, без унифицированных диагностических критериев. В течение последующих двух десятилетий в литературе были предложены различные определения СКМП, варьирующиеся по степени допустимого снижения ФВ ЛЖ, доле желудочковой стимуляции и срокам наблюдения [4]. Лишь после 2010г началось формирование консенсусных подходов, получивших к настоящему времени широкую поддержку в ряде крупных клинических исследований и международных рекомендациях [8].
Несмотря на отсутствие единых универсально признанных диагностических критериев СКМП, большинство современных исследований сходятся в использовании следующих клинико-инструментальных признаков, позволяющих идентифицировать данное состояние: снижение ФВ ЛЖ на ≥10% по сравнению с исходными значениями при исходно нормальной сократительной функции (ФВ ЛЖ >50%) до начала стимуляции ПЖ; доля желудочковой стимуляции не менее 20%; а также отсутствие других объяснимых причин снижения насосной функции миокарда после начала стимуляции [8].
Тем не менее представленные критерии в их стандартной интерпретации могут быть слабо применимы у пациентов с исходно сниженной ФВ ЛЖ. В этой когорте даже минимальное нарушение координации сокращений, вызванное диссинхронной активацией желудочков вследствие стимуляции ПЖ, может нарушить компенсаторный баланс между остаточной сократительной способностью миокарда и системной гемодинамической нагрузкой. Такая повышенная уязвимость объясняется выраженным миокардиальным фиброзом, сниженным коронарным резервом, ограниченными энергетическими возможностями кардиомиоцитов и высокой чувствительностью миокарда к дополнительному электрическому и механическому стрессу [9].
В данной клинической ситуации определяющее значение приобретает не столько абсолютное значение ФВ ЛЖ, сколько динамика изменения этого показателя во времени под воздействием желудочковой стимуляции. Даже умеренное, но стойкое снижение ФВ у пациента с исходной систолической дисфункцией может приводить к клинически значимому ухудшению состояния, усугублению симптомов СН, прогрессированию патологического ремоделирования ЛЖ и повышению риска декомпенсации и госпитализации. Следовательно, в условиях исходно сниженной сократительной функции миокарда диагностика СКМП должна опираться не только на количественные параметры ФВ, но и на комплексную оценку клинической картины [10], результатов кардиовизуализационных методик, отражающих структурные и функциональные изменения, а также динамики биомаркеров СН [11]. Такой мультифакторный подход позволяет повысить чувствительность диагностики и своевременно определить потребность в модификации стратегии стимуляции.
Одним из нерешённых вопросов, сопровождающих диагностику СКМП, остаётся оптимальная продолжительность наблюдения после имплантации устройств, достаточная для достоверной верификации патологии. Несмотря на наличие общих диагностических критериев временные рамки для постановки диагноза в разных исследованиях существенно варьируют, что отражает как гетерогенность популяций, так и неоднородность методик контроля.
Так, группа исследователей из Японии предложили ориентироваться на интервал 12-24 мес., указав, что большинство случаев СКМП возникает в течение первых 2 лет после начала стимуляции при высокой доле стимуляции ПЖ (>40%) [12]. В свою очередь, согласно данным Abdin А, et al., среднее время до манифестации СКМП составило ~40 мес., что подчёркивает важность пролонгированного эхокардиографического мониторинга у пациентов с постоянной желудочковой стимуляцией и исходно сохранённой ФВ ЛЖ [13]. Kiehl EL, et al. в одном из наиболее цитируемых проспективных исследований предложили ориентироваться на интервал 4 года [14]. Tayal В, et al. указывают, что одно из частых клинических проявлений СКМП — ФП может возникать уже через 3 мес. после имплантации [15].
Однако удлинение сроков наблюдения может сопровождаться ростом диагностической неопределённости. По мере увеличения временного интервала с момента имплантации, повышается вероятность того, что ухудшение функции миокарда может быть обусловлено другими факторами, не связанными непосредственно с желудочковой стимуляцией. В таких условиях верификация СКМП становится затруднительной, особенно при отсутствии данных о динамике структурно-функциональных параметров сердца в более ранние сроки.
Таким образом, продолжительность наблюдения, необходимая для верификации СКМП, остаётся дискуссионной, а избыточно длительный срок может привести к смещению (bias) за счёт включения случаев, обусловленных альтернативными причинами. Это подчёркивает необходимость регулярного и стандартизированного функционального мониторинга сердечной деятельности в первые 1-2 года после имплантации устройства, особенно у пациентов с высоким прогностическим потенциалом развития СКМП.
Предикторы СКМП
Предимплантационные факторы. Мужской пол рассматривается как независимый предиктор развития СКМП, что подтверждено данными некоторых наблюдательных исследований и когортных анализов. В метаанализе Abbas J, et al. отмечается, что мужчины чаще демонстрируют снижение ФВ ЛЖ при длительной правожелудочковой стимуляции по сравнению с женщинами при прочих равных условиях [16]. Потенциальными объяснениями этой закономерности являются большая масса миокарда у мужчин, более высокая предрасположенность к фиброзу, а также различия в молекулярной и клеточной реакции миокарда на диссинхронную активацию. Кроме того, известно, что мужчины в целом менее чувствительны к протективному эффекту эстрогенов, которые, согласно экспериментальным данным, могут ограничивать развитие воспаления и ремоделирования в ответ на механическую перегрузку и электрическую диссинхронию. Тем не менее механизм этого феномена до конца не изучен, и большинство данных получено ретроспективно, без стратификации по гормональному статусу, массе миокарда или типу сердечной патологии. Это ограничивает точность прогноза на индивидуальном уровне, но в совокупности с другими предикторами пол пациента может учитываться при оценке риска развития СКМП.
В ряде исследований было показано, что у пациентов с исходно сниженной ФВ ЛЖ высокое бремя правожелудочковой стимуляции не только усугубляет дисфункцию ЛЖ, но и увеличивает риск неблагоприятных исходов, включая возникновение желудочковых аритмий, нанесение обоснованной электротерапии имплантированного кардиовертера-дефибриллятора и смерть [17][18]. Вероятно, большую предрасположенность к развитию СКМП также могут иметь пациенты с сохраненной ФВ ЛЖ, но имеющие диастолическую дисфункцию ЛЖ до имплантации [19].
Многие клинические предикторы СКМП — такие как мужской пол, ФП, инфаркт миокарда и ХБП — по сути оказывают влияние на общий сердечно-сосудистый риск и склонность к систолической дисфункции, а не специфический эффект стимуляции. Эти факторы являются промежуточными: они повышают уязвимость миокарда к десинхронизирующему действию стимуляции, но не указывают напрямую на риск СКМП. По этой причине для точной стратификации риска необходимы многофакторные модели, которые включают как эти фоновые факторы, так и более специфические параметры, доступные для анализа во время имплантации либо в послеоперационном периоде.
Интраоперационные факторы. Продолжительность стимуляционного комплекса QRS (paced QRS duration, pQRSd) является признанным независимым предиктором развития СКМП. Важность этого показателя подтверждается предложениями ряда исследователей внедрить его регулярный мониторинг с помощью имплантируемых устройств и отображение в интерфейсе программаторов для отслеживания изменений во времени и своевременного выявления пациентов с повышенным риском СКМП [20]. Однако, несмотря на высокую прогностическую значимость показателя, остаётся неопределённой оптимальная точка отсечения, ассоциированная с высоким риском развития кардиомиопатии. В различных исследованиях фигурируют пороговые значения от 150 до 180 мс. Отсутствие консенсуса затрудняет широкое клиническое применение pQRSd как изолированного критерия и подчёркивает необходимость его использования в составе интегрированных прогностических моделей, учитывающих другие клинико-функциональные параметры.
Доказано, что альтернативные зоны стимуляции в ПЖ, такие как выводной тракт и верхняя часть межжелудочковой перегородки, могут формировать более узкий комплекс QRS за счёт близости к проводящей системе. Однако позиционирование электродов в этих анатомических областях сопряжено с техническими трудностями, а уровень успешной имплантации может быть невысок. В исследовании Protect-Pace высокая септальная стимуляция не показала преимуществ по сохранению систолической функции ЛЖ по сравнению с традиционной апикальной стимуляцией в течение первых 2 лет [21]. Различие между группами по степени снижения ФВ ЛЖ было незначимым (p=0,43). Также не наблюдалось различий по вторичным исходам: госпитализациям по поводу СН, смертности, частоте ФП и уровням натрийуретического пептида. Установка электрода в высокую септальную позицию требовала существенно большего времени (70±25 мин vs 56±24 мин, p<0,0001) и флюороскопии (11±7 мин vs 5±4 мин, p<0,0001).
Высказывается мнение, согласно которому применение апикальной стимуляции ассоциировано с ухудшением функции ЛЖ по сравнению с альтернативными неверхушечными позициями электрода в случае исходно сниженной ФВ ЛЖ (<40%) [22].
Гипотеза о наличии преимуществ септальной стимуляции получила новое рождение по мере развития технологий LBBAP. В ретроспективное когортное исследование Hayashi K, et al. были включены 173 пациента (изначально скринировано 565 больных) с атриовентрикулярной блокадой и сохранённой ФВ ЛЖ (≥50%), которым в клинике Кливленда в 2018-2022гг была предпринята попытка LBBAP. СКМП развилась у 13 из 173 пациентов (7,5%) в медиане 26 нед. после имплантации [23]. В группе с успешно достигнутой LBBAP (n=118) частота СКМП составила 4,2%, тогда как в группе без LBBAP (n=55) — 14,6% (p=0,048). Авторами было установлено, что длительность интервала V6RWPT (время от стимула до пика R в отведении V6) ≥80 мс достоверно ассоциирована с повышенным риском СКМП: при V6RWPT <80 мс СКМП возникала у 1,3%; при V6RWPT 80-89 мс — у 10,4%; при V6RWPT ≥90 мс — у 14,6% (p=0,02). Проведенное исследование продемонстрировало, что достижение захвата зоны левой ножки проводящей системы снижает риск СКМП у пациентов с высокой зависимостью от желудочковой стимуляции и сохранённой ФВ ЛЖ. Несмотря на то, что даже в группе с LBBAP риск СКМП не был равен нулю, резидуальный риск был значительно ниже, особенно при достижении V6RWPT <80 мс. В отличие от процента желудочковой стимуляции, который у большинства пациентов был >80%, именно способ стимуляции и степень анатомо-функционального захвата проводящей системы стали критичными факторами.
Постимплантационные факторы. Полученные Kim SS, et al. данные подтверждают, что снижение глобального продольного стрейна (global longitudinal strain, GLS) выступает в роли раннего маркера субклинической дисфункции ЛЖ. Авторы доказали, что постимплантационное значение GLS <-15 было независимым предиктором развития СКМП (отношение шансов =1,715; 95% доверительный интервал: 1,174-2,504; p=0,005) с чувствительностью 100% и специфичностью 80,9% (AUC=0,92) [24].
Считается, что бремя стимуляции желудочков >20% ассоциируется с прогрессирующим снижением сократительной функции ЛЖ [20]. Более высокая нагрузка (>40%) сопряжена с увеличенным риском, хотя СКМП может развиться и при меньших значениях у уязвимых пациентов [25].
Несмотря на то, что высокая доля желудочковой стимуляции традиционно рассматривается как один из ключевых факторов риска развития СКМП, в клинической практике точная оценка этого показателя часто сопряжена с существенными ограничениями. Современные устройства для электрокардиостимуляции, как правило, предоставляют информацию о проценте стимуляции желудочков на основании подсчёта числа искусственно инициированных желудочковых комплексов, однако такой подход не всегда отражает реальное воздействие стимуляции на гемодинамику. В частности, наличие сливных и псевдо-сливных комплексов, при которых артифициальный стимул сочетается со спонтанной деполяризацией миокарда, затрудняет интерпретацию данных, т.к. устройство может как переоценивать, так и недооценивать степень участия электрокардиостимуляции в активации желудочков.
Дополнительным препятствием для корректной оценки доли желудочковой стимуляции в контексте риска развития СКМП является отсутствие стандартизированного подхода к выбору временного окна анализа. В рутинной практике интерпретация данных о нагрузке на стимуляцию часто опирается на показатели, автоматически собираемые устройством за неопределённый или плавающий интервал времени — например, со времени последнего программирования или контрольного визита. Если счётчики не были вручную обнулены при имплантации или в начале наблюдения, указанный процент может отражать усреднённую величину за недели или месяцы с переменными режимами стимуляции и клиническими условиями. Такая неопределённость делает невозможным точную корреляцию между уровнем желудочковой стимуляции, меняющимися программами стимуляции и изменениями в функции ЛЖ в краткосрочной перспективе.
Вероятно, с клинической точки зрения важно не только общее количество стимулированных желудочковых сокращений, но и характер их распределения во времени. В этом контексте всё большую значимость приобретает гипотеза о существовании критически чувствительных периодов, в частности — в ночные часы, когда физиологически снижается симпатическая активность и преобладает вагусное влияние на проводящую систему. В этих условиях интермиттирующие эпизоды атриовентрикулярной блокады могут сопровождаться периодами длительной желудочковой стимуляции с потенциально неблагоприятной гемодинамической конфигурацией, особенно при апикальной локализации электрода. Хотя прямые клинические доказательства роли циркадных вариаций в патогенезе СКМП пока ограничены, экспериментальные данные на животных моделях могут указывать на повышенную чувствительность миокарда к искусственной диссинхронной активации в разные циркадные периоды [26].
Данные о предикторах СКМП отличаются выраженной гетерогенностью из-за различий в дизайне исследований (часто ретроспективных), составе когорт (смешение типов устройств, степеней зависимости от стимуляции, исходного статуса ЛЖ) и отсутствии согласованных диагностических критериев. Ассоциация между процентом желудочковой стимуляции и снижением ФВ ЛЖ нелинейна: часть пациентов переносит высокое бремя стимуляции без ремоделирования, тогда как у других дисфункция развивается и при доле <20%. Это подчёркивает необходимость перехода от выделения изолированных «факторов риска» к построению интегральных прогностических моделей, объединяющих параметры стимуляции (pQRSd, V6RWPT), эхокардиографические показатели (ФВ, GLS) и клинико-демографические характеристики (ишемическая болезнь сердца, ФП, ХБП, пол, возраст). Будущие исследования должны иметь проспективный дизайн, использовать унифицированные критерии СКМП и стандартизированные методы визуализации для формирования объективной шкалы риска.
Стратификация риска СКМП
Стратификация риска СКМП необходима для индивидуализации подходов к выбору типа стимуляции, раннего выявления пациентов, у которых с высокой вероятностью разовьется кардиомиопатия, и своевременного принятия решений о целесообразности смены типа стимуляционной системы. Очевидно, что оценка риска СКМП позволяет планировать более частый эхокардиографический мониторинг и при необходимости инициировать превентивную терапию во избежание ремоделирования и ухудшения прогноза.
Возможность модификации риска СКМП с помощью медикаментозной терапии, направленной на нейрогуморальную регуляцию, все чаще становится предметом научного интереса. В ретроспективном исследовании Agha MS, et al. оценивалось влияние ингибиторов ангиотензинпревращающего фермента (иАПФ), блокаторов рецепторов ангиотензина II (БРА) и β-блокаторов (ББ) на частоту развития СКМП у пациентов с полной АВ-блокадой, нормальной исходной ФВ ЛЖ и высоким уровнем желудочковой стимуляции [27]. В исследование были включены 642 пациента, наблюдаемых на протяжении до 10 лет после имплантации обычного одно- или двухкамерного электрокардиостимулятора с правожелудочковым электродом. СКМП развилась у 6,2% пациентов, медианный срок до манифестации составил 4,7 года. Частота СКМП была ниже в группе пациентов, получавших любую из указанных групп препаратов (4,7% vs 7,0%). При этом наиболее выраженное снижение риска было зарегистрировано в группе комбинированной терапии иАПФ/БРА и ББ. Монотерапия иАПФ/БРА или ББ демонстрировала тенденцию к снижению риска, но не достигала статистической значимости. На основании этих результатов авторы предположили, что благоприятное влияние данных препаратов связано с их способностью подавлять хроническую активацию ренин-ангиотензин-альдостероновой и симпатической систем, которые могут патогенетически способствовать развитию СКМП при длительной диссинхронной стимуляции. Таким образом, наличие или отсутствие нейрогуморальной терапии может рассматриваться не только как фактор, ассоциированный с риском СКМП, но и как потенциально модифицируемый предиктор этого состояния, что подчеркивает важность информации о фармакологическом анамнезе пациента при проведении стратификации риска СКМП.
Проблема стратификации риска СКМП представляет собой исключительно сложную задачу, не поддающуюся решению с помощью одного единственного предиктора. Это связано с тем, что патофизиология СКМП многофакторна и гетерогенна, а большинство факторов риска могут быть модифицированы. В связи с этим наиболее перспективным решением проблемы является разработка многофакторных моделей, способных интегрировать структурные, электрофизиологические, функциональные и клинико-демографические параметры в единую систему оценки риска.
Примером реализации такого подхода может быть представленная в 2025г модель BREECH Score, в которую вошли факторы: ишемическая болезнь сердца, наличие СН с сохраненной ФВ ЛЖ, исходная величина ФВ ЛЖ, продолжительность стимулированного комплекса QRS, процент желудочковой стимуляции и частота сердечных сокращений после имплантации (AUC составила 0,74) [28].
Малое число прогностических моделей объясняется рядом объективных препятствий: необходимостью в длительном наблюдении больших когорт, гетерогенностью техник имплантации, а также отсутствием универсального определения СКМП. Всё это замедляет формирование валидированных инструментов стратификации, что подчеркивает актуальность и востребованность исследований в этом направлении и требует от практикующих врачей наличие знаний о СКМП.
Заключение
Актуальность изучения СКМП определяется её высокой распространённостью, потенциальной обратимостью, значительным влиянием на прогноз пациентов и возможностях профилактики за счёт индивидуализации подхода к стимуляции. На фоне растущего числа пациентов с имплантированными антиаритмическими устройствами, своевременное выявление и коррекция стимуляционно-индуцированных нарушений становятся критически важной задачей для врачей терапевтов, кардиологов и организаторов здравоохранения.
Обобщение данных литературы позволяет заключить, что СКМП следует рассматривать не как неизбежное следствие хронической правожелудочковой стимуляции, а как предотвратимое и прогнозируемое осложнение, риск которого может быть существенно снижен при целенаправленном управлении клиническими, электрофизиологическими и морфофункциональными факторами. Ключевым направлением является интеграция данных различных уровней — от параметров стимуляции и эхокардиографических показателей до клинико-демографических характеристик и динамики их изменений во времени. Такой подход смещает фокус с констатации факта дисфункции к её раннему прогнозированию и профилактике.
Важнейшим практическим выводом является необходимость стандартизированного функционального мониторинга в первый год после имплантации устройства с обязательной оценкой GLS, ФВ и параметров стимуляции. Выявление ранних признаков ремоделирования должно служить основанием для коррекции программирования или перехода к физиологическим стратегиям стимуляции. При прогнозируемо высокой зависимости от стимуляции применение иАПФ/БРА и ББ может рассматриваться как элемент нейрогуморальной профилактики ремоделирования.
Современные данные показывают, что переход от описательного анализа отдельных предикторов к построению интегральных прогностических моделей, основанных на комплексной оценке морфологических, функциональных и электрических признаков, открывает путь к персонифицированному ведению пациентов. Такая стратегия позволяет не только уменьшить частоту СКМП, но и повысить эффективность использования ресурсов здравоохранения.
В целом полученные обобщения позволяют рассматривать СКМП как модель управляемого ремоделирования миокарда, в которой ряд звеньев патогенеза потенциально обратим. Системный, многоуровневый подход к оценке риска и ранняя реализация профилактических мер формируют новую парадигму ведения пациентов с постоянной стимуляцией сердца и создают основу для снижения доли стимуляционно-обусловленной СН в клинической практике.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Илов Н.Н., Каримов И.Р. Стимуляционная кардиомиопатия: современные критерии диагностики и стратификация риска (обзор литературы). Российский кардиологический журнал. 2025;30(3S):6485. https://doi.org/10.15829/1560-4071-2025-6485. EDN: UJFXCA
Скопировать