Пейсмейкер-индуцированная кардиомиопатия
Аннотация
Расположение электрода в верхушке правого желудочка является стандартным местом для проведения электрокардиостимуляции. Электрическая и механическая диссинхрония, приводящая к аномальному сокращению желудочков, ведет к ремоделированию миокарда левого желудочка, что, в свою очередь, вызывает появление симптомов сердечной недостаточности, повышение случаев госпитализаций при декомпенсации сердечной недостаточности, появление предсердных аритмий и повышение смертности от сердечно-сосудистых причин. Пейсмейкер-индуцированная кардиомиопатия (ПИКМП) является осложнением длительной правожелудочковой стимуляции. Нет точного определения ПИКМП, но обычно она подразумевает под собой снижение фракции выброса левого желудочка <50%, либо снижение её на ≥10% от исходной. Основным вариантом лечения ПИКМП является переход на ресинхронизирующую терапию. Однако последние данные указывают на то, что стимуляция проводящей системы сердца может являться не только лечением, но и профилактикой развития ПИКМП. Цель обзора — провести всесторонний анализ и систематизировать имеющиеся данные о ПИКМП, определить наиболее значимые предикторы её раннего выявления и, опираясь на полученные результаты, сформировать научно обоснованные подходы к совершенствованию стратегий профилактики и лечения данного состояния.
Имплантация электрокардиостимулятора (ЭКС) является основным методом лечения брадиаритмий, таких как атриовентрикулярная (АВ) блокада (АВБ) и синоатриальная блокада. Частота имплантации постоянных ЭКС увеличивается с возрастом, и по некоторым оценкам 70-80% всех ЭКС имплантируются пациентам в возрасте 65 лет и старше. Ежегодно в мире имплантируется >1 млн. ЭКС, при чем треть из них приходится на пациентов с АВБ [1]. В России в 2022г было имплантировано 53486 ЭКС, причем из них 48,2% по поводу АВБ [2].
С момента первой операции по имплантации постоянного ЭКС в 1958г верхушка правого желудочка (ПЖ) стала предпочтительным местом для имплантации электродов, что объясняется значительной простотой имплантации, надежностью и стабильностью фиксации электродов [3-5].
Однако было замечено, что хроническая многолетняя стимуляция ПЖ приводит к желудочковой диссинхронии, снижению функции левого желудочка (ЛЖ) и приводит к сердечной недостаточности (СН). Такое явление известно как пейсмейкер-индуцированная кардиомиопатия (ПИКМП) [6][7]. ПИКМП ассоциируется с повышенным риском развития фибрилляции предсердий (ФП), госпитализациями по поводу СН и сердечной смертностью [8]. Было показано, что у пациентов с ПИКМП переход с моновентрикулярной стимуляции на бивентрикулярную стимуляцию (БиВ-СРТ) облегчал симптомы, связанные с СН, и способствовал обратному ремоделированию миокарда ЛЖ. В последнее время набирающая популярность постоянная стимуляция проводящей системы, такая как электрокардиостимуляция пучка Гиса (СПГ) и электрокардиостимуляция области левой ножки пучка Гиса (СОЛНПГ), продемонстрировала существенное улучшение показателей фракции выброса (ФВ) ЛЖ и СН у пациентов с ПИКМП [9].
Определение и распространенность
В настоящее время нет четкого определения ПИКМП. В большинстве исследований оно характеризуется снижением ФВ ЛЖ на фоне правожелудочковой электрокардиостимуляции. Ключевым для ПИКМП является снижение ФВ ЛЖ <40% или 50%, либо на 5-10% от исходных показателей после имплантации ЭКС с правожелудочковой стимуляцией (ПЖС) [10].
Используя эти критерии, исследования показывают, что примерно у 10-20% пациентов с нормальной ФВ ЛЖ на исходном этапе развивается ПИКМП на фоне ПЖС, которая обычно проявляется в течение 3-4 лет [11].
Большинством исследователей критериями ПИКМП
признаются:
- Снижение ФВ ЛЖ как минимум на 10%, при исходной ФВ ЛЖ >50% до начала электрокардиостимуляции ПЖ.
- Процент желудочковой стимуляции должен составлять >20%.
- Отсутствие других явных причин для снижения ФВ ЛЖ.
В то же время в некоторых исследованиях определение ПИКМП включало симптомы СН, эпизоды ФП и госпитализацию по поводу декомпенсации СН [12].
Поскольку нет четкого определения данной патологии, то и встречаемость, и регистрация заболеваемости во многих исследованиях сильно различаются.
Так, в исследовании Kaye G, et al., включавшем 118 пациентов, сравнили 3 различных определения ПИКМП: 1) ФВ ЛЖ ≤40%, если исходная ФВ ЛЖ составляла ≥50%, или абсолютное снижение ФВ ЛЖ ≥5%, если исходная ФВ ЛЖ была <50%; 2) ФВ ЛЖ ≤40%, если исходная ФВ ЛЖ была ≥50%, или абсолютное снижение ФВ ЛЖ ≥10%, если исходная ФВ ЛЖ была <50%; 3) абсолютное снижение ФВ ЛЖ ≥10%, независимо от исходного уровня. За период наблюдения в 3,4±1,4 года распространенность ПИКМП составила 9,3%, 5,9% и 39,0%, соответственно. Используя определение 3, при самой высокой зарегистрированной частоте у 31 из 46 пациентов, которые соответствовали критериям ПИКМП, ФВ ЛЖ при последующем наблюдении все еще составляла >50%, несмотря на снижение на ≥10% по сравнению с исходным уровнем [13].
Хотя оценка сократительной способности миокарда по-прежнему имеет решающее значение, именно появление симптомов СН играет важную роль в выявлении ПИКМП. У некоторых пациентов могут развиться симптомы, связанные с желудочковой диссинхронии прежде, чем станет очевидным заметное снижение ФВ ЛЖ.
Помимо снижения ФВ ЛЖ и увеличения частоты госпитализаций пациентов по поводу СН, предполагаем, что появление ФП у некоторых пациентов также может служить признаком ПИКМП. Nielsen JC, et al. в своем исследовании, включавшем 177 человек с синдромом слабости синусового узла, продемонстрировали, что изолированная предсердная стимуляция ассоциировалась с меньшей частотой возникновения ФП, по сравнению с двухкамерной стимуляцией с короткой АВ задержкой (7,4% vs 23,3%, p=0,03) [14].
Аналогичным образом, в исследовании MOST (Mode Selection Trial) частота возникновения ФП продемонстрировала относительно линейное увеличение при высоком проценте желудочковой стимуляции [15].
Однако важно понимать, что не всегда возникновение ФП обусловлено ПИКМП.
Хотя ПИКМП в первую очередь рассматривается как кардиомиопатия, возникающая в условиях высокого процента ПЖС, без других каких-либо причин, она же может и усугубить уже существующую дисфункцию ЛЖ и даже нанести еще больший вред, ухудшая уже сниженную ФВ [16]. В исследовании MADIT (Multicenter Automatic Defibrillator Implantation Trial) процент стимуляции ПЖ >50% был связан с почти удвоением риска появления новых или ухудшением уже существующих симптомов СН [17].
Все это говорит о том, что ПИКМП нельзя рассматривать как изолированное снижение ФВ ЛЖ, необходим более широкий взгляд, который будет включать и симптомы СН, и количество госпитализаций по поводу декомпенсации СН, и случаи возникновения ФП на фоне высокого процента ПЖС.
Патофизиология
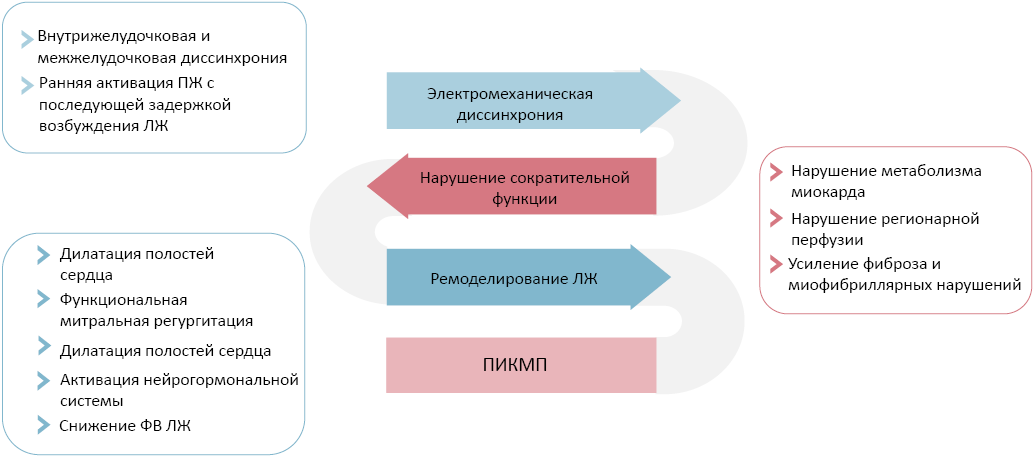
В настоящее время не изучены специфические патофизиологические механизмы, приводящие к развитию ПИКМП, но существует теория о том, что желудочковая диссинхрония является ключевым звеном в ее развитии. Считается, что межжелудочковая и внутрижелудочковая диссинхрония, является следствием ранней электрической активации ПЖ, с последующей задержкой сокращения ЛЖ, поскольку импульс передается не по системе Гиса-Пуркинье, а по кардиомиоцитам [18, 19]. Нарушение электрической активации приводит к нарушению механического сокращения. Области, наиболее близкие к месту проведения электрокардиостимуляции, подвергаются быстрому систолическому сокращению, что приводит к предварительному растяжению областей, активирующихся чуть позже. Этот процесс приводит к перераспределению нагрузки на миокард, что в конечном итоге приводит к снижению эффективности общего сокращения [20]. Как результат — происходит нарушение метаболизма миокарда и регионарной перфузии, усиление фиброза и миофибриллярных нарушений, появление функциональной митральной регургитации, снижение сердечного выброса [21].
ПИКМП тесно связана с изменениями в ренин-ангиотензиновой системе (РАС), провоспалительных факторах, протеолитических ферментах и клеточной структуре. РАС — это нейрогормональный компонент, который играет жизненно важную роль в сердечно-сосудистых патологических процессах и может быть обнаружен в кровотоке и тканях [22]. Растяжение сердечной стенки усиливает активацию РАС, усиливает воспалительную реакцию и повышает протеолитические ферменты. Эти три процесса приводят к изменениям в механотрансдукции и механочувствительности, что приводит к ремоделированию и дисфункции ЛЖ [23]. Исследования показали, что в процессе ремоделирования миокарда отмечается снижение уровня микроРНК-155, повышение уровня интерлейкина-6, растворимого фактора некроза опухоли 2, матриксной металлопротеиназы-9, N-кадгерина, Zonula Occludens протеина 1 [24] (рис. 1). Повышенная экспрессия фактора некроза опухоли-α у пациентов с СН считается одной из потенциальных причин дисфункции ЛЖ. Это объясняется активацией проапоптотического эффекта, способствующего гибели кардиомиоцитов [25].
Принято считать, что ремоделирование миокарда при электрокардиостимуляции является длительным хроническим процессом, на который могут уйти месяцы или годы, но изменения в сократительной способности ЛЖ можно обнаружить в течение нескольких часов после начала кардиостимуляции [26]. Так, Fornwalt BK, et al. оценили влияние ПЖС на систолическую диссинхронию, используя тканевую допплеровскую визуализацию у 14 пациентов с нормальной структурой и насосной функцией сердца. После 1-мин стимуляции верхушки ЛЖ была отмечена значительная систолическая диссинхрония ЛЖ по сравнению с синусовым ритмом [27].
С уменьшением степени диссинхронии может и уменьшиться степень выраженности ПИКМП. Снижение процента желудочковой стимуляции, использование альтернативных зон для постоянной стимуляции, таких как СПГ и СОЛНПГ, применение БиВ-СРТ — все это направлено на уменьшение межжелудочковой и внутрижелудочковой диссинхронии [28].

Рис. 1. Патофизиология развития ПИКМП.
Сокращения: ЛЖ — левый желудочек, ПЖ — правый желудочек, ПИКМП — пейсмейкер-индуцированная кардиомиопатия, ФВ — фракция выброса.
Факторы риска
Такие факторы риска, как пожилой возраст, мужской пол, наличие ФП в анамнезе, высокий процент желудочковой стимуляции, сниженная ФВ ЛЖ, широкий комплекс QRS, диастолическая дисфункция и аномальная глобальная продольная деформация, являются независимыми предикторами развития ПИКМП [29].
ПЖС вызывает электрическую активацию ЛЖ, напоминающую блокаду левой ножки пучка Гиса, что приводит к электрической диссинхронии и увеличению продолжительности QRS, за счет замедления проводимости в миокарде. Некоторые исследователи предполагают, что увеличение продолжительности QRS >150 мс является предиктором в развитии ПИКМП [30]. Исследования показали, что диастолическая дисфункция также является фактором риска развития ПИКМП у пациентов с сохранной функцией ЛЖ [31]. Диастолическая функция представляет собой не менее важный аспект сердечного цикла, тесно связанный с систолической функцией. Нарушение диастолического расслабления, наполнения или растяжимости ЛЖ, возникающее в результате диастолической дисфункции, снижает сократительную способность ЛЖ [32]. В результате ПЖС может способствовать увеличению степени систолической дисфункции ЛЖ и увеличению вероятности клинических проявлений СН. В исследовании, основанном на тканевой допплерографии, в котором приняли участие 99 пациентов с дисфункцией синусового узла и ФВ ЛЖ ≥50%, Fang F, et al. [33] показали, что ПЖС была связана со значительным нарушением диастолической функции. У пациентов с уже существующей диастолической дисфункцией ПЖС может увеличиться риск возникновения СН, несмотря на сохраненную систолическую функцию ЛЖ [31]. Деформация миокарда является новым параметром для более детальной оценки систолической функции камер сердца. Среди параметров деформации наибольшее внимание уделяется глобальной продольной деформации. Он обладает большей чувствительностью, чем ФВ ЛЖ, и может выявлять субклиническую дисфункцию ЛЖ [34]. Недавние исследования показывают, что глобальная продольная деформация может служить предиктором снижения систолической функции ЛЖ после имплантации ЭКС, потенциально выявляя пациентов с риском развития ПИКМП [35].
Некоторые пациенты могут в течение длительного времени жить с имплантируемыми ЭКС и не иметь симптомов СН, сохраняя физическую работоспособность и качество жизни, сравнимое с людьми, у которых ПИКМП отсутствует [36]. Существует значительная вариабельность в индивидуальной восприимчивости к негативным воздействиям ПЖС, что подчеркивает необходимость проведения дополнительных исследований для выявления лиц, подверженных наибольшему риску развития ПИКМП и нуждающихся в проведении профилактических мероприятий.
Профилактика и лечение
Программирование ЭКС. Пациентам без АВБ рекомендуется свести к минимуму процент желудочковой стимуляции. Этого можно достичь с помощью режима AAI, установки минимальной приемлемой резервной частоты сердечных сокращений желудочков, применения длительной АВ задержки для облегчения внутренней АВ-проводимости. Существуют специальные алгоритмы по поиску своего АВ-проведения (АВ-гистерезис), позволяющие стимулировать естественную проводимость в АВ-узле и минимизировать стимуляцию ПЖ у пациентов с преходящей АВБ и другими брадиаритмиями. Например, в исследовании INTRINSIC RV (Inhibition of Unnecessary RV Pacing With AVSH in ICDs) данный алгоритм оценивался и применялся у 988 пациентов с имплантируемым кардиовертером-дефибриллятором, и было показано, что двухкамерная стимуляция с данным алгоритмом поиска АВ-проведения была сопоставима с результатами однокамерной желудочковой страховочной стимуляцией [37]. Но применение данного метода должно быть взвешено и обдумано в каждом конкретном случае, поскольку имеет место удлинение интервала PR. Чрезмерное удлинение этого интервала может приводить к нарушению функции ЛЖ, повышению в нем давления и повышению риска возникновении аритмий. Так, в метаанализе [38], в котором оценивались методы по снижению желудочковой стимуляции, данный алгоритм не показал превосходства над традиционной двухкамерной стимуляцией в снижении частоты впервые возникшей ФП, смертности от всех причин или госпитализации по всем причинам, хоть он эффективно и снижал нагрузку на желудочки при проведении электрокардиостимуляции.
Использование неапикальных методов постоянной стимуляции. В последние годы увеличивается количество исследований, которые демонстрируют улучшение клинических исходов при применении неапикальных зон постоянной кардиостимуляции, таких как СПГ и СОЛНПГ, по сравнению с ПЖС.
Так, в исследовании Abdelrahman M, et al. у 332 пациентов, находившихся на СПГ в одной больнице, по сравнению с 433 пациентами с ПЖС в другой, конечные точки смерти по любым причинам, случаи хронической СН, необходимость перехода на БиВ-СРТ наступали значительно реже в группе СПГ (25%; p=0,02), чем в группе ПЖС (32%; p=0,02). Продолжительность QRS была также значительно ниже в группе СПГ, чем в группе ПЖС (128±27 мс vs 166±22 мс; р<0,01) [39].
Vijayaraman P, et al. [40] показали целесообразность применения СПГ у пациентов с уже имеющейся ПЖС, нуждающихся в ресинхронизирующей терапии. Среди 60 пациентов с признаками ПИКМП, у которых ФВ ЛЖ снизилась с 54% до 34% после имплантации ЭКС со стандартной ПЖС, отмечалось повышение ФВ ЛЖ до 48%, после замены области стимуляции на область пучка Гиса. Однако есть определенные ограничения в этой технике в виде более высокого порога захвата, частой дислокацией электродов, преждевременного разряда батареи и длительного периода обучения.
СОЛНПГ была предложена в качестве альтернативы для преодоления ограничений СПГ. В работе Sharma PS, et al., включавшей 703 пациента, сравнивались клинические исходы пациентов сохранной ФВ (59±7%), которым была проведена имплантация кардиостимулятора с СОЛНПГ (n=321) и с ПЖС (n=382). Показатели смертности от всех причин (7,8% vs 15%; p=0,03), случаев застойной СН (3,7% vs 10,5%; p=0,004) и необходимости в БиВ-СРТ (10% vs 23,3%; p<0,001) были значительно ниже при использовании СОЛНПГ по сравнению с ПЖС. Продолжительность QRS была значительно ниже в группе СОЛНПГ, чем в группе ПЖС (121±23 мс vs 156±2 мс, соответственно; p<0,001) [41].
Несколько исследований подтвердили целесообразность, безопасность и эффективность СОЛНПГ в качестве альтернативного метода проведения БиВ-СР Т. Так, Rademakers LM, et al. [42] показали целесообразность применения СОЛНПГ для лечения пациентов с ПИКМП. У 20 пациентов, у которых произошла замена ПЖС на СОЛНПГ, отмечалось значительное снижение продолжительности QRS с 193±18 мс до 130±17 мс, а также увеличение ФВ ЛЖ с 32±6% до 47±8% и функционального класса (ФК) Нью-Йоркской ассоциации сердца (NYHA) с 2,8±0,4 до 1,4±0,5 в течение 6 мес. СОЛНПГ по сравнению с СПГ в перспективе обладает более стабильными параметрами стимуляции, с меньшим числом дислокаций.
Peng X, et al. [43] опубликовали метаанализ безопасности и эффективности физиологических методов стимуляции (СПГ/СОЛНПГ) в сравнении с традиционной ПЖС. В этот метаанализ были включены 27 статей (n=2787 пациентов), где было показано, что физиологическая стимуляция была связана с укорочением интервала QRS и улучшением сердечной деятельности. Данный вид стимуляции коррелировал с более низкой частотой митральной регургитации, симптомов СН, госпитализацией по поводу СН, новых случаев ФП и смертностью от всех причин, хотя вышеуказанные результаты не были статистически значимыми.
Использование ресинхронизирующей терапии. Использование сердечной БиВ-СРТ является наиболее эффективным методом лечения ПИКМП. Несколько исследований подтвердило эффективность БиВ-СРТ в устранении дилатации полостей сердца, дисфункции ЛЖ и уменьшении степени митральной регургитации [44].
В исследовании PACE (Pacing to Avoid Cardiac Enlargement) 177 пациентов с нормальной исходной ФВ разделили на две группы: 1-я — пациенты с БиВ-СРТ, 2-я с ПЖС. Средняя ФВ ЛЖ у пациентов в начале исследования составляла 61,7%. Через 12 мес. наблюдения средняя ФВ ЛЖ снизилась до 54,8% в группе с ПЖС, но осталась неизменной на уровне 62,2% в группе с БиВ-СРТ (р<0,001). Несмотря на то, что ФВ ЛЖ оставалась в пределах нормы в группе с ПЖС, отмечалось заметное увеличение конечного систолического объема (КСО) ЛЖ. На протяжении всего периода наблюдения, длившегося в среднем 4,8 года, эти группы продолжали демонстрировать различия, при этом ФВ ЛЖ продолжала снижаться в группе ПЖС — в среднем до 53,2% и увеличивался КСО ЛЖ, тогда как в первой группе эти параметры оставались стабильными. Также было отмечено увеличение частоты госпитализаций по поводу СН в группе с ПЖС (23,9% vs 14,6%, р=0,006) [45].
Исследование HOBIPACE (The Homburg Biventricular Pacing Evaluation) показало, что БиВ-СРТ стимуляция по сравнению с ПЖС снижала конечный диастолический объем (-9,0%, p=0,022), КСО (-16,9%, p<0,001), уровень N-концевого промозгового натрийуретического пептида (-31,0%, p<0,002), а также повысился показатель жизни согласно Миннесотскому опроснику качества жизни у больных с хронической СН (MLHFQ) [46]. В другом проспективном исследовании COMBAT были включены пациенты со II-IV ФК по классификации NYHA с ФВ ЛЖ <40% и имеющие АВБ, которым была показана имплантация ЭКС. Всем пациентам была имплантирована бивентрикулярная система, а затем они были распределены на две группы: группа А — в ней ЭКС изначально был запрограммирован на режим ПЖС, затем переведен на БиВ-СРТ, а потом снова переведен на ПЖС; группа Б — в ней устройство изначально программировалось на режим БиВ-СРТ, дальше переводилось на ПЖС и снова возвращалось на БиВ-СРТ. Каждый период длился 3 мес., в течение которых оценивались: качество жизни, ФК по NYHA, эхокардиографические параметры, тест 6-минутной ходьбы и пиковое потребление кислорода. В исследование были включены 60 пациентов, средний период наблюдения составил 17,5±10,7 мес. При применении СРТ по сравнению с ПЖС наблюдалось значительное улучшение качества жизни, повышение ФК, ФВ ЛЖ. Смертность была выше при правожелудочковом режиме стимуляции [47].
Khurshid S, et al. [48] провели ретроспективное исследование 69 пациентов с ПИКМП. Апгрейд ПЖС до БиВ-СРТ привел к повышению ФВ ЛЖ с 29,3% до 45,3% в среднем за 7 мес. наблюдения. Многофакторный анализ показал уменьшение продолжительности QRS (уменьшение с 1,92 мс до 1,09 мс; р=0,06). Исследование подтвердило, что, несмотря на длительную существующую ПИКМП, возможно существенное улучшение насосной функции сердца, так >70% пациентов с тяжелой ПИКМП (25% из них имели ее симптомы уже в течение >2 лет) достигли ФВ ЛЖ >35% после замены ЭКС.
Но, как и любое медицинское вмешательство, имплантация ЭКС несет за собой определенные интра- и постоперационные риски. Поэтому профилактика ПИКМП представляет лучшую стратегию, чем лечение путем замены ЭКС.
Заключение
ПИКМП является частым осложнением ПЖС. С учетом ежегодного роста пациентов с имплантируемыми устройствами, как никогда важно выявлять пациентов, предрасположенных к развитию данной кардиомиопатии. Пожилой возраст, мужской пол, исходно широкий комплекс QRS, наличие ФП в анамнезе, измененная ФВ ЛЖ, высокий процент желудочковой стимуляции — все это является предикторами развития ПИКМП. Определение четко сформулированных критериев ПИКМП упростит выявляемость данной патологии, а значит позволит разработать критерии профилактики и лечения. Основными направлениями лечения ПИКМП является БиВ-СРТ и стимуляция проводящей системы сердца (рис. 2). Учитывая перспективность последней и продолжающиеся многочисленные исследования, можно ожидать снижение частоты ПИКМП в будущем.

Рис. 2. Варианты лечения ПИКМП.
Сокращения: ЛНПГ — левая ножка пучка Гиса, ПИКМП — пейсмейкер-индуцированная кардиомиопатия, ЭКС — электрокардиостимулятор.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Протасова Е.А., Протасов М.Е., Бабокин В.Е., Баталов Р.Е., Фурман Н.В., Карзакова И.В. Пейсмейкер-индуцированная кардиомиопатия. Обзор литературы. Российский кардиологический журнал. 2025;30(3S):6656. https://doi.org/10.15829/1560-4071-2025-6656. EDN: VTKYWC
Скопировать