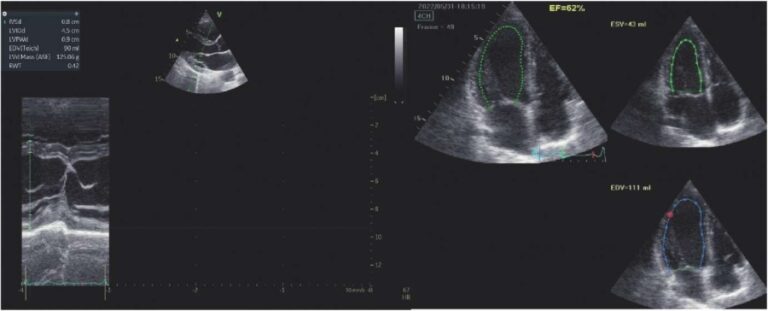
Оценка эффективности комплексной системы амбулаторного мониторинга пациентов с фибрилляцией предсердий, перенесших кардиоэмболический инсульт
Фибрилляция предсердий (ФП) — один из видов нарушения ритма работы сердца, который встречается у 2-4% взрослого населения. В ближайшие годы ожидается дальнейшее увеличение распространенности ФП как за счет повышения продолжительности жизни населения в целом, так и вследствие усовершенствования методов поиска недиагностированной ФП [1]. Данный вид аритмии ассоциирован с высоким риском развития острого нарушения мозгового кровообращения (ОНМК) и других тромбоэмболических осложнений (ТЭО) [2][3]. Инсульт является лидирующей причиной инвалидизации населения во всем мире, а также занимает второе место среди причин смертности вследствие сердечно-сосудистых заболеваний (ССЗ) [4]. Согласно современным статистическим данным, доля кардиоэмболического инсульта (КЭИ) достигает 38% от всех ОНМК ишемического генеза [5]. В основе патогенеза КЭИ лежит окклюзия церебральных артерий тромбами, сформированными в камерах сердца, вследствие чего для снижения риска ТЭО пациенты с ФП должны длительно принимать оральные антикоагулянты [1][6].
После выписки из специализированных неврологических отделений больные, перенесшие ОНМК, поступают на амбулаторный этап лечения. Задачи данного этапа состоят в продолжении реабилитационных мероприятий и проведении комплекса профилактических мер с целью предотвращения развития повторных ТЭО и вторичных осложнений инсульта. Успех профилактики ОНМК у пациентов с ФП зависит от назначения оптимальной медикаментозной терапии лечащим врачом и высокой приверженности пациентов к лечению. Однако, несмотря на наличие целого ряда клинических рекомендаций, регламентирующих длительную терапию пациентов с ФП, к настоящему моменту отсутствуют четко разработанные программы их амбулаторного ведения после перенесенного КЭИ [7].
Целью данного исследования являлось улучшение отдаленных результатов лечения пациентов с ФП, перенесших КЭИ, путем создания и апробации комплексной системы амбулаторного мониторинга.
Материал и методы
Исследование проводилось в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования одобрен этическим комитетом ФГБОУ ВО “СамГМУ Минздрава РФ”. В настоящее исследование было включено 139 пациентов с ФП, перенесших КЭИ за период 2016-2019гг, из них 80 (57,55%) женщин и 59 (42,45%) мужчин. Средний возраст пациентов составил 72,25±6,33 лет.
Диагноз КЭИ был подтвержден у всех пациентов посредством проведения компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) головного мозга; наличие ФП было документально доказано с помощью данных электрокардиографии (ЭКГ) или суточного мониторирования (СМ) ЭКГ. Лечение пациентов проводилось в соответствии с действующими версиями международных рекомендаций по ведению больных с ОНМК и ФП.
Всем пациентам на момент госпитализации было проведено следующее обследование:
- физикальный осмотр;
- лабораторная диагностика (клинический анализ крови, биохимический анализ крови: альбумины, мочевина, креатинин, липидный спектр, глюкоза, аланинаминотрансфераза, аспартатаминотрансфераза, общий билирубин, калий, натрий, коагулограмма, общий анализ мочи);
- инструментальное обследование (ЭКГ, рентгенография органов грудной клетки, эхокардиография, КТ или МРТ головного мозга, цветное допплеровское картирование артерий брахиоцефального ствола; при необходимости — СМ ЭКГ и фиброгастродуоденоскопия).
Во время стационарного лечения все больные прошли обучение в школе “Реабилитация”, в программу которой входили занятия, посвященные повышению информированности пациентов и их родственников о ФП и КЭИ, формированию мотивации к выздоровлению и выполнению рекомендаций врача, приобретению умений и навыков по самоконтролю общего состояния, правильному питанию, адекватной двигательной активности, отказу от вредных привычек. На момент выписки всем пациентам была подобрана оптимальная индивидуализированная медикаментозная терапия (антикоагулянтная, гипотензивная, гиполипидемическая; при необходимости — антиаритмическая, гипогликемическая, коррекция хронической сердечной недостаточности (ХСН), почечной и печеночной функции).
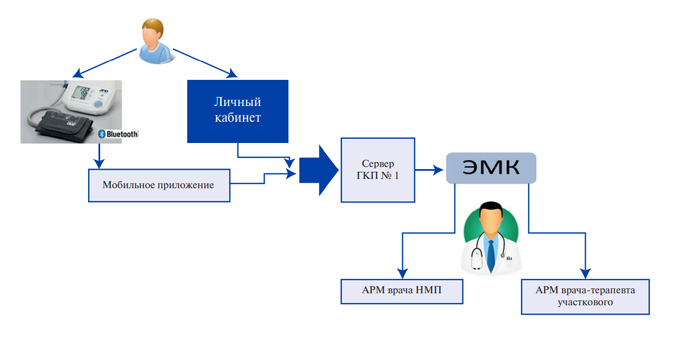
Перед выпиской из стационара все пациенты подписали добровольное информированное согласие на участие в исследовании, после чего были рандомизированы на две группы методом случайных чисел. Пациенты I (изучаемой) группы (n=72) в течение одного года наблюдались в соответствии со специально разработанной комплексной системой амбулаторного мониторинга. Данная система включала в себя не только реабилитационную программу, созданную индивидуально для каждого больного в соответствии с его клиническими характеристиками, но и регулярные ежемесячные визиты к врачу-исследователю, во время которых проводился комплекс физикальных, лабораторных и инструментальных методов исследования в соответствии с существующими в настоящее время подходами. На каждом визите оценивались динамика жалоб и симптомов, приверженность к терапии, и при необходимости проводилась ее коррекция. Также врач проводил беседу с пациентом и его родственниками о необходимости соблюдения рекомендованного режима жизни и приема лекарственных препаратов, поддерживая мотивацию к лечению. Пациенты II (контрольной) группы (n=67) наблюдались на уровне первичного звена в соответствии с существующим организационным порядком, принятым в лечебно-профилактическом учреждении по месту жительства, а контрольный визит к врачуисследователю был выполнен для них однократно — через 12 мес.
В качестве первичной конечной точки эффективности рассматривалась комбинация инфаркта миокарда (ИМ), ишемического инсульта и сердечно-сосудистой смерти; за вторичные конечные точки эффективности были приняты общая смертность и госпитализация по поводу декомпенсации ХСН. За первичную конечную точку безопасности был принят эпизод большого или клинически значимого небольшого кровотечения по классификации Международного общества тромбоза и гемостаза (ISTH).
Статистический анализ проводился при помощи компьютерных программ IBM SPSS Statistic 22.0 (IBM, США), пакеты прикладных программ Statisticа 10.0.228.8, Excel-2013, Access-2010, Word-2010 (Microsoft Corp., США). Различия рассматривали как статистически значимые при p<0,05; при р?0,01 — очень значимые; при р?0,001 — высокозначимые.
В исследовании был использован анализ бинарной классификации с применением кривых (ROCанализ — Receiver Operator Characteristic analysis), который позволяет классифицировать положительные и отрицательные примеры. Графическим отражением данного статистического метода является ROCкривая, которая отражает результаты бинарной классификации и показывает зависимость количества верно классифицированных положительных примеров от количества неверно классифицированных отрицательных примеров. Количественную интерпретацию метода дает параметр “площадь под ROCкривой” (Area Under ROC Curve — AUC) — площадь, ограниченная ROC-кривой и осью доли ложных положительных классификаций. Принято считать, что коэффициент AUC, находящийся в интервале 0,9- 1,0, отражает отличное качество классификационной модели; 0,8-0,9 — очень хорошее; 0,7-0,8 — хорошее; 0,6-0,7 — среднее; 0,5-0,6 — низкое качество.
Для проверки независимости категориальных переменных в кросс-таблицах применяли критерий хиквадрат (?2). Оценка силы связи между воздействием и заболеванием проводилась посредством расчета величины отношения шансов (ОШ) возникновения события в группах сравнения. При ОШ >1 вероятность развития исхода в изучаемой группе выше, чем в контрольной. При этом чем больше значение ОШ, тем выше вероятность развития события. При ОШ <1 вероятность развития исхода в изучаемой группе ниже, чем в контрольной.
Результаты
На первом этапе статистического анализа группы больных, сформированные по итогам рандомизации, были оценены на предмет соответствия нормальному распределению. Вследствие того, что в данных группах распределение признаков отличалось от нормального, для их сравнения нами был применен критерий Колмогорова-Смирнова. Данные о структуре изучаемой и контрольной групп по возрасту, основным антропометрическим параметрам, полу, частоте встречаемости сопутствующей патологии и основных факторов риска развития ССЗ, по форме ФП и наличию геморрагических осложнений в анамнезе, с последующим межгрупповым сопоставлением указанных параметров на предмет поиска статистически значимых отличий, представлены в таблицах 1 и 2.
Таблица 1
Структура сравниваемых групп по возрасту и основным антропометрическим параметрам*

Примечание: * — показатели представлены в виде медианы (Ме) и интерквартильного размаха (Q1-Q2).
Сокращение: ИМТ — индекс массы тела.
Таблица 2
Структура сравниваемых групп по полу, сопутствующим заболеваниям, факторам риска ССЗ, форме ФП, наличию кровотечений в анамнезе

Сокращения: ЖКТ — желудочно-кишечный тракт, ИМ — инфаркт миокарда, КШ — коронарное шунтирование, РЧА — радиочастотная аблация, ССЗ — сердечнососудистые заболевания, ФП — фибрилляция предсердий, ХСН — хроническая сердечная недостаточность, ЭКС — электрокардиостимулятор.
Таким образом, изучаемая (I) и контрольная (II) группы на момент рандомизации были сопоставимы по возрасту, основным антропометрическим параметрам, полу, частоте встречаемости сопутствующей патологии, формам ФП, наличию в анамнезе геморрагических осложнений.
Исходно группы сравнивались по риску развития тромбоэмболических и геморрагических осложнений с использованием шкал стратификации CHA2DS2- VASc и HAS-BLED, соответственно, при этом было установлено, что по данным показателям группы между собой не различались (табл. 3).
Таблица 3
Структура сравниваемых групп по риску тромбоэмболических и геморрагических осложнений*

Примечание: * — показатели представлены в виде медианы (Ме) и интерквартильного размаха (Q1-Q2).
Сокращения: ХСН — хроническая сердечная недостаточность, ISTH — Международное общество тромбоза и гемостаза.
Таким образом, на момент выписки из стационара группы больных, сформированные в результате рандомизации, были сопоставимы по всем основным статистическим характеристикам, что исключает возможное влияние последних на исходы нашего исследования.
По результатам годового наблюдения было проведено сравнение I и II групп по частоте развития запланированных конечных точек (табл. 4).
Таблица 4
Частота запланированных конечных точек (сердечно-сосудистая смерть, ИМ, инсульт) в сравниваемых группах

Таким образом, через 12 мес. амбулаторного этапа реабилитации сравниваемые группы статистически значимо различались по частоте возникновения следующих событий: первичная комбинированная конечная точка эффективности (сердечно-сосудистая смерть, ИМ и ишемический инсульт) и две вторичные точки эффективности (общая смертность и госпитализация по поводу ХСН), которые у пациентов группе I наблюдались реже. При этом различий по частоте развития первичной конечной точки безопасности между группами установлено не было.
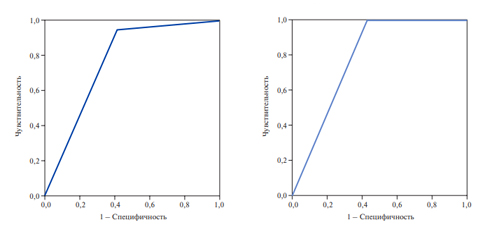
Кроме того, в группе II выявлена зависимость возникновения смертельного исхода с отсутствием приема антикоагулянтной терапии (ОШ 7,68; 95% доверительный интервал 1,59-37,03; p=0,01). Результаты ROC-анализа подтвердили наличие связи между отсутствием приема антикоагулянтной терапии и развитием смертельного исхода, при этом качество регрессии соответствовало хорошему (площадь под кривой AUC составила 0,77, чувствительность — 94,74%, специфичность — 59,17%) (рис. 1).
В нашей работе также была установлена взаимосвязь между декомпенсацией ХСН в группе II с отсутствием приема диуретиков (?2 — 7,38, уровень достоверности p=0,007). При проведении сравнительного логистическогорегрессионного анализа в отношении декомпенсации ХСН была показана прогностическая значимость приема диуретической терапии, при этом качество регрессии соответствовало хорошему (площадь под кривой AUC — 0,783, чувствительность — 100%, специфичность — 57,14%) (рис. 2).

Рис. 1. Соотношение частоты смертельного исхода в течение 12 мес. с фактом приема антикоагулянтов.
Рис. 2. Соотношение частоты декомпенсации ХСН в течение 12 мес. с фактом приема диуретиков.
В группе I в течение 12 мес. амбулаторного наблюдения значительной части больных потребовалось внесение изменений в медикаментозную терапию, назначенную при выписке из стационара. Это могли быть замена препарата, уменьшение или увеличение его дозы, присоединение другого лекарственного средства с иным механизмом действия для усиления эффекта. Например, коррекция антигипертензивной терапии была необходима 34 больным (47,22%), антикоагулянтной терапии — 13 пациентам (18,06%). Наиболее часто изменение дозы требовалось на фоне терапии варфарином — из 12 человек, принимавших данный антикоагулянт, у 8 отмечалась нестабильность уровня международного нормализованного отношения. Однако в итоге в I группе по результатам годового наблюдения приверженность антикоагулянтному и антигипертензивному лечению составила 100%. Коррекция лечения ХСН потребовалась 24 больным (33,33%), при этом ни один пациент I группы в течение нашего исследования не был госпитализирован вследствие декомпенсации ХСН. В группе II по итогам заключительного визита было установлено, что в целом по группе антигипертензивные препараты принимали 53 (79,10%), антикоагулянты — 26 (38,81%), а адекватную терапию ХСН — 13 (19,40%) пациентов, что, безусловно, повлияло на частоту развития запланированных конечных точек.
Обсуждение
Важность вторичной профилактики инсульта в настоящее время сомнений не вызывает. За прошедшие годы подходы к долгосрочному лечению пациентов, перенесших инсульт, претерпели кардинальные изменения. В настоящее время пациенты, перенесшие инсульт, в т.ч. и кардиоэмболического генеза, при выписке из специализированного стационара получают перечень рекомендаций для дальнейшего лечения, который состоит из немедикаментозных и медикаментозных мероприятий по вторичной профилактике повторного инсульта и других сердечно-сосудистых событий.
Медикаментозная терапия у таких больных, как правило, состоит из лекарственных препаратов нескольких классов. Первостепенное значение у пациентов с ФП, перенесших КЭИ, имеет антикоагулянтная профилактика ТЭО, которая должна проводиться больным данного профиля пожизненно (класс рекомендации — I, уровень доказательств — А) [1][6]. Кроме того, необходимо оценить целесообразность назначения антиаритмических препаратов в зависимости от выбранной стратегии контроля ритма или частоты сердечных сокращений. Необходимость приема других лекарственных средств определяется наличием сопутствующих заболеваний. Например, подавляющее большинство пациентов с ФП нуждаются в антигипертензивной терапии. Так, в популяции больных, включенных в наше исследование, распространенность артериальной гипертензии достигала 100% в группе I и 98,51% в группе II. Выбор препарата для контроля уровня артериального давления во многом зависит от коморбидного статуса конкретного пациента, и зачастую требуется назначение комбинации антигипертензивных средств. Наличие у пациента ишемической болезни сердца, в зависимости от фазы ее течения, может потребовать усиления антитромботической терапии, что повышает риск геморрагических осложнений. Кроме того, в рамках вторичной профилактики должна быть проведена коррекция ХСН и сахарного диабета. Нарушение функции печени и почек также необходимо принимать во внимание при выборе конкретных лекарственных средств, вследствие возможного изменения их фармакокинетических параметров.
Все эти факторы оцениваются и учитываются при составлении плана стационарного лечения и при формулировке рекомендаций на момент выписки пациента. Далее, на амбулаторном этапе ведения требуется периодическая переоценка клинической симптоматики и некоторых лабораторных и инструментальных показателей. Например, прием варфарина требует обязательного ежемесячного определения международного нормализованного отношения, а прием антиаритмических препаратов — регулярного подсчета длительности интервала QТ на ЭКГ. Всем больным с ФП показан контроль почечной функции, регулярность которого зависит от исходной величины скорости клубочковой фильтрации конкретного пациента и рассчитывается по специальной формуле. Кроме того, необходимо регулярно переоценивать риски тромботических и геморрагических осложнений, а также соотношение пользы и риска от проводимого лечения. Все эти особенности ведения больных с ФП отражены в современных регламентирующих документах [1][6], и прогноз жизни пациентов напрямую зависит от оптимального выполнения современных рекомендаций.
Выполнение данной программы вторичной профилактики КЭИ в полном объеме возможно лишь при регулярном наблюдении у специально подготовленного специалиста. О целесообразности широкого внедрения именно такого подхода к амбулаторному этапу реабилитации свидетельствуют и результаты нашего исследования — при ведении пациентов в соответствии с разработанной комплексной системой амбулаторного мониторинга в течение года после выписки из специализированного стационара было получено статистически значимое снижение первичной комбинированной конечной точки (сердечно-сосудистая смерть, ИМ, ишемический инсульт), а также таких вторичных точек эффективности, как общая смертность и госпитализация вследствие декомпенсации ХСН.
Регулярные ежемесячные визиты к специалисту позволяли своевременно корректировать лечение, а также поддерживать на высоком уровне приверженность к терапии, которая в группе I достигала 100%. В литературе опубликован ряд исследований, подтверждающих, что именно высокая приверженность больных назначенному лечению позволяет влиять на прогноз их жизни [8][9][10][11]. Однако до настоящего времени качество ведения пациентов, перенесших инсульт, на амбулаторном этапе остается недостаточным [10][12][13]. Согласно нашим собственным данным, опубликованным ранее, адекватная профилактика ТЭО в реальной клинической практике проводится крайне редко — только в 16,2% случаев врачи амбулаторного этапа рекомендовали пациентам с ФП прием антикоагулянта [14]. Несоблюдение современных рекомендаций поведению пациентов врачами амбулаторного звена можно объяснить их значительной загруженностью ежедневной клинической работой, а также, возможно, и недостаточной осведомленностью о современных подходах к лечению.
Заключение
На основании изложенного выше мы считаем, что разработка комплексной программы амбулаторного мониторинга пациентов с ФП, перенесших КЭИ, доказала свою эффективность, а ее широкое применение является актуальной задачей современного здравоохранения. Следует глобально пересмотреть подходы к амбулаторному ведению пациентов с ФП, перенесших КЭИ. Целесообразным представляется создание амбулаторных кабинетов вторичной профилактики инсульта, которые будут заниматься коррекцией факторов риска, подбором оптимальной лекарственной терапии и контролем за приверженностью к ней.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Ефимова О.И., Павлова Т.В., Пыщева Л.В., Хохлунов С.М. Оценка эффективности комплексной системы амбулаторного мониторинга пациентов с фибрилляцией предсердий, перенесших кардиоэмболический инсульт. Российский кардиологический журнал. 2021;26(1S):4402. https://doi.org/10.15829/1560-4071-2021-4402
Скопировать