Электрокардиографические признаки блокады левой ножки пучка Гиса и прогнозирование ответа на бивентрикулярную стимуляцию и стимуляцию проводящей системы сердца
Аннотация
В статье представлен анализ отечественных и зарубежных исследований, посвященных диагностике блокады левой ножки пучка Гиса (БЛНПГ) и анализу электрокардиографических (ЭКГ) критериев для отбора пациентов на сердечную ресинхронизирующую терапию. Рассмотрены особенности классификации БЛНПГ, включая истинную и ложную формы, а также различия в локализации блока проведения при схожей ЭКГ картине. Особое внимание уделено проблеме вариабельности существующих ЭКГ-критериев и прогностической значимости отдельных ЭКГ-признаков. Подчеркивается важность разработки новых критериев для улучшения диагностики и повышения эффективности лечения пациентов с БЛНПГ для улучшения отбора на бивентрикулярную стимуляцию и стимуляцию проводящей системы сердца.
Результаты эндокардиального и эпикардиального активационного картирования у пациентов с блокадой левой ножки пучка Гиса (БЛНПГ) свидетельствуют о неоднородности паттерна активации левого желудочка (ЛЖ) [1-4]. Примерно в 30% случаев регистрируются нормальные время и направление транссептальной активации, что может свидетельствовать о сохранном проведении по волокнам левой ножки пучка Гиса (ЛНПГ) у значимой части пациентов [1][2].
Для разделения пациентов со схожей электрокардиографической (ЭКГ) картиной были предложены термины «истинная» и «ложная» БЛНПГ 1 [4]. В первом случае наблюдаются характерные изменения активации желудочков сердца, в то время как во втором случае регистрируется сохранное проведение по волокнам ЛНПГ, а последовательность возбуждения сердца соответствует норме. Считается, что при ложной БЛНПГ наблюдается сочетание блока передней ветви ЛНПГ и гипертрофии ЛЖ или неспецифического нарушения проведения [5].
Развитие сердечной ресинхронизирующей терапии (СРТ) привело к увеличению интереса исследователей к этой проблеме. Крупные многоцентровые исследования продемонстрировали, что БЛНПГ является одним из важнейших критериев отбора пациентов на СРТ [6-10]. Однако примерно 30% пациентов не отвечают на эту терапию, что частично может объясняться имплантацией СРТ устройств пациентам с ложной БЛНПГ [11-13].
ЭКГ в 12-ти стандартных отведениях считается основным методом диагностики БЛНПГ, однако диагностические критерии, представленные в рекомендациях Американской ассоциацией сердца (AHA) и Европейским обществом кардиологов (ESC), соответственно, имеют существенные различия [9][14-16]. Более того, в рандомизированных клинических исследованиях (РКИ), которые продемонстрировали эффективность СРТ при различной морфологии комплекса QRS, также использовали неодинаковые ЭКГ-критерии [6-8]. Во многих исследованиях было показано, что существующие диагностические критерии БЛНПГ характеризуются низкой согласованностью и разной прогностической ценностью в предсказании ответа на СРТ [17-22].
Ренессанс стимуляции проводящей системы сердца (СПСС) дополнительно увеличил интерес к изучению не только факта наличия, но и локализации блока проведения при БЛНПГ. Исследования с использованием эндокардиального картирования показали, что эффективность ресинхронизации при стимуляции пучка Гиса зависит от расположения блока проведения при БЛНПГ: чем дистальнее блок, тем ниже вероятность успеха [23-25]. В связи с этим, помимо «истинной» и «ложной» БЛНПГ, современные исследования выделяют «проксимальную» и «дистальную» формы. Предполагается, что проксимальная форма соответствует истинной БЛНПГ, однако на сегодняшний день отсутствует консенсус о соответствии дистальной локализации блока проведения и ложной БЛНПГ [26]. Более того, Upadhya GA, et al. выделяют не два, а три варианта БЛНПГ: проксимальную (left intrahisian), дистальную (left bundle branch block) и интактное проведение по волокнам Пуркинье (intact Purkinje activation) БЛНПГ [25]. Для улучшения отбора пациентов на стимуляцию пучка Гиса были предложены новые ЭКГ-критерии проксимальной БЛНПГ, разработанные при изучении пациентов после повреждения проксимальных отделов ЛНПГ [27-29]. Однако на сегодняшний день эти критерии не были верифицированы в группах пациентов СПСС.
Учитывая разнообразие классификаций БЛНПГ, различия в диагностической ценности актуальных ЭКГ-критериев, а также их важную роль в отборе пациентов на СРТ и СПСС, диагностика этого нарушения проводимости остается актуальной проблемой современной медицины.
ЭКГ-критерии БЛНПГ в эпоху СРТ
Первые свидетельства о неоднородности паттерна активации при ЭКГ картине БЛНПГ были опубликованы еще в середине XXв. Еще в 1956г Grant и Dodge обнаружили, что у трети пациентов с БЛНПГ расширение комплекса QRS на поверхностной ЭКГ не сопровождается изменением направления вектора активации межжелудочковой перегородки (МЖП) [30][31]. Первое эндокардиальное картирование пациентов с БЛНПГ также показало, что в 30% случаев регистрируется несколько точек наиболее ранней активации в эндокарде ЛЖ, что свидетельствует о сохранном проведении электрических сигналов через волокна ЛНПГ [2]. Тем не менее интерес исследователей к этой проблеме возрос только после выявления связи между БЛНПГ и ответом на СРТ. В частности, после публикации субанализов многоцентровых исследований MADIT-CRT, REVERSE и RAFT БЛНПГ была признана важным критерием отбора на СРТ, что нашло отражение в зарубежных и российских клинических рекомендациях [6-10].
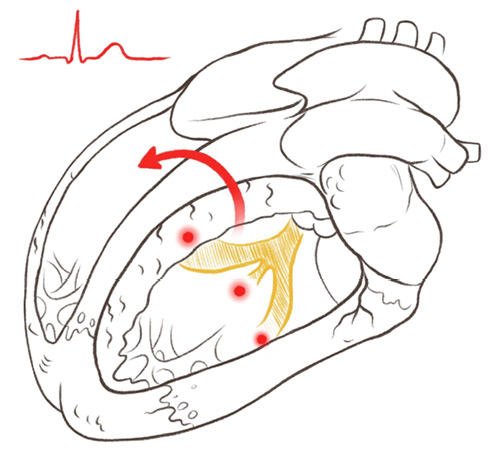
Auricchio A, et al. в 2004г с помощью эндокардиального электроанатомического картирования подтвердили неоднородность паттернов активации желудочков сердца среди кандидатов на СРТ с БЛНПГ. Примерно у трети пациентов время транссептального проведения оставалось нормальным. Последующие исследования с использованием наиболее современных методов инвазивного активационного картирования также подтвердили, что среди кандидатов на СРТ примерно треть пациентов имеют нормальный паттерн активации желудочков сердца, что свидетельствует об отсутствии субстрата для ресинхронизации, несмотря на ЭКГ картину БЛНПГ (рис. 1).


Рис. 1. Паттерн активации желудочков сердца в норме (слева) и при БЛНПГ (справа).
Значимость БЛНПГ при отборе пациентов на СРТ привела к систематическому пересмотру ЭКГ-критериев БЛНПГ в клинических рекомендациях на протяжении XXIв. Стоит отметить, что ЭКГ-критерии AHA и ESC эволюционировали автономно, что привело к существенным расхождениям в предлагаемых критериях.
Рекомендации AHA 2009г адаптировали критерии БЛНПГ из публикации Всемирной организации здравоохранения 1985г (табл. 1) [14][32][33]. Эта концепция сохранила свою актуальность и была интегрирована без изменений в новейшие рекомендации AHA 2023г [16]. С другой стороны, ESC неоднократно модифицировала свои критерии. Изначальные рекомендации ESC 2006г включали 6 ЭКГ-признаков (табл. 1) [32]. Критерии 2009г практически полностью повторяли рекомендации AHA того же периода, однако из них были исключены 3 признака, связанные с определением внутреннего отклонения зубца R, и включено наличие QS или rS в V1 (табл. 1) [33].
При пересмотре критериев ESC в 2013г по сравнению с 2009г были исключены ранее используемые признаки: отсутствие зубца q в I стандартном отведении и наличие дискордантного зубца T [9]. Кроме того, была модифицирована интерпретация зазубренности и сглаженности зубца R. Новая формулировка допускала более гибкий подход к оценке этих характеристик в отведениях I, aVL, V5 и V6, не требуя их обязательного присутствия во всех указанных отведениях, а лишь частой встречаемости этого признака (табл. 1).
Наиболее значительные изменения произошли в рекомендациях ESC 2021г. Новый набор ЭКГ-признаков значительно отличался от рекомендаций 2006, 2009 и 2013гг [15]. В частности, изменились формулировки, описывающие зазубренность и сглаженность зубца R, а также были добавлены новые ЭКГ-признаки, которые ранее не фигурировали в клинических рекомендациях.
Важно подчеркнуть, что вариативность критериев проявляется не только в клинических рекомендациях, но и в РКИ, которые продемонстрировали эффективность СРТ при различной морфологии комплекса QRS [6-8][34][35]. Из всего спектра проведенных РКИ лишь исследование RAFT полностью придерживалось критериев, установленных в клинических рекомендациях, в частности, AHA (табл. 1). В рамках исследования REVERSE некоторые ЭКГ-признаки были исключены из критерия AHA.
Критерий, используемый в MADIT-CRT, практически полностью совпадал с критерием ESC 2013, однако, учитывая специфику отбора пациентов, ширина комплекса QRS в этом критерии обычно указывается >130 мс [6]. В исследованиях MIRACLE и CARE-HF также использовали уникальные, ни на что не похожие критерии [34][35]. Таким образом, комбинации ЭКГ-признаков, применяемые в упомянутых исследованиях, существенно различались между собой и не соответствовали критериям, предложенным в клинических рекомендациях (табл. 1). Среди всех существующих критериев XXIв полное совпадение наблюдается только между рекомендациями AHA и критерием, использованным в RAFT, тогда как в остальных случаях были использованы уникальные комбинации из различных ЭКГ-признаков (табл. 1).
Наряду с официальными критериями, содержащимися в клинических рекомендациях и используемыми в РКИ, существуют альтернативные критерии, разработанные отдельными научными коллективами. Одним из наиболее известных является критерий БЛНПГ, предложенный Strauss DG, et al. в 2011г [5]. Опираясь на электрофизиологические и электрокардиографические данные, исследователи разработали метод, позволяющий дифференцировать истинную БЛНПГ от комбинации блокады передней ветви ЛНПГ и гипертрофией ЛЖ.
Ключевой особенностью данного подхода является установление более высокого минимального порога длительности комплекса QRS: 140 мс для мужчин и 130 мс для женщин [5]. Эти значения базируются на предположении о минимальной продолжительности желудочковой активации в 140 мс, включающей 40 мс на проведение от эндокарда правого желудочка к эндокарду ЛЖ, 50 мс на достижение свободной стенки ЛЖ и еще 50 мс на активацию заднебоковой стенки ЛЖ [5]. В поддержку своей теории авторы приводят результаты дополнительного анализа исследования MADIT-CRT. Согласно этим данным, положительный эффект СРТ чаще наблюдался у женщин при QRS ≥130 мс, в то время как у мужчин эффективность терапии отмечалась при QRS ≥140 мс [5][6]. Исследователи объясняют гендерные различия разницей в массе миокарда желудочков сердца. Однако стоит отметить, что одним из критериев отбора пациентов на СРТ в РКИ MADIT-CRT было QRS ≥130 мс для всех участников [6], что ставит под вопрос обоснованность выбора нижнего порога ширины QRS для женщин в критерии Strauss. Более того, параметры активации желудочков могут существенно варьироваться даже среди пациентов одного пола в зависимости от наличия рубцовых изменений, фиброза миокарда, размеров камер сердца и массы миокарда. Это указывает на необходимость дальнейшего изучения оптимальных порогов QRS при истинной БЛНПГ.
Критерий Strauss также отличается в оценке зазубренности или сглаженности зубца R от подходов, предложенных AHA в 2009г и ESC в 2013г [5, 9, 14]. Во-первых, данный признак должен наблюдаться в средней части комплекса QRS. Во-вторых, помимо «левых» отведений (I, aVL, V5, V6), анализируются также V1 и V2. В-третьих, изменения должны быть зафиксированы как минимум в двух из следующих отведений: I, aVL, V1-V2, V5-V6. Этот подход отличается от подхода в рекомендациях AHA, где необходимо наличие зазубренности или сглаженности во всех отведениях I, aVL, V5-V6, тогда как ESC 2013 предполагает их «частое» присутствие. Интересно отметить, что в критериях ESC 2021 был скопирован подход к определению этого признака, предложенный Strauss DG, et al. [15].
Таблица 1
ЭКГ-критерии и ЭКГ-признаки БЛНПГ
|
Критерии Признаки |
ESC 2006 |
AHA 2009 |
ESC 2009 |
Strauss 2011 |
ESC 2013 |
ESC 2021 |
MIRACLE |
CARE-HF |
MADIT-CRT |
REVERSE |
RAFT |
|
Длительность комплекса QRS ≥ (мс) |
120 |
120 |
120 |
ж — 130, м — 140 |
120 |
120 |
130 |
120 |
130 |
120 |
120 |
|
QS или rS в V1 с положительным Т |
+ |
— |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
— |
— |
|
Монофазный QS в V1 |
— |
— |
— |
— |
— |
— |
+ |
— |
— |
— |
— |
|
Нормальный интервал ВО R в V1-V3 |
— |
+ |
— |
— |
— |
— |
— |
— |
— |
— |
+ |
|
Интервал ВО R в I ≥60 мс |
+ |
— |
— |
— |
— |
— |
— |
— |
— |
— |
— |
|
Интервал ВО R в V5 ≥60 мс |
— |
+ |
— |
— |
— |
+ |
— |
— |
— |
+ |
+ |
|
Интервал ВО R в V6 ≥60 мс |
+ |
+ |
— |
— |
— |
+ |
— |
— |
— |
+ |
+ |
|
Монофазный зубец R в I и aVL |
— |
— |
— |
— |
— |
+ |
— |
— |
— |
— |
— |
|
Монофазный зубец R в V6 |
— |
— |
— |
— |
— |
+ |
— |
— |
— |
— |
— |
|
Зазубренный/сглаженный зубец R в I, aVL и V5-V6 |
— |
+ |
+ |
— |
— |
— |
— |
— |
+ |
+ |
+ |
|
Зазубрина/сглаженность в середине QRS, как минимум, в двух отведениях: I, aVL, V1-V2, V5-V6 |
— |
— |
— |
+ |
— |
+ |
— |
— |
— |
— |
— |
|
Уширенный (с часто встречающимися зазубриной и сглаженностью) зубец R в I, aVL, V5-V6 |
— |
— |
— |
— |
+ |
— |
— |
— |
+ |
— |
— |
|
Зазубренный/сглаженный зубец R в I и V6 |
— |
— |
— |
— |
— |
— |
— |
— |
— |
— |
— |
|
Отсутствие зубца q в I |
— |
+ |
+ |
— |
— |
— |
— |
+ |
— |
— |
+ |
|
Отсутствие зубца q в V5-V6 |
— |
+ |
+ |
— |
+ |
— |
+ |
+ |
+ |
+ |
+ |
|
QS с положительным зубцом T в aVR |
+ |
— |
— |
— |
— |
+ |
— |
— |
— |
— |
— |
|
rS в aVF |
— |
— |
— |
— |
— |
— |
— |
— |
— |
— |
— |
|
Дискордантный зубец Т |
+ |
+ |
+ |
— |
— |
+ |
— |
+ |
— |
— |
— |
Сокращения: ВО — внутреннее отклонение, AHA — Американская ассоциация сердца, ESC — Европейское общество кардиологов.
Сравнение диагностической ценности различных ЭКГ-критериев
Важным этапом в изучении диагностической ценности различных критериев БЛНПГ стало исследование van Deursen C, et al., которые в 2014г впервые провели сравнительный анализ критериев ESC, AHA, Strauss, MADIT-CRT и REVERSE [17]. По результатам 6 мес. наблюдения после имплантации СРТ наибольшее снижение конечно-систолического объема (КСО) ЛЖ было зафиксировано у пациентов, у которых БЛНПГ была диагностирована только по критерию Strauss [17].
Исследование, проведенное группой ученых под руководством van Stipdonk A, обнаружило существенные расхождения в диагностировании БЛНПГ при применении различных критериев, включая AHA, ESC, Strauss и MADIT-CRT [21]. Примечательно, что лишь у небольшой части пациентов (13,8%) диагноз БЛНПГ был подтвержден всеми четырьмя методами одновременно. Анализ показал значительную вариабельность в чувствительности, специфичности и согласованности при выявлении БЛНПГ, с коэффициентом каппа, колеблющимся в широком диапазоне от 0,09 до 0,92. Независимо от выбранного критерия, наличие БЛНПГ было связано со снижением частоты комбинированной первичной конечной точки (смерть, трансплантация сердца или имплантация устройства для поддержки функции ЛЖ) [21].
Анализ, проведенный Caputo M, et al., продемонстрировал, что у пациентов, у которых БЛНПГ была диагностирована согласно всем современным критериям (ESC 2013, Strauss и AHA), на фоне СРТ наблюдаются более высокие показатели выживаемости и сниженная частота госпитализаций по поводу хронической сердечной недостаточности [19]. Тем не менее при оценке комбинированной конечной точки (летальность и госпитализация) статистически достоверные отличия были обнаружены лишь при применении критериев ESC 2009, ESC 2013 и Strauss. Согласно мультивариантному анализу, только критерии ESC 2009 и 2013 оказались статистически значимо связанными с положительным ответом на СРТ (отношение шансов (ОШ) 8,8; 95% доверительный интервал (ДИ): 1,3-56,5; p<0,01 и ОШ 8,7; 95% ДИ: 1,4-56,4; p<0,01, соответственно) [19].
Согласно исследованию Кузнецова В. А. и др., современные критерии БЛНПГ (AHA, ESC 2013 и Strauss) чаще встречались среди респондеров с положительным эффектом от СРТ [22]. Критерий AHA продемонстрировал наибольшую специфичность (94,7%), однако был выявлен менее чем у половины респондеров. Высокая специфичность AHA, вероятно, связана с более точным выявлением электрической диссинхронии. Тем не менее из-за низкой чувствительности многие потенциальные респондеры могут не получить эффективную терапию. Наибольшую чувствительность показал критерий Strauss (80,3%). Однако БЛНПГ по этому критерию была диагностирована у значительной части нереспондеров, что указывает на его ограниченную специфичность. Критерий Strauss также продемонстрировал наибольшую общую точность в предсказании снижения КСО ЛЖ ≥15% на фоне СРТ (72,4%) [22]. Аналогичные выводы были сделаны в многоцентровом исследовании van Stipdonk А, где чувствительность и специфичность критерия AHA составили 21% и 87%, соответственно [21]. Критерий Strauss продемонстрировал наибольшую общую точность в прогнозировании уменьшения КСО ЛЖ на фоне СРТ.
Кузнецов В. А. и др. дополнительно оценили согласованность между различными критериями БЛНПГ [22]. Критерии, предложенные в клинических рекомендациях AHA и ESC 2013, продемонстрировали сильную согласованность в отношении определения БЛНПГ (коэффициент κ =0,818, 95% ДИ: 0,7-0,936, p<0,001). Однако между критериями Strauss и ESC 2006/AHA/ESC 2013 была установлена минимальная согласованность. Согласованность в определении БЛНПГ для критериев, описанных в РКИ, в большинстве случаев также была минимальной. Тем не менее в исследованиях, результаты которых послужили поводом для включения БЛНПГ в качестве критерия отбора (MADIT-CRT, REVERSE, RAFT), были использованы критерии с умеренной или сильной согласованностью [22].
Интересно отметить, что пересмотренные критерии ESC 2021г не принесли ожидаемого улучшения в прогнозировании ответа на СРТ [15]. Calle S, et al. выполнили сравнительный анализ диагностической ценности критериев ESC 2013 и ESC 2021 [36]. Результаты показали, что БЛНПГ по критерию ESC 2013 диагностировалась у всех обследованных, а по критерию ESC 2021 только в 12% случаев. Такая низкая частота обусловлена увеличением числа ЭКГ-признаков, включенных в обновленный критерий, что, по мнению авторов, приводит к излишней специфичности и ухудшает отбор пациентов на СРТ [36]. В другом исследовании 2023г было показано, что применение критерия ESC 2021 исключает значительную долю пациентов из I класса показаний для имплантации СРТ [37]. Кроме того, данный критерий не был с механической диссинхронией и обратным ремоделированием ЛЖ на фоне терапии, в сравнении с критерием ESC 2013 [37]. Анализ данных регистра MUG, включающего 1202 пациента, показал, что частота диагностики БЛНПГ значительно снижалась при использовании критерия ESC 2021 в сравнении с ESC 2013 (31,6% и 80,9%, соответственно) [38]. При этом только критерий ESC 2013 позволял прогнозировать эффект от СРТ, пациенты с БЛНПГ по критерию ESC 2021 не отличались по результатам терапии от пациентов с другой морфологией QRS [38].
Помимо анализа эффективности СРТ, дополнительно была изучена распространенность ЭКГ-критериев при проксимальной БЛНПГ. С этой целью были проанализированы пациенты с расширением комплекса QRS вследствие хирургического повреждения ЛНПГ. Примером клинической ситуации, при которой может произойти повреждение проксимальных отделов ЛНПГ, является транскатетерная имплантация аортального клапана (ТИАК) [39]. Интраоперационное нарушение проводимости в этом случае связано с близостью аортального клапана к проводящей системе сердца [39]. Calle S, et al. сравнили встречаемость ЭКГ-критериев у пациентов с БЛНПГ после ТИАК (n=59) и у кандидатов на СРТ (n=118). После ТИАК в 100% случаев встречалась БЛНПГ по критерию ESC 2013, в 95% случаев — по Strauss и только у 18% пациентов была выявлена БЛНПГ по критерию AHA [27]. Среди пациентов с БЛНПГ после ТИАК значимо чаще встречалась БЛНПГ по всем трем анализируемым критериям. Схожие результаты были получены в исследовании Римской Е. М. и др. 2023г, БЛНПГ по критерию Strauss встречалась среди 100% пациентов после ТИАК, в связи с чем этот критерий был предложен в качестве наилучшего для определения проксимальной БЛНПГ [28]. Однако без дополнительных неинвазивных критериев БЛНПГ по Strauss не была связана с ответом среди кандидатов на СРТ (ОШ 3,5, 95% ДИ: 0,37-33,3, p=0,3) [28]. Анализ других ЭКГ-критериев в этой группе выполнен не был.
Таким образом, в отличие от критериев БЛНПГ из клинических рекомендаций, критерий Strauss во многих исследованиях продемонстрировал лучшую связь с клиническим и гемодинамическим ответом на СРТ, а также наличием проксимальной БЛНПГ [13][17][18][22][28]. Однако этот критерий характеризуется низкой специфичностью в предсказании обратного ремоделирования на фоне СРТ [22]. Более того, при эндокардиальном картировании МЖП было установлено, что у 39% пациентов с БЛНПГ, определенной по критерию Strauss, регистрируется остаточное проведение электрических импульсов по ЛНПГ [25]. В связи с этим актуален поиск и разработка новых ЭКГ-критериев БЛНПГ для предсказания ответа на СРТ.
Анализ отдельных ЭКГ-признаков БЛНПГ
Хотя существующие критерии БЛНПГ имеют свои особенности и ограничения, каждый конкретный ЭКГ-признак, входящий в состав этих критериев (табл. 1), отражает специфические изменения последовательности активации желудочков сердца при БЛНПГ. Так, замедленное транссептальное проведение косвенно отражает увеличение внутреннего отклонения зубца R ≥60 мс; изменение направления транссептальной активации — отсутствие зубца q в «левых» отведениях, а также монофазный QS в V1; изменение последовательности активации желудочков сердца и U-образный паттерн — зазубрена/сглаженность зубца R или комплекса QRS, а также более редкие признаки в стандартных и грудных отведениях.
Группа исследователей во главе с Perrin M предложила новый диагностический признак, который, по их мнению, позволяет выявить сохранное проведение по проксимальным волокнам ЛНПГ: наличие зубца r ≥1 мм в отведении V1 и/или зубца q ≥1 мм в отведении aVL [40]. В ходе субанализа данных исследования PREDICT авторы установили, что пациенты с БЛНПГ и сохранным поведением, которое было определено с помощью этого ЭКГ-признака, демонстрируют менее выраженный гемодинамический ответ на СРТ в сравнении с пациентами с БЛНПГ и без этого признака [40]. Однако в исследовании Grebmer C, et al. подобной закономерности выявлено не было [41]. Пациенты как с зубцом r ≥1 мм в отведении V1 и/или зубцом q ≥1 мм в отведении aVL (признак сохранного проведения по Perrin M, et al.), так и без этого ЭКГ-признака не продемонстрировали значимых различий ни в отношении гемодинамического ответа, ни в отношении прогноза на фоне СРТ [41].
Помимо разработки новых ЭКГ-признаков, перспективным направлением является независимый анализ уже существующих ЭКГ-признаков. Отечественные исследователи впервые выполнили анализ диагностической ценности ранее предложенных ЭКГ-признаков в предсказании ответа на СРТ [42]. При сравнении отдельных признаков между группами ответа было показано, что многие из них (10 из 17 анализируемых) значимо чаще встречались среди респондеров, которые были определены при снижении КСО ЛЖ на ≥15% за 12-мес. период наблюдения. Отсутствие зубца q в V5-V6 продемонстрировало наибольшие чувствительность (92,31%), прогностическую ценность отрицательного результата (70,59%) и общую точность (73,47%). Этот ЭКГ-признак отражает изменение направления транссептальной активации, встречается в большинстве современных критериев, но не был включен в критерий Strauss. В ходе мультивариантного анализа были выявлены ЭКГ-признаки, независимо связанные с обратным ремоделированием на фоне СРТ: ширина комплекса QRS (ОШ 1,022; 95% ДИ: 1,001-1,043; р=0,040), отсутствие зубца q в V5-V6 (ОШ 4,076; 95% ДИ: 1,071-15,51; р=0,039), наличие дискордантного зубца T (ОШ 4,565; 95% ДИ: 1,708-12,202; р=0,002). Объединение этих ЭКГ-признаков в математическую модель демонстрирует высокую прогностическую способность обратного ремоделирования (AUC=0,81) и значимое увеличение 5-летней выживаемости на фоне СРТ (84,4% vs 50%, p=0,001). Учитывая наибольшую вероятность ответа на СРТ, этот критерий можно отнести к критериям истинной БЛНПГ [42].
Как отмечалось выше, исследование пациентов при впервые возникшей БЛНПГ при хирургическом вмешательстве предоставляет возможность изучения ЭКГ картины проксимальной БЛНПГ. Calle S, et al. в 2021г проанализировали отдельные ЭКГ-признаки у 59 пациентов с БЛНПГ вследствие ТИАК [27]. Авторы отобрали признаки, которые встречались в 100% случаев после операции и объединили их в критерий проксимальной БЛНПГ. Критерий Calle S, et al. включал четыре основных ЭКГ-признака и один вспомогательный, которые представлены в таблице 2. Примечательно, что в качестве вспомогательного ЭКГ-признака исследователи включили отклонение электрической оси сердца влево [27]. Это решение вызывает сомнения, поскольку пациенты, направляемые на ТИАК, часто страдают гипертрофией ЛЖ. В связи с этим более выраженное отклонение влево в сравнении с кандидатами на СРТ, может быть связано с более выраженной гипертрофией ЛЖ в группе пациентов ТИАК, а не связью с проксимальным уровнем блока проведения.
Дополнительный анализ ЭКГ-признаков среди пациентов с БЛНПГ вследствие хирургического вмешательства выполнили Римская Е. М. и др. в 2023г [28]. Исследование включало 58 пациентов с БЛНПГ, возникшей после ТИАК, и 22 пациента с ДКМП, отобранных на СРТ. При анализе ЭКГ-признаков в группе ТИАК авторы отобрали те из них, что встречались в 100% случаев после операции. В результате в критерий проксимальной БЛНПГ были включены три ЭКГ-признака (табл. 2). Выявленная комбинация признаков полностью совпадает с критерием Strauss (табл. 1). В сравнении с критерием Calle S, et al. авторы предлагают более широкий QRS для увеличения эффективности СРТ при отборе пациентов. В дополнение к ЭКГ-критериям Римская Е. М. и др. также проанализировали результаты неинвазивного активационного картирования и предложили два дополнительных признака проксимальной БЛНПГ. Разработанный критерий проксимальной БЛНПГ продемонстрировал относительно сильную статистически значимую связь с положительным эффектом от СРТ среди пациентов с хронической сердечной недостаточностью (критерий Хи-квадрат =5,46, р=0,02, критерий Крамера =0,5, ОШ 15,0, 95% ДИ: 1,32-169,9, р=0,002). Такой подход оказался лучше в предсказании ответа на СРТ, чем использование ЭКГ-критерия.
В приведенных исследованиях сравнивали пациентов с проксимальной БЛНПГ и кандидатов на СРТ с неопределенной локализацией блока проведения. В другом отечественном исследовании пациентов с проксимальной БЛНПГ была проанализирована динамика изменения ЭКГ до и после септальной миоэктомии по поводу гипертрофической кардиомиопатии (ГКМП) [29]. Во время хирургического лечения обструктивной формы ГКМП при трансаортальном доступе формируется изолированное повреждение базальных отделов МЖП без формирования дополнительных ятрогенных линий блока проведения. Такой подход наряду с исследованием пациентов с ТИАК позволяет изучить ЭКГ картину при известной проксимальной локализации блока проведения. В исследование были включены пациенты с узким QRS до операции, с расширением ≥120 мс в послеоперационном периоде [29]. Иссечение небольшого участка миокарда базальных отделов МЖП весом в среднем 4,9±2 г приводило к статистически значимому увеличению ширины комплекса QRS (на 61±14,6 мс) и частоты встречаемости практически всех ЭКГ-признаков БЛНПГ. В ЭКГ-критерий проксимальной БЛНПГ были включены ЭКГ-признаки, соответствующие двум условиям: статистически значимая динамика до/после операции (для исключения признаков, встречающихся и при ГКМП) и 100% встречаемость после септальной миоэктомии. Таким образом, были отобраны три ЭКГ-признака (табл. 2) наряду с шириной QRS ≥120 мс. Выявленные ЭКГ-признаки практически полностью совпали с критерием Calle S, et al., за исключением QS или rS V1, потому что у пациентов с ГКМП этот ЭКГ-признак встречался и до операции в 98% случаев. Также в этот критерий не было включено отклонение электрической оси сердца влево по причинам, описанным выше.
Таким образом, анализ отдельных ЭКГ-признаков БЛНПГ позволяет более точно прогнозировать эффективность СРТ. Однако для увеличения точности диагностики истинной БЛНПГ актуально дополнительно использовать и другие методы неинвазивной диагностики. Исследования, проведенные на пациентах с ТИАК и септальной миоэктомией, предоставили ценную информацию о проксимальной БЛНПГ и помогли разработать новые критерии. Эти критерии, включающие специфические ЭКГ-признаки, могут быть использованы для улучшения отбора пациентов на СПСС. Однако необходимы дальнейшие исследования для валидации этих критериев на более широкой популяции пациентов и оценки их долгосрочной прогностической ценности.
Таблица 2
Новые ЭКГ-критерии проксимальной БЛНПГ
|
Критерии Признаки |
Критерий проксимальной БЛНПГ (Calle S, et al.) |
Критерий проксимальной БЛНПГ (Малишевский и др.) |
Критерий проксимальной БЛНПГ (Римская и др.) |
|
Длительность комплекса QRS ≥ (мс) |
120 |
120 |
ж — 130, м — 140 |
|
QS или rS в V1 |
+ |
— |
+ |
|
Зазубрина/сглаженность в середине QRS, как минимум, в двух отведениях: I, aVL, V1-V2, V5-V6 |
+ |
+ |
+ |
|
Отсутствие зубца q в V5-V6 |
+ |
+ |
— |
|
Дискордантный зубец Т |
— |
+ |
— |
|
Дополнительные критерии |
|||
|
Отклонение электрической оси сердца влево |
+ |
— |
— |
|
Наличие линии блока проведения в передне-перегородочной или задне-боковой области |
— |
— |
+ |
|
Локализация точки поздней активации на базальном или среднем уровне задне-боковой стенки ЛЖ |
— |
— |
+ |
Сокращения: БЛНПГ — блокада левой ножки пучка Гиса, ЛЖ — левый желудочек.
Заключение
Диагностика БЛНПГ является сложной задачей в связи с гетерогенностью паттернов активации желудочков сердца при схожей ЭКГ картине и несогласованности существующих ЭКГ-критериев. Развитие СПСС требует разработки дополнительных ЭКГ-критериев для определения проксимальной и дистальной локализации блока проведения. В данный момент отечественными и зарубежными научными группами были предложены новые ЭКГ-критерии, которые требуют дополнительной валидации.
Учитывая сложность и многообразие форм БЛНПГ, а также их влияние на выбор терапии, необходимы дальнейшие исследования для разработки новых ЭКГ-критериев, а также других неинвазивных диагностических критериев для улучшения отбора пациентов на СРТ.
Отношения и деятельность. Государственное задание А22-122012000074-3: Разработка программы персонифицированного подхода к выбору оптимальной стратегии лечения и профилактики пациентов с гипертрофической кардиомиопатией.
1. Tung, Roderick & Sung, Weiping & Shatz, Nathan & Upadhyay, Gaurav. (2021). B-PO02-186 high resolution mapping of lv activation during left bundle branch block: correlation of transseptal breakthrough and strauss criteria. Heart Rhythm. 18. S174. doi:10.1016/j.hrthm.2021.06.439.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Малишевский Л.М., Лебедев Д.С. Электрокардиографические признаки блокады левой ножки пучка Гиса и прогнозирование ответа на бивентрикулярную стимуляцию и стимуляцию проводящей системы сердца. Российский кардиологический журнал. 2024;29(4S):6182. https://doi.org/10.15829/1560-4071-2024-6182. EDN: OBRYEU
Скопировать