Артериальная гипертензия у беременных: дискуссионные вопросы национальных и международных рекомендаций
Определение и классификация
Определение артериальной гипертензии (АГ) у беременных не всегда было стандартизировано. В соответствии с рекомендациями “Национальной рабочей группы по образованию в области высокого артериального давления при беременности” (2000) критерием АГ у беременных являются уровни систолического артериального давления (АД) (САД) ?140 мм рт.ст. и/или диастолического АД (ДАД) ?90 мм рт.ст. [1]. Необходимо подтвердить повышение уровня АД как минимум двумя измерениями [2].
В настоящее время выделяют следующие формы АГ беременных: хроническую АГ (ХАГ), гестационную АГ (ГАГ), преэклампсию (ПЭ) и ПЭ, развившуюся на фоне ХАГ [3][4][5][6][7][8][9][10][11][12][13].
ХАГ — это АГ, диагностированная до наступления беременности или до 20 нед. ее развития. Критерием ХАГ служит повышение АД ?140/90 мм рт.ст. до беременности или в течение первых 20 нед., которое не исчезает после родов, обычно сохраняется в течение >42 дней после родов.
ГАГ — определяется как изолированное повышение САД ?140 мм рт.ст. и/или ДАД >90 мм рт.ст. при измерении не менее 2 раз с интервалом в 4 ч, развивающееся после 20-й нед. у женщин с нормальным уровнем АД до беременности и не сопровождающееся протеинурией.
ПЭ — мультисистемное патологическое состояние, осложняющее течение беременности, родов и послеродового периода, характеризующееся повышением после 20-й нед. беременности САД ?140 мм рт.ст. или ДАД ?90 мм рт.ст. при измерении не менее 2 раз через 4 ч у женщин, имевших нормальное АД до наступления беременности, в сочетании с одним и более из следующих параметров:
— протеинурия (?30 мг/моль протеина к уровню креатинина; ?300 мг/сут.; или показатель индикаторной полоски ?2+);
— поражение почек (уровень креатинина ?90 мкмоль/л);
— поражение печени (повышенный уровень транс — аминаз, например, аланинаминотрансфераза или аспартатаминотрансфераза >40 МЕ/л), возможно, с болью в правом верхнем квадранте живота или эпигастральной области;
— неврологические осложнения (например, изменение психического состояния, слепота, инсульт, клонус, сильные головные боли и персистентная скотома);
— гематологические осложнения (тромбоцитопения — количество тромбоцитов <150000/мкл, диссеминированное внутрисосудистое свертывание, гемолиз);
— маточно-плацентарная дисфункция (например, задержка внутриутробного роста плода, нарушение кровотока в артерии пуповины по данным допплеровского исследования или мертворождение).
ПЭ на фоне ХАГ диагностируется у беременных с ХАГ при присоединении признаков ПЭ.
Несмотря на то, что многие исследователи поддерживают позицию, согласно которой АГ при беременности можно классифицировать как ХАГ, если она сохраняется >12 нед. после родов [14][15], эксперты Российского кардиологического общества (РКО) и Европейского кардиологического общества (ESC) предлагают считать ХАГ гипертензию, сохраняющуюся в течение 6 нед. (42 дней) после родов, что соответствует послеродовому периоду [5][13]. Кроме того, рекомендации ESC включают категорию “антенатально неклассифицируемая АГ”, которая возникает до 20 нед., но еще повторно не классифицирована через 42 дня после родов [5]. В ряде рекомендаций выделяют также “гипертензию белого халата”, “маскированную АГ”, HELLP-синдром (гемолиз, повышение уровня печеночных ферментов, низкий уровень тромбоцитов), эклампсию [4][6][7][8][9][10][11][12]. Канадское общество акушеров-гинекологов в рекомендациях 2014г также выделяет ХАГ и ГАГ с наличием/отсутствием сопутствующих заболеваний [6].
Помимо уточнения формы АГ важная роль принадлежит оценке её степени. Классификация степени повышения уровня АД у беременных может использоваться для характеристики степени АГ при любой ее форме (ХАГ, ГАГ, ПЭ).
Выделяют умеренную (нетяжелую) и тяжелую АГ [14]:
— умеренная АГ устанавливается при повышении САД 140-159 мм рт.ст. и/или ДАД 90-109 мм рт.ст.;
— тяжелая АГ соответствует уровням САД ?160 мм рт.ст. и/или ДАД ?110 мм рт.ст.
В некоторых рекомендациях выделяют 3 степени повышения АД: легкая (140-149/90-99 мм рт.ст.), умеренная (150-159/100-109 мм рт.ст.) и тяжелая (?160/110 мм рт.ст.) [10].
Выделение двух степеней АГ, умеренной и тяжелой, при беременности имеет принципиальное значение для оценки прогноза, выбора тактики ведения, лечения и родовспоможения [11, 12]. Кроме того, известно, что тяжелая АГ при беременности ассоциируется с высоким риском развития инсульта [2][10] и гипертензивной энцефалопатии даже при более низких уровнях АД в сравнении с общей популяцией [15].
Следует отметить, что Американская коллегия акушеров-гинекологов (ACOG) в своих последних рекомендациях признала, что определения АГ у беременных противоречат изменённым диагностическим критериям Американской коллегии кардиологов (ACC) и Американской кардиологической ассоциации (AHA), выделившим I стадию АГ при уровне АД 130-139/80-89 мм рт.ст. и 2 стадию при уровне АД 140/90 мм рт.ст. [16], что требует пересмотра диагностических критериев [3][12]. Остальные общества, опубликовавшие свои рекомендации после 2017г, не изменили диагностические критерии, несмотря на рекомендации ACC/AHA.
Целевое АД
В соответствии с международными рекомендациями нет никаких сомнений в том, что целевыми уровнями АД являются значения ниже 160/110 мм рт.ст. [3][4][5][6][7][8][9][10]. Кросс-секционное исследование более чем 81 млн госпитализаций показало, что гипертензивные расстройства при беременности увеличивают риск инсульта в 5,2 раза [17]. Кроме того, исследование CHIPS (Control of Hypertension In Pregnancy Study) подтвердило, что тяжелая АГ ассоциирована с более высокими показателями материнской смертности, потери беременности, преждевременных родов, рождения маловесных детей, оказания помощи новорожденным спустя 48 ч и ряда других неблагоприятных акушерских исходов по сравнению с таковыми при нетяжелой АГ независимо от наличия ПЭ [18].
Вопрос агрессивного лечения умеренной (нетяжёлой) АГ при рассмотрении различных рекомендаций остается спорным [3][5][6][8][10][19]. Различия связаны с нехваткой данных, которые четко подтверждают явные преимущества и возникающие риски при достижении различных уровней АД. В недавнем Кокрановском систематическом обзоре антигипертензивных препаратов в лечении лёгкой и умеренной АГ во время беременности проанализировано 31 исследование с участием 3485 женщин, в которых сравнивались различные лекарственные средства с плацебо или отсутствием лечения, а также 29 исследований с включением 2774 женщин, сравнивающих антигипертензивные препараты между собой. Результаты обзора показали, что применение антигипертензивных средств вдвое уменьшает число женщин, у которых в последующем развивается тяжелая АГ, однако влияние на уменьшение частоты акушерских осложнений и неблагоприятных исходов беременности оказалось недоказанным. Полученные данные объясняются разными подходами в терминологии, а также малочисленностью и гетерогенностью групп, включенных в обзор [20].
В исследовании CHIPS (рандомизированное контролируемое открытое многоцентровое международное исследование) было включено примерно 1 тыс. женщин с ХАГ или ГАГ (ДАД 90-105 мм рт.ст. или 85-105 мм рт.ст. при приёме антигипертензивных препаратов), распределенных на 2 группы с “менее строгим контролем” (целевой ДАД <100 мм рт.ст.) и с “жёстким контролем” (целевой ДАД <85 мм рт.ст.). Совокупные первичные исходы (потеря беременности или потребность в неонатальной помощи спустя 48 ч после родов в течение первых 28 дней) и вторичные исходы (серьезные осложнения со стороны матери в первые 6 нед. после родов) не различались в обеих группах. Однако тяжелая АГ чаще развивалась в группе “менее строгого контроля”, чем в группе “жёсткого контроля” [21]. Эксперты попрежнему обсуждают результаты данного исследования, хотя проведенные два субанализа подтверждают, что профилактика тяжелой АГ имеет преимущества как для матери, так и для ребенка [18][22].
В США в настоящее время проводится ещё более крупное многоцентровое рандомизированное контролируемое исследование CHAP (Chronic Hypertension and Pregnancy), включающее беременных женщин с ХАГ, которым назначается или не назначается монотерапия при уровне АД 140-159/90-104 мм рт.ст. Кроме того, у пациентов в группе назначения антигипертензивной терапии оценивают конечные точки при достижении целевого АД <140/90 мм рт.ст. или <160/105 мм рт.ст. Первичные конечные точки включают неблагоприятные перинатальные исходы вплоть до 2 нед. после родов (смерть плода и новорождённого, тяжелая ПЭ, отслойка плаценты и преждевременные роды <35 нед. беременности) и рождение маловесного ребёнка (вес при рождении <10-го процентиля). Ожидается, что в исследовании примут участие 4700 больных, что почти в 5 раз больше, чем в исследовании CHIPS [23].
С учетом того, что почти 75% участников, включенных в исследование CHIPS, имели ХАГ, результаты исследования CHAP, вероятно, смогут подтвердить или опровергнуть его результаты, несмотря на то, что дизайны исследований отличаются. Если результаты исследования CHAP в конечном итоге подтвердят преимущества более агрессивной тактики контроля АД, вероятно, потребуется последующий анализ безопасности и преимуществ контроля АД во время беременности при более низких целевых уровнях АД, определенных в рекомендациях AHA/ACC 2017г по контролю АД.
Лечение тяжёлой АГ
В соответствии с различными рекомендациями для снижения АД у беременных ранее использовались такие препараты, как гидралазин, блокаторы кальциевых каналов, метилдопа, урапидил, празозин, изосорбид и даже сульфат магния [24]. В последние годы чаще используются внутривенные формы лабеталола, гидралазин, блокаторы кальциевых каналов (например, нифедипин короткого действия) и метилдопа (не являющийся средством первой линии в большинстве стран).
Проведенные 2 метаанализа по изучению эффективности гидралазина, включавшие 35 исследований (3573 женщины) и 21 исследование (893 женщины), показали, соответственно, что беременные, принимающие блокаторы кальциевых каналов, по сравнению с гидралазином, имели меньшую вероятность повышения АД [24][25]. Было также отмечено, что применение гидралазина связано с увеличением неблагоприятных исходов со стороны как женщины (таких как артериальная гипотензия, кесарево сечение, отслойка плаценты, олигурия), так и плода (влияние на частоту сердечных сокращений (ЧСС) и более низкие показатели по шкале Апгар в течение 1-й минуты по сравнению с другими антигипертензивными препаратами [25]).
По данным метаанализа семи исследований (с участием 363 женщин) при сравнении перорального нифедипина с внутривенным лабеталолом было обнаружено только статистически значимое снижение частоты побочных эффектов со стороны матери при приеме нифедипина (относительный риск (ОР) 0,57; 95% доверительный интервал (ДИ) 0,35-0,94), при этом не было статистически значимых различий по контролю уровня АД, частоте материнской заболеваемости или смертности, а также влияния на перинатальные показатели [26].
В тройном слепом плацебо-контролируемом исследовании на небольшой популяции (34 пациента) с диагнозом тяжёлой ПЭ на фоне лечения сульфатом магния сравнивали сублингвальный нифедипин и внутривенный нитроглицерин. Исследование показало более выраженный и быстрый гипотензивный ответ с меньшей вариабельностью в группе нитроглицерина и отсутствие значимых изменений ЧСС плода, несмотря на терапию вазодилататорами, с сопоставимой частотой побочных эффектов у плода и матери в обеих группах [27].
Таким образом, все 3 агента (нифедипин, лабетолол, гидралазин) продолжают входить в рекомендации международных сообществ [3][4][5][6][7][9][10]. В соответствии с российскими клиническими рекомендациями (2020) для пероральной терапии следует использовать метилдопу или нифедипин замедленного высвобождения. Применение диуретиков не показано, т.к. при ПЭ уменьшается объем циркулирующей крови. Для предотвращения эклампсии и лечения судорог рекомендовано внутривенное введение сульфата магния [13].
Тяжёлая АГ во время беременности без признаков органной дисфункции расценивается как неосложненный гипертонический криз (“urgency”). АД необходимо снижать менее уровня 160/110 мм рт.ст.
с первоначальным снижением на 25% в первые часы лечения и более постепенным снижением в последующие часы. Более интенсивное снижение АД может подвергнуть плод риску вследствие недостаточной перфузии. Напротив, тяжелая АГ, связанная с органной дисфункцией в виде отёка лёгких или острого повреждения почек, считается осложненным гипертоническим кризом (“emergency”), и АД в таком случае следует снижать намного быстрее.
Особое внимание следует уделять предотвращению резкого падения АД, которое может вызвать осложнения у матери или плода в результате падения ниже критических порогов перфузии. Повышенное АД следует снижать до уровня САД 130-140 мм рт.ст./ ДАД 80-90 мм рт.ст. со скоростью 10-20 мм рт.ст. каждые 10-20 мин.
При ПЭ, осложненной отёком лёгких, ESC и РКО рекомендуют использовать нитроглицерин в виде внутривенной инфузии [13][28]. АД следует снижать со
скоростью примерно 30 мм рт.ст. в течение 3-5 мин, после чего следует снижать скорость до достижения целевого АД <140/90 мм рт.ст. [29]. Длительность его применения не должна составлять >4 ч из-за отрицательного воздействия на плод и риска развития отёка мозга у матери.
У пациентов с ПЭ с признаками органной дисфункции (например, тяжелой АГ и протеинурией или АГ и неврологическими осложнениями) или эклампсией рекомендуется немедленно назначать
сульфат магния для профилактики судорог [3][12]. Эта рекомендация была определена по данным рандомизированного плацебо-контролируемого исследования Magpie Trial, в котором >10 тыс. женщин получали сульфат магния либо плацебо при наличии АД >140/90 мм рт.ст. и протеинурии не менее 30 мг/дл. В результате применения сульфата магния было показано снижение риска ПЭ на 58% и уменьшение материнской смертности по сравнению с плацебо [30]. Эти данные подтверждены в другом исследовании, которое продемонстрировало, что у женщин с тяжёлой ПЭ частота эклампсии была ниже на фоне назначения сульфата магния по сравнению с больными, получавшими блокатор кальциевых каналов нимодипин [31].
Данные по применению сульфата магния для профилактики эклампсии у женщин с ПЭ без признаков органной дисфункции более противоречивы и показывают большое количество пациентов (~100), необходимых для лечения для предотвращения одного случая эклампсии [3][8].
Лечение умеренной (нетяжёлой) АГ
В случаях умеренной (нетяжёлой) АГ препаратами первого ряда являются метилдопа, лабеталол и нифедипин [3][4][5][6][7][8][9][10]. Очевидно, что существуют определенные различия в рекомендациях, что обусловлено отсутствием данных о преимуществах конкретного лекарственного препарата для предотвращения неблагоприятных исходов матери и плода [3][4][5][6][7][9][10][11][12][13].
Метилдопа рекомендуется в качестве средства первой линии для контроля АД в соответствии с американскими, канадскими, европейскими, австралийскими/новозеландскими и российскими рекомендациями [3][4][5][9][10][11][12][13][32][33]. Препарат изучался с 1960-х годов и имеет долгосрочные данные о безопасности у детей, чьи матери принимали его во время беременности [34]. Проспективное когортное исследование, оценивающее исходы беременности в первом триместре воздействия, показало, что его применение не сопровождалось тератогенными эффектами, однако отмечался более высокий уровень самопроизвольных выкидышей и преждевременных родов [33]. По данным Кокрановского обзора по применению антигипертензивных препаратов для лечения лёгкой и умеренной АГ, применение метилдопы уступает блокаторам кальциевых каналов и бета-блокаторам в отношении предотвращения тяжелой АГ (ОР 0,70; 95% ДИ 0,56-0,88, 11 исследований, 638 женщин) и может быть связано с большей частотой кесаревых сечений (скорректированный ОР 0,84; 95% ДИ, 0,84-0,95, 13 исследований, 1330 женщин) [20]. Тем не менее, субанализ исследования CHIPS показал, что женщины, получавшие метилдопу в сравнении с лабеталолом, имели лучшие первичные и вторичные исходы, включая массу тела новорожденного, меньшую частоту тяжёлой АГ, ПЭ и преждевременных родов [35]. Кроме того, ретроспективное когортное исследование показало, что применение метилдопы было связано с меньшим числом неблагоприятных исходов у детей, включая респираторный дистресс синдром, судороги и сепсис, по сравнению с пероральным лабеталолом [36]. Таким образом, метилдопа остается препаратом выбора, пока не будет получено более убедительных доказательств превосходства других антигипертензивных средств.
Пероральный лабеталол считается препаратом первого ряда при умеренной (нетяжёлой) АГ во время беременности в соответствии с международными рекомендациями [3-7, 9] и фактически является единственным лекарственным средством первого ряда, рекомендованным британскими руководствами [10]. В проспективном обсервационном исследовании примерно 75% женщин имели положительный ответ на монотерапию пероральным лабеталолом [37]. В более ранних рандомизированных исследованиях, непосредственно сравнивавших его с метилдопой, не было обнаружено его преимуществ в отношении безопасности и эффективности [38][39], а в другом исследовании показано пограничное превосходство лабеталола в профилактике протеинурии, тяжелой АГ и госпитализаций во время беременности; лабеталол также был независимо связан с меньшим количеством совокупных неблагоприятных материнских и перинатальных событий [40]. Кроме того, исследование, в котором сравнивались амбулаторные показатели АД у беременных, принимающих перорально лабеталол или нифедипин замедленного высвобождения, продемонстрировало, что в группе лабеталола отмечалось более частое снижение ДАД ниже 80 мм рт.ст., что может ассоциироваться с ухудшением маточно-плацентарной перфузии [41]. ?-адреноблокаторы (?-АБ) считаются препаратами первого ряда в Канаде (ацебутолол, метопролол, пиндолол, пропранолол) [4]. Австралийские/новозеландские рекомендации включают окспренолол в первую линию лечения нетяжёлой АГ во время беременности [10]. Однако существуют некоторые противоречия в отношении тератогенности и влияния ?-АБ на массу тела новорождённых. Известно, что атенолол вызывает задержку внутриутробного развития [41], и многие сообщества не рекомендуют его применять [3][10][11][12]. В 2003г Кокрановский обзор применения пероральных ?-АБ для лечения лёгкой и умеренной АГ у беременных (12 исследований, 1346 женщин), в сравнении с отсутствием лечения или плацебо, показал повышенный риск рождения маловесных детей (ОР 1,36; 95% ДИ, 1,02-1,82) [42]. Однако недавнее ретроспективное когортное исследование показало, что после поправки на возраст матери, индекс массы тела и сопутствующие заболевания не было никакой связи между применением ?-АБ и сердечными аномалиями плода [43]. Кроме того, международное когортное исследование, которое объединило >15 тыс. женщин, применявших ?-АБ в первом триместре беременности, не выявило значимого увеличения риска врождённых пороков развития (ОР 1,07; 95% ДИ 0,89-1,30) [44]. В отличие от этих данных другое когортное исследование, в которое было включено >10 тыс. женщин, использовавших ?-АБ на поздних сроках беременности, показало, что риск неонатальной брадикардии и гипогликемии был выше (OP >1) в группе применения ?-АБ (лабеталол, метопролол и атенолол), за исключением неонатальной брадикардии в группе с применением метопролола (ОР 0,59; 95% ДИ 0,32-1,09) [45].
Блокаторы кальциевых каналов, в частности нифедипин пролонгированного действия, являются лекарственными средствами первой линии в большинстве руководств [3][4][5][6][7][8][9][10]. Проспективное когортное исследование показало минимальный профиль тератогенности при приеме блокаторов кальциевых каналов в первом триместре [46]. Кроме того, было выявлено, что они превосходят метилдопу в отношении контроля АД и, возможно, безопаснее, чем лабеталол, в отношении достижения целевых уровней АД [20]. В одном рандомизированном контролируемом клиническом исследовании сравнивался пероральный прием нифедипина и лабеталола у беременных с ХАГ. В группе нифедипина отмечено более выраженное снижение центрального аортального давления (на 7,4 мм рт.ст.) при сопоставимом снижении периферического АД на обеих руках, а также незначительное увеличение количества госпитализаций в отделение интенсивной терапии и побочных эффектов со стороны новорождённых [47].
Данные по амлодипину, другому дигидропиридиновому блокатору кальциевых каналов, очень ограничены. В серии случаев его применения в I триместре беременности был сделан вывод о том, что амлодипин, по-видимому, не обладает тератогенным эффектом [48], а небольшое пилотное исследование, в котором сравнивали амлодипин с фуросемидом для лечения ХАГ, не выявило различий между ними по материнским или перинатальным исходам [49].
Послеродовая АГ
У большинства женщин АД нормализуется в течение первых дней после родов (29-57% в течение первых трёх дней, 50-85% в течение первой недели), причём сроки нормализации зависят от степени тяжести состояния [50]. В течение первых 5-7 сут. после родов на фоне физиологического увеличения объема циркулирующей крови появляется опасность повышения АД, что требует проведения тщательного мониторинга АД. В исследовании с участием 151 женщины было показало, что у 5,7% из них развилась ПЭ или эклампсия после родов [50]. Другое исследование показало, что из 22 пациенток, поступивших в отделение неотложной помощи с ПЭ в течение 4 нед. после родов, 55% случаев были de novo [51]. Послеродовая АГ, помимо гипертензивных нарушений во время беременности, может быть обусловлена ятрогенными причинами: приемом нестероидных противовоспалительных препаратов, гиперволемией (после регионарной анестезии), болью (при неадекватной анальгезии) и тревожностью [52][53].
Все антигипертензивные средства, принимаемые кормящей матерью, экскретируются с грудным молоком, однако большинство из них присутствует там в очень низких концентрациях, за исключением пропранолола и нифедипина, концентрация которых в молоке аналогична концентрации в материнской плазме [5][28].
Для лечения тяжелой послеродовой АГ рекомендуется проводить антигипертензивную терапию до целевых значений САД ниже 160 мм рт.ст. и ДАД <110 мм рт.ст. с возможным использование урапидила и нитропруссида натрия [10][54][55]. Однако данные препараты могут быть использованы в нашей стране в соответствии с инструкцией по применению только после регистрации в установленном порядке. При тяжёлой форме АГ или при сосудистых кризах (>150-160/100-110 мм рт.ст. на протяжении >15 мин или изолированном повышении ДАД >120 мм рт.ст. с поражением органов-мишеней) необходимо начинать терапию с предпочтительным применением препаратов быстрого действия (нифедипин, нитроглицерин, нитропруссид натрия внутривенно) [3][56]. В соответствии с российскими клиническими рекомендациями по АГ у взрослых для лечения послеродовой АГ можно использовать любые классы антигипертензивных препаратов. Однако следует избегать применения метилдопы из-за риска развития послеродовой депрессии. В нашей стране проблема осложняется тем, что практически все препараты имеют противопоказания в инструкции по медицинскому применению, что затрудняет назначение медикаментозной коррекции на фоне лактации. В данном аспекте представляют клинический интерес немедикаментозные методы лечения АГ у этой категории пациентов, в т.ч. с учетом рекомендаций по тщательному контролю АД.
Коррекция АД с помощью электростимулятора чрескожного “АВР-051” (ООО “Инферум”, г. Екатеринбург, Россия; регистрационное удостоверение № РЗН 2016/3776 от 31 марта 2016г) представляет собой неинвазивное физиотерапевтическое воздействие импульсным электрическим током низкой частоты в зонах дистальных отделов дерматомеров, расположенных на предплечье левой руки, продолжительностью 5 мин дважды в день [57].
Целью нашего исследования явилась оценка влияния неинвазивной чрескожной электростимуляции на показатели АД и ее безопасность у родильниц в послеродовом периоде.
Рабочая гипотеза: применение “АВР-051” в дополнение к стандартной антигипертензивной терапии позволяет улучшать контроль АД в течение 14 дней после родов.
Критерии включения:
1) возраст от 18 до 44 лет,
2) наличие АГ — повышение АД ?140/90 мм рт.ст. как минимум при двухкратном измерении с интервалом не менее 4-х ч,
3) согласие на участие в исследовании.
Критерии исключения:
1) ассоциированные клинические состояния (инсульты, инфаркты и т.д.),
2) острые лихорадочные состояния,
3) тяжёлые нарушения функций жизненно важных органов,
4) повреждение кожных покровов в месте наложения прибора.
Алгоритм проведения исследования
1. 1-3 день после родов:
— отбор пациентов, получение информированного согласия, инструктаж, получение аппаратов “АВР-051” и дневников самоконтроля АД.
2. В течение 14 дней после родов:
— применение аппарата “АВР-051” 2 раза/сут. (утро, вечер), дневников самоконтроля АД с ведением графика, мониторинг по телефону. Максимальная длительность курса процедур “АВР-051” — 14 дней.
Результаты и оценка результатов клинических испытаний
В группу воздействия вошли 8 женщин с различными формами АГ, которым проводилась неинвазивная чрескожная электростимуляция с помощью аппарата “АВР-051” наряду с принимаемыми антигипертензивными препаратами.
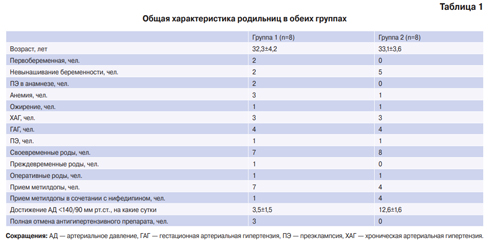
В группу сравнения нами были включены 8 женщин с АГ, сопоставимые по возрасту и сопутствующей патологии, которые принимали только антигипертензивные препараты без воздействия аппаратом “АВР-051” (табл. 1).
Таблица 1
Общая характеристика родильниц в обеих группах
|
|
Группа 1 (n=8) |
Группа 2(n=8) |
|
Возраст, лет |
32,3±4,2 |
33,1±3,6 |
|
Первобеременная, чел. |
2 |
0 |
|
Невынашивание беременности, чел. |
2 |
5 |
|
ПЭ в анамнезе, чел. |
2 |
0 |
|
Анемия, чел. |
3 |
1 |
|
Ожирение, чел. |
1 |
1 |
|
ХАГ, чел. |
3 |
3 |
|
ГАГ чел. |
4 |
4 |
|
ПЭ, чел. |
1 |
1 |
|
Своевременные роды, чел. |
7 |
8 |
|
Преждевременные роды, чел. |
1 |
0 |
|
Оперативные роды, чел. |
1 |
1 |
|
Прием метилдопы, чел. |
7 |
4 |
|
Прием метилдопы в сочетании с нифедипином, чел. |
1 |
4 |
|
Достижение АД <140/90 мм рт.ст., на какие сутки |
3,5±1,5 |
12,6±1,6 |
|
Полная отмена антигипертензивного препарата, чел. |
3 |
0 |
Сокращения: АД — артериальное давление, ГАГ — гестационная артериальная гипертензия, ПЭ — преэклампсия, ХАГ — хроническая артериальная гипертензия.
В группе 1 в 7 случаях беременности завершались своевременными родами с рождением здоровых детей, в 1 случае (при ПЭ) проведено экстренное кесарево сечение на сроке 36-37 нед. с рождением нормального ребёнка. В группе 2 7 беременностей завершились своевременно, в одном случае было проведено экстренное кесарево сечение на сроке 38 нед. в связи с ПЭ и отслойкой нормально расположенной плаценты. Среди принимаемых препаратов на момент включения родильницы продолжали монотерапию метилдопой (допегитом) в дозе от 500 до 1000 мг или в сочетании с пролонгированным нифедипином в дозе от 30 до 60 мг/сут.
Динамика показателей АД и ЧСС у родильниц в сравниваемых группах представлена в таблице 2.
Таблица 2
Показатели АД и частоты сердечных сокращений у родильниц в сравниваемых группах
|
Показатель |
Группа 1 (воздействие) |
|
|
Группа 2 (сравнение) |
|
|
||
|
|
1-е сут. |
7-е сут. |
14-е сут. |
Эффект |
1-е сут. |
7-е сут. |
14-е сут. |
Эффект |
|
САД |
141,5±8,2 |
129,3±4,4 |
122,3±4,8 |
-19,2 |
143,6±76 |
141,2±5,8 |
133,3±5,4 |
-13,3 |
|
ДАД |
90,9±3,0 |
80,5±3,1 |
79 5±2 3 |
-10,4 |
93±3,5 |
875±4,8 |
86,0±4,3 |
-7 |
|
ЧСС |
84,3±6,2 |
80,1±6,1 |
78,8±3,8 |
—5,5 |
86,3±3,5 |
80,0±5,7 |
79,3±6,5 |
-6,3 |
Сокращения: ДАД — диастолическое артериальное давление, САД — систолическое артериальное давление, ЧСС — частота сердечных сокращений.
В результате проведенного испытания медицинского изделия Электростимулятор чрескожный для коррекции АД “ABP-051” в лечении родильниц с различными формами АГ в виде курсового лечения в течение 2 нед. на примере серии родильниц с нетяжёлой АГ можно сделать следующие выводы:
1) достижение целевых уровней АД <140/90 мм рт.ст. наблюдалось уже к 3-5 дню послеродового периода в отличие от группы сравнения, где достижение показателей обеспечивалось только к 10-14 дню на фоне стандартного подхода;
2) минимизация дозы принимаемых антигипертензивных препаратов, преимущественно метилдопы (250-500 мг) у 5 из 8 родильниц, а у 3 женщин — с последующим полным отказом от приема препарата спустя 14 дней динамического наблюдения; в группе сравнения уменьшить дозу принимаемых препаратов, которые нередко назначались в форме комбинированной терапии, не удавалось;
3) обеспечение положительной динамики показателей систолического и ДАД уже спустя 1 нед. в группе воздействия и отсутствие значимой динамики в группе стандартного подхода;
4) безопасность применения медицинского изделия у родильниц ввиду отсутствия побочных эффектов при его использовании во всех случаях.
Для оценки эффективности данного метода контроля АД у женщин в послеродовом периоде необходимо проведение дальнейших исследований.
Заключение
Международное общество по изучению АГ у беременных (ISSHP) начиная с 1998г активно изучает подходы различных обществ к проблеме АГ у беременных [58]. До сих пор существуют расхождения в правилах измерения АД, критериях протеинурии и даже терминологии, используемой для классификации гипертензивных нарушений при беременности [3][4][5][6][7][8][9][10][11][12][13]. Всё это отражает необходимость дальнейших исследований, прежде чем будет достигнут консенсус в отношении подходов к диагностике и лечению различных форм АГ у беременных. Несмотря на отличия в рекомендациях различных международных сообществ, в целом, существует консенсус в отношении подходов ведения беременных с тяжёлой АГ и умеренной (нетяжёлой) АГ с признаками органной дисфункции. Тем не менее, целевые уровни АД у беременных остаются предметом дискуссии. В дополнение к исследованиям с прямым сравнением различных антигипертензивных препаратов, необходима разработка целенаправленных персонифицированных стратегий по ведению беременных с различными формами АГ.
Отношения и деятельность: авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Благодарности. Исследование влияния курсового применения стимулятора “АВР-051” на показатели артериального давления у женщин с АГ в послеродовом периоде проводится при поддержке Российского научного медицинского общества терапевтов (РНМОТ) и OOO “Инферум” (г. Екатеринбург, Россия).
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Чулков В.С., Мартынов А.И., Кокорин В.А. Артериальная гипертензия у беременных: дискуссионные вопросы национальных и международных рекомендаций. Российский кардиологический журнал. 2020;25:4181. https://doi.org/10.15829/1560-4071-2020-4181
Скопировать