Изучение ассоциации полиморфизмов гена ADRB2 (rs1042713 и rs1042714) в развитии нарушений ритма сердца и проводимости у профессиональных спортсменов
Аннотация
Полиморфизмы гена ADRB2, кодирующего β2-адренорецепторы, играют важную роль в регуляции вегетативной нервной системы и гемодинамических реакциях в ответ на физическую нагрузку. Аллели Arg16/Gly16 rs1042713 и Gln27/Glu27 rs1042714 различаются по экспрессии и функциям, что подтверждено в исследованиях in vitro и in vivo, и оказывают влияние на развитие нарушений ритма сердца и проводимости в профессиональном спорте. Аллель Gly16 может вызывать электрическую нестабильность миокарда и аритмии, особенно при хронических нагрузках. Аллель Arg16 ассоциирован с повышенной исходной симпатической активностью и более интенсивной гемодинамической реакцией на стресс, что также может являться фактором риска электрической нестабильности миокарда. Для более глубокого понимания роли генетических вариантов ADRB2 в качестве проаритмогенных маркеров у спортсменов необходимы дальнейшие исследования.
Регулярная аэробная физическая активность ассоциируется со снижением риска развития сердечно-сосудистых и ряда онкологических заболеваний, а также общей и сердечно-сосудистой смертности в общей популяции [1-3]. В то же время высокоинтенсивный тренировочный процесс в большом спорте характеризуется экстремальными физическими нагрузками, включающими сложные техники физической активности, что приводит к адаптивному структурно-функциональному ремоделированию миокарда, которое может лежать в основе различных нарушений ритма сердца.
Цель исследования: провести анализ имеющихся современных данных о роли полиморфизмов rs1042713 и rs1042714 гена ADRB2 в развитии нарушений сердечного ритма и проводимости у лиц, профессионально занимающихся спортом.
Методология исследования
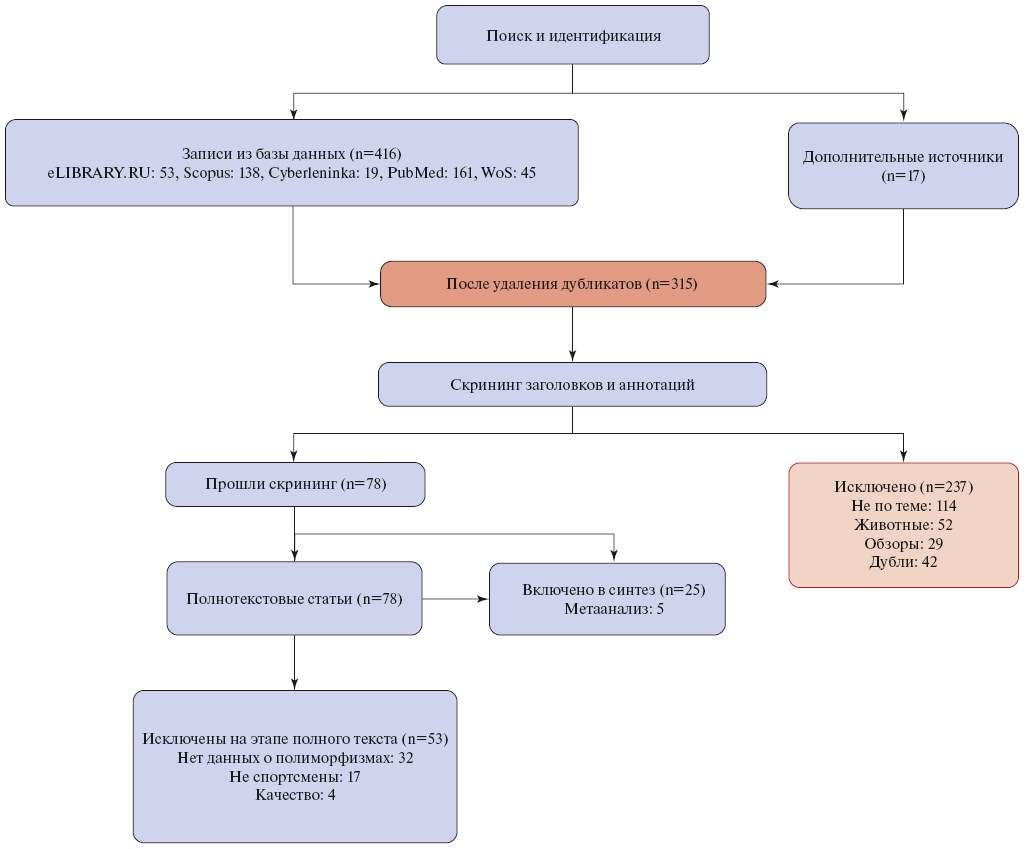
Проведен систематический поиск и анализ, посвященный изучению ассоциативной роли полиморфизмов rs1042713 и rs1042714 гена ADRB2 с развитием нарушений ритма сердца и проводимости у профессиональных спортсменов. Большинство источников взято для обзора за последние 5 лет, а также имеются единичные редкие и высокоинформативные источники по теме за 20 лет. Анализ литературных источников проводится через базы eLIBRARY.RU, Scopus, Cyberleninka, PubMed, Web of Science. Ключевые поисковые термины: «ARBD2 polymorphism», «rs1042713», «rs1042714», «arrhythmia», «cardiac arrhythmia», «conduction disturbance», «sports genetics». Критериями включения служили оригинальные исследования, систематические обзоры и метаанализы, посвященные изучению генетических полиморфизмов ARBD2 у спортсменов. Исключались из анализа исследования с малым объемом выборки, дублирующие публикации, не относящиеся к спортивной медицине (рис. 1).

Рис. 1. Схема PRISMA. Поток отбора литературы.
Результаты
Развитие нарушений ритма сердца и проводимости в большом спорте
В ряде эпидемиологических исследований была продемонстрирована связь длительных интенсивных тренировок с нарушениями сердечного ритма, среди которых наиболее часто упоминаются синусовая брадикардия, экстрасистолии, фибрилляция предсердий (ФП), а также внезапная сердечная смерть. В крупном исследовании Boraita A, et al. (2022) оценивалась частота нарушений сердечного ритма среди 6579 профессиональных спортсменов, 654 из которых прошли углубленное обследование, включающее холтеровское мониторирование сердечного ритма и эхокардиографию [4].
Согласно проведенному анализу мониторирования сердечного ритма, наиболее часто регистрируемым нарушением была синусовая брадикардия, которая наблюдалась у 95,6% обследованных, а брадикардия с частотой <30 ударов в минуту в ночные часы встречалась у 9% спортсменов. Одиночные предсердные и желудочковые экстрасистолы встречались у 61,9 и 39,4% спортсменов, парные желудочковые экстрасистолы зарегистрированы у 10,7% выборки, при этом частота групповых (>3) желудочковых экстрасистол, неустойчивой желудочковой тахикардии и ФП была очень низкой и составила 1,8%, 1,5% и 0,5%, соответственно. Стоит отметить, что авторами исследования не была обнаружена статистически значимая связь между аритмиями и структурной патологией миокарда.
В работе российских авторов с участием 2245 спортсменов без установленной структурной патологии миокарда, прошедших углубленное медицинское обследование, нарушения ритма сердца зарегистрированы у 4,4% участников исследования, при этом частота аритмий у мужчин вдвое превышала таковую у женщин (5,8% vs 2,7%, соответственно (p<0,001)) [5]. В структуре зарегистрированных нарушений ритма преобладали желудочковые экстрасистолы (61,2%) и брадиаритмии (28,6%), реже встречались полные блокады ножек пучка Гиса (5,1%), атриовентрикулярная блокада (4,1%) и ФП. Наджелудочковые экстрасистолы в указанном исследовании выявлены у 4,2% лиц, однако они не включались в общую статистику нарушений ритма сердца из-за их относительно доброкачественного клинического значения.
Согласно результатам систематического обзора Wernhart S, Halle M. (2015), распространенность ФП среди спортсменов варьирует в диапазоне от 0,3 до 12,8%, что, вероятно, обусловлено различиями характеристик исследуемых групп, в т.ч. пола, возраста, вида спортивной деятельности, а также применяемых методов диагностики [6].
Частота зарегистрированной ФП в группе атлетов составила 147 (23%) случаев, а в контрольной группе — 116 (12,5%). Результаты анализа показали, что у профессиональных спортсменов риск развития ФП в 5 раз выше по сравнению с лицами, не занимающимися регулярной физической активностью (отношение шансов (ОШ) 5,29; 95% доверительный интервал (ДИ): 3,57-7,85, p=0,0001) [7].
По данным метаанализа Newman W, et al. (2021), включающего результаты 13 исследований с совокупным участием >70 тыс. человек, риск развития ФП у спортсменов в 2,4 раза выше, чем у нетренированных лиц (ОШ 2,46; 95% ДИ: 1,73-3,51, р<0,001) [8].
Результаты исследования Ricci C, et al. (2018) свидетельствуют о наличии криволинейной J-образной взаимосвязи между объемом физических нагрузок и риском развития ФП. Авторы выполнили нелинейный метарегрессионный анализ на основе результатов 19 исследований с 29855 зарегистрированными случаями ФП, стратифицировав участников на подгруппы в зависимости от уровня физической активности в неделю, который определялся с использованием показателя метаболического эквивалента (МЕТ-часов в неделю). В ходе работы было установлено, что у лиц, занимающихся физической активностью в диапазоне от 5 до 20 МЕТ-часов в неделю, отмечается протекторный в отношении развития ФП эффект, в то время как в группе спортсменов с высоким уровнем физической активности, превышающим 55 МЕТ-часов в неделю, что соответствует более чем 9,5 ч интенсивных тренировок в неделю, наблюдается статистически значимое повышение риска развития ФП [9].
Согласно работе Zorzi A, et al. (2018), желудочковые нарушения ритма у профессиональных спортсменов выявляются с той же частотой, что и у лиц, ведущих малоподвижный образ жизни (10% vs 11%), и не зависят от интенсивности, продолжительности и вида выполняемой физической активности [10].
Множественные желудочковые экстрасистолы при записи электрокардиограммы (ЭКГ) регистрируются менее чем у 1% спортсменов [11]. При этом эксперты рекомендуют направлять на комплексную диагностику спортсменов, у которых зарегистрировано более 2 желудочковых экстрасистол на ЭКГ, с целью выявления органической патологии миокарда [11].
Результаты исследований указывают, что у 30% профессиональных спортсменов с частой желудочковой экстрасистолией, зарегистрированной по данным холтеровского мониторирования ЭКГ, выявляются структурные изменения сердца, в то время как оставшаяся часть, по мнению авторов исследования, вероятно, обусловлена синдромом спортивного сердца [12].
Согласно современным представлениям, длительные физические нагрузки высокой интенсивности сопровождаются процессом адаптивного ремоделирования миокарда, который детерминирован видом и интенсивностью, а также общей продолжительностью воздействия физической нагрузки. Так, тренировки на выносливость ассоциируются с дилатацией желудочков и предсердий без существенной гипертрофии кардиомиоцитов, в то время как силовые тренировки сопровождаются выраженной гипертрофией миокарда с сохранением объема полостей сердца. В работе Lakin R, et al. (2021) были обнаружены значимые различия в гемодинамической реакции левого желудочка (ЛЖ) и правого желудочка (ПЖ) на воздействие острой высокоинтенсивной физической нагрузки. Так, на пике физической активности отмечалось двукратное увеличение гемодинамической нагрузки на ПЖ по сравнению с ЛЖ, что обусловлено выраженным повышением конечного диастолического давления в ЛЖ. Кроме того, было продемонстрировано выраженное нарушение диастолической и систолической функции ПЖ, которое достигало своего максимума на пике физической активности и сохранялось на протяжении 24 ч после нагрузки [13].
В исследовании Sørensen E, et al. (2022) также показано асимметричное ремоделирование ПЖ, характеризующееся увеличением соотношения объема ПЖ к ЛЖ у спортсменов, занимающихся спортом на выносливость, пропорциональное количеству лет выполняемой физической нагрузки [14].
При этом врачу не всегда удается дифференцировать выраженные морфологические изменения миокарда, обусловленные физиологической адаптацией к высокоинтенсивной физической нагрузке, от патологических состояний, таких как гипертрофическая кардиомиопатия, аритмогенная дисплазия ПЖ или другие генетически детерминированные заболевания сердца. Так, в небольшом исследовании с участием 47 спортсменов с фенотипическими признаками аритмогенной дисплазии ПЖ, включающими структурную патологию ПЖ в сочетании с правожелудочковыми нарушениями ритма, патогенные мутации в генах, кодирующих десмосомные белки, были обнаружены только у 12,8% выборки [15]. В то же время некоторые исследователи предполагают, что существует синергетический эффект взаимодействия генотипа и факторов окружающей среды (нагрузки), влияющий на развитие морфофункциональных изменений миокарда [15].
Влияние полиморфизмов гена ADRB2 в спортивной генетике
Влияние симпатической нервной системы на миокард реализуется через высвобождение нейромедиаторов (адреналина и норадреналина) из постганглионарных окончаний симпатических волокон сердца и последующей активацией β1- и β2-адренорецепторов миокардиальных клеток, которые посредством связи со стимулирующим Gs-белком увеличивают концентрацию внутриклеточного циклического аденозинмонофосфата [16]. Стимуляция β1-адренорецепторов сердца эндогенными катехоламинами запускает ряд физиологических процессов, среди которых повышение силы, частоты сердечных сокращений (ЧСС) и потребности миокарда в кислороде, активация β2-адренорецепторов кардиомиоцитов вызывает увеличение сократимости миокарда и укорочение фазы систолы, а активация β2-адренорецепторов, экспрессируемых в сосудистой стенке, ассоциируется с вазодилатацией, что способствует улучшению коронарного кровотока [16][17].
Экспериментальные данные свидетельствуют, что соотношение β1- к β2-адренорецепторам в стенках желудочков у здоровых лиц составляет примерно 80:20, в то время как в предсердиях оно снижается до 70:30 [18]. Считается, что количество β-адренергических рецепторов на поверхности кардиомиоцитов варьирует в зависимости от множества факторов, таких как возраст, уровень физической активности, соотношение активности симпатической и парасимпатической нервных систем, различные патологические состояния, а также генетическая вариативность.
Согласно данным проекта ALFA Allele Frequency, частота аллеля Gly (rs1042713) в европейской популяции составляет 62%, а аллеля Glu27 (rs1042714) около 42%.
Профессиональный спорт сопряжен с экстремальными нагрузками на сердечно-сосудистую систему, которые сопровождаются массивным выбросом катехоламинов, а также перераспределением кровотока из областей с пониженной потребностью в кислороде, таких как пищеварительная система, в области с повышенной потребностью, включая работающие скелетные и дыхательные мышцы, которые регулируются уровнем циркулирующих катехоламинов и β2-адренорецепторами. В исследовании генетические особенности регуляции адренергического ответа при хронических высокоинтенсивных физических нагрузках могут стать критическими в процессах адаптации к физической нагрузке и развитии электрической нестабильности миокарда [19].
Ген ADRB2, кодирующий β2-адренорецепторы, согласно результатам молекулярно-генетических исследований демонстрирует высокую степень полиморфной изменчивости в нескольких различных структурных доменах кодируемых белков, что ассоциируется с изменениями агонист-индуцированной экспрессии, интернализации и десенситизации рецептора. Наиболее изученные и распространённые несинонимичные полиморфизмы гена ADRB2, известные как rs1042713 и rs1042714, локализованы в 47 и 79 нуклеотидах, что приводит к заменам аминокислот в позициях 16 (Arg->Gly) и 27 (Gln->Glu) [20]. С целью изучения функциональной роли указанных полиморфизмов гена ADRB2 ранее были проведены генетические исследования с использованием рекомбинантных клеточных моделей. Результаты исследований демонстрируют, что с учетом локализации всех указанных точечных замен нуклеотидов в N-концевой области рецептора степень аффинности агониста, базовая и максимальная агонист-индуцированная активность аденилатциклазы, скорость синтеза рецепторов или интернализация рецепторов в клетку, стимулированная агонистом, не различались между диким типом и мутациями Arg16Gly, Gln27+Glu и Arg16Gly+Gln27+Glu. Основное функциональное различие проявлялось в степени агонист-индуцированного подавления общего количества рецепторов на поверхности клетки. Так, после 24-ч воздействия агониста отмечена следующая закономерность: экспрессия рецепторов Arg16/Gln27 (дикий тип) снизилась на 26±3%, в то время как степень агонист-индуцированного снижения экспрессии рецепторов с мутациями Arg16Gly и Arg16Gly + Gln27Glu оказалась статистически значимо более выраженной в сравнении с рецептором дикого типа (на 41±3% и 39±4%, соответственно), а рецепторы с мутацией Gln27Glu не подвергались даунрегуляции в ответ на воздействие агониста. Полученные данные свидетельствуют, что ключевым фактором более выраженного снижения регуляции рецептора является наличие аминокислоты Gly в позиции 16. Механизмы этого эффекта малоизучены, но вероятно, реализуются после интернализации рецептора на этапах его сортировки и деградации [20].
В клинических исследованиях также выявлена связь однонуклеотидных полиморфизмов гена ADRB2 с различными показателями гемодинамики. Так, наличие аллеля Gly16 ассоциировалось с более низкой ЧСС в покое, а также более выраженным снижением системного сосудистого сопротивления и большим увеличением сердечного выброса в ответ на системное введение агониста по сравнению с Arg16. Другим выводом указанной работы стало подтверждение более высокой плотности ADRB2 на лимфоцитах у носителей аллеля Gly16, что коррелирует с плотностью ADRB2 в сердечной ткани и может обусловливать более сильный ответ на катехоламины [21].
В некоторых исследованиях изучалось влияние полиморфизмов гена ADRB2 на реакцию сердечно-сосудистой системы во время проведения ортостатической пробы. Авторы пришли к выводу, что аллель Arg16 ассоциируется с более выраженной активацией симпатической нервной системы, что проявляется более высокой ЧСС в покое, более выраженным снижением сердечного выброса и ударного индекса, а также более сильным выбросом норадреналина и большим увеличением системного сосудистого сопротивления. В отношении позиции 27 аминокислотной последовательности авторы обнаружили, что у лиц, имеющих хотя бы одну копию гена глутаминовой кислоты (Glu), ЧСС была ниже в состоянии покоя, при этом связи с изменениями гемодинамических или катехоламиновых показателей в процессе ортостатической пробы не выявлено [22].
Результаты исследований, проведенных с участием лиц из общей популяции и среди пациентов с сердечно-сосудистой патологией, демонстрируют противоречивые данные о связи полиморфизмов гена ADRB2. В некоторых работах обнаружена связь однонуклеотидных полиморфизмов гена ADRB2 с желудочковыми аритмиями в турецкой популяции. Так, у пациентов с идиопатическими желудочковыми аритмиями чаще встречались гаплотипы Gly16Gln27Thr164, Gly16Glu27Thr164 и Gly16Glu27Ile164 гена ADRB2 по сравнению с контрольной группой [23].
Ряд ученых оценивали связь полиморфизма Gln27Glu гена ADRB2 с внезапной сердечной смертью среди 492 лиц европейской популяции, у которых зарегистрирован случай внезапной сердечной смерти. Согласно полученным результатам гомозиготность по аллелю Gln27 ассоциировалась с незначительным повышением скорректированного по возрасту отношения шансов (ОШ 1,22; 95% ДИ: 0,98-1,53; p=0,08) для внезапной сердечной смерти, которое сохранялось после коррекции на факторы риска сердечно-сосудистых заболеваний (ОШ 1,30; 95% ДИ: 1,01-1,67; p=0,046). Также был проведен метаанализ, в котором объединили полученные результаты с результатами из других ранее опубликованных работ, согласно которому гомозиготность по Gln27 ассоциировалась с повышением шанса внезапной сердечной смерти как в нескорректированном (ОШ 1,35; 95% ДИ: 1,15-1,60; p=0,0003), так и в скорректированном анализе (ОШ 1,43; 95% ДИ: 1,20-1,71; p=0,0001) [24].
В работе китайских исследователей изучалась связь генетических полиморфизмов гена ADRB2 с развитием идиопатической очаговой желудочковой тахикардии из выводного тракта в китайской популяции. Согласно проведенному генотипированию, аллель 16Gly варианта Arg16Gly гена ADRB2 является фактором риска развития идиопатической очаговой желудочковой тахикардии из выводного тракта (ОШ 1,40; 95% ДИ: 1,12-1,75, p=0,003 в аддитивной модели и ОШ 1,62; 95% ДИ: 1,14-2,31, p=0,007 в доминантной модели) [25].
Согласно имеющимся данным, прямых исследований, изучающих связь аритмии у профессиональных спортсменов на пике физической нагрузки с полиморфизмом гена ADRB2, ранее не проводилось. В исследовании, проведенном под руководством Балберовой О. В. и Быкова Е. В. (2025), анализировалась ассоциация между генетическим полиморфизмом rs1042713 гена ADRB2 с вариабельностью сердечного ритма, которая является интегральным показателем функционального состояния вегетативной нервной системы. В работе показано, что в состоянии покоя у спортсменов, гомозиготных по аллелю Gly16 (rs1042713), наблюдается достоверно более высокий индекс LF/HF по сравнению с гомозиготами Arg16Arg. Индекс LF/HF характеризует баланс между симпатическим и парасимпатическим отделами вегетативной нервной системы, высокое значение которого свидетельствует о преобладании симпатического тонуса. Полученные результаты согласуются с гипотезой о гиперактивности β2-адренорецепторов у носителей аллеля Gly16 [19].
Заключение
Таким образом, проведенный анализ демонстрирует, что интенсивные физические нагрузки, характерные для профессионального спорта, могут быть ассоциированы с повышенным риском нарушений сердечного ритма. При этом ряд исследователей предполагает, что генотип спортсмена при взаимодействии с факторами окружающей среды может определять эффективность адаптации сердечно-сосудистой системы спортсмена к экстремальным нагрузкам, а также оказывать проаритмогенное действие при длительном воздействии катехоламинов. Особое внимание в контексте индивидуального риска развития аритмий у спортсменов уделяется генетическим факторам, влияющим на адренергический ответ. В частности, полиморфизмы гена ADRB2, кодирующего β2-адренорецепторы, играют важную роль в регуляции вегетативной нервной системы и гемодинамических реакциях в ответ на физическую нагрузку. Аллели Arg16/Gly16 и Gln27/Glu27 различаются по экспрессии и функциям, что подтверждено в исследованиях in vitro и in vivo. Аллель Gly16 в условиях острого воздействия агониста обеспечивает более эффективную вазодилатацию и улучшение перфузии, однако он ассоциируется с повышенной симпатической активацией в покое, а также усиленной десенситизацией и даунрегуляцией β2-адренорецепторов при длительном воздействии, что может вызывать электрическую нестабильность миокарда и аритмии, особенно при хронических нагрузках. Напротив, аллель Arg16 ассоциирован с повышенной исходной симпатической активностью и более интенсивной гемодинамической реакцией на стресс, что также может являться фактором риска электрической нестабильности миокарда. Для более глубокого понимания роли генетических вариантов ADRB2 в качестве проаритмогенных маркеров у спортсменов необходимы дальнейшие исследования.
Отношения и деятельность. Исследование выполнено за счет гранта Российского научного фонда № 25-25-20159 «Ассоциативная роль полиморфных аллельных вариантов генов ренин-ангиотензин-альдостероновой системы с ремоделированием левого желудочка и нагрузочной артериальной гипертензией у профессиональных спортсменов как маркерами предрасположенности к формированию «спортивного» сердца», https://rscf.ru/project/25-25-20159, гранта Красноярского краевого фонда науки, в организации: Федеральное государственное бюджетное учреждение «Федеральный Сибирский научно-клинический центр Федерального медико-биологического агентства».
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Кардашова О.О., Суздалева И.А., Гизатулин О.Е., Чернова А.А., Никулина С.Ю. Изучение ассоциации полиморфизмов гена ADRB2 (rs1042713 и rs1042714) в развитии нарушений ритма сердца и проводимости у профессиональных спортсменов (обзор литературы). Российский кардиологический журнал. 2026;31(1S):6798. https://doi.org/10.15829/1560-4071-2026-6798. EDN: KXKYTA
Скопировать