Внутрисердечное эхокардиографическое исследование. Нефлюороскопическая методика криобаллонной аблации фибрилляции предсердий
Аннотация
Криобаллонная аблация (КБА) наряду с радиочастотной аблацией и аблацией высоким импульсным полем зарекомендовала себя как безопасный и не уступающий другим по эффективности метод с короткой кривой обучения и минимальными временными затратами. Методика КБА фибрилляции предсердий (ФП) подразумевает окклюзию устьев лёгочных вен криобаллоном, что подтверждается отсутствием протекания контрастного вещества из целевой вены на обзорной рентгеноскопии. После чего на устье окклюзированной вены наносится криовоздействие. Во многих работах было показано негативное влияние рентгеноскопии на организм человека. Особенно актуально это становится в центрах, осуществляющих выполнение большого объема оперативных вмешательств. В данной работе представлены непосредственные и отдаленные результаты нефлюороскопической КБА ФП с описанием методологии. Данная методика подразумевает манипуляции в сосудах и полостях сердца под контролем внутрисосудистого ультразвукового исследования (ВСУЗИ), что исключает введение контрастного вещества, ионизирующего излучения, с одновременным мониторированием положения инструментов в полостях сердца, а также эхо-свободного пространства. Методика описана пошагово и иллюстрирована скриншотами ВСУЗИ с пояснениями. Опыт применения нефлюороскопической методики КБА ФП в клинике более 8 лет показал, что её эффективность и безопасность не уступает классической с применением флюороскопии и венографии, исключает негативное воздействие ионизирующего излучения и рентгенконтрастного вещества, сохраняет принцип «одного выстрела», не увеличивает время операции, воспроизводима.
Изоляция устьев легочных вен (ЛВ) (УЛВ) является конечной точкой интервенционного лечения фибрилляции предсердий (ФП). В последние десятилетия для этих целей были разработаны методики, использующие разные виды энергии. Криобаллонная аблация (КБА), наряду с радиочастотной аблацией (РЧА) и аблацией высоким импульсным полем, зарекомендовала себя как безопасный и не уступающий другим по эффективности метод с короткой кривой обучения и минимальными временными затратами [1]. Новые генерации баллонов позволили снизить количество аппликаций криоэнергии на УЛВ, включая так называемые бонусные — повторные, когда УЛВ уже было изолировано после предыдущего воздействия [2]. Более того, материалы и технологии новых баллонов позволили лучше адаптировать сферическую форму баллона к более овальной форме УЛВ. В итоге технология одного выстрела для изоляции УЛВ, с использованием криобаллона, наряду с РЧА, стала рутинно использоваться во многих центрах, включая клиники с небольшим ежегодным объемом аблаций ФП [3].
Методика КБА ФП подразумевает окклюзию УЛВ криобаллоном, что подтверждается отсутствием протекания контрастного вещества из целевой вены на обзорной рентгеноскопии. После чего на устье окклюзированной вены наносится криовоздействие [4][5]. Позиционирование криобаллона, диагностического циркулярного катетера в УЛВ, диагностического катетера в верхнюю полую вену (ВПВ), для стимуляции диафрагмального нерва, осуществляются под контролем рентгеноскопии. Во многих работах было показано негативное влияние рентгеноскопии на организм человека [6]. Ионизирующему излучению в рентген операционной подвергается весь медицинский персонал, участвующий в проведении оперативного лечения. Особенно актуально это становится центрах, осуществляющих выполнение большого объема оперативных вмешательств [7].
Технологии 3D навигационного картирования и внутрисердечной ультразвуковой (УЗ) визуализации значительно изменили историю выполнения определенного вида интервенционных аритмологических вмешательств, позволив выполнять значительное количество процедур полностью без использования рентгеновского излучения [8]. В мировой литературе есть описания методики КБА под контролем внутрисосудистого УЗ исследования (ВСУЗИ). Данная методика подразумевает манипуляции в сосудах и полостях сердца под контролем ВСУЗИ, что исключает введение контрастного вещества, ионизирующего излучения, с одновременным мониторированием положения инструментов в волостях сердца, а также эхо-свободного пространства [9].
В данной работе мы представляем непосредственные и отдаленные результаты нефлюороскопической КБА ФП с описанием методологии.
Смена методики КБА ЛВ с классической, основанной на флюороскопической и ангиографической визуализации, на УЗ визуализацию в нашей клинике шла постепенно. Применение ВСУЗИ, как и у многих врачей, началось ограниченно с проведения транссептальной пункции и контроля эхо-свободного пространства. Следом ангиографию ЛВ для контроля окклюзии их криобаллоном стали сравнивать с применением для этой цели цветной допплероскопии и «пузырьковой» пробы, подтвердив сопоставимость результатов на двадцати процедурах, оставили только УЗ контроль. Учитывая, что для РЧА ФП нами уже активно использовались навигационные системы, в т.ч. без флюороскопии, не обошлось без их применения для КБА ФП. Так как использование криоконсоли в сочетании с магнитной навигацией было проблемно, применялась импедансная методика. Однако изучение возможности ВСУЗИ позволило найти позиции УЗ датчика для визуализации всех ЛВ в поперечном срезе и проводить визуализацию криобаллона в УЛВ с нескольких проекций, что при включении режима цветной допплероскопии и проведении «пузырьковой» пробы позволяет провести селективную его репозицию для достижения окклюзии [10][11].
Методика нефлюороскопической КБА ЛВ
Венозный сосудистый доступ с обеих бедренных вен проводится в большинстве случаев под тактильным контролем, использование линейного УЗ датчика для визуализации бедренных вен проводится в случаях проблемной пункции и катетеризации. Двусторонний доступ используется по причине большого диаметра применяемого инструмента (10-12 Fr). Через левую бедренную вену проводится УЗ датчик Accunav Biosense Webster, через правую бедренную вену транссептальное доставляющее устройство и катетер для стимуляции. Исходное положение внутрисердечного датчика: рассматриваем поперечный срез рукоятки датчика как циферблат часов, нос пациента указывает на 12 ч, поворот датчика от себя — по часовой стрелке, к себе — против часовой стрелки; все три метки датчика в исходном положении должны указывать на 12 ч.
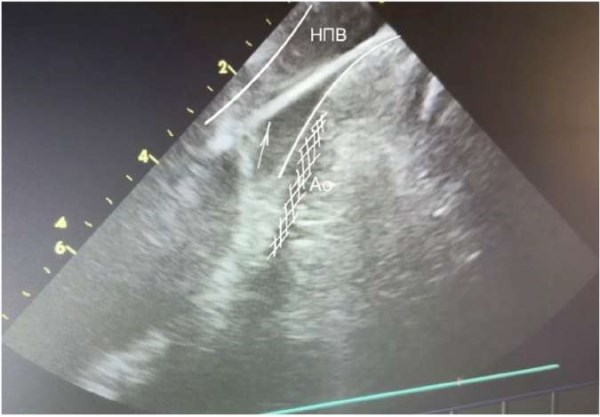
Основными УЗ анатомическими ориентирами при проведении УЗ катетера являются подвздошные артерии, брюшная аорта, печень. Для выведения данного изображения необходимо плавно провести датчик эхокардиографии по подвздошной вене, развернув основную метку (нижнюю неподвижную) в области 3 часов. Если возникают трудности в прохождении датчика в нижней полой вене (НПВ) — верхнюю метку датчика (A/P) нужно плавно повернуть в сторону метки «A». По УЗ исследованию: датчик нырнет в просвет НПВ, плавно продвигаем датчик далее в просвет на 1-2 см, после — поворачиваем метку «А» в исходное положение (рис. 1).
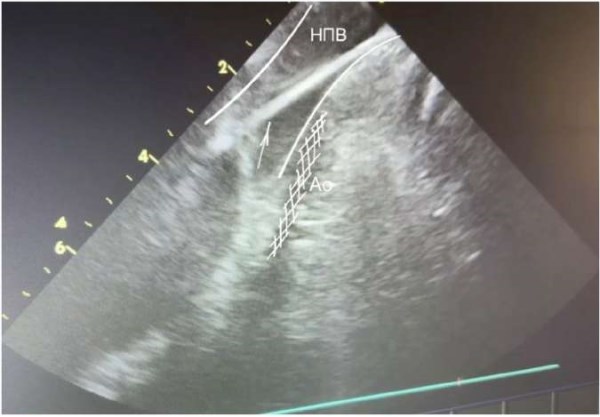
Рис. 1. Проводник в НПВ (белая стрелка). Видимый просвет аорты заштрихован в белую сетку.
Сокращения: Ао — брюшной отдел аорты, НПВ — нижняя полая вена.
После проведения датчика в правое предсердие (ПП) его ось ориентируется на 12 ч (нос пациента в положении на спине без поворота головы), что отражается УЗ «домашней позицией», ориентиры ПП, трикуспидальный клапан, правый желудочек, корень аорты (рис. 2). Для безопасного позиционирования проводника транссептального интродьюсера необходимо визуализировать ВПВ. Следующее движение УЗ датчика — поворот по часовой стрелке на 3 ч. Анатомические ориентиры: ПП, левое предсердие (ЛП), межпредсердная перегородка, корень аорты, из этой позиции визуализируется ушко ЛП (рис. 3), при отсутствии признаков тромбоза принимается окончательное решение о проведении процедуры в ЛП. Для выведения ВПВ с помощью верхнего и нижнего колец управления луч датчика поворачивается кзади и вправо на 45°. Анатомические ориентиры: ВПВ, восходящая аорта, ЛП. Проводник через НПВ, ПП заводится в ВПВ под УЗ контролем и далее по нему транссептальный интродьюсер (рис. 4). После замены проводника на транссептальную иглу управляющие кольца УЗ датчика возвращаются в нейтральную позицию для визуализации межпредсердной перегородки, интродьюсер с иглой смещается вниз на овальную ямку. При затруднении пункции телом иглы возможна пункция внутренним стилетом с дальнейшим поэтапным проведением иглы на стилет, дилататора на иглу, интродьюсера на дилататор (рис. 5). По проведенному через интродьюсер в левую верхнюю ЛВ жёсткому проводнику проводится смена интродьюсера на доставляющее устройство для криобаллона. Выведенный за пределы доставляющего устройства баллон и циркулярный катетер хорошо определяются визуально (рис. 5), также показателем выведения баллона является метка на катетере. Управляя УЗ катетером вращением по и против часовой стрелки, а также с помощью управляющих колец изгибая катетер вперёд-назад и вправо-влево выводятся поочерёдно (по часовой стрелке) левые ЛВ, далее правая нижняя и правая верхняя ЛВ (рис. 6, 7). Стимуляционный катетер проводится в правый желудочек из «домашней позиции», а ВПВ по описанной ранее методике. Контроль окклюзии УЛВ осуществляется с помощью цветной допплероскопии (рис. 8, 9) и «пузырьковой пробы», для чего в просвет криобаллонного катетера вводится физиологический раствор. Контроль полости перикарда проводится из ПП (поворот из «домашней позиции» против часовой стрелки) и из правого желудочка (загибание управляющим кольцом кпереди), эту манипуляцию мы проводим как во время процедуры, так и перед завершением и извлечением УЗ катетера.
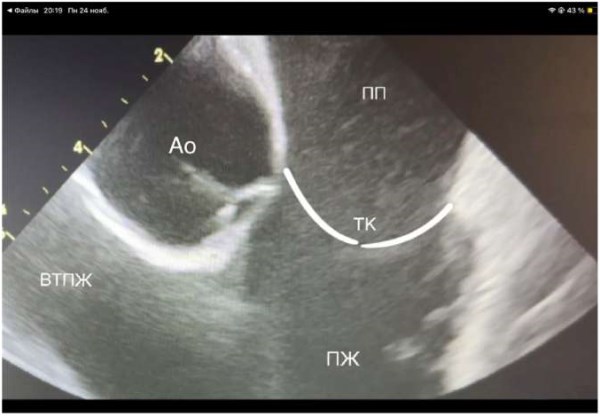
Рис. 2. «Домашняя позиция». Белым контуром выделены створки трикуспидального клапана и границы правого желудочка.
Сокращения: Ао — корень аорты, ВТПЖ — выходной тракт правого желудочка, ПЖ — правый желудочек, ПП — правое предсердие, ТК — трикуспидальный клапан.
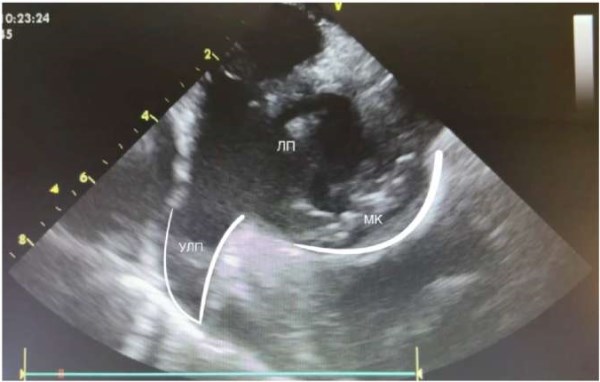
Рис. 3. Визуализация ушка ЛП.
Сокращения: ЛП — левое предсердие (полость), МК — митральный клапан, УЛП — ушко левого предсердия.
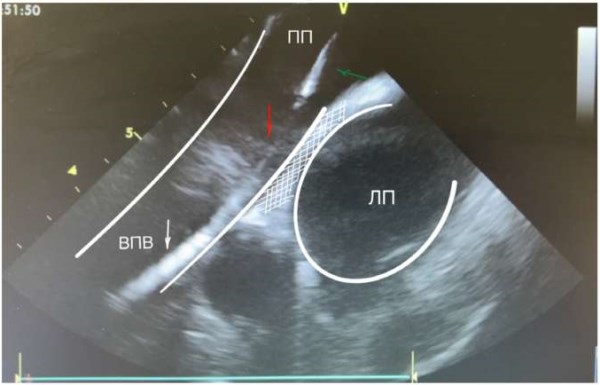
Рис. 4. На изображении выведены: проводник (белая стрелка) с шифтом (зеленая стрелка) и бужом (красная стрелка) в ВПВ. Белым контуром выделены ВПВ и ЛП. Стенка ВПВ, переходящая на межпредсердную перегородку (заштрихованная белым зона).
Сокращения: ВПВ — верхняя полая вена, ЛП — левое предсердие, ПП — правое предсердие.
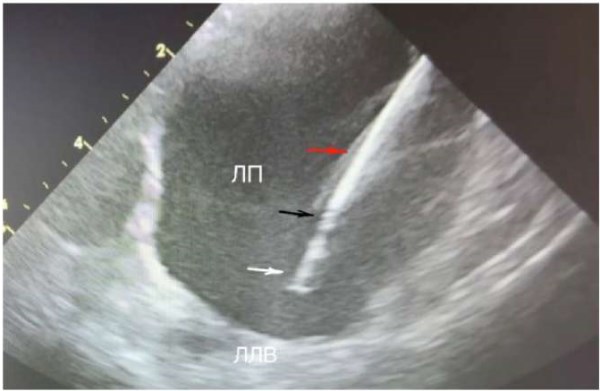
Рис. 5. Буж и шифт в полости ЛП. Белой стрелкой указан буж, красной — шифт, черной — граница между шифтом и бужом.
Сокращения: ЛЛВ — левая легочная вена, ЛП — левое предсердие.
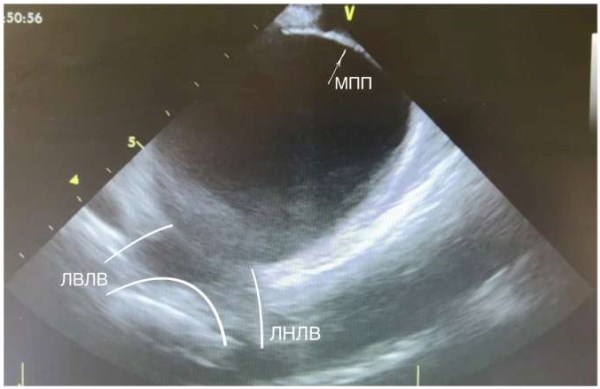
Рис. 6. Межпредсердная перегородка (указана белой стрелкой), полость ЛП, устья левых ЛВ, левая верхняя ЛВ, левая нижняя ЛВ (выделены белым контуром).
Сокращения: ЛВЛВ — левая верхняя легочная вена, ЛНЛВ — левая нижняя легочная вена, МПП — межпредсердная перегородка.
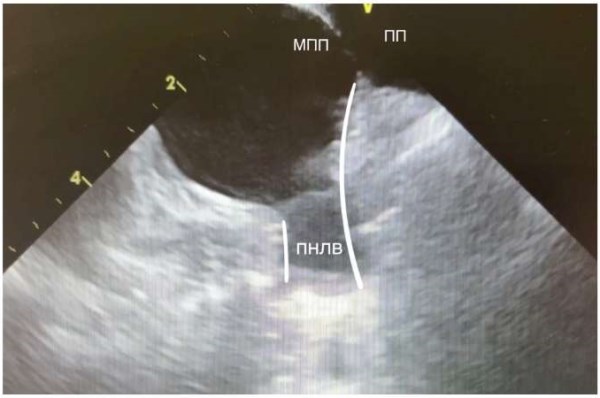
Рис. 7. Правая нижняя ЛВ. Межпредсердная перегородка, переходящая на нижнюю стенку правой нижней ЛВ (выделено белым контуром).
Сокращения: МПП — межпредсердная перегородка, ПНЛВ — правая нижняя легочная вена, ПП — правое предсердие.
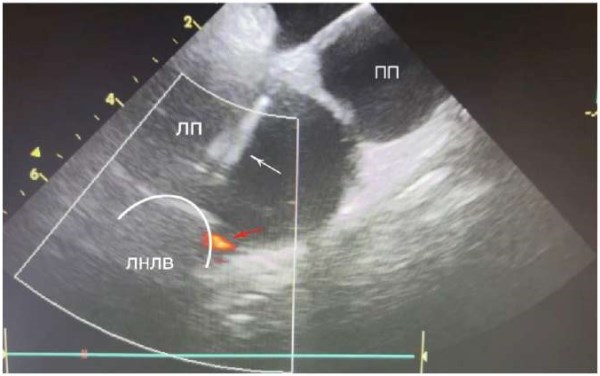
Рис. 8. Криобаллон раздут в левой нижней ЛВ. Красной стрелкой указан «leak» по нижнему краю баллона. Белая стрелка — шифт в полости ЛП.
Сокращения: ЛНЛВ — левая нижняя легочная вена, ЛП — левое предсердие, ПП — правое предсердие.
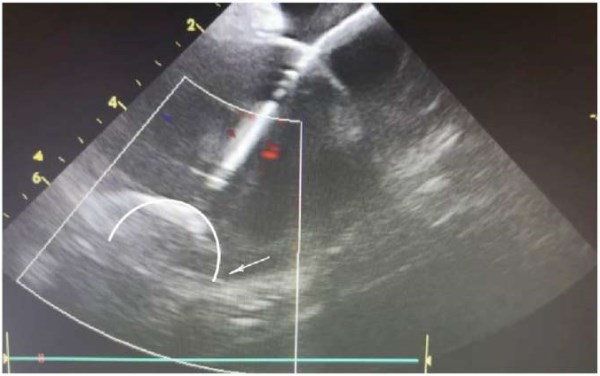
Рис. 9. После изменения положения баллона под контролем внутрисердечной эхокардиографии «leak» по нижнему краю прекратился.
Опыт катетерной и торакоскопической аблации ФП в ФЦ ССХ г. Красноярска более 10 тыс. операций. Криобаллонные процедуры составляют 10% с тенденцией к увеличению в 2025г, когда этот вид помощи выделен в отдельную группу (рис. 10). С 2017г применяется нефлюороскопическая методика. Непосредственная эффективность КБА ФП, достижение конечной точки — изоляции УЛВ во время первой процедуры составляет 98%. Средняя продолжительность операции 60±10 мин, учитывая что около 1/3 времени составляет подготовка инструмента. Зафиксировано 3 больших осложнения — гемоперикард после манипуляций в ПП, купированные дренированием полости перикарда. Осложнений во время процедуры в ЛП и пареза диафрагмального нерва не было. Осложнения со стороны сосудистого доступа составляют 0,5% после всех катетерных аблаций ФП, включая радиочастотные процедуры.
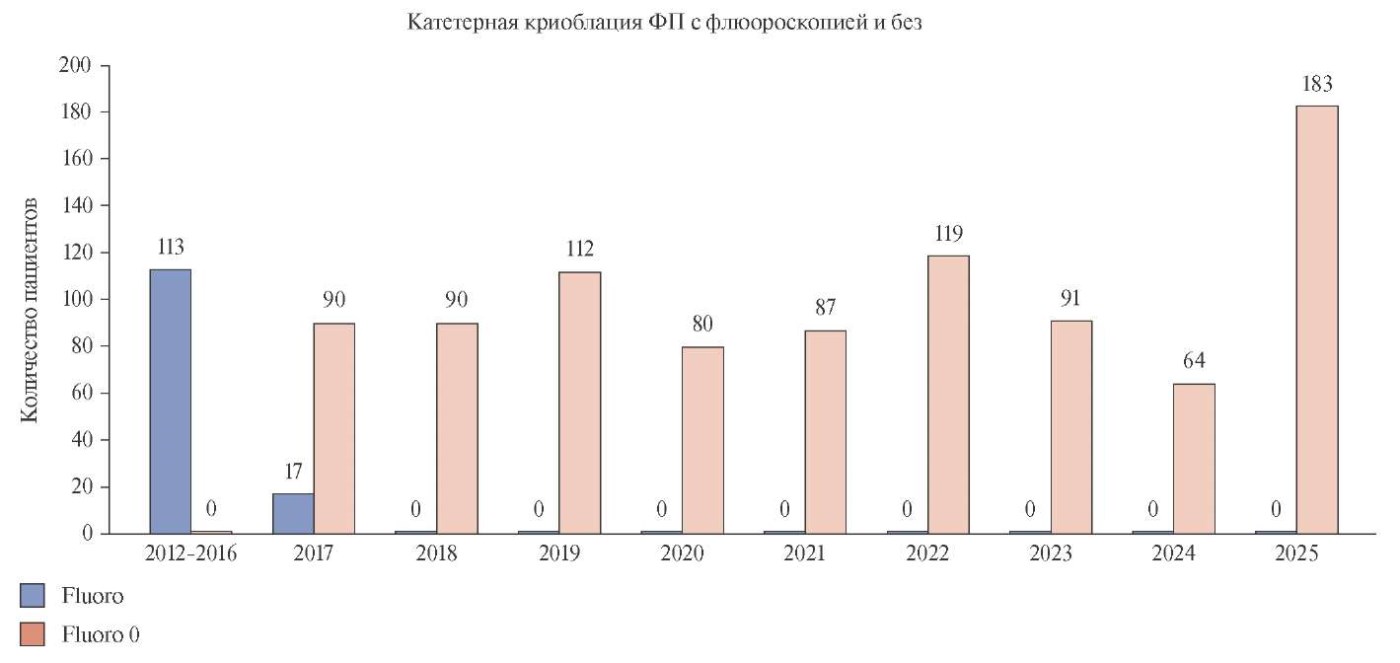
Рис. 10. Нефлюороскопическая КБА ФП в ФЦ ССХ г. Красноярск.
Сокращение: ФП — фибрилляция предсердий.
Заключение
Нефлюороскопическая катетерная КБА ФП по эффективности и безопасности не уступает флюороскопической методике. Общее время операции сопоставимо при обеих методиках. При проведении нефлюороскопической катетерной аблации исключается отрицательное влияние лучевой нагрузки и рентгенконтраста. Наш опыт показал воспроизводимость методики.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Шляков Д.А., Кропоткин Е.Б., Прокопенко А.В., Иваницкий Э.А., Сакович В.А. Внутрисердечное эхокардиографическое исследование. Нефлюороскопическая методика криобаллонной аблации фибрилляции предсердий. Мнение по проблеме. Российский кардиологический журнал. 2025;30(4S):6730. https://doi.org/10.15829/1560-4071-2025-6730. EDN: IYGXSU
Скопировать