Кавутилид: необычные варианты восстановления синусового ритма при фибрилляции предсердий
Аннотация
В статье представлены четыре клинических случая успешного восстановления синусового ритма с использованием кавутилида у пациентов с неблагоприятными для фармакологической кардиоверсии характеристиками. Рассматриваются случаи фибрилляции и трепетания предсердий на фоне транстиретинового амилоидоза сердца, обструктивной гипертрофической кардиомиопатии, длительно (3 года) персистирующей формы аритмии, а также кардиомиопатии, ассоциированной с аритмией, осложнённой выраженным снижением насосной функции сердца. Во всех наблюдениях применение кавутилида в дробных дозах под контролем QTc-интервала приводило к восстановлению синусового ритма. Полученные результаты сопоставлены с данными ранее опубликованных исследований III фазы и пострегистрационных, в которых кавутилид продемонстрировал высокую эффективность и благоприятный профиль безопасности. В эти исследования, однако, не включались пациенты со столь выраженными структурными изменениями сердца и с такой длительной фибрилляцией предсердий. Представленные данные свидетельствуют об эффективности и безопасности применения кавутилида у существенно более широкого контингента пациентов.
Фибрилляция предсердий (ФП) и трепетание предсердий (ТП) при наличии выраженного структурного поражения сердца, длительного анамнеза аритмии или резко сниженной фракции выброса (ФВ) левого желудочка (ЛЖ) традиционно рассматриваются как ситуации с достаточно низкой вероятностью успешного восстановления и дальнейшего контроля ритма. Предпочтение часто отдаётся стратегии контроля частоты сердечных сокращений (ЧСС), а не попыткам восстановления синусового ритма (СР). Однако в целом ряде случаев аритмия является высокосимптомной, резко снижая качество жизни пациентов (III-IV функциональный класс по модифицированной шкале EHRА). В таких случаях при выборе стратегии контроля ритма его восстановление обычно выполняется с помощью электрической кардиоверсии (ЭИТ). Возможности фармакологической кардиоверсии ранее сводились к использованию единственного антиаритмического препарата амиодарона, эффективность которого в перечисленных клинических ситуациях невысока. Положение изменилось с появлением отечественного антиаритмического препарата III класса кавутилида (4-Нитро-N-[(1RS)-1-(4-фторфенил)- 2-(1-этилпиперидин-4-ил) этил] бензамида гидрохлорида) с его единственным торговым названием Рефралон® (Россия). Этот антиаритмик все еще можно считать достаточно новым: первое посвященное ему клиническое исследование появилось в 2011г [1]. В 2012г были опубликованы результаты регистрационного многоцентрового исследования III фазы: первых в России клинических испытаний эффективности и безопасности антиаритмического препарата, проведенных в соответствии с требованиями GCP [2]. Далее последовали крупное исследование его эффективности и безопасности в сравнении с ЭИТ [3][4], а также ретроспективное многоцентровое исследование, включившее >700 пациентов [5][6]. Все эти исследования продемонстрировали необычно высокую (89%) эффективность кавутилида при небольшом его проаритмическом действии. В соответствии с официальной инструкцией ограничения для его применения сравнительно невелики и не включают, в частности, выраженную гипертрофию ЛЖ. В российских клинических рекомендациях «Фибрилляция и трепетание предсердий» [7][8] и «Наджелудочковые тахикардии» [9][10] предложено использовать кавутилид для купирования ФП/ТП любой продолжительности, в т.ч. персистирующей и длительно персистирующей. Специально отмечено, что он является альтернативой плановой ЭИТ, не уступая ей по эффективности (~90%). В то же время описания применения кавутилида в сложных клинических ситуациях практически отсутствуют. Восполняя этот пробел, приводим четыре клинических случая восстановления СР у пациентов с амилоидозом сердца, гипертрофической кардиомиопатией (КМП) с обструкцией выходного тракта ЛЖ, КМП, ассоциированной с аритмией (КАА) с выраженным снижением насосной функции сердца и с длительно (>3 лет) персистирующей ФП.
Клинический случай 1
Пациент Х., 73 года. Первые симптомы заболевания отметил в 2020г, когда впервые появились онемение и покалывание в стопах, нарушение их чувствительности, шаткая походка. Наблюдался неврологами амбулаторно и в условиях стационара (неоднократно) с диагнозом «Полинейропатия», которую связывали с перенесенной новой коронавирусной инфекцией. Лишь через 3 года при целенаправленном обследовании была обнаружена истинная причина полинейропатии: выявлен транстиретиновый амилоидоз (семейная транстиретиновая амилоидная полинейропатия). Диагноз подтвержден результатами молекулярно-генетического исследования (патогенный вариант гена TTR). Амилоидоз сердца подтвержден результатами магнитно—резонансной томографии с гадолинием. Около 2 мес. назад впервые в жизни почувствовал сердцебиение, одышку. На электрокардиограмме (ЭКГ) документировано левопредсердное ТП, сохраняющееся по настоящее время (персистирующее ТП). Отмечает существенное ухудшение качества жизни. При эхокардиографии (ЭхоКГ) диаметр левого предсердия (ЛП) — 51 мм (объем 102 мл). Толщина задней стенки ЛЖ и межжелудочковой перегородки (МЖП) 19 мм. ФВ ЛЖ 54,8%. Постоянно принимает метопролола сукцинат 100 мг в сутки, апиксабан 10 мг в сутки, тафамидис 20 мг в сутки. От неоднократно предложенной ранее ЭИТ отказался. В Северо-западный центр диагностики и лечения аритмий был направлен для определения лечебной тактики. Было принято решение о восстановления СР. Чреспищеводная ЭхоКГ — отсутствие тромбов в ушке ЛП.
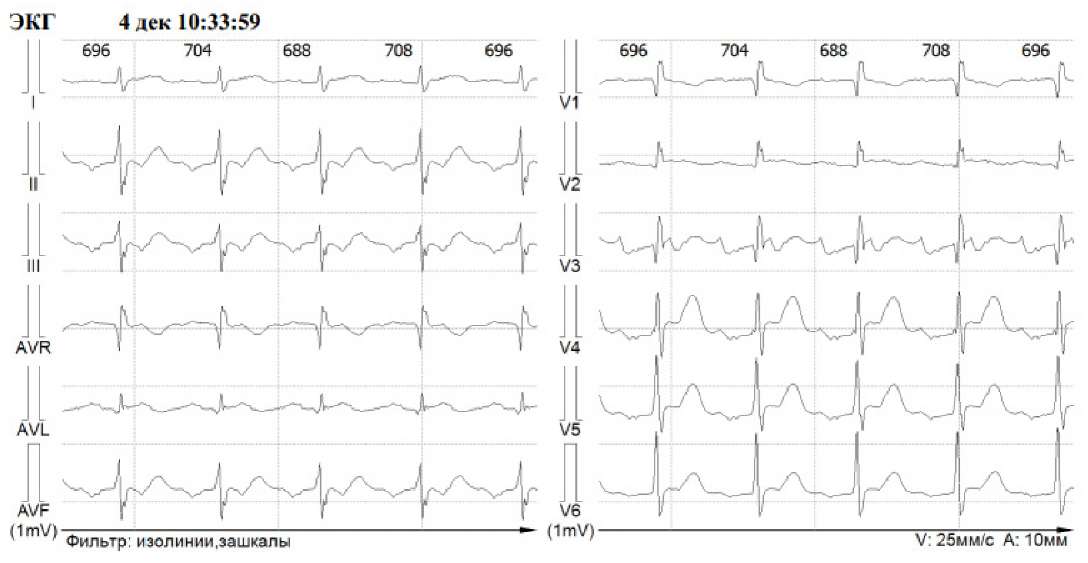
После отмены за 1 сутки метопролола сукцината, в условиях палаты интенсивной терапии пунктирована и катетеризирована периферическая вена. Внутривенно капельно введено: Sol. KCl 4% — 30 ml, Sol. Mg sulfatis 25% — 10 ml, Sol. NaCl 0,9% — 200 ml. Далее под контролем QTc-интервала внутривенно, медленно, дробно Sol. Cavutilidi 5 мкг/кг № 4 с восстановлением СР после введения 4‑й дозы препарата. Исходная ЭКГ с левопредсердным ТП с атриовентрикулярным проведением возбуждения 2:1 и ЭКГ после восстановления СР представлены на рисунках 1 и 2, соответственно.
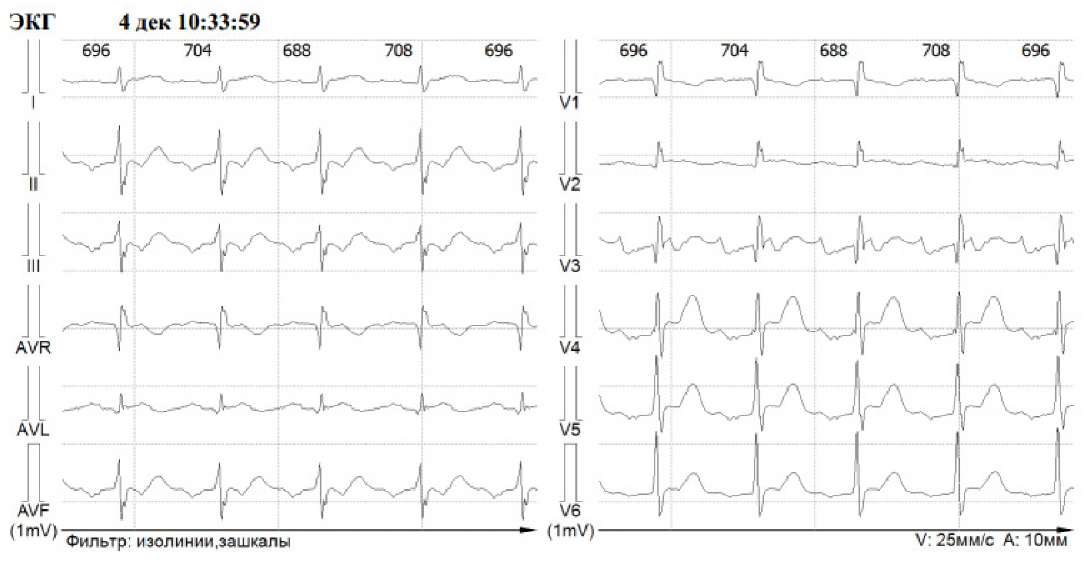
Рис. 1. Пациент Х. Исходная ЭКГ. Левопредсердное ТП с атриовентрикулярным проведением возбуждения 2:1.

Рис. 2. Пациент Х. ЭКГ после восстановления СР.
Клинический случай 2
Пациент Д., 48 лет. Около 10 лет назад установлен диагноз: гипертрофическая КМП, семейная форма, ассоциированная с мутацией гена MYH7 (β-миозина тяжёлой цепи), обструктивный вариант. Высокий семейный риск внезапной сердечной смерти (отец умер внезапно в возрасте 67 лет). Без жалоб, заболевание было выявлено при обследовании членов семьи (гипертрофическая КМП у отца и старшего брата). Обследован. При магнитно-резонансной томографии сердца с гадолинием была выявлена асимметричная гипертрофия миокарда ЛЖ с максимальной толщиной МЖП в базальном сегменте до 26 мм, преимущественно с вовлечением септальной и антеросептальной стенок. Объёмные показатели ЛЖ и его глобальная систолическая функция сохранены (ФВ ЛЖ — 61,7%). Признаков дилатации полостей сердца не было, ЛП не увеличено. Имелись признаки диастолической дисфункции ЛЖ, соответствующей рестриктивному типу наполнения. В режиме позднего контрастирования выявлялось очаговое субэндокардиальное и мезокардиальное накопление контраста в области гипертрофированной МЖП, общей протяжённостью не более 5-7% массы миокарда ЛЖ, без признаков трансмурального фиброза. При ЭхоКГ: асимметричная гипертрофическая КМП с выраженной обструкцией выходного отдела ЛЖ. Максимальное утолщение МЖП в базальном сегменте до 26 мм. Градиент давления в выходном отделе ЛЖ 52 мм рт.ст. в покое (выраженная обструкция). Диастолическая дисфункция ЛЖ 2 ст., повышение давления наполнения. ФВ ЛЖ 63,2%. При холтеровском мониторировании (ХМ) ЭКГ — без клинически значимых аритмий (63 полиморфных желудочковых и 134 предсердных экстрасистол). HCM Risk—SCD низкий: <4% за 5 лет.
В январе 2024г впервые в жизни развился приступ неритмичного сердцебиения, идентифицированный как ФП, продолжительностью около 5 сут. В рамках госпитализации после безуспешной попытки восстановления СР внутривенным капельным введением амиодарона выполнена эффективная ЭИТ. С этого времени принимает бисопролол 5 мг, ривароксабан 20 мг в сутки. Второй приступ ФП — спустя ровно 1 год, в январе 2025г. Его продолжительность составила 3 сут. В течение этого времени самостоятельно принимал по рекомендации кардиолога дополнительно только пропранолол: неоднократно, по 20 мг, суммарно 80 мг. В Северо-западный центр диагностики и лечения аритмий был направлен для восстановления СР.
После отмены за 1 сутки бисопролола, в условиях палаты интенсивной терапии пунктирована и катетеризирована периферическая вена. Внутривенно капельно введено: Sol. KCl 4% — 30 ml, Sol. Mg sulfatis 25% — 10 ml, Sol. NaCl 0,9% — 200 ml. Далее под контролем QTc-интервала внутривенно, медленно, дробно Sol. Cavutilidi 5 мкг/кг № 2, затем Sol. Cavutilidi 10 мкг/кг № 1, с восстановлением СР после введения 3‑й дозы препарата. Исходная ЭКГ с ФП и ЭКГ с восстановлением СР представлены на рисунках 3 и 4, соответственно.
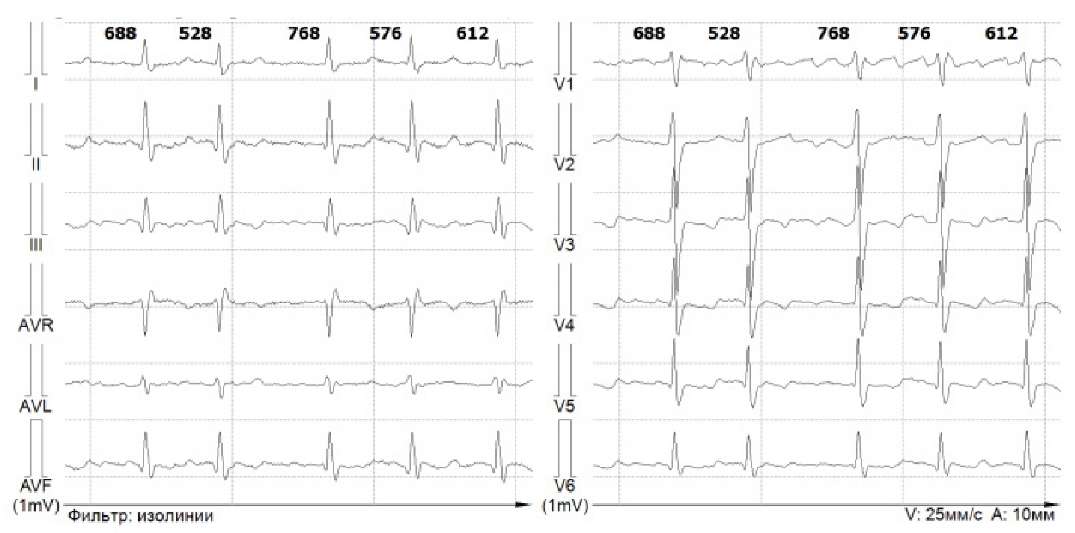
Рис. 3. Пациент Д. Исходная ЭКГ. ФП.

Рис. 4. Пациент Д. Восстановление СР.
Клинический случай 3
Пациент Б., 61 год. В анамнезе в течение многих лет гипертоническая болезнь, максимальные цифры артериального давления неизвестны. Низкая приверженность к рекомендованной гипотензивной терапии. Приступ сердцебиения впервые в жизни в 2008г на фоне эмоциональной нагрузки и алкогольного эксцесса (был идентифицирован как ФП/ТП, купирован внутривенным струйным введением прокаинамида). Далее последовала длительная ремиссия. Возобновление приступов сердцебиения с 2020г, что связывает с перенесенной неоднократно новой коронавирусной инфекцией. С этого времени принимал последовательно практически все доступные антиаритмические препараты (лаппаконитина гидробромид, пропафенон, этацизин, соталол, амиодарон) — без эффекта. На протяжении последних 3-х лет (с весны 2021г) на многочисленных представленных ЭКГ и ХМ ЭКГ СР зарегистрирован не был, что полностью соответствовало субъективным ощущениям пациента. ФП высокосимптомна, существенно снижает качество жизни (IV функциональный класс по модифицированной шкале EHRA). За это время дважды был госпитализирован в разные стационары Санкт-Петербурга для восстановления СР с помощью ЭИТ. Обе попытки успеха не имели. Около 1 месяца назад настоял на торакоскопической процедуре аблации ФП, в настоящее время находится в листе ожидания. Обследован. По результатам ЭхоКГ гипертрофия ЛЖ до 12 мм. ЛП 55 мм (объем 134 мл). ФВ ЛЖ сохранена. ХМ ЭКГ — ФП/ТП с ЧСС средней дневной 109 в 1 минуту, без других клинически значимых аритмий. В настоящее время принимает ривароксабан 20 мг, аторвастатин 20 мг, лозартан 50 мг, метопролола сукцинат 200 мг. В Северо-западный центр диагностики и лечения аритмий обратился самостоятельно, категорически отказываясь от стратегии контроля ЧСС и настаивая на восстановлении СР. Было принято решение о попытке фармакологической кардиоверсии. Чреспищеводная ЭхоКГ — отсутствие тромбов в ушке ЛП.
За 1 сутки до процедуры доза метопролола сукцината была уменьшена с 200 мг до 100 мг в сутки: полная отмена бета-адреноблокатора была сочтена нецелесообразной ввиду высокой ЧСС и плохой субъективной переносимости тахисистолической ФП/ТП. Далее в условиях палаты интенсивной терапии была пунктирована и катетеризирована периферическая вена. Внутривенно капельно введено: Sol. KCl 4% — 30 ml, Sol. Mg sulfatis 25% — 10 ml, Sol. NaCl 0,9% — 200 ml. Затем под контролем QTc-интервала внутривенно, медленно, дробно Sol. Cavutilidi 5 мкг/кг № 2, затем Sol. Cavutilidi 10 мкг/кг № 2, с восстановлением СР после введения 4‑й дозы препарата. Исходная ЭКГ с ФП/ТП и ЭКГ с восстановлением СР представлены на рисунках 5 и 6, соответственно. После кардиоверсии пациенту был назначен амиодарон по стандартной схеме с поддерживающей дозой 200 мг в сутки, с одновременным приемом метопролола сукцината в суточной дозе 50 мг.

Рис. 5. Пациент Б. Исходная ЭКГ. ФП/ТП.

Рис. 6. Пациент Б. Восстановление СР.
Клинический случай 4
Пациентка Г., 54 года. Ранее практически не болела, в анамнезе лишь редкие подъемы артериального давления, непостоянный прием гипотензивных препаратов (периндоприл 2-4 мг в сутки). Плохое самочувствие в течение 1 года: нарастающая повышенная утомляемость, одышка, отеки стоп, а затем и нижних третей голеней, сердцебиение. Обратилась к врачу лишь в мае 2025г. Была выявлена тахисистолическая ФП/ТП: по результатам ХМ ЭКГ средняя дневная ЧСС составила 150 в 1 мин. По данным ЭхоКГ: ЛП 45 мм (объем 92 мл), ФВ ЛЖ 28,1%. Пациентке был рекомендован прием метопролола сукцината 175 мг в сутки (максимально возможная доза с учетом артериальной гипотензии), дигоксин 0,25 мг, спиронолактон 25 мг, лозартан 25 мг, торасемид 10 мг, ривароксабан 20 мг. В Северо-западный центр диагностики и лечения аритмий была направлена в сентябре 2025г для определения лечебной тактики в связи с отсутствием клинического эффекта. В соответствии с Клиническими рекомендациями «Фибрилляция и трепетание предсердий» было принято решение о коррекции терапии с последующим восстановлением СР пациентке с КАА. Лозартан и дигоксин были отменены, дополнительно рекомендованы комплекс сакубитрил/валсартан 100 мг в сутки (стартовая доза) и дапаглифлозин 10 мг в сутки. Пациентка категорически отказалась от ЭИТ. В связи с этим консилиумом было принято решение о фармакологической кардиоверсии, несмотря на наличие у больной КАА с низкой ФВ ЛЖ. Чреспищеводная ЭхоКГ — отсутствие тромбов в ушке ЛП.
После отмены за 5 суток дигоксина и уменьшения за 1 сутки дозы метопролола сукцината до 50 мг, в условиях палаты интенсивной терапии пунктирована и катетеризирована периферическая вена. Внутривенно капельно введено: Sol. KCl 4% — 30 ml, Sol. Mg sulfatis 25% — 10 ml, Sol. NaCl 0,9% — 200 ml. Далее под контролем QTc-интервала внутривенно, медленно, дробно Sol. Cavutilidi 5 мкг/кг № 2, затем Sol. Cavutilidi 10 мкг/кг № 1, с восстановлением СР после введения 3‑й дозы препарата. Исходная ЭКГ с ФП и ЭКГ с восстановлением СР представлены на рисунке 7.

Рис. 7. Пациентка Г. Исходная ЭКГ с ФП и ЭКГ с восстановлением СР.
После кардиоверсии пациентке был назначен амиодарон по стандартной схеме с поддерживающей дозой 200 мг в сутки, с сохранением приема метопролола сукцината в суточной дозе 50 мг. Значительное улучшение самочувствия (прекращение повышенной утомляемости, слабости и одышки, исчезновение отеков нижних конечностей) — в течение 1 недели после кардиоверсии. Через 8 дней от восстановления СР у больной вновь развился пароксизм ФП продолжительностью около 2 ч, который прекратился спонтанно.
ЭхоКГ через 2 нед. после фармакологической кардиоверсии: ЛП 42 мм (объем 86 мл), ФВ ЛЖ 49,4%. ЭхоКГ через 1 мес. после фармакологической кардиоверсии: ЛП 39 мм (объем 81 мл), ФВ ЛЖ 54,3%. ХМ ЭКГ — СР без клинически значимых аритмий. В связи с очевидной положительной динамикой КАА терапия была скорректирована: отменены сакубитрил/валсартан, торасемид, спиронолактон.
Обсуждение
Приведённые клинические наблюдения демонстрируют возможность успешного применения кавутилида в ситуациях, которые традиционно считаются неблагоприятными для фармакологической кардиоверсии. Во всех четырёх случаях имелись факторы, снижающие вероятность восстановления ритма:
— кардиальный амилоидоз, сопровождающийся выраженным инфильтративным поражением миокарда;
— гипертрофическая КМП с выраженной обструкцией выносящего тракта ЛЖ, когда ФП/ТП обычно плохо поддаётся медикаментозной конверсии;
— длительно (>3 лет) персистирующая ФП с предшествующей неэффективностью многочисленных антиаритмических препаратов и двух попыток ЭИТ;
— КАА на фоне продолжительной персистирующей тахисистолической ФП/ТП, с выраженным снижением ФВ ЛЖ, когда фармакологическая кардиоверсия традиционно считается весьма рискованной.
Несмотря на перечисленные обстоятельства, во всех четырёх случаях была достигнута успешная конверсия ритма с помощью кавутилида, без зарегистрированных эпизодов клинически значимых желудочковых аритмий или удлинения QTc-интервала. При этом лишь в одном случае из четырех потребовалось введение максимальной суммарной дозы препарата: 30 мкг/кг. Дополнительным важным наблюдением явилось быстрое улучшение гемодинамических параметров у пациентки с КАА: увеличение ФВ ЛЖ с 28% до 54% за 1 месяц, что подчёркивает преходящий характер сердечной недостаточности и значимость восстановления СР у этой категории больных. Приведенные наблюдения вполне согласуются с ранее опубликованными исследованиями III фазы и пострегистрационными работами, подтверждавшими высокую эффективность кавутилида (~85-90%) при низком риске проаритмии. Однако в этих исследованиях практически отсутствовали пациенты с настолько значимыми структурными изменениями сердца или столь длительно персистирующей ФП. Настоящие наблюдения дополняют имеющиеся сведения о возможностях кавутилида. Очевидным ограничением публикации является отсутствие длительного наблюдения за пациентами после восстановления СР. Это обстоятельство представляется особенно важным. Известно, что кавутилид позиционирован как средство для кардиоверсии не столько при пароксизмальной, сколько при персистирующей ФП, т.е. в наиболее сложных клинических ситуациях. Но подавляющее большинство таких пациентов получает постоянную антиаритмическую терапию, чаще всего — амиодарон. Инструкция не позволяет вводить кавутилид больным, принимающим антиаритмики III класса. Однако формальное соблюдение правила, в соответствии с которым следующий антиаритмический препарат может быть использован не ранее, чем через 5 периодов полувыведения предыдущего, делает применение кавутилида при пероральном приеме амиодарона практически невозможным. Между тем, сложившаяся клиническая практика свидетельствует о безопасности этого препарата при конверсии ФП после кратковременной (1-3 сут.) отмены амиодарона. Данный аспект заслуживает особого внимания, поскольку в отсутствие постоянной антиаритмической терапии вероятность раннего рецидива при персистирующей ФП весьма велика. Вопрос о возможности (безопасности) восстановления СР кавутилидом на фоне приема поддерживающей дозы амиодарона важен и может быть решен в рамках специального клинического исследования.
Заключение
Приведённые клинические случаи показывают, что кавутилид может быть эффективным и безопасным средством восстановления СР даже у пациентов с выраженным структурным поражением сердца, длительным анамнезом аритмии, КАА с низкой ФВ ЛЖ. Во всех четырёх наблюдениях удалось достичь успешной фармакологической кардиоверсии, несмотря на неблагоприятные исходные характеристики. Полученные данные расширяют возможности применения кавутилида.
Заявление о получении информированного согласия у пациента. У всех пациентов было получено информированное согласие на публикацию анонимизированных данных.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Шубик Ю.В., Медведев М.М., Берман М.В., Корнеев А.Б. Кавутилид: необычные варианты восстановления синусового ритма при фибрилляции предсердий (клинические случаи). Российский кардиологический журнал. 2025;30(4S):6731. https://doi.org/10.15829/1560-4071-2025-6731. EDN: ZEJLKX
Скопировать