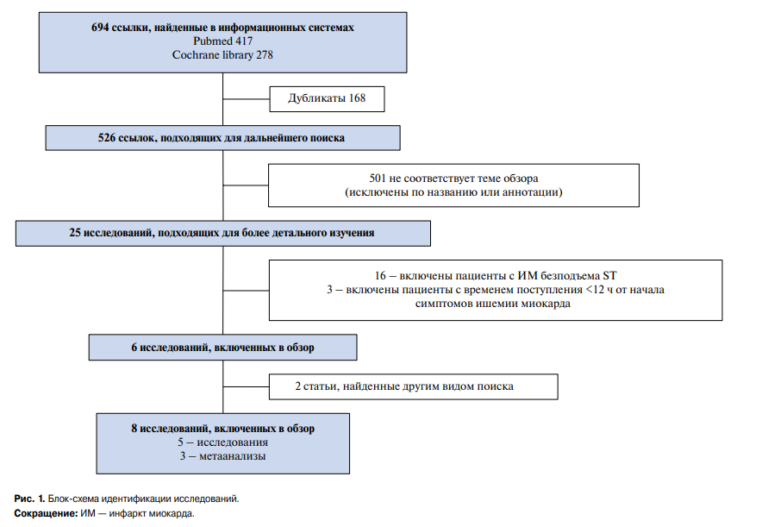
Возможные факторы риска, способствующие развитию фибрилляции предсердий у пациентов с сердечной недостаточностью с умеренно сниженной фракцией выброса
Аннотация
Цель. Изучение возможных факторов риска (ФР) развития пароксизмальной и персистирующей фибрилляции предсердий (ФП) у пациентов с хронической сердечной недостаточностью с умеренно сниженной фракцией выброса (ХСНусФВ).
Материал и методы. В исследование были включены 193 пациента с ХСНусФВ и неклапанной пароксизмальной/персистирующей ФП. В качестве контрольной группы обследовались 76 сопоставимых пациентов, но без ФП. Все пациенты были подвергнуты детальному физикальному обследованию, включая электрокардиографию (ЭКГ), эхокардиографию, суточное мониторирование артериального давления и холтеровское мониторирование ЭКГ. Уровни маркеров воспаления, а именно высокочувствительного С-реактивного белка, интерлейкина-6, фактора некроза опухоли-a и фиброзного маркера, трансформирующего фактора роста-b1 (TGF-b1) измеряли с помощью метода ELISA. Полученные результаты анализировались, используя метод бинарной логистической регрессии и отношения шансов (OШ), который позволяет оценить взаимосвязь конкретного исхода с возможными ФР и сравнить группы исследования по частоте выявления данного ФР.
Результаты. Установлено, что более высокий уровень диастолического артериального давления (ДАД) (ОШ 1,09, доверительный интервал (ДИ): 1,011,17, р=0,017) является возможным ФР возникновения пароксизмальной ФП у больных с ХСНусФВ. Возможными ФР пароксизмальной и персистирующей ФП у подобных больных являются учащение эпизодов гипертонического криза (ОШ 1,17, ДИ: 1,07-1,43, р=0,001) и увеличение индекса массы тела (ИМТ) (ОШ 1,13, ДИ: 0,93-1,27, р=0,031). Увеличение индекса ОШ диастолических и систолических показателей левого желудочка ассоциировалось со значительным ремоделированием предсердий и желудочков, что способствует прогрессированию ФП от пароксизмальной к персистирующей. Более высокие уровни маркеров воспаления наблюдались у пациентов с ФП по сравнению с пациентами с ХСНусФВ без ФП. Увеличение ОШ уровня маркера фиброза TGF-b1 (ОШ 3,84, ДИ: 2,10-6,23, p=0,005) было статистически значимым у пациентов с персистирующей ФП.
Заключение. Используя метод ОШ, можно предположить, что повышение ДАД, частоты гипертонических кризов, ИМТ, ремоделирование левого предсердия и желудочков, увеличение маркеров системного воспаления и фиброза являются возможными ФР возникновения ФП у пациентов с ХСНусФВ.
Сердечная недостаточность (СН) широко распространена во всем мире: число случаев СН удвоилось с 33,5 млн в 1990г до 64,3 млн в 2018г, глобальная распространенность остается высокой [1]. В основе СН лежат функциональные и структурные нарушения миокарда. Основные патогенетические механизмы, способствующие СН, включают повышенную гемодинамическую перегрузку, дисфункцию миокарда, часто связанную с ишемией, мутации сократительных белков, ремоделирование желудочков и измененную нейрогуморальную стимуляцию [2]. СН развивается вследствие множества причин, которые затрудняют точную классификацию и лечение [3-5]. СН с умеренным снижением фракции выброса (ФВ) (СНусФВ) была впервые признана Европейским обществом кардиологов в качестве нового фенотипа СН в 2016г. Из более чем 6,5 млн пациентов с СН в США 13-24% составляли больные с СНусФВ [6]. Тем не менее характеристики СНусФВ и ее терапевтический потенциал остаются недостаточно изученными. Фибрилляция предсердий (ФП) является наиболее частым устойчивым и гетерогенным типом аритмии. Имеются опубликованные данные, связывающие возникновение и прогрессирование ФП с воспалением и фиброзом [7][8]. Хотя ФП и СН являются разными заболеваниями, все чаще обнаруживается, что в принципе они имеют общность определенных патогенетических механизмов. Данные Фремингемского исследования сердца показывают, что ФП возникает более чем у половины лиц с СН, а СН встречается более чем у трети лиц с ФП. Таким образом, СН и ФП часто встречаются вместе, тесно взаимосвязаны и каждое из этих заболеваний может способствовать появлению другого. Причем пациенты с сопутствующей СН и ФП имеют более тяжелые симптомы и худший прогноз, а также более высокую летальность [9]. Однако, хотя СНусФВ хорошо описана, детерминанты (основные клинические и функциональные характеристики) и прогноз хронической СНусФВ (ХСНусФВ) с сопутствующей ФП остаются неясными. В настоящем исследовании мы постарались выявить возможные факторы риска (ФР), связанные с возникновением и прогрессированием ФП у пациентов с ХСНусФВ.
Материал и методы
Клинико-функциональные характеристики обследованных пациентов
Нами проведено исследование пациентов с неклапанной ФП и СН, поступивших в НИИ кардиологии в период с 2018 по 2022гг. Всего выявлено 373 пациента с ХСНусФВ. Из этих пациентов у 273 с пароксизмальной/персистирующей ФП проведена успешная кардиоверсия и только они были включены в исследование. Из вовлеченных в исследование больных у 103 был пароксизм ФП, а у 90 — персистирующая форма ФП. Для сравнения в качестве контрольной группы были обследованы сопоставимые 76 пациентов с ХСНусФВ, но без ФП. Критериями включения были: ФВ 49-40% и N-концевой промозговой натрийуретический пептид >125 пг/мл, а также наличие ишемической болезни сердца и/или артериальной гипертонии. Ишемическая этиология определялась на основании документированного анамнеза инфаркта миокарда или коронарографии. Критериями исключения были: СН вследствие клапанных пороков сердца, хронической обструктивной болезни легких, острого коронарного синдрома, некоронарогенных заболеваний сердца (кардиомиопатии, миокардиты) и системных воспалительных заболеваний. Пациенты с диабетом и нарушениями функции щитовидной железы также не включались в исследование.
Наблюдение за пациентами осуществлялось в соответствии со стандартной клинической практикой центра. Все участники прошли детальное физикальное обследование, которое включало запись электрокардиограммы (ЭКГ) в покое в 12 отведениях, эхокардиограммы (ЭхоКГ), суточное мониторирование артериального давления и 24-часовое холтеровское мониторирование. Все обследуемые пациенты заполняли анкету об их образе жизни (курение, употребление алкоголя >50 мл, питание). Были изучены ФР, клинические, инструментальные и лабораторные характеристики пациентов. Для холтеровского мониторирования ЭКГ использовались 12-канальные портативные кардиорегистраторы «Norav Medical LTD» с непрерывной 24-часовой записью ЭКГ. Так как одним из основных электрофизиологических факторов возникновения и поддержания ФП является негомогенность скорости предсердного проведения, то ЭКГ отображением данного процесса является дисперсия волны Р (Рdis или ДВР), которая определяется как разница между максимальной (Рmax) и минимальной (Рmin) продолжительностью волны Р, регистрируемой во II отведении ЭКГ.
Для измерения ФВ левого желудочка (ЛЖ) по стандартным критериям использовали традиционную трансторакальную ЭхоКГ «Medison SonoAceX6» (Венгрия). Использовались двухмерный режим, стандартные позиции с определением интегральных параметров левого предсердия (ЛП) и ЛЖ, размер ЛП (РЛП), объём ЛП (ОЛП), конечно-диастолический размер ЛЖ, конечно-диастолический объём ЛЖ, конечно-систолический объём ЛЖ, толщина задней стенки ЛЖ, толщина межжелудочковой перегородки, относительная толщина стенки ЛЖ. Были рассмотрены следующие характеристики диастолической функции ЛЖ: максимальная скорость раннего наполнения (Е пик) ЛЖ, максимальная скорость предсердной систолы (А пик), отношение пиковых скоростей трансмитральных потоков Е и А (Е/А), время спада пика Е или время замедления раннего диастолического наполнения ЛЖ, а также время изоволюметрического расслабления миокарда ЛЖ.
Биохимические и иммунологические исследования крови были проведены в лаборатории НИИ кардиологии. Уровни интерлейкина-6 (ИЛ-6), фактора некроза опухоли-α, трансформирующего фактора роста-β1 и высокочувствительного С-реактивного белка измеряли с помощью стандартных наборов для ELISA с использованием анализатора Stat Fax 303 Plus. Количественные характеристики определялись с использованием стандартных лабораторных процедур.
Статистически значимые различия между параметрами были выявлены с помощью двухэтапного кластерного анализа. Полученные данные были смоделированы с помощью бинарной логистической регрессии с использованием индекса отношения шансов (OШ) или «odds ratio» (OR). Результаты применения индекса ОШ включают в себя определение статистической значимости связи между фактором и результатом (исходом), а также ее количественную оценку. Очень важно оценить статистическую значимость выявленной связи между исходом и ФР. При этом в каждом случае статистическая значимость индекса ОШ обязательно оценивается на основе значений 95% доверительного интервала (ДИ) (значение p<0,05 считалось значимым). Исследования проводились по простым рандомизированным протоколам с использованием универсального статистического пакета SPSS 13.0.
Исследование было выполнено в соответствии с правилами GCP и принципами Хельсинкской Декларации, а также было утверждено этическим комитетом в каждом исследовательском центре. Каждый участник исследования до выполнения каких-либо связанных с исследованием процедур дал письменное согласие на участие.
Результаты
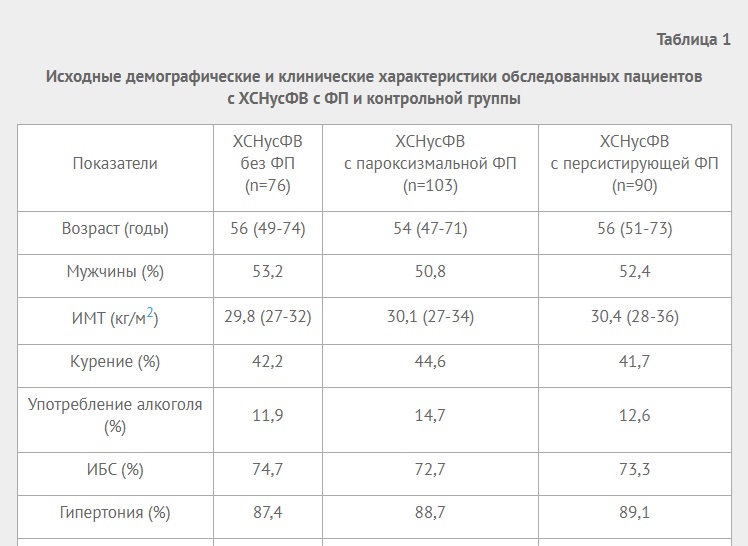
В таблице 1 представлены демографические и клинические характеристики всех обследуемых пациентов. При анализе демографических характеристик пациентов все группы были сопоставимы по полу, возрасту и индексу массы тела (ИМТ). Группы были также схожи по доле пациентов с курением и употреблением алкоголя.
Как было указано выше для оценки риска развития пароксизмальной ФП по сравнению с группой без ФП использовали значения показателя ОШ. При этом значимыми ФР для пациентов с ХСНусФВ и ФП относительно группы контроля, т. е. подобных больных, но без ФП были: возраст (ОШ 1,18; ДИ: 1,08-1,28; р=0,05); диастолическое артериальное давление (ОШ1,09; ДИ: 1,01-1,17; р=0,017); частота гипертонических кризов (ОШ 1,17; ДИ: 1,07-1,43; р=0,01); ИМТ (ОШ 1,13; ДИ: 0,93-1,27; р=0,031) (табл. 2). По данным ЭКГ, максимальная продолжительность зубца P (Pmax) и дисперсия зубца P (Pdis) были значительно удлинены и по всей вероятности связаны с повышенным риском ФП: как пароксизмальной (Pmax: ОШ 3,92; ДИ: 3,88-3,96; p=0,002; Pdis: ОШ 3,91; ДИ: 3,87-3,95; р=0,002), так и персистирующей (Pmax: ОШ 4,81; ДИ: 4,07-5,94; р<0,001; Pdis: ОШ 4,90; ДИ: 4,86-5,93; р<0,001) (табл. 2 и 3). Более того, на основании ЭхоКГ измерений установлено, что при увеличении ОЛП достоверно увеличивается риск возникновения пароксизмальной ФП (ОШ 1,76; ДИ: 1,66-1,88; р=0,002). Стоит отметить также повышение уровня маркеров системного воспаления (высокочувствительного С-реактивного белка: ОШ 5,57; ДИ: 3,38-7,87; р=0,01; цитокин ИЛ-6: ОШ 4,80; ДИ: 2,72-6,88; р=0,001; цитокин фактора некроза опухоли-α: ОШ 2,56; ДИ: 1,43-4,73; р=0,002) у пациентов с ФП, что способствует высокому риску развития пароксизмальной и персистирующей ФП у пациентов с ХСНусФВ (табл. 2).
У больных ХСНусФВ с персистирующей ФП (табл. 3) значимыми ФР относительно группы контроля были: частота гипертонических кризов (ОШ 1,56; ДИ: 1,04-1,97; р=0,001) и ИМТ (ОШ 1,97; ДИ: 0,98-2,21; р=0,044). Значения ОШ для РЛП и ОЛП также были значительно выше (OШ 3,69; ДИ: 2,58-4,82; p=0,002; OШ 3,80; ДИ: 2,65-4,09; p=0,04, соответственно). Анализ ЭхоКГ данных показал, что диастолическая дисфункция ЛЖ является возможным ФР у пациентов с персистирующей ФП по сравнению с пациентами с пароксизмальной ФП. Статистически значимое увеличение значения ОШ наблюдалось для толщины межжелудочковой перегородки (OШ 1,69; ДИ: 1,48-1,98; p=0,042), пика E (OШ 3,05; ДИ: 3,01-3,05; p=0,012) и время изоволюметрического расслабления миокарда ЛЖ (OШ 3,94; ДИ: 3,90-4,99; р=0,016). Выявлено также, что у пациентов с персистирующей ФП важное значение имеет нарушение систолической функции ЛЖ, риск персистирующей ФП был связан с увеличением конечно-диастолического размера ЛЖ (OШ 1,76; ДИ: 1,58-1,99; p=0,046), конечно-диастолического объёма ЛЖ (OШ 1,93; ДИ: 1,89-2,09; p=0,02) и некоторым снижением ФВ (OШ 1,30; ДИ: 1,08-1,57; р=0,05). Помимо повышенного значения ОШ маркеров системного воспаления наблюдается увеличенный ОШ профибротического маркера трансформирующего фактора роста-β1 (ОШ 3,84; ДИ: 2,10-6,23; p=0,005), что также может служить возможным ФР персистирующей ФП у пациентов с ХСНусФВ (табл. 3).
Таблица 1
Исходные демографические и клинические характеристики обследованных пациентов с ХСНусФВ с ФП и контрольной группы
|
Показатели |
ХСНусФВ без ФП |
ХСНусФВ с пароксизмальной ФП (n=103) |
ХСНусФВ с персистирующей ФП |
|
Возраст (годы) |
56 (49-74) |
54 (47-71) |
56 (51-73) |
|
Мужчины (%) |
53,2 |
50,8 |
52,4 |
|
ИМТ (кг/м2) |
29,8 (27-32) |
30,1 (27-34) |
30,4 (28-36) |
|
Курение (%) |
42,2 |
44,6 |
41,7 |
|
Употребление алкоголя (%) |
11,9 |
14,7 |
12,6 |
|
ИБС (%) |
74,7 |
72,7 |
73,3 |
|
Гипертония (%) |
87,4 |
88,7 |
89,1 |
|
Гиперхолестеринемия (%) |
47,9 |
48,9 |
46,8 |
|
ЧСС в покое (уд./мин) |
75,2 (68-89) |
76,7 (72-91) |
74,3 (65-90) |
|
САД в покое (мм рт.ст.) |
145,9 (125-155) |
148,9 (131-160) |
147,6 (131-150) |
|
ДАД в покое (мм рт.ст.) |
83,7 (75-95) |
78,1 (70-90) |
84,7 (75-95) |
Сокращения: ДАД — диастолическое артериальное давление, ИМТ — индекс массы тела, ИБС — ишемическая болезнь сердца, САД — систолическое артериальное давление, ЧСС — частота сердечных сокращений, ФП — фибрилляция предсердий, ХСНусФВ — хроническая сердечная недостаточность с умеренной сниженной фракцией выброса.
Таблица 2
Анализ значений ОШ различных клинико-гемодинамических и структурно-функциональных показателей, а также маркеров воспаления и фиброза у пациентов СНусФВ с пароксизмальной ФП по сравнению с контрольной группой*
|
Показатель |
ХСНусФВ с пароксизмальной ФП (n=103) |
||
|
OШ |
95% ДИ |
P |
|
|
Пол |
0,24 |
0,10-0,58 |
0,07 |
|
Возраст |
1,18 |
1,08-1,28 |
0,05* |
|
САД |
1,00 |
0,94-1,05 |
0,987 |
|
ДАД |
1,09 |
1,01-1,17 |
0,017* |
|
ЧСС |
1,03 |
0,98-1,08 |
0,182 |
|
ГК |
1,17 |
1,07-1,43 |
0,01* |
|
Преходящие ишемические атаки |
0,65 |
0,14-2,93 |
0,583 |
|
ИБС |
1,16 |
0,39-3,42 |
0,788 |
|
Инфаркт миокарда в анамнезе |
1,6 |
0,65-4,33 |
0,285 |
|
Pmax |
3,92 |
3,88-3,96 |
0,002* |
|
Pdis |
3,91 |
3,87-3,95 |
0,002* |
|
ИМТ |
1,13 |
0,93-1,27 |
0,031* |
|
РЛП |
0,86 |
0,70-1,06 |
0,167 |
|
ОЛП |
1,76 |
1,66-1,88 |
0,002* |
|
КДД ЛЖ |
0,92 |
0,71-1,20 |
0,558 |
|
КДО ЛЖ |
0,99 |
0,94-1,04 |
0,811 |
|
КСД ЛЖ |
0,98 |
0,89-1,08 |
0,770 |
|
ТМЖП |
0,94 |
0,68-1,31 |
0,751 |
|
ТЗС ЛЖ |
0,96 |
0,64-1,45 |
0,877 |
|
ФВ |
1,11 |
0,94-1,30 |
0,188 |
|
Е пик |
1,00 |
0,96-1,03 |
0,959 |
|
А пик |
1,00 |
0,93-1,08 |
0,927 |
|
Е/А |
1,05 |
0,04-2,32 |
0,975 |
|
ВСЕ |
0,99 |
0,97-1,02 |
0,777 |
|
ВИР |
0,99 |
0,95-1,03 |
0,661 |
|
вчСРБ |
5,57 |
3,38-7,87 |
0,01* |
|
ИЛ-6 |
4,80 |
2,72-6,88 |
0,001* |
|
ФНО-α |
2,56 |
1,43-4,73 |
0,002* |
|
ТФР-β1 |
0,57 |
0,00-4,2 |
0,995 |
Сокращения: ВИР — время изоволюметрической релаксации левого желудочка, ВСЕ — время спада пика Е, вчСPБ — высокочувствительный С-реактивный белок, ГК — гипертонический криз, ДАД — диастолическое артериальное давление, ДИ — доверительный интервал, ИБС — ишемическая болезнь сердца, ИЛ-6 — интерлейкин-6, ИМТ — индекс массы тела, КДД ЛЖ — конечно-диастолический диаметр левого желудочка, КДО ЛЖ — конечно-диастолический объем левого желудочка, КСД ЛЖ — конечно-систолический диаметр левого желудочка, ОЛП — объем левого предсердия, OШ — отношение шансов, Пик А — пик позднего диастолического наполнения, Пик Е — пик раннего диастолического наполнения левого желудочка, РЛП — размер левого предсердия, САД — систолическое артериальное давление, ТМЖП — толщина межжелудочковой перегородки, ТЗС ЛЖ — толщина задней стенки левого желудочка, ТФР-β1 — трансформирующий фактор роста-β1, ФВ — фракция выброса, ФНО-α — фактор некроза опухоли-α, ФП — фибрилляция предсердий, ХСНусФВ — хроническая сердечная недостаточность с умеренной сниженной фракцией выброса, ЧСС — частота сердечных сокращений, Pdis — дисперсия P-волны, Pmax — максимальная продолжительность зубца P.
Таблица 3
Анализ значения ОШ различных клинико-гемодинамических и структурно-функциональных показателей, а также маркеров воспаления и фиброза у пациентов СНусФВ с персистирующей ФП по сравнению с контрольной группой*
|
Показатель |
ХСНусФВ с персистирующей ФП (n=90) |
||
|
ОШ |
95% ДИ |
P |
|
|
Пол |
0,30 |
0,12-0,74 |
0,09 |
|
Возраст |
1,06 |
0,98-1,14 |
0,101 |
|
САД |
0,98 |
0,94-1,04 |
0,661 |
|
ДАД |
1,00 |
0,94-1,07 |
0,801 |
|
ЧСС |
0,96 |
0,92-1,01 |
0,142 |
|
ГК |
1,56 |
1,04-1,97 |
0,001* |
|
Преходящие ишемические атаки |
0,69 |
0,14-2,93 |
0,583 |
|
ИБС |
1,32 |
0,45-3,83 |
0,608 |
|
Инфаркт миокарда в анамнезе |
2,20 |
0,81-5,95 |
0,120 |
|
Pmax |
4,81 |
4,07-5,94 |
0,001* |
|
Pdis |
4,90 |
4,86-5,93 |
0,001* |
|
ИМТ |
1,97 |
0,98-2,21 |
0,044* |
|
РЛП |
3,80 |
2,65-4,09 |
0,04* |
|
ОЛП |
3,69 |
2,58-4,82 |
0,002* |
|
КДР ЛЖ |
1,76 |
1,58-1,99 |
0,046* |
|
КДО ЛЖ |
1,93 |
1,89-2,09 |
0,019* |
|
КСО ДЖ |
0,96 |
0,88-1,06 |
0,480 |
|
ТМЖП |
1,69 |
1,48-1,98 |
0,042* |
|
ТЗС ЛЖ |
0,83 |
0,55-1,24 |
0,368 |
|
ФВ |
1,30 |
1,08-1,57 |
0,05* |
|
Е пик |
3,05 |
3,01-3,09 |
0,012* |
|
А пик |
0,93 |
0,86-1,00 |
0,059 |
|
Е/А |
1,05 |
1,02-2,55 |
0,720 |
|
ВСЕ |
0,97 |
0,95-1,00 |
0,071 |
|
ВИР |
3,94 |
3,90-4,99 |
0,016* |
|
вчCРБ |
6,37 |
5,24-8,59 |
0,002* |
|
ИЛ-6 |
5,78 |
4,71-7,87 |
0,001* |
|
ФНО-α |
2,51 |
2,37-4,68 |
0,002* |
|
ТФР-β1 |
3,84 |
2,10-6,23 |
0,005* |
Сокращения: ВИР — время изоволюметрической релаксации левого желудочка, ВСЕ — время спада пика Е, вчСPБ — высокочувствительный С-реактивный белок, ГК — гипертонический криз, ДАД — диастолическое артериальное давление, ДИ — доверительный интервал, ИБС — ишемическая болезнь сердца, ИЛ-6 — интерлейкин-6, ИМТ — индекс массы тела, КДО ЛЖ — конечно-диастолический объем левого желудочка, КДР ЛЖ — конечно-диастолический размер левого желудочка, КСД ЛЖ — конечно-систолический диаметр левого желудочка, КСО ЛЖ — конечно-систолический объем левого желудочка, ОЛП — объем левого предсердия, OШ — отношение шансов, Пик А — пик позднего диастолического наполнения, Пик Е — пик раннего диастолического наполнения левого желудочка, РЛП — размер левого предсердия, САД — систолическое артериальное давление, ТМЖП — толщина межжелудочковой перегородки, ТЗС ЛЖ — толщина задней стенки левого желудочка, ТФР-β1 — трансформирующий фактор роста-β1, ФВ — фракция выброса, ФНО-α — фактор некроза опухоли-α, ФП — фибрилляция предсердий, ХСНусФВ — хроническая сердечная недостаточность с умеренной сниженной фракцией выброса, ЧСС — частота сердечных сокращений, Pdis — дисперсия P-волны, Pmax — максимальная продолжительность зубца P.
Обсуждение
ФП является наиболее частой и неоднородной аритмией по спектру симптомов. В настоящее время большое внимание уделяется оценке качества жизни, возможных ФР и сопутствующих заболеваний, которые способствуют ремоделированию предсердий, тем самым приводя к ухудшению течения и прогноза ФП.
Было продемонстрировано, что дисфункция ЛП, а также их структурные нарушения играют важную роль в инициировании ФП, т. е. электрическое и структурное ремоделирование предсердий способствует развитию и прогрессированию ФП [10]. В настоящее время существующие данные неоспоримо свидетельствуют об участии воспаления в патогенезе ФП. Более того, известно, что ФП имеет тесную связь с СН, поскольку многие исследования показали, что ФП и СН часто сосуществуют, имеют общие предрасполагающие факторы и могут ухудшить общий прогноз [9][11]. Мы изучили клинические, структурные и биохимические предикторы пароксизмальной/персистирующей ФП у пациентов с ХСНусФВ и сравнили их с подобными пациентами с ХСНусФВ без ФП. Результаты наших исследований показывают, что склонность к ожирению является одним из возможных ФР возникновения ФП у пациентов с ХСНусФВ. У людей с избыточным весом частота, распространенность, тяжесть и прогрессирование ФП выше, чем у людей с нормальным весом. Пациенты с ожирением часто имеют множественные ФР развития ФП, которые улучшаются в ответ на потерю веса; это делает предпочтительным консолидированный подход к снижению веса и управлению ФР возникновения ФП. Аналогичным образом, стабильная потеря веса снижает тяжесть ФП и рецидивов после лечения, а обратное структурное ремоделирование сердца в ответ на потерю веса предполагает улучшение профиля аритмии. Метаанализ 10 исследований с участием 108996 пациентов показал, что на каждые 5% увеличения веса частота возникновения ФП увеличивается на 13% (отношение рисков 1,13; 95% ДИ: 1,04-1,23; p<0,01). Авторы этого исследования пришли к выводу, что увеличение веса связано с повышенным риском ФП [12]. Наши данные свидетельствуют о том, что ИМТ пациентов является значимым ФР возникновения пароксизмальной и персистирующей ФП у пациентов с ХСНусФВ.
Исследования последних лет продемонстрировали корреляцию между изменениями анатомической структуры предсердий и уровнем воспалительных цитокинов. Этот феномен был принят как новый взгляд на изучение патогенеза ФП, особенно у пациентов с СН [13]. Многие исследователи указывают на связь маркеров воспаления ИЛ-6 и высокочувствительного С-реактивного белка с возникновением и прогрессированием ФП [14][15]. Проведенное нами сравнение возможных ФР, связанных с пароксизмальной и персистирующей ФП, позволяет предположить, что факторы-предикторы по-разному способствуют возникновению и прогрессированию ФП. Так, ОШ показателей электрического ремоделирования предсердий (Pmax и Pdis) оказался достаточно информативным при анализе, что может подчеркнуть особую важность повреждения предсердий в возникновении ФП.
На основании изучения взаимосвязи между диастолической функцией ЛЖ и риском возникновения ФП выяснилось, что эти параметры, возможно, не играют особой роли при формировании пароксизмальной формы ФП, но имеют достаточно решающее значение для персистирующей формы ФП.
Ограничения исследования. В исследование не включены пациенты с ХСНусФВ, у которых кардиоверсия не дала положительных результатов; в исследование не включены пациенты с сахарным диабетом; ROC-анализ для определения отрезных значений факторов, ассоциированных с ФП, не проводился.
Заключение
У пациентов с ХСНусФВ возможными ФР возникновения ФП являются повышенное диастолическое артериальное давление, частота гипертонических кризов, РЛП, диастолическая дисфункция ЛЖ, а также повышение уровня маркеров воспаления и фиброза.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Азарапетян Л.Г., Айрапетян Г.Г., Григорян С.В. Возможные факторы риска, способствующие развитию фибрилляции предсердий у пациентов с сердечной недостаточностью с умеренно сниженной фракцией выброса. Российский кардиологический журнал. 2024;29(1S):5769. https://doi.org/10.15829/1560-4071-2024-5769. EDN: IAADCO
Скопировать