Случай сложной диагностики редкой причины легочной гипертензии
Интерес к изучению причин формирования и под — ходов к лечению легочной гипертензии (ЛГ) существенно возрос в последние 2 десятилетия. Это связано с расширением как диагностических методик, так и терапевтических стратегий лечения, что способствовало существенному прогрессу в улучшении качества и длительности жизни пациентов с ЛГ. В классификации причин ЛГ Европейского общества кардиологов (2015) выделяют 5 основных групп [1]:
1) Легочная артериальная гипертензия (ЛАГ);
2) ЛГ, обусловленная поражением левых камер сердца;
3) ЛГ, обусловленная патологией легких и/или гипоксией;
4) ЛГ из-за обструкции легочной артерии (ЛА);
5) ЛГ, обусловленная неясными многофакторными механизмами.
Последняя (пятая) группа представляет собой достаточно разнородный по своим этиологическим и патогенетическим проявлениям набор заболеваний, редко встречающихся в практике врача-кардиолога.
В представленной работе разбирается поэтапный диагностический анализ крайне редкого случая развития ЛГ при миелопролиферативном заболевании.
Описание клинического случая
Пациентка В., 50 лет, доставлена в клинику с жалобами на выраженную слабость, одышку при минимальной физической нагрузке и в покое, сердцебиение, перебои в работе сердца, повышение артериального давления до 160 170/95 мм рт.ст.; увеличение живота в объеме; боли в суставах; выраженную сухость и шелушение кожи.
Из анамнеза известно, что описанные жалобы имелись в течение одного года с прогрессирующим снижением толерантности к физическим нагрузкам. При сборе анамнеза жизни установлено, что 2 года назад пациентка обследовалась у гинеколога по поводу миомы матки, были выявлены анемия, лейкоцитоз, тромбоцитоз. В течение 2-х лет похудела на 18 кг. Около 1 года беспокоят боли в разных суставах, выраженная слабость, увеличение периферических лимфатических узлов различной локализации (шейных, затылочных, паховых, подмышечных). Консультирована ревматологом и гематологом: диагностирован деформирующий артроз стоп, высказано предположение о лимфопролиферативном заболевании, в связи с чем была выполнена стернальная пункция и биопсия лимфатического узла, по данным которых признаков острого и хронического гемобластоза не получено. Назначена терапия витамином В12 и фолиевой кислотой, на фоне которой анемия скорректирована.
Данные объективного осмотра. Общее состояние: тяжелое. Астеническое телосложение, истощена. Рост — 160 см, вес — 40 кг. Индекс массы тела — 15,62 кг/м2. Кожные покровы: сухие; гиперпигментация кожи, мелко- и крупнопластическое шелушение; умеренный акроцианоз (рис. 1). Увеличены подчелюстные и подмышечные лимфоузлы. Видимые слизистые оболочки: бледные, цианотичные. Подкожная клетчатка практически отсутствует. Отечность голеней и стоп; отечность передней брюшной стенки, асцит. Сердечно-сосудистая система: ритм правильный с частотой сердечных сокращений (ЧСС) 98 уд./мин. 2 тон — акцентирован на ЛА, определяется мягкий систолический шум на верхушке; пульс 98 уд./мин, ритмичный, слабого наполнения, артериальное давление: 100/60 мм рт.ст. Органы дыхания: грудная клетка — правильной формы; дыхание везикулярное, ослабленное; хрипы не выслушиваются; частота дыхания 20 в 1 мин. Органы пищеварения: язык — сухой, обложен белым налетом. Живот увеличен, при пальпации болезненный в правом подреберье, определяется свободная жидкость в брюшной полости. Печень: пальпаторно увеличена — нижний край на 2,5-3 см выступает из-под реберной дуги; край плотный, ровный, размер по Курлову 12?10?9 см. Опорно-двигательный аппарат: деформация суставов (рис. 2). Мочеполовая система: Симптом поколачивания отрицательный с обеих сторон.
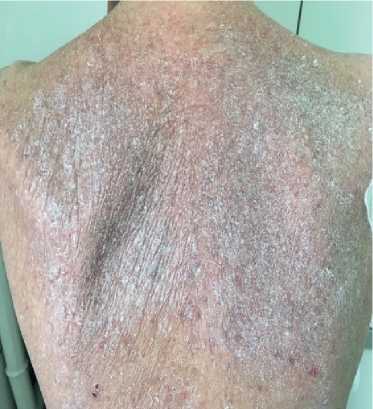
Рис. 1. Кератоз кожи спины пациентки В., 50 лет.
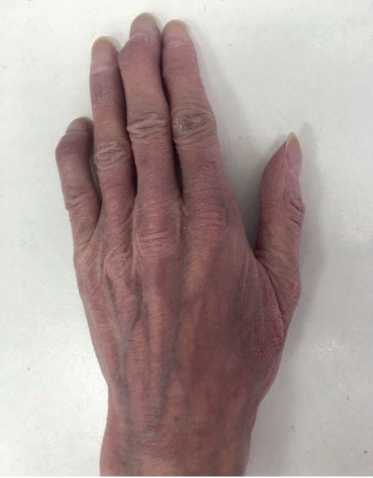
Рис. 2. Деформация суставов кисти пациентки В., 50 лет.
Таким образом, у пациентки имели место следующие симптомокомплексы: 1) отечный (асцит, отеки нижних конечностей); 2) гепатомегалия; 3) кожный; 4) суставной; 5) дыхательная недостаточность; 6) лимфаденопатия.
По данным инструментальных методов исследования выявлены следующие изменения:
Электрокардиограмма — синусовая тахикардия с ЧСС 100 уд./мин. Электрическая ось сердца отклонена вправо. Снижен вольтаж зубцов. Нарушение проводимости по правой ножке пучка Гиса. Признаки нагрузки на правый желудочек (ПЖ) (рис. 3).
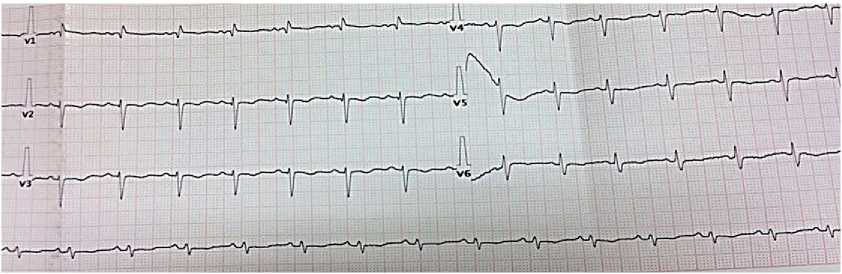
Рис. 3. Электрокардиограмма при поступлении пациентки В., 50 лет: синусовый ритм, ЧСС 86 уд./мин. QT 400 мс. Электрическая ось сердца отклонена вправо.
Неполная блокада правой ножки пучка Гиса.
Эхокардиография (ЭхоКГ) — аорта: восходящий отдел: 30 мм Регургитация на аортальном клапане: ++. Левое предсердие 29 мм. Конечный диастолический размер левого желудочка (ЛЖ): 38 мм, межжелудочковая перегородка (МЖП) 9 мм, задняя стенка (ЗС) ЛЖ 10 мм. Фракция выброса ЛЖ (по Симпсону): 43%. Диффузный гипокинез стенок ЛЖ с парадоксальным движением МЖП. Допплерография митрального клапана: +. Без выраженной реакции на фазы дыхания. Правое предсердие (ПП) 55?58 мм. ПЖ 32 мм. Приточный отдел ПЖ 53 мм. Диффузный гипокинез стенок ПЖ. Верхушка сердца выполнена преимущественно ПЖ. Трикуспидальный клапан (ТК) створки: уплотнены утолщены. Прогиб створок ТК в полость ПП. Допплерография ТК: +++, (+++/++++) ЛА: с признаками выраженной гипертензии. Давление диастолическое: 25 мм рт.ст. Систолическое давление 90 мм рт.ст. Допплерография ЛА: ++. Нижняя полая вена: 20 мм, реакция неадекватная, с эффектом спонтанного контрастирования. По всему периметру сердца эхо-свободное пространство: перед ПЖ из эпигастрального доступа 12 мм, над ПП 5 мм, у верхушки ЛЖ 5 мм, за боковой стенкой 12 мм, за ЗС ЛЖ 17 мм (рис. 4, 5).
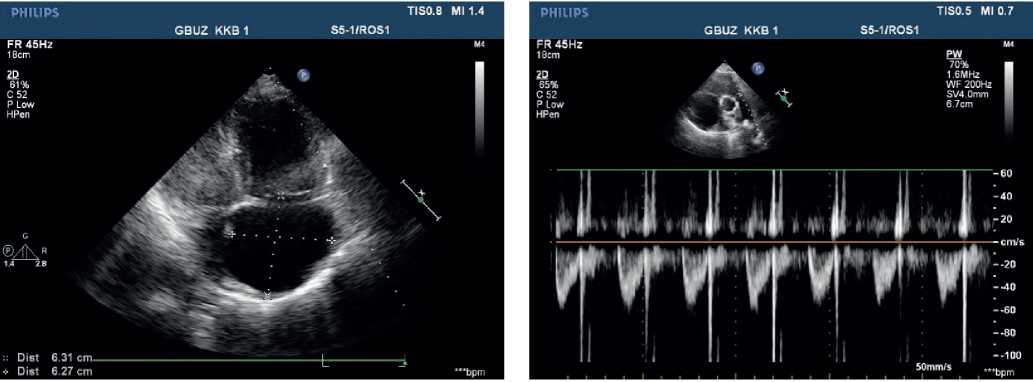
Рис. 4, 5. ЭхоКГ при поступлении пациентки В., 50 лет: высокая ЛГ. Выраженная недостаточность ТК. Дилатация правых отделов.
Рентгенография органов грудной клетки — легкие без очаговых и инфильтративных изменений. Кардиомегалия 3 ст., кардиоторакальный индекс 52% (рис. 6).
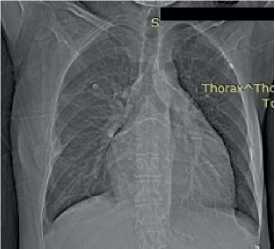
Рис. 6. Рентгенография органов грудной клетки пациентки В., 50 лет: легочные поля без очаговых и инфильтративных изменений. Правый корень структурен. Левый перекрыт тенью сердца. Синусы свободны. Сердце расширено влево. Кардиоторакальный индекс 52%.
На основании вышеописанных данных дифференциально-диагностический ряд включал: онкологическое заболевание с паранеопластическим синдромом, патологию сердечно-сосудистой системы, патологию легких с формированием легочного сердца и хронической сердечной недостаточности. Не исключалось сочетание нескольких заболеваний.
Пациентке выполнены фиброгастроскопия, колоноскопия, ультразвуковое исследование гениталий, данных за новообразование не выявлено.
При анализе ЭхоКГ обратило внимание высокое значение давления в ЛА и расширение правых отделов сердца в отсутствие структурной патологии левых камер сердца.
Согласно клиническим рекомендациям по диагностике и лечению пациентов с ЛГ, наиболее часто встречается ЛГ вследствие патологии левых камер сердца [1].
Для исключения патологии левых отделов сердца как возможной причины ЛГ было выполнено зондирование правых отделов сердца катетером СванГанса, по данным которого давление заклинивания в ЛА — 13 мм рт.ст., систолическое давление в ЛА — 48 мм рт.ст., легочное сосудистое сопротивление — 380 мм; индекс легочного сосудистого сопротивления — 412, что говорит в пользу прекапиллярной ЛГ.
С целью исключения легочной патологии выполнена компьютерная томография (КТ) легких и оценена функция внешнего дыхания (ФВД). КТ органов грудной клетки: структурной патологии легких не выявлено. ФВД: умеренные нарушения по рестриктивному типу. Учитывая возможность наличия высокой ЛГ на фоне хронической тромбоэмболической болезни легких, выполнена КТ ЛА с контрастированием, по данным которой признаков тромбоза не выявлено (рис. 7).
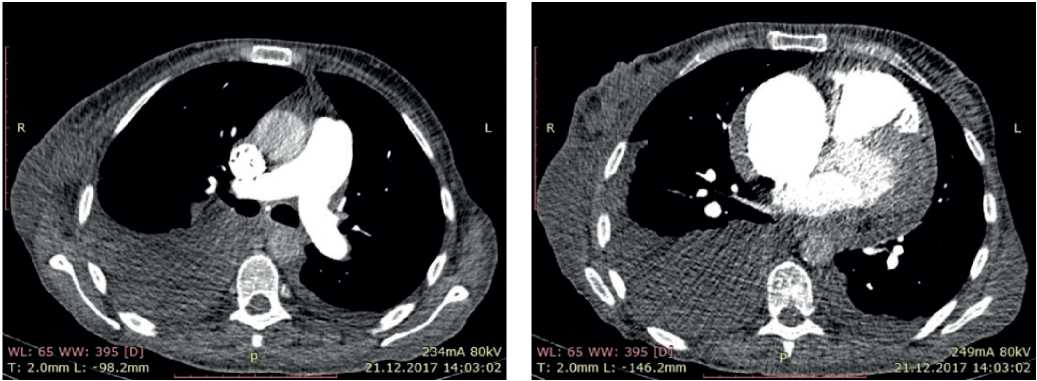
Рис. 7. КТ пациентки В., 50 лет: лимфаденопатия подмышечных областей. гидроперикард. двусторонний гидроторакс.
Как известно, ЛАГ наиболее часто может быть обусловлена наличием врожденных пороков сердца (дефекты межпредсердной перегородки/МЖП, открытый артериальный проток, частичный аномальный дренаж легочных вен), а также ВИЧ-инфекцией и портальной гипертензией. По данным чреспищеводной ЭхоКГ, КТ сердца с контрастированием, ультразвукового исследования органов брюшной полости и лабораторных исследований данные причины были исключены, наличие ВИЧ-инфекции также не выявлено.
Возраст пациентки на момент развития симптомов и наличие сопутствующих синдромов системного поражения (кожный, кахексия, лимфаденопатия) делало маловероятным наследственный характер ЛГ.
В последующем диагностический поиск был направлен на выявление патологий, входящих в группу ЛГ с неясными и/или множественными механизмами. Наличие лимфаденопатии, суставного синдрома, гепатомегалии позволило заподозрить наличие лимфопролиферативного заболевания.
Данные морфологического и иммунногистохимического анализа биоптатов:
Морфологически: кожа — эпидермис с гиперкератозом, неравномерно истончен, в базальном слое лимфоидный инфильтрат с педжетоидным типом роста, выраженным экзоцитозом, представлен клетками среднего размера с ядрами неправильной формы, выраженной складчатостью ядерной мембраны. Лимфоузлы — структура лимфоузлов нарушена за счет резкого расширения паракортикальной зоны, инфильтрированной полигональными клетками
с ядрами неправильной формы, складчатой ядерной мембраной. Предсуществующие фолликулы мелкие с истонченной мантийной зоны, оттеснены опухолевым инфильтратом. Синусы расширены. Мозговой слой с липоматозом. (серия биопсий представлена на рисунках 8-10). Заключение гистологического исследования: иммуноморфологическая картина соответствует синдрому Сезари с поражением лимфатических узлов. Диагноз: Синдром Сезари — Т клеточная лимфома с поражением лимфатических узлов.
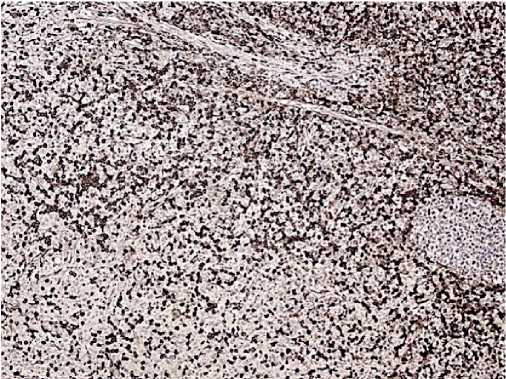
Рис. 8. CD4, clone 4B12 реакция положительная в большинстве клеток опухолевого инфильтрата.
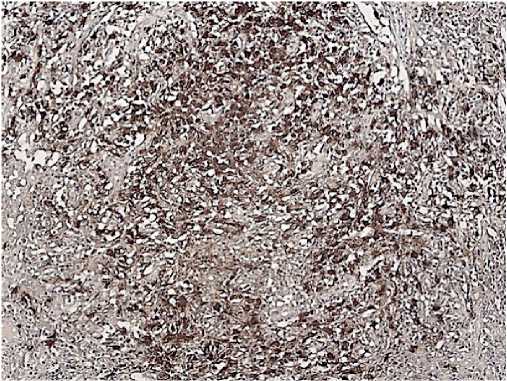
Рис. 9. CD8, Clone C8/144B реакция положительная в части клеток опухолевого инфильтрата.
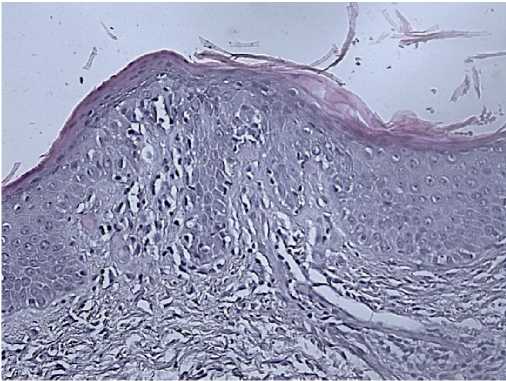
Рис. 10. Биопсия кожи пациентки В., 50 лет.
Заключительный диагноз: Синдром Сезари (grade III), II клин. группа. Высокая ЛАГ на фоне лимфопролиферативного заболевания (синдром Сезари). Хроническое легочное сердце, хроническая сердечная недостаточность II Б стадии.
На фоне проводимой терапии (диуретическая, пульсурежающая) увеличилась толерантность к физической нагрузке, регрессировал отечный синдром. Спустя 4 года динамического наблюдения пациентка жива, чувствует себя удовлетворительно, получает рекомендуемую терапию.
Синдром Сезари — крайне редкое заболевание — 3 случая на 1 млн населения [2][3], которое является вариантом Т-клеточной лимфомы (вовлечены CD4+ Т-лимфоциты периферические) и характеризуется генерализованной эритродермией, лимфаденопатией и наличием клеток Сезари в коже, лимфатических узлах и периферической крови [3][4].
Важное значение имеет ранняя диагностика этого синдрома для начала адекватной терапии, т.к. случаи полной реконвалесценции или длительной ремиссии у больных синдромом Сезари казуистически редки [5].
Согласно литературным данным, случаи высокой ЛГ описываются у пациентов с В-клеточной лимфомой. Подобные случаи при Т-клеточных лимфомах крайне редки [4][5].
Обсуждение
Представленный клинический случай, согласно последней классификации, относится к пятой группе причин ЛГ.
По классификации лимфоидных опухолей ВОЗ (2008) грибовидный микоз/синдром Сезари относится к первичным Т-клеточным лимфомам кожи из зрелых (периферических) клеток [2]. Заболевание впервые описал французский дерматолог Алибер в 1806г. Он же в 1832г предложил название, подчеркнув характерные клинические проявления болезни, — грибовидные опухоли. В 1879г французский дерматолог Базен подробно описал клинику классической формы заболевания, и с тех пор оно носит имя Алибера-Базена. Первое описание болезни в России сделал А.М. Стуковенков в 1889г [1][5]. Французский дерматолог Сезари в 1938г впервые описал 59-летнюю женщину с генерализованной эритродермией, лимфаденопатией, интенсивным зудом и наличием в периферической крови “чудовищных”, “уродливых” моноцитоидных клеток [1]. Синдром Сезари составляет 2-3% всех злокачественных лимфом [2]. Он рассматривается как лейкемический вариант заболевания, характеризующийся хронической эритродермией с диффузной лимфоидной инфильтрацией дермы, выходом аномальных лимфоцитов в кровь и поражением костного мозга [4]. Классические клетки Сезари имеют крупные складчатые ядра, сходные с головным мозгом, в связи с чем и получили название “церебриформных” или “мозговидных” клеток. В основном они локализуются в верхних слоях дермы и эпидермисе и имеют иммунологический фенотип Т-хелперов (СD2+, CD3+, CD4+, CD5+) [2].
Данный диагноз устанавливается на основании комплексной оценки клинической картины заболевания, гистологического и иммунофенотипического исследования биоптатов из очагов поражения кожи, определения перестройки гена Т-клеточного рецептора. Необходимо отметить, что в настоящее время не существует единых общепринятых диагностических критериев грибовидного микоза, а клинические руководства значительно различаются между собой в объеме рекомендуемых исследований, необходимых для постановки диагноза. Клиническое обследование пациента остается основополагающим методом в диагностике, т.к. дает возможность определить разновидность и стадию этого заболевания, но при лейкемической форме Т-клеточной лимфомы кожи возрастает значимость обычного клинического анализа периферической крови [5].
Поражение легких при Т-клеточных лимфомах встречается примерно в 10% случаев [6]. Основным механизмом развития ЛГ у таких пациентов считается стимуляция эндотелиальных клеток сосудов факторами, связанными с тромбоцитами — в первую очередь серотонином и фактором роста [7]. Другими вероятными причинами рассматриваются повышенная вязкость крови при аномалиях функции иммуноглобулинов [8][9] и микроэмболия опухолевыми клетками [8].
Заключение
В представленном клиническом случае продемонстрирован последовательный алгоритм диагностических шагов, позволивший установить редкую причину ЛГ. Учитывая нечастое упоминание синдрома Сезари в кардиологической литературе, объединение разобщенных клинических синдромов, характерных для данного заболевания, в единую нозологию представляет диагностическую сложность.
Отсутствие рекомендаций по терапии ЛГ у пациентов с лимфопролиферативными заболеваниями требует индивидуального подхода к назначению ЛАГ-специфической терапии в каждом конкретном случае.