Пероральные антикоагулянты в сравнении с антагонистами витамина К в лечении неклапанной фибрилляции предсердий у пациентов с хронической болезнью почек 4-5 стадии
Применение пероральных антикоагулянтов у пациентов с неклапанной фибрилляцией предсердий (ФП) и хронической болезнью почек (ХБП), в т. ч. находящихся на гемодиализе (ГД), вызывает затруднения в клинической практике [1]. Наличие ХБП у пациентов с ФП обуславливает увеличение риска как тромбоэмболических, так и геморрагических осложнений. Таким образом, при подборе антикоагулянтной терапии у данной категории пациентов необходимо учитывать соотношение максимальной эффективности в отношении профилактики тромбоэмболических осложнений при наименьшем риске развития кровотечений и прогрессировании почечной дисфункции. Антагонисты витамина К (АВК) являются стандартом лечения пациентов с высоким риском развития тромбоэмболических осложнений, однако необходимость регулярного контроля международного нормализованного отношения и возможных межлекарственных взаимодействий создает определенные трудности для пациентов и ухудшает приверженность к терапии. Наблюдательные исследования не смогли убедительно продемонстрировать влияние АВК на снижение риска тромбоэмболии в популяции, находящейся на ГД [2][3]. Кроме того, пациенты, находящиеся на ГД, получающие АВК, имеют непропорционально высокий риск кровотечений, в частности геморрагического инсульта [3][4]. По данным крупного метаанализа 15 рандомизированных исследований (Wald R, et al., 2020) с участием 47840 пациентов с терминальной почечной недостаточностью, получающих хронический ГД, не было выявлено статистически значимой разницы относительно частоты развития ишемического инсульта, клинически значимого кровотечения и общей смертности при сравнении групп на терапии варфарином и плацебо, однако прием варфарина достоверно увеличивал частоту случаев геморрагического инсульта [5]. Имеются научные данные о повышенном риске кальцификации сосудов у пациентов, принимающих АВК, что особенно важно в популяции диализных пациентов, для которых характерна данная проблема. Однако, по данным недавнего рандомизированного контролируемого исследования (РКИ) Jame S и Barnes G (2020), влияние АВК на кальцификацию сосудов не было подтверждено [6][7].
Использование прямых пероральных антикоагулянтов (ПОАК) неуклонно растет в рутинной клинической практике, несмотря на небольшое количество данных об их безопасности и эффективности, отсутствие утвержденных инструкций и рекомендаций по применению в группе пациентов, находящихся на ГД. Ожидается, что ПОАК будут иметь лучший профиль в отношении риска и пользы, чем АВК в данной категории пациентов. ПОАК обеспечивают более предсказуемый и пропорциональный дозе антикоагулянтный эффект, что особенно важно для диализных пациентов, которым крайне сложно контролировать международное нормализованное отношение. Кроме того, ПОАК ассоциируются с более низким риском внутричерепного кровотечения и не влияют на кальцификацию сосудов [6]. Пациентам с ФП и сохраненной функцией почек рекомендуется назначать ПОАК в качестве первой линии антикоагулянтной терапии, учитывая их эффективность и низкий риск кровотечений [6]. При ХБП с умеренно сниженной функцией почек субанализы ведущих РКИ продемонстрировали эквивалентную или превосходящую эффективность и безопасность ПОАК по сравнению с АВК при условии снижения рекомендуемой дозы препаратов в зависимости от клиренса креатинина [8-10]. Однако, учитывая особенности популяции, находящейся на заместительной почечной терапии, данные по использованию антикоагулянтной терапии неоднозначны. Метаанализ, проведенный Kuno T, et al. (2020), показал, что прием ряда антикоагулянтных препаратов не был связан со снижением риска тромбоэмболии у пациентов с ФП, находящихся на длительном ГД: варфарин, дабигатран и ривароксабан ассоциировались со значительно более высоким риском кровотечения по сравнению с апиксабаном и отсутствием антикоагулянтной терапии. Наибольшую безопасность относительно риска развития больших кровотечений имел апиксабан. По результатам анализа, авторы делают выводы, что соотношение пользы и риска ПОАК у пациентов с ФП, находящихся на длительном ГД, требует проверки в рандомизированных клинических исследованиях [8]. Более того, снижение риска крупных кровотечений при применении апиксабана по сравнению с АВК, по-видимому, увеличивается по мере снижения функции почек [11][12].
Предположения о преимуществах применения ПОАК по сравнению с АВК у пациентов с ХБП 4-5 стадии и получающих хронический ГД не имеют достоверных доказательств. Обсервационные исследования демонстрируют, что апиксабан связан с более низким риском крупного кровотечения и инсульта по сравнению с АВК [13], с более высоким риском смертельного или внутричерепного кровотечения и аналогичным риском инсульта по сравнению с отсутствием антикоагулянтов [14] в группе пациентов на ГД. Результаты наблюдательных исследований следует интерпретировать с осторожностью, поскольку нельзя исключить предвзятость вследствие избирательного назначения препарата. В настоящее время проведены три РКИ, оценивающие безопасность апиксабана по сравнению с АВК у пациентов с ФП, находящихся на ГД. В РКИ AXADIA (NCT02933697) рандомизировано 222 пациента (прием АВК или 2,5 мг апиксабана 2 раза/сут. в течение 6-24 мес.) [15]. SAFE-D (NCT03987711) включает 150 участников, за которыми наблюдали в течение 26 нед. (сравнение АВК с 5 мг апиксабана 2 раза/сут. (или 2,5 мг 2 раза/сут. у пациентов, соответствующих критериям снижения дозы) и группа без антикоагулянта). В исследовании RENAL-AF (NCT02942407) участвовало 760 пациентов с наблюдением в течение 15 мес. Сравнивались АВК с 5 мг апиксабана 2 раза/сут. (или 2,5 мг 2 раза/сут. у пациентов, отвечающих критериям снижения дозы). Исследование было преждевременно прекращено после включения 154 пациентов. Предварительные данные не показали разницы между группами лечения в отношении развития инсульта, кровотечения и смертельного исхода [16].
Таким образом, применение антикоагулянтов у пациентов с ФП и ХБП 4-5 стадии, в т. ч. находящихся на заместительной почечной терапии, требует обоснования путем проведения систематического обзора и метаанализа для оценки риска инсульта, кровотечений и иных исходов.
Целью представленного метаанализа является оценка и сопоставление рисков развития инсульта, кровотечений и иных неблагоприятных исходов у пациентов с ХБП 4-5 стадии и неклапанной ФП, принимающих АВК и ПОАК.
Материал и методы
Систематический обзор и метаанализ выполнены в соответствии с международными рекомендациями (PRISMA) (рис. 1). Для поиска статей использовалась стратегия PICO:
- пациент (Patient) — пациенты старше 18 лет с ФП и ХБП 4-5 стадии (в т. ч. получающие хронический ГД);
- вмешательство (Intervention) — применение ПОАК;
- сравнение (Comparison) — применение АВК;
- исходы (Outcomes) — количество конечных точек: ишемический инсульт, системные эмболии, геморрагический инсульт, большие кровотечения, малые кровотечения, желудочно-кишечные кровотечения, общая смертность.
Включенные в метаанализ 6 исследований содержат информацию о 873 пациентах.
Среди 6 РКИ одно исследование проведено в Российской Федерации. Исследование Pokorney S, 2019г было остановлено в связи с отсутствием финансирования, однако часть его результатов доступна [13]. Остальные РКИ проведены в соответствии с протоколами и включали небольшие выборки. Таким образом, вероятность смещений на различных этапах проведения данных исследований расценивается как достаточно низкая. Ниже представлен график «светофор» (рис. 2). Все включенные исследования по-разному декларировали оценку конечных точек, учет критериев безопасности и эффективности. Цели данных исследований также не были идентичны, что потенциально может привести к конфаундингу при оценке взвешенного эффекта.
Отбор исследований. В метаанализ были включены все исследования, сравнивающие ПОАК и АВК у лиц с ФП и ХБП 4-5 стадии, в т. ч. получающих хронический ГД. На рисунке 1 показана PRISMA-диаграмма отбора.
Критерии исключения:
- исследования, в которых не сообщалось о клинических исходах,
- статьи, в которых не вся группа имела ФП,
- статьи, в которых пациенты имели расчетную скорость клубочковой фильтрации >29 мл/мин/1,73 м2.
Извлечение данных и оценка качества. 5 рецензентов независимо друг от друга извлекли данные, включая подробности публикаций, критерии включения/исключения, демографические данные пациентов, объем выборок и полученные результаты. Системные ошибки публикаций оценивались с помощью воронкообразного графика. Асимметричность графика свидетельствовала о системной ошибке публикации (табл. 1).
В исследование включено 873 пациента, из которых на терапии АВК находились 406 пациентов, на апиксабане — 348, на ривароксабане — 119 пациентов. В целом группы были сопоставимы по основным демографическим показателям.

Рис. 1. Диаграмма отбор PRISMA.

Рис. 2. График оценки публикационного смещения типа «светофор».
Таблица 1
Характеристики пациентов, включенных в исследование
|
Автор и ссылка на исследование |
Количество пациентов |
Препарат ПОАК |
Средний возраст, лет |
Женский пол, % |
Средний балл по CHA2DS2-VASc |
Инсульт, % |
СН, % |
АГ, % |
СД, % |
ИМ, % |
Средний балл по шкале НАSBLED |
Прием антиагрегантов, % |
|
De Vriese AS (2020) [18] |
АВК — 44 Р — 46 |
ривароксабан |
АВК — 80,3 Р — 79,9 |
АВК — 43,3 Р — 23,9 |
АВК — 4,8 Р — 4,7 |
АВК — 36,4 Р — 32,6 |
АВК — 20,5 Р — 37,0 |
нет данных |
АВК — 45,5 Р — 45,5 |
АВК — 47,7 Р — 45,7 |
АВК ‒ 4,7 Р — 4,6 |
АВК ‒ 31,8 Р ‒ 32,6 |
|
Pokorney S (2019) [13] |
АВК — 72 A — 82 |
апиксабан |
нет данных |
АВК — 3٠,6 A — 41,5 |
АВК ‒ 16,7 А ‒ 20,7 |
АВК ‒ 52,9 А ‒ 52,4 |
АВК ‒ 93,1 А ‒ 96,3 |
АВК ‒ 65,3 А ‒ 51,2 |
АВК ‒ 30,6 А ‒ 19,5 |
АВК ‒ АСК 45,7; клопидогрел 2,5; А ‒ АСК 36,7; клопидогрел 2,5 |
||
|
Chashkina M (2020) [31] |
АВК — 36 Р — 73 |
ривароксабан |
АВК — 78 Р — 77 |
АВК — 61 Р — 56 |
АВК — 4,7 Р — 4,6 |
АВК — 36 Р — 10 |
АВК — 44 Р — 56 |
АВК — 96 Р — 98 |
АВК — 44 Р — 37 |
АВК ‒ 44 Р ‒ 40 |
АВК ‒ 3,1 Р ‒ 3 |
нет данных |
|
Reinecke H (2022) [17] |
АВК ‒ 49 А ‒ 48 |
апиксабан |
АВК ‒ 74,8 А ‒ 74,7 |
АВК ‒ 24,5 А ‒ 35,4 |
АВК ‒ 4,54 А ‒ 4,5 |
нет данных |
АВК ‒ 22,5 А ‒ 33,3 |
нет данных |
нет данных |
АВК ‒ 24,5 А ‒ 18,8 |
АВК ‒ 4,15 А ‒ 4,25 |
АВК ‒ 34,7 А ‒ 33,3 |
|
Stanifer JW (2020) [13] |
АВК ‒ 133 А ‒ 136 |
апиксабан |
‒ |
АВК ‒ 59,4% А ‒ 61,8 |
АВК ‒ 4,7 А ‒ 4,9 |
АВК ‒ 24,8 А ‒ 29,4 |
АВК ‒ 40,6 А ‒ 56,6 |
АВК ‒ 88,7 А ‒ 87,5 |
АВК ‒ 23,3 А ‒ 2٠,6 |
‒ |
АВК, А ‒ 2,3 |
АВК ‒ АСК 41,4; клопидогрел 2,3; А ‒ АСК 32,4; клопидогрел ‒ 1,5 |
Сокращения: А — апиксабан, АВК — антагонист витамина К, АГ — артериальная гипертензия, АСК — ацетилсалициловая кислота, ПОАК — прямые пероральные антикоагулянты, Р — ривароксабан, СД — сахарный диабет, СН — сердечная недостаточность.
Результаты
Оценка критериев эффективности. Основной целью приема антикоагулянтов среди пациентов с ФП является профилактика тромбоэмболических осложнений. Среди критериев эффективности были оценены развитие нового ишемического инсульта и артериальные эмболии.
Ишемический инсульт. В отношении ишемического инсульта ПОАК в целом оказались сопоставимыми с варфарином во всех исследованиях, отношение шансов (ОШ) 0,42 [ 0,14; 1,24], р=0,12 (рис. 3).
Визуально на воронкообразном графике результаты РКИ смещены больше в сторону преимущества ПОАК. Однако другое крупное РКИ уравновешивает влияние, минимизируя публикационное смещение (рис. 4).
При добавлении субанализа РКИ ARISTOTLE trial [12], где ишемический инсульт входил в состав комбинированной конечной точки ишемического инсульта/системной эмболии, значимого изменения выявлено не было, хотя тенденция к преобладанию ПОАК становилась более отчетливой (ОШ 0,51 [ 0,25; 1,04], р=0,06) (рис. 5).
Тенденция на воронкообразном графике также осталась прежней (рис. 6).
При оценке системных эмболий возникла техническая сложность, т. к. в исследовании De Vriese AS, et al. (2020) в обеих группах отсутствовали пациенты, поэтому был добавлен субанализ РКИ ARISTOTLE trial (Stanifer JW, et al. 2020) [12], где системная эмболия входила в состав комбинированной конечной точки «ишемический инсульт/системная эмболия» (рис. 7).
Взвешенный эффект продемонстрировал эквивалентную эффективность ПОАК и варфарина (ОШ=0,51 [ 0,20; 1,43], р=0,21).
Оценка критериев безопасности. Среди критериев безопасности были оценены геморрагические осложнения, связанные с приемом антикоагулянтов, а также общая смертность. Необходимо учитывать возраст, высокую коморбидность и полипрагмазию в категории пациентов, имеющих ХБП 4 и 5 стадии, что будет обуславливать неблагоприятный прогноз.
Результаты по общей смертности были доступны для всех РКИ. В целом преимущества варфарина или ПОАК не отмечалось (рис. 8).
График публикационного смещения в целом симметричный, что говорит о низкой вероятности публикационного смещения (рис. 9).
В отношении больших кровотечений динамика выглядела следующим образом: в двух исследованиях De Vriese AS, 2020 [4] и Stanfer JW, 2020 [13] наблюдалась тенденция превосходства ПОАК, что сместило общий эффект в сторону ПОАК (ОШ 0,47 [ 0,29; 0,77], р=0,03) (рис. 10).
Воронкообразная диаграмма в общем была симметрична, что минимизировало эффект публикационного смещения (рис. 11).
Также прием ПОАК снижал риск развития геморрагического инсульта, хотя статистически значимого превосходства получено не было (ОШ 0,23 [ 0,05; 1,11], р=0,07) (рис. 12).
Воронкообразная диаграмма была симметрична, учитывая, что 2 исследования для ПОАК уравновешивали исследование для варфарина (рис. 13).
В отношении желудочно-кишечных кровотечений значимого доминирования эффекта не было (ОШ 0,57 [ 0,24; 1,34], р=0,20) (рис. 14).
Воронкообразная диаграмма была симметрична, что исключает публикационное смещение.
При изучении развития малых кровотечений преимущество ПОАК было зафиксировано в двух исследованиях, в то время как в других двух приоритета выявлено не было (рис. 15, 16).
Воронкообразная диаграмма была относительно симметричной, поэтому вероятность публикационного смещения низкая (рис. 17).
Суммарный эффект для больших и малых кровотечений был также с тенденцией к наличию статистически значимой взаимосвязи (ОШ 0,45 [ 0,19; 1,04], р=0,06) (рис. 18).
Воронкообразная диаграмма была симметричной, в связи с чем вероятность публикационного смещения низкая (рис. 19).

Рис. 3. График Forrest-plot в отношении количества ишемического инсульта.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 4. График оценки публикационного смещения в отношении ишемического инсульта.

Рис. 5. График Forrest-plot в отношении количества событий комбинированной конечной точки ишемического инсульта/системной эмболии.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 6. График оценки публикационного смещения в отношении комбинированной конечной точки ишемического инсульта/системной эмболии.

Рис. 7. График Forrest-plot в отношении субанализа профилактики комбинированной конечной точки ишемического инсульта/системной эмболии.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 8. График Forrest-plot в отношении субанализа профилактики комбинированной конечной точки ишемического инсульта/системной эмболии.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 9. График оценки публикационного смещения субанализа профилактики комбинированной конечной точки ишемического инсульта/системной эмболии.

Рис. 10. График Forrest-plot в отношении количества больших кровотечений.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 11. График оценки публикационного смещения в отношении количества больших кровотечений.

Рис. 12. График Forrest-plot в отношении количества геморрагического инсульта.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 13. График оценки публикационного смещения в отношении количества геморрагического инсульта.

Рис. 14. График Forrest-plot в отношении количества желудочно-кишечных кровотечений.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 15. График оценки публикационного смещения в отношении количества желудочно-кишечных кровотечений.

Рис. 16. График Forrest-plot в отношении количества малых кровотечений.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 17. График оценки публикационного смещения в отношении количества малых кровотечений.
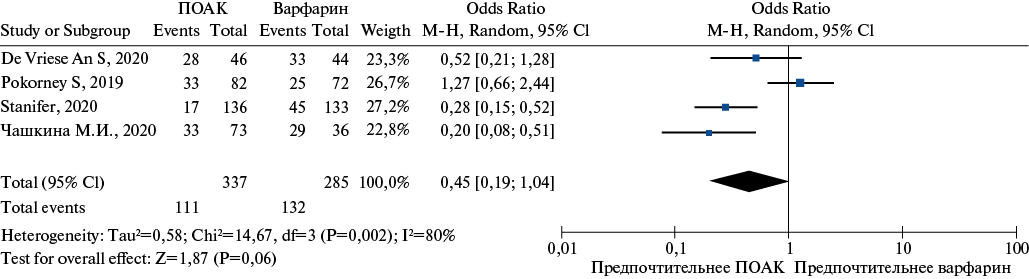
Рис. 18. График Forrest-plot в отношении количества больших и малых кровотечений.
Сокращение: ПОАК — прямые пероральные антикоагулянты.

Рис. 19. График оценки публикационного смещения в отношении количества больших и малых кровотечений.
Обсуждение
Как известно, наличие ХБП у пациентов с ФП ухудшает прогноз, приводит к повышению риска смерти и инвалидизации, а также затрат на лечение. ФП — прогностически неблагоприятный фактор прогрессирования ХБП, в свою очередь ХБП приводит к возникновению ФП. Данный «коморбидный дуэт» объясняется общностью факторов риска и едиными системными процессами 1 [17-20]. Среди пациентов европейской популяции с ФП распространенность ХБП составляет >30% [21], в российской популяции нарушения функции почек встречаются у 47% пациентов с ФП [22].
Наличие у пациента с ФП ХБП сопровождается увеличением как риска развития тромбоэмболических, так и геморрагических осложнений [23-25], что нередко затрудняет назначение антикоагулянтной терапии в реальной клинической практике, особенно у пациентов с выраженным снижением функции почек. В соответствии с современными клиническими рекомендациями по ФП, решение о назначении антикоагулянтной терапии у пациентов с клиренсом креатинина <15 мл/мин, а также находящихся на программном ГД должно приниматься мультидисциплинарной командой специалистов с обязательным учетом индивидуальных особенностей пациента [26]. Проблема с назначением антикоагулянтной терапии в данном случае усугубляется тем, что в подавляющем большинстве исследований терминальная почечная недостаточность служила критерием исключения. В то же время назначение сниженных доз ривароксабана, апиксабана и эндоксабана может быть рассмотрено у пациентов с клиренсом креатинина 15-30 мл/мин [27-28]. Однако вопрос назначения ПОАК у пациентов с терминальной ХБП, а также находящихся на ГД, требует дальнейшего изучения ввиду малого количества исследований в данном направлении.
В настоящий метаанализ из 8247 найденных источников литературы было включено лишь 4 РКИ, имеющие полнотекстовые публикации, посвященные изучению популяции пациентов с ХБП 4 и 5 стадии, и получающих программный ГД. При этом 2 из 4 исследований сравнивали между собой апиксабан и варфарин, в то время как 2 других — ривароксабан и варфарин. Дабигатран в данные исследования не включался, т. к. известно, что он противопоказан при клиренсе креатинина <30 мл/мин, поскольку имеет преимущественный почечный путь выведения.
В соответствии с поставленной целью метаанализа, проводилось сравнение риска развития тромбоэмболических и геморрагических осложнений на фоне терапии ПОАК (апиксабан, ривароксабан), с одной стороны, и варфарином — с другой стороны.
По данным нашего метаанализа, применение ПОАК приводило к статистически незначимому снижению частоты инсультов и/или системных эмболий, по сравнению с терапией варфарином, что в целом сопоставимо с данными метаанализа Ha JT, et al. (2019), который подтвердил более высокую эффективность ПОАК в профилактике инсульта/системных эмболий по сравнению с варфарином у пациентов с терминальной ХБП [11] 2, а также с данными Coleman CI, et al. (2019), также не получивших статистически значимых различий в частоте развития инсульта/системных эмболий на фоне терапии ривароксабаном, по сравнению с варфарином [29]. Данный результат согласовывается с мнением экспертов Европейского общества кардиологов [28]. В то же время в ретроспективном когортном исследовании Siontis KC, et al. (2018) назначение сниженной дозы апиксабана (2,5 мг 2 раза/сут.) пациентам с терминальной ХБП и находящимся на лечении ГД не приводило к статистически значимому снижению частоты инсульта/системных эмболий, по сравнению с варфарином. Однако при назначении стандартной дозы апиксабана (5 мг 2 раза/сут.) происходило статистически значимое уменьшение частоты развития инсульта/системных эмболий, по сравнению с варфарином [30], что отличается от полученных нами результатов.
По данным нашего метаанализа выявлено, что назначение ПОАК пациентам с 4 и 5 стадиями ХБП, а также находящимся на ГД, сопровождалось статистически значимым уменьшением количества больших кровотечений, по сравнению с терапией варфарином. Полученные результаты согласуются с данными ретроспективного когортного исследования Siontis KC, et al. (2018), показавшими статистически значимое снижение частоты больших кровотечений на фоне терапии апиксабаном, по сравнению с варфарином [14], а также обсервационного исследования Coleman CI, et al. (2019), показавшего преимущество ривароксабана в снижении частоты развития больших кровотечений, по сравнению с варфарином [29]. Этот результат также сопоставим с мнением экспертов Европейского общества кардиологов [28].
В ходе метаанализа нами не было продемонстрировано статистически значимого снижением смерти от всех причин среди пациентов, принимающих ПОАК, по сравнению с варфарином, что согласовывается с данными Siontis KC, et al. (2018), не продемонстрировавшими статистически значимое снижение риска смерти у пациентов, принимавших сниженную дозу апиксабана (2,5 мг 2 раза/сут.), по сравнению с терапией варфарином [14]. Однако, по данным этих же авторов, прием пациентами стандартной дозы апиксабана (5 мг 2 раза/сут.) сопровождался статистически значимым снижением риска смерти, по сравнению с терапией варфарином, что отличается от результатов нашего метаанализа.
Ограничения исследования. Проведенное исследование имеет ряд ограничений, многие из которых связаны с дизайном, исключением когортных исследований и представленной неоднородностью данных РКИ, на которые авторы опирались при анализе.
Представленный метаанализ имеет определенные ограничения, связанные с малым количеством исследований, включенных в него, а также сравнительно небольшим количеством пациентов в этих исследованиях, что могло повлиять на полученные результаты.
В опубликованном в прошлом году систематическом обзоре и метаанализе [31] авторами было проведено сравнение, включавшее в себя как РКИ, так и не РКИ, и количество исследований было меньше. В этой публикации проведен другой литературный поиск, включающий в себя только РКИ: рассмотрены два исследования Pokorney S, добавлено последнее исследование 2022г [32], которое к моменту подготовки предыдущей публикации не было обнародовано.
Заключение
В целом, основываясь на результатах проведенного метаанализа, следует отметить, что назначение ПОАК пациентам с терминальной ХБП, а также находящимся на программном ГД, как минимум будет сопоставимо с терапией варфарином по частоте инсульта/системных эмболий, однако при этом будет сопровождаться меньшей частотой развития больших кровотечений. В реальной клинической практике назначение ПОАК категории пациентов с терминальной ХБП, в т. ч. получающей заместительную почечную терапию, при отсутствии показаний в официальных инструкциях к препаратам в каждом конкретном случае следует рассматривать индивидуально междисциплинарной командой специалистов.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1 American College of Cardiology: RENal hemodialysis patients ALlocated apixaban versus warfarin in Atrial Fibrillation — RENAL-AF. Available at: https://www.acc.org/latest-in-cardiology/clinical-trials/2019/11/15/17/29/renal-af. Accessed October 24, 2020.
2 Фибрилляция и трепетание предсердий. Клинические рекомендации. Российское кардиологическое общество. При участии Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции, Ассоциации сердечно-сосудистых хирургов России. 2020. 185 с.
