Стимуляция пучка Гиса. Технические аспекты и доказательная база для применения в качестве альтернативы ресинхронизирующей терапии и традиционной электрокардиостимуляции
Аннотация
Стимуляция проводящей системы представляет собой прямую стимуляцию специализированной проводящей системы сердца Гиса-Пуркинье с целью физиологической активации желудочков, в отличие от диссинхронной активации, производимой обычной стимуляцией миокарда.
В этой обзорной статье, посвященной стимуляции проводящей системы Гиса-Пуркинье, авторы оценивают имеющиеся данные и текущую практику, а также оценивают появляющиеся и будущие направления в этой быстро развивающейся области. Проведен анализ имеющихся публикаций по теме стимуляции пучка Гиса (СПГ) и проводящей системы.
С момента первого сообщения о постоянной СПГ в 2000г методика с использованием стилета в ее самом раннем воплощении была заменена более эффективным подходом без стилета. Широкое внедрение в практику привело к формированию большой доказательной базы. Одноцентровые наблюдательные исследования дополнились крупными многоцентровыми международными регистрами, механистическими исследованиями и первыми рандомизированными контролируемыми трайлами. Новые данные прояснили механизмы СПГ и проиллюстрировали природу и масштаб ее потенциальных преимуществ для предотвращения стимуляционной кардиомиопатии и коррекции блокады ножек пучка Гиса.
Стимуляция проводящей системы сердца является наиболее физиологическим видом кардиостимуляции у пациентов с узким комплексом QRS. Стимуляция проводящей системы сердца может явиться эффективной альтернативой бивентрикулярной стимуляции при кардиоресинхронизирующей терапии. Необходимо проведение рандомизированных контролируемых исследований для расширения доказательной базы.
Правожелудочковая апикальная стимуляция (ПЖАС) приводит к диссинхронной активации желудочков, которая может привести к ухудшению их функции. Альтернативные места стимуляции миокарда, такие как стимуляция перегородки правого желудочка (ПЖ) и стимуляция выходного тракта ПЖ, по-прежнему полагаются на межклеточную проводимость миокарда и не продемонстрировали своей способности предотвращать кардиомиопатию, вызванную стимуляцией [1]. Бивентрикулярная стимуляция (БВС) безусловно лучше ПЖАС, но все еще производит нефизиологический паттерн активации [2]. Прямая стимуляция проводящей системы Гиса-Пуркинье (СПГ) дает возможность сохранить физиологическую активацию желудочков у пациентов с изначально нормальными, узкими комплексами QRS. У пациентов с блокадой ножек пучка Гиса кардиоресинхронизирующая терапия (КРТ) может корректировать нарушения проводимости путем стимуляционной синхронизации активации желудочков [3].
Изначально наиболее предпочтительным местом стимуляции проводящей системы был пучок Гиса, и в настоящее время накоплен большой мировой опыт стимуляции в этой области с публикацией значительного количества данных. В последнее время новые методы привлекли внимание к стимуляции в области левой ветви пучка Гиса, что подтверждается растущим количеством публикаций [4]. В этом современном обзоре СПГ мы оцениваем последние данные и текущую практику, а также изучаем новые и будущие направления в этой быстро развивающейся области.
Терминология
Терминология стимуляции пучка Гиса
Классификация и номенклатура стимуляции проводящей системы сердца изменились с момента своего появления [5], и многие определения теперь стандартизированы [6][7]. В ранних публикациях упоминалась прямая СПГ [8], а также парагисиальная стимуляция [9]. Селективная и неселективная СПГ (ССПГ и НСПГ, соответственно) — это два термина, которые сейчас используются для обозначения СПГ, и их особенности описаны в этом обзоре. При ССПГ происходит захват только пучка Гиса без захвата миокарда. При НСПГ в дополнение к СПГ происходит захват окружающего миокарда межжелудочковой перегородки (МЖП), что приводит к предвозбуждению МЖП на протяжении большей части времени проведения возбуждения от пучка Гиса к желудочкам (HV).
Терминология блока пучка Гиса
Когда СПГ позволяет сузить QRS у пациентов с блокадой левой или правой ножки пучка Гиса (БПНПГ и БЛНПГ), для объяснения основных явлений используются различные термины. Термины «Гис ресинхронизация» или «Гис-КРТ» не отражают механизм укорочения QRS [2]. «Захват ножки» относится к захвату ранее нефункционировавших проводящих волокон, и этот термин используется для дифференциации от сливного фронта волн активации в миокарде, которое может вызывать сужение QRS, когда НСПГ не может захватить правую ножку у пациентов с БПНПГ.
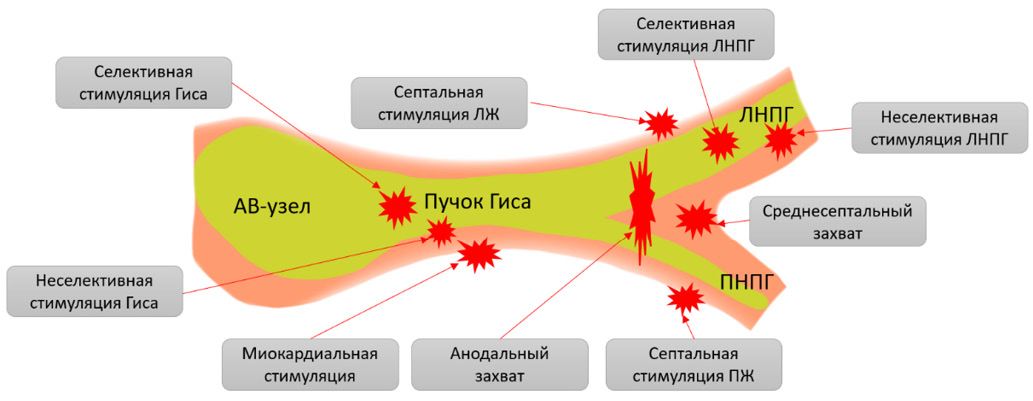
Иллюстрация современной терминологии, анатомии и концептуальной классификации стимуляции проводящей системы представлена на рисунке 1.

Рис. 1. Стимуляция проводящей системы.
Примечание: терминология в зависимости от захваченных стимуляцией проводящей системы структур. Зеленый цвет представляет проводящую систему, а миокард перегородки представлен оранжевым цветом. Красные «звезды» представляют область расположения электрода при различных видах стимуляции. Цветное изображение доступно в электронной версии журнала.
Сокращения: АВ — атриовентрикулярный, ЛЖ — левый желудочек, ЛНПГ — левая ножка пучка Гиса, ПЖ — правый желудочек, ПНПГ — правая ножка пучка Гиса.
Возможные показания для стимуляции проводящей системы
Можно выделить три широкие категории потенциальных показаний для стимуляции проводящей системы: когда ожидается большой процент желудочковой стимуляции, это будет при атриовентрикулярной блокаде (АВБ), при брадисистолическом варианте фибрилляции предсердий (ФП), при стимуляционной кардиомиопатии, после аблации атриовентрикулярного соединения; КРТ у пациентов с сердечной недостаточностью (СН) и блокадой ножек пучка Гиса; дисфункция синусового узла (ДСУ), когда нарушение атриовентрикулярной проводимости может уже сосуществовать или развиться за время наблюдения, для хирурга операция у последней категории пациентов может стать источником опыта в стимуляции проводящей системы, поскольку неуспех этой стимуляции не так критичен для пациента с ДСУ. Учитывая, что СПГ выполняется все более широко, крупные регистры собрали международный опыт, чтобы отразить текущую практическую картину, включая показания [6][10][11]. В работе Keene D, et al. (2019) в многоцентровом регистре, куда было включено 529 пациентов, наиболее распространенным показанием была АВБ, которая была отмечена в половине случаев, а следующее по частоте — брадисистолическая ФП (27,8%) [11]. У остальных пациентов были КРТ, ДСУ и аблация атриовентрикулярного соединения в схожих пропорциях (6,6-8,9%). В многоцентровом исследовании Zanon F, et al. (2019) включены данные 844 пациентов, АВБ (41,2%) и ФП (39,7%) также были наиболее распространенными показаниями, но меньшее количество пациентов получили Гис-КРТ (1,7%) [10]. АВБ первой степени с узким QRS, где стимуляция проводящей системы может быть использована для сокращения предсердно-желудочковой задержки с сохранением физиологической активации желудочков, стоит особняком как потенциальное показание, СПГ при этом показании оценивалась в His Optimized Pacing Evaluated for Heart Failure (HOPE-HF) слепом рандомизированном перекрестном исследовании [12]. В исследование было включено и рандомизировано 167 пациентов с АВ-блокадой I степени, узким комплексом QRS и сниженной фракцией выброса (ФВ) левого желудочка (ЛЖ), всем пациентам была реализована СПГ, в одной группе стимуляцию включали на 6 мес., в другой выключали, на 6 месячном контроле производили переход в другую группу еще на 6 мес. В результате исследователи пришли к выводу, что у пациентов достоверно улучшилось качество жизни и большинство из них предпочло режим с включенной стимуляцией, при этом показатели основного обмена не менялись и функция ЛЖ не ухудшалась [13].
Методы стимуляции проводящей системы
История техники СПГ
Стимуляция в области проводящей системы сердца для достижения физиологической активации желудочков и нормализованного вида QRS посредством прямого захвата пучка Гиса или его ветвей была впервые описана у людей в 1970г [14]. Диагностическая парагисиальная стимуляция была стандартным маневром в электрофизиологических исследованиях в течение десятилетий [15], но имплантация электрода с активной фиксацией в пучок Гиса была впервые описана в 2000г [8]. Первоначальная техника включала картирование области пучка Гиса с помощью управляемого электрофизиологического катетера, проведенного через бедренную вену, после чего формировалась кривизна стилета для позиционирования электрода к области с откартированным пучком Гиса [16]. Этот трудоемкий метод был усовершенствован до современной техники, при которой электрод направляется к пучку Гиса с помощью направляющего катетера специальной формы [15]. На начальном этапе эта методика была дополнена картированием области Гиса с помощью электрофизиологического катетера, также группой, занимающейся СПГ в медицинских центрах Geisinger, была описана возможность картирования сигналов проводящей системы и прилегающего миокарда с использованием встроенного картирующего биполя внутри самой доставочной системы [17].
Современная техника СПГ
Сигнал Гиса и соответствующие предсердные и желудочковые компоненты (желудочковый сигнал, как правило, в 2 раза превышает амплитуду предсердного сигнала) регистрируются на эндокардиальной электрограмме с имплантируемого электрода. Характеристики эндокардиальной электрограммы и электрокардиограммы (ЭКГ) (табл. 1) во время стимуляции помогают определиться с местом для фиксации. В зависимости от используемой модели электрода производится либо вращение самого тела электрода, если это безстилетный электрод с открытой спиралью фиксации, либо выдвижение спирали активной фиксации путем вращения катода на коннекторной части. Когда спирали удается проникнуть в фиброзную капсулу пучка Гиса, волокна проводящей системы внутри пучка Гиса могут быть захвачены при относительно низких порогах.
Регистровые исследования продемонстрировали, что основным методом было использование безстилетного электрода SelectSecure 3830, который показал свою эффективность в стимуляции проводящей системы [6][10][11]. В подавляющем большинстве случаев использовалась доставочная система с фиксированной кривизной C315HIS (Medtronic) для достижения пучка Гиса, значительно реже используется управляемая доставочная система C304 (Medtronic), а еще реже модифицированные доставочные системы для коронарного синуса [18]. Вероятно, популярность системы доставки C315HIS связана прежде всего с тем, что в ней реализованы две кривизны — одна для прохождения трикуспидального клапана и вторая для перпендикулярного позиционирования относительно МЖП. С 2020-х годов свои решения для стимуляции проводящей системы предложили все основные производители — Biotronik, Boston Scientific, Abbott. Их основной отличительной особенностью является использование стандартных стилетных электродов, которые проводятся через специальную доставочную систему в область проводящей системы.
Электрические характеристики при стимуляции пучка Гиса
ССПГ возникает, когда стимуляция происходит без локального захвата окружающего желудочкового миокарда. При этом у пациентов с узкими собственными комплексами QRS на ЭКГ в 12 отведениях регистрируется изоэлектрический интервал между артефактом стимула и началом комплекса QRS (интервал St-нQRS), который обычно приблизительно равен собственному интервалу от потенциала пучка Гиса до начала QRS (интервал HV). Ширина комплексов QRS во время стимуляции равна ширине на собственном ритме, поскольку ЛЖ и ПЖ активируются полностью через проводящую систему Гиса-Пуркинье. Следовательно, время от артефакта стимула до окончания комплекса QRS (St-кQRS) равно времени от потенциала Гиса до окончания комплекса QRS (H-кQRS). Локальная желудочковая электрограмма будет регистрироваться отдельно от артефакта стимула, что указывает на отсутствие локального захвата миокарда (рис. 2).
При НСПГ вместе с захватом пучка Гиса происходит локальный захват миокарда МЖП. Пока волна возбуждения проходит через пучок Гиса и далее по проводящей системе, из-за локального захвата начинается локальная активация рабочего миокарда в базальной части МЖП. В связи с этим комплекс QRS начинается сразу после стимула и характеризуется медленной начальной частью из-за низкой скорости межклеточного проведения в рабочем миокарде. Остальная часть желудочков активируется быстро через систему Гиса-Пуркинье, поэтому активация желудочков (и, следовательно, комплекс QRS) завершается с той же продолжительностью от стимула до конца QRS, что и при ССПГ, но ширина QRS при НСПГ получается больше из-за более раннего начала активации желудочков. Медленное «преждевременное» возбуждение желудочков при НСПГ похоже на дельта-волну у пациентов с манифестными дополнительными путями и называется псевдо-дельта-волной. Из-за наличия местного захвата миокарда локальная желудочковая электрограмма включается в состав артефакта стимуляции или начинается сразу после него (рис. 3).
Если захват пучка Гиса отсутствует, но стимул тем не менее вызывает желудочковую активацию, говорят о миокардиальной стимуляции (МС). Это приводит к медленной активации от клетки к клетке всего миокарда как ПЖ, так и ЛЖ. Измерения, которые помогают различить ССПГ, НСПГ и МС, приведены в таблице 1, показывающей, что интервал H-кQRS является ключевым референтным измерением для различения отдельных комплексов НСПГ от МС. Во время неселективного захвата пучка Гиса H-кQRS будет равен St-кQRS. Для этого требуется одновременная визуализация отведений электрограммы и 12-канальной ЭКГ, предпочтительно в условиях лаборатории для электрофизиологических исследований. При отсутствии возможности измерить длительность референсного интервала H-кQRS можно увидеть внезапное изменение ширины QRS и изменения в морфологии QRS от НСПГ к ССПГ или МС при снижении амплитуды стимула во время проверки порога стимуляции. Это явление позволяет отличить НСПГ от МС.
Если описанный переход одной морфологии в другую не наблюдается (и отсутствует возможность измерения H-кQRS), то при всех амплитудах стимуляции может иметь место либо НСПГ, либо МС, и установить различие может быть не просто. Данные о различии в рефрактерных периодах между проводящей системой и рабочим миокардом привели к разработке метода, впервые предложенного Jastrzebski M, et al. (2019). Этот метод позволяет различать СПГ и МС в подобных случаях [19]. Программируемая стимуляция с фиксированным интервалом S1 и укороченным интервалом сцепления S2 может выявить переход от НСПГ при более длинных интервалах сцепления к МС при самых коротких интервалах сцепления экстрастимула. Поскольку критерии и маневры для подтверждения захвата становятся все более сложными, использование искусственного интеллекта может приобрести важное значение, и было продемонстрировано доказательство этой гипотезы [20]. Оценка и определение захвата проводящей системы у пациентов с нарушением проводимости является более сложной задачей (табл. 2).
ССПГ и НСПГ
Превосходство НСПГ над МС имеет четкую физиологическую основу, и из этих двух видов стимуляции только НСПГ обеспечивает захват проводящей системы. Хотя при МС морфология QRS иногда может лишь слегка отличаться от НСПГ, при МС активация ЛЖ происходит за счет медленного распространения волны возбуждения от клетки к клетке (а не за счет быстрой физиологической активации по проводящей системе) [21]. Однако относительные достоинства и недостатки ССПГ и НСПГ являются темой продолжающейся дискуссии среди специалистов по стимуляции проводящей системы сердца. Морфология ЭКГ в 12 отведениях при ССПГ предполагает, что оба желудочка активируются физиологически, тогда как при НСПГ наблюдается нефизиологическая активация некоторой части септального миокарда. Физиологические последствия этого локального захвата МЖП имеют важное значение, поскольку НСПГ имеет некоторые потенциальные преимущества по сравнению с селективным захватом пучка Гиса. Во-первых, локальный захват миокарда допускает возможность продолжения желудочковой стимуляции в случае развития инфра-гисиальной блокады. Во-вторых, вызванный потенциал захвата миокарда при НСПГ может быть обнаружен с помощью алгоритмов автоматического определения порога стимуляции, что не наблюдается при ССПГ, ограничивая ценность этих алгоритмов [22].
Результаты электроанатомического картирования показывают, что локально происходит захват средне-базального отдела ПЖ, а по данным оценки индексов механической синхронности диссинхрония активации ЛЖ проявляется только при отсутствии захвата проводящей системы (как это происходит при МС), и что при НСПГ диссинхрония ЛЖ не развивается [13, 23]. Измерения с использованием сверхвысокочастотной ЭКГ, которая может пространственно разделять сигналы в пределах комплекса QRS для измерения электрической синхронности ЛЖ, подтверждают данные неинвазивного ЭКГ-картирования о том, что при НСПГ синхронность ЛЖ существенно не отличается от ССПГ или спонтанного проведения [24]. Beer D, et al. (2019) сравнили долгосрочные результаты, включающие госпитализацию по поводу СН или смерть, между ССПГ и НСПГ и не обнаружили существенных отличий [25]. Область локальной активации миокарда при НСПГ слишком мала и скорее похожа на область предвозбуждения от дополнительного пути проведения, которая лишь изредка вызывает кардиомиопатию, связанную с диссинхронией [26].
В настоящее время эксперты сходятся в том, что в подавляющем большинстве случаев диссинхрония, вызванная НСПГ, минимальна, если только спонтанный интервал HV не слишком велик, и в основном ограничивается миокардом ПЖ. В относительно редких случаях, предположительно у лиц с генетической предрасположенностью к дилатационной кардиомиопатии и/или при наличии значительного предвозбуждения миокарда на фоне НСПГ, диссинхрония, вызванная этой стимуляцией, может приводить к нежелательным последствиям. С этим может быть связано небольшое, статистически незначимое расхождение в результатах между ССПГ и НСПГ, наблюдаемое в обсервационном исследовании Beer D, et al. (2019) (хотя эти отличия могут быть связаны с различиями исследуемых групп) [25].
Детекция по электродам, имплантированным в пучок Гиса
Амплитуда зубцов R, измеряемая на электроде в пучке Гиса, как правило, имеет значения <5 мВ. Кроме того, на записи электрической активности с этого электрода могут присутствовать предсердные потенциалы различной амплитуды [3]. Таким образом, существует вероятность недостаточного восприятия желудочковой активности (гипосенсинг) и избыточного (неуместного) восприятия предсердной активности (гиперсенсинг).
Пороги стимуляции по электродам, имплантированным в пучок Гиса
Порог захвата пучка Гиса обычно выше, чем для захвата миокарда ПЖ, но усовершенствования в технике имплантации значительно уменьшили эту проблему. Средние значения порогов захвата пучка Гиса, наблюдавшиеся в двух последних крупных регистрах, составили 1,4±0,9 В при 0,8±0,3 мс и 1,6±1,0 В при 0,8±0,4 мс [8][10][11]. Данные регистра, собранного Keene D, et al. (2019), показали, что существует кривая обучения при СПГ, и что после 30-50 операций получаемый порог стимуляции, как и время рентгеноскопии, снижается [11]. Недавнее исследование, посвященное оценке «тока повреждения» на электрограмме с электрода, имплантированного в пучок Гиса, для определения надежности фиксации электрода в проводящей системе, также позволило улучшить пороги стимуляции [11].
Повышение порога после имплантации наблюдается примерно в 7% случаев при СПГ и может быть вызвано микродислокацией или развитием фиброза. Это явление наблюдается достаточно часто и побуждает некоторых хирургов имплантировать страховочный электрод в ПЖ (хотя эта практика становится все более редкой) [11]. Повышение порога может происходить рано (до первичного контрольного осмотра), хотя случаи очень позднего повышения порога (позже 6 мес. и даже через 1 год после имплантации) также наблюдались, несмотря на стабильные низкие предыдущие пороги [10].
Таблица 1
Электрокардиографические параметры при стимуляции проводящей системы у пациентов с узким комплексом QRS
|
Параметр |
Стимуляция пучка Гиса |
|
Ширина QRS |
МС > НСПГ > ССПГ = спонтанный |
|
Стимул — кQRS |
МС > НСПГ = ССПГ = Гис-кQRS |
|
Стимул — нQRS |
МС = НСПГ < спонтанный H-V = ССПГ |
|
Подтверждение захвата |
Несколько порогов стимуляции* Программированная стимуляция** Гис-кQRS = стимул кQRS |
Примечание: сравнение параметров ЭКГ с различными видами захвата, наблюдаемыми при стимуляции проводящей системы при исходно узком QRS. * — во время проверки порога СПГ: переход от НСПГ к ССПГ или захвату только миокарда (МС) при снижении амплитуды стимуляции, за которым следует второй переход от любого из них до потери захвата. Переходы оцениваются по длительности и морфологии QRS, Стимул-V и времени Стимул-конец QRS (кQRS) из таблицы. Например, переход от НСПГ к ССПГ приведет к сокращению длительности QRS, потере предвозбуждения, удлинению Стимул-V и сохранению времени Стимул-кQRS. ** — программированная стимуляция может помочь, когда нет нескольких порогов стимуляции. Один порог при широком стимулированном QRS до потери захвата может говорить либо о MС, либо НСПГ до потери захвата одновременно миокарда и пучка Гиса. Во время программируемой стимуляции (аналогично декрементному изменению проводимости во время электрофизиологического исследования при наджелудочковых тахикардиях) постепенно укорачивающиеся экстрастимулы, могут выявить разницу рефрактерного периода между тканью пучка Гиса и миокардом.
Сокращения: Гис-кQRS — длительность от потенциала Гиса до окончания QRS, MC — захват только миокарда, НСПГ — неселективная стимуляция пучка Гиса, ССПГ — селективная стимуляция пучка Гиса, Стимул-кQRS — интервал от стимула до окончания QRS, Стимул-V — интервал от стимула до начала QRS, ЭКГ — электрокардиограмма, H-V — интервал от потенциала Гиса до начала QRS.

Рис. 2. ССПГ.
Примечание: стандартные отведения ЭКГ и электрограммы области коронарного синуса и области регистрации пучка Гиса. Во время стимуляции с электрода, регистрирующего Гис, виден селективный захват с морфологией QRS, идентичной исходной.
Сокращения: H — потенциал Гиса, H-кQRS — время от сигнала Гиса до окончания комплекса QRS, HV — интервал Гис-желудочек, St-кQRS — время от стимула до окончания комплекса QRS, St-QRS — интервал между стимулом и началом QRS.

Рис. 3. НСПГ и миокардиальный захват.
Примечание: ЭКГ в стандартных отведениях и электрограммы из коронарного синуса и области пучка Гиса (СПГ). При СПГ виден неселективный захват с морфологией QRS по типу предвозбуждения миокарда (псевдо-дельта-волна). Стимуляция с меньшей амплитудой демонстрирует захват только миокарда межжелудочковой перегородки с более широкими QRS и более длинным интервалом от стимула до конца QRS по сравнению с комплексами с захватом ПГ. Короткое или отсутствующее время Stim-V является общей чертой НСПГ и МС.
Сокращения: МС — миокардиальная стимуляция, НСПГ — неселективная стимуляция пучка Гиса, СПГ — стимуляция пучка Гиса, ЭКГ — электрокардиограмма, H — потенциал Гиса, H-кQRS — время от сигнала Гиса до окончания комплекса QRS, HV — интервал Гис-желудочек, St-кQRS — время от стимула до окончания комплекса QRS, Stim-V — интервал между стимулом и началом QRS.
Таблица 2
Варианты электрического ответа при СПГ при широких собственных комплексах QRS
|
Спонт QRS |
Степень коррекции при СПГ |
Признаки стимуляции пучка Гиса |
|
|
БЛНПГ |
Полная коррекция |
ССПГ Stim-кQRS < H-кQRS |
НСПГ Stim-кQRS < H-кQRS (обычно) Стим шQRS > 120 мс Стим шQRS < Спонт шQRS (обычно) |
|
Частичная коррекция |
ССПГ Stim-кQRS < H-кQRS Стим шQRS < Спонт шQRS |
НСПГ Stim-кQRS </= H-кQRS Стим шQRS > 120 мс Стим шQRS < Спонт шQRS (обычно) |
|
|
Нет коррекции |
Stim-кQRS = H-кQRS |
||
|
ССПГ Стим шQRS = Спонт шQRS |
НСПГ Стим шQRS > Спонт шQRS |
||
|
Захват только миокарда |
Морфология БЛНПГ Stim-кQRS > H-кQRS (обычно) Стим шQRS > Спонт шQRS |
||
|
БПНПГ* |
Захват ПНПГ |
ССПГ Stim-кQRS < H-кQRS Стим шQRS < 120 мс < Спонт шQRS |
НСПГ Stim-кQRS < H-кQRS Стим шQRS <=> Спонт шQRS (обычно) |
|
Ресинхронизация |
НСПГ без захвата ПНПГ Нормальный QRS с предвозбуждением (без блокады ножек ПГ) Stim-кQRS < H-кQRS Стим шQRS < Спонт шQRS |
||
|
Нет захвата |
ССПГ без захвата ПНПГ Морфология БПНПГ Stim-кQRS = H-кQRS |
||
|
Захват только миокарда |
Морфология БЛНПГ Stim-кQRS > H-кQRS |
||
|
НВЖБ |
Частичная коррекция |
Возможны различные варианты морфологии QRS и соотношения интервалов † |
|
|
Нет коррекции |
ССПГ |
НСПГ Стим шQRS <=> Спонт шQRS (обычно) |
|
|
Захват только миокарда |
Морфология БЛНПГ Stim-кQRS <=> H-кQRS Стим шQRS <=> Спонт шQRS |
||
Примечание: сравнение вариантов ответов ЭКГ в 12 отведениях на различные виды захвата проводящей системы при СПГ при широких спонтанных комплексах QRS. * — блокада ПНПГ может быть ресинхронизирована двумя способами: захват ПНПГ с захватом миокарда или без него; и НСПГ без захвата ПНПГ, которая ресинхронизирует правый желудочек из-за наличия по крайней мере двух волновых фронтов в правом желудочке (один от локального захвата миокарда и один от левого желудочка). † — ЭКГ-ответ на стимуляцию проводящей системы при неспецифической внутрижелудочковой блокаде зависит от наличия участков, предрасположенных к коррекции, в правых и левых отделах проводящей системы.
Сокращения: БЛНПГ — блокада левой ножки пучка Гиса, БПНПГ — блокада правой ножки пучка Гиса, НВЖБ — неспецифическая внутрижелудочковая блокада, ПНПГ — правая ножка пучка Гиса, СПГ — стимуляция пучка Гиса, ССПГ — селективная стимуляция пучка Гиса, шQRS — ширина QRS, ЭКГ — электрокардиограмма, H-кQRS — длительность от потенциала пучка Гиса до окончания QRS, Stim-кQRS — длительность от стимула до окончания QRS.
Результаты стимуляции проводящей системы
Вероятность успеха имплантации и профиль безопасности стимуляции проводящей системы
Сообщения об успешности имплантации электродов для СПГ варьируют от 72 до 92%, но в определении, что является успехом отсутствует стандартизованный подход. К тому же при СПГ с целью КРТ (СПГ-КРТ) отмечаются более низкие показатели успеха [3][11][27][28]. Во время имплантации могут наблюдаться преходящая АВБ и БПНПГ. Макродислокации встречаются не часто, но с другой стороны — повышение порогов не является редкостью. Объединяя макродислокацию и высокий порог стимуляции в качестве показаний для повторных интервенций, в наиболее крупных долгосрочных исследованиях частота повторных вмешательств составляет от 6% до 8% [10][11][28][29].
Клинические результаты стимуляции проводящей системы
Несмотря на более чем 20-летний опыт применения постоянной СПГ, несколько лет широкого интереса и внедрения во всем мире, а также значительное присутствие в социальных сетях [30], долгосрочные, крупномасштабные, ориентированные на клинические результаты рандомизированные контролируемые исследование (РКИ) до сих пор не проводились. В первое десятилетие использования БВС в рамках РКИ было рандомизировано >6 тыс. пациентов для сравнения со стандартными методиками, но если текущие темпы сохранятся, то маловероятно, что даже десятая часть этого количества будет рандомизирована в РКИ, посвященные СПГ [31]. Действительно, наличие БВС, которая является стандартом лечения, затрудняет разработку исследований, посвященных СПГ [31]. Поэтому нам приходится полагаться на данные обсервационных исследований, чтобы сделать какие-либо выводы о долгосрочных клинических результатах стимуляции проводящей системы. Улучшение качества жизни, повышение результата теста с 6-минутной ходьбой, увеличение ФВ ЛЖ, уменьшение размеров ЛЖ, снижение риска госпитализаций по поводу СН и смертности были показаны при СПГ по сравнению со стимуляцией ПЖ. Некоторые из наиболее убедительных доказательств получены при сравнении результатов в разных лечебных учреждениях: выполняющем СПГ и выполняющем имплантацию в ПЖ, но со схожими параметрами пациентов и стандартами лечения [32]. СПГ ассоциировалась со статистически значимым снижением на 29% достижения первичной конечной точки, состоящей из смерти, развития СН или смены на БВС. При 2-летнем наблюдении в этом исследовании с участием 756 пациентов эффект был наиболее выражен в подгруппе с бременем желудочковой стимуляции >20% [32].
Ресинхронизирующая терапия с помощью СПГ
Роль стимуляции проводящей системы для ресинхронизации при блокадах ножек пучка Гиса у пациентов с СН является особым показанием. Недавние открытия в этом направлении существенно изменили наш взгляд на данную проблему. El-Sherif N, et al. (1978) наблюдали в 1970-х годах, что стимуляция дистальной части пучка Гиса может скорректировать БЛНПГ и привести к сужению комплексов QRS [33]. В 2010г Lustgarten DL, et al. (2009) продемонстрировали, что этого можно достичь с помощью постоянной СПГ [34]. Последующие обсервационные исследования показали, что СПГ может уменьшить ширину QRS и улучшить насосную функцию сердца, снизить выраженность симптомов у пациентов с СН и БЛНПГ [35-37].
Учитывая эти данные, СПГ-КРТ приобрела распространение как спасение в случаях отсутствия ответа на БВС, но актуальный вопрос заключался в том, дает ли более физиологическая ресинхронизация при СПГ-КРТ лучшие результаты, чем БВС. В 2019г были опубликованы результаты пилотного прямого сравнения двух методик — исследования HIS-SYNC [38], СПГ-КРТ приводила к более выраженному сужению ширины QRS, чем БВС, но статистически значимой разницы в улучшении ФВ ЛЖ обнаружено не было. К сожалению, слабой стороной этого исследования стала высокая частота перехода из группы СПГ в группу БВС, и причины этих переходов показывают текущие проблемы, связанные с СПГ-КРТ. Половина переходов была связана с выявлением по ЭКГ признаков задержки внутрижелудочковой проводимости, а не БЛНПГ. 30% переходов были связаны с невозможностью коррекции БЛНПГ [38]. Arnold AD, et al. (2018) продемонстрировали, что при успешной коррекции БЛНПГ с помощью СПГ гемодинамические и электрические улучшения более выражены, чем при БВС [2]. В то же время результаты HIS-SYNC указывают, что для успешной СПГ-КРТ требуется отбор пациентов с нарушениями в проводящей системе, поддающимися коррекции с помощью СПГ, и что для облегчения коррекции у этих пациентов требуются специализированные инструменты для имплантации [38].
Upadhyay GA, et al. (2019) выявили физиологические основы нарушений проводимости, которые можно использовать для отбора пациентов [39]. Они обнаружили, изучая левостороннюю часть проводящей системы сердца, что у пациентов с картиной БЛНПГ по ЭКГ в 12 отведениях наблюдаются отличия в характере нарушений проводимости. У большинства наблюдалась блокада проведения внутри пучка Гиса, очевидно поддающаяся коррекции с помощью СПГ. У меньшей доли пациентов наблюдалась блокада проведения в рамках проксимальных отделов проводящей системы, но дистальнее пучка Гиса: уровень блока был расположен в левой ножке пучка Гиса [39]. Такие пациенты могли бы ответить на коррекцию с помощью СПГ, но стимуляция левой ножки пучка Гиса представляется более реальным методом коррекции таких дефектов проведения. Важно, что в этой группе, состоящей из поступающих для радиочастотной аблации по поводу желудочковой тахикардии, у существенного количества пациентов (36%) левосторонняя часть проводящей системы оказалась интактной, а наиболее вероятной причиной расширения QRS у этих пациентов была задержка внутрижелудочковой проводимости. Очевидно наличие типичной БЛНПГ по данным ЭКГ в 12 отведениях не позволяют надежно отличать эти подгруппы. Поэтому для повышения эффективности СПГ-КРТ необходимы разработка методов для выявления этих фенотипов БЛНПГ в рутинной практике, а также внедрение инструментов, позволяющих достигать максимальной ресинхронизации при СПГ. Следует отметить, что даже если стимуляция проводящей системы не осуществима, остается возможность стимуляции перегородки ЛЖ, которая может помочь у пациентов с задержкой внутрижелудочковой проводимости и сохранной проводящей системой. К этой группе, например, относятся пациенты с комбинацией гипертрофии ЛЖ и отклонением оси влево, которая может выглядеть на 12-канальной ЭКГ как БЛНПГ. В такой ситуации можно рассчитывать на оптимизацию атриовентрикулярной задержки и улучшение паттерна активации ЛЖ по сравнению со спонтанным проведением [40].
Учитывая, что при стимуляции левой ножки пучка Гиса по ЭКГ наблюдается паттерн БПНПГ, СПГ, вероятно, будет иметь преимущество для пациентов с БПНПГ. СПГ может ресинхронизировать БПНПГ двумя способами: прямым захватом правой ножки пучка Гиса; или через НСПГ столкновение волны возбуждения из базального отдела ПЖ (локальный захват миокарда) с волной возбуждения, возникающей более апикально (от активации ПЖ через левую ножку пучка Гиса) [41].
Достижения и будущие направления в стимуляции проводящей системы
Новые, специализированные доставочные системы для СПГ от разных производителей продолжают развиваться, и вполне вероятно, что последует и специализированное оборудование для стимуляции левой ножки пучка Гиса. Недавно некоторые хирурги вернулись к СПГ с использованием стилета [42][43]. Это позволяет изменять форму электрода, а также использовать альтернативный подход в сложных случаях. Использование трехмерного электроанатомического картирования дает хирургу возможность исключить или минимизировать использование флюороскопии, но сильно увеличивает общее время процедуры [44][45]. В качестве альтернативы подход с использованием только электрограмм и ЭКГ для успешной СПГ с минимальной флюороскопией был описан группой Zanon F, et al. (2020) для электродов SelectSecure 3830 и доставочных интродьюсеров C315 His (Medtronic) [46]. Автоматизированный анализ ЭКГ при СПГ находится в стадии разработки, и это также может способствовать повышению скорости имплантации [20].
Заключение
Таким образом, стимуляция проводящей системы рассматривается как набор методов: СПГ, проксимальной левой проводящей системы и области вокруг нее. Первоначальные исследования СПГ в основном ограничивались одноцентровыми сериями наблюдений, но широкий интерес и внедрение СПГ привели к крупным многоцентровым международным регистрам, долгосрочным исследованиям наблюдения и первым РКИ. С увеличением объема доказательной базы мы получили новое представление о механизмах СПГ, природе и масштабах ее преимуществ, включая ее способность предотвращать вызванную стимуляцией кардиомиопатию и ресинхронизировать БЛНПГ. Более тщательное изучение также выявило ограничения СПГ, такие как высокие пороги, малую амплитуду спонтанной активности, длительное время рентгеноскопии и более низкую вероятность успеха имплантации, но значимость этих ограничений существенно снижается при совершенствовании опыта хирурга. Разработка новых электродов и систем доставки, специально предназначенных для стимуляции проводящей системы, устраняющих текущие ограничения, необходима для ее более широкого использования. Поскольку постоянная стимуляция проводящей системы вступает в свое третье десятилетие, в ближайшие годы мы надеемся, что физиологическая стимуляция раскроет свой полный потенциал.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Криволапов С.Н., Горев М.В., Гуляев Ю.Ю., Хлынин М.С., Баталов Р.Е. Стимуляция пучка Гиса. Технические аспекты и доказательная база для применения в качестве альтернативы ресинхронизирующей терапии и традиционной электрокардиостимуляции. Российский кардиологический журнал. 2024;29(4S):6211. https://doi.org/10.15829/1560-4071-2024-6211. EDN: WTIJUW
Скопировать