Прогностическая роль продольной деформации и механической дисперсии левого желудочка по данным спекл-трекинг эхокардиографии у пациентов с ишемической и неишемической кардиомиопатией: систематическии? обзор и метаанализ
Аннотация
Цель. Настоящее исследование направлено на проведение систематического обзора и метаанализа с целью изучения прогностической роли глобальной продольной деформации (ГПД) левого желудочка (ЛЖ) и механической дисперсии (МД) ЛЖ у пациентов с ишемической и неишемической кардиомиопатией по данным спекл-трекинг эхокардиографии.
Материал и методы. Поиск повели в базах данных PubMed, Google Scholar и Embase для исследовании?, в которых изучалась прогностическая ценность ГПД ЛЖ и МД ЛЖ у больных с ишемической и неишемической кардиомиопатией. Значения отношения рисков (ОР) в исследованиях, где были доступны аналогичные оценочные критерии, были объединены для метаанализа.
Результаты. Для данного систематического обзора и метаанализа было отобрано 12 исследований из 314 публикаций. Всего в анализ было включено 2624 пациента (средний возраст 57,9 года, средний срок наблюдения 40,8 мес.). Метаанализ показал, что ухудшение ГПД ЛЖ было ассоциировано с повышенным риском развития жизнеугрожающих желудочковых аритмий (ЖА): скорректированное ОР: 1,10 на каждый 1% ГПД ЛЖ; 95% доверительный интервал (ДИ): 1,01-1,19; p=0,03, и больших сердечнососудистых неблагоприятных событий: скорректированное ОР: 1,22 на каждый 1% ГПД ЛЖ; 95% ДИ: 1,11-1,33; p<0,0001. Пациенты с ЖА имели более высокие значения МД ЛЖ, чем у пациентов без нее (разница средневзвешенных значений 33,69 мс; 95% ДИ: от -41,32 до -26,05; p<0,0001). Прирост МД ЛЖ на каждые 10 мс статистически значимо и независимо ассоциировался с развитием ЖА: скорректированное ОР: 1,18; 95% ДИ: 1,08-1,29; р=0,0002. Заключение. Оценка ГПД ЛЖ и МД ЛЖ с использованием спекл-трекинг эхокардиографии имеет важную прогностическую роль и может использоваться в качестве эффективного инструмента для стратификации риска у пациентов с ишемической и неишемической кардиомиопатией.
Ишемическая и неишемическая кардиомиопатия на данный момент являются основными причинами хронической сердечной недостаточности (СН) со сниженной фракцией выброса (ФВ) левого желудочка (ЛЖ) [1]. Она ассоциирована со значительной заболеваемостью и преждевременной смертностью, прежде всего, из-за развития декомпенсированной СН и внезапной сердечной смерти (ВСС) [1][2]. Текущие критерии стратификации риска далеки от совершенства, существует потребность в новых инструментах стратификации риска, поскольку у большинства пациентов, которым в частности проводится имплантация кардиовертера-дефибриллятора для первичной профилактики ВСС, так и не происходит мотивированных срабатываний устройств [3].
Появление методик оценки деформации миокарда с помощью технологии отслеживания движения пятен серой шкалы в двухмерном изображении (спеклтрекинг эхокардиографии (STE)) дало возможность оценить ранние нарушения функции желудочков при отсутствии явных структурных изменений в миокарде [4]. В течение последнего десятилетия появляется все больше исследований, изучающих роль глобальной продольной деформации (ГПД) ЛЖ (LV GLS, left ventricular global longitudinal strain), определяемой с помощью 2D STE для прогнозирования неблагоприятных событий у пациентов с ХСНнФВ [5]. В большинстве данных исследований показано, что ухудшение ГПД ЛЖ, ассоциировано с развитием неблагоприятных сердечно-сосудистых событий. Следует отметить, что не только ГПД ЛЖ, но и механическая дисперсия (МД) ЛЖ (LV MD (left ventricular mechanical dispersion)) показала себя в качестве суррогатного маркера замедленной и неоднородной проводимости в миокарде и была связана с риском развития аритмических событий как при ишемической, так и неишемической кардиомиопатиях [6]. Однако в настоящее время использование этих новых эхокардиографических маркеров ограничивается только небольшими одноцентровыми обсервационными клиническими исследованиями, с небольшими размерами выборки и небольшим количеством событий.
В свете этих недостатков был проведен систематический обзор и метаанализ исследований, в которых проводилось изучение прогностической роли ГПД и МД ЛЖ у пациентов с ишемической и неишемической кардиомиопатией.
Материал и методы
Поиск публикаций и отбор исследований. Алгоритм поиска информации был разработан в соответствии с требованиями и положениями отчетности для систематических обзоров и метаанализов (PRISMA) [7] в базе данных PubMed, Google Scholar и Embase. Последний поиск данных для включения в данный анализ был проведен 4 февраля 2022г. Для поиска данных в базах данных PubMed и Embase мы использовали следующие ключевые слова: ((dilated cardiomyopathy) OR (nonischemic dilated cardiomyopathy) OR (ischemic dilated cardiomyopathy) OR (Heart Failure)) AND ((Echocardiography) AND (speckle tracking) OR (Strain) OR (Global Longitudinal Strain) OR (Myocardial strain) OR (dyssynchrony) OR (dispersion)) AND ((risk assessment) OR (predictive value) OR (prognostic value)). Для поиска в базе данных Google Scholar использовали запрос: speckle tracking echocardiography, Global Longitudinal Strain, dispersion, Nonischemic Dilated Cardiomyopathy, Ischemic Dilated Cardiomyopathy, Heart Failure, prognostic value, hazard ratio cox regression.
Для отбора подходящих исследований для включения в этот систематический обзор и метаанализ двое авторов независимо друг от друга изучили абстракты и полнотекстовые отчеты на соответствие критериям включения.
Критерии включения/исключения. Критериями включения первичных исследований в систематический обзор с последующим метаанализом были: исследования с доступом к полным текстам; все участники были взрослыми (18 лет и старше); исследования с адекватно представленными исходными данными, главным образом данными оценки продольной деформации и/или МД ЛЖ по данным STE. Кроме того, обязательным условием включения публикаций в метаанализ было представление данных о клинических исходах, а также результаты унивариантного и/или многофакторного регрессионного анализа Кокса с данными отношения рисков (ОР). Нижним порогом длительности периода наблюдения за пациентами был установлен срок 12 мес. (средний период). Статьи на других языках кроме английского, описания отдельных случаев, доклинические исследования, обзоры и мнения экспертов исключались из метаанализа.
Оценка методологического качества. Качество исследований определялось по шкале оценки качества когортных исследований Ньюкасл-Оттава [8]. Оценка исследований проводилась на основе определения следующих основных критериев: отбор исследовательских групп; сопоставимость групп; и установка интересующего исхода. Все несоответствия устранялись путем обсуждения авторами работы.
Статистический анализ. Статистическая обработка данных выполнялась в программах Review Manager (RevMan), версия 5.4.1 (The Cochrane Collaboration, 2020) и Comprehensive Meta-Analysis 3.0 (Biostat, NJ). Метаанализ проводился по модели случайных эффектов, с применением метода обратной дисперсии. Графически основные результаты представлены в виде «форест» диаграммы (forest plot). Оценку статистической гетерогенности выполняли с использованием критерия хи-квадрат Пирсона, а также индекса гетерогенности I2. Интерпретация оценки статистической гетерогенности согласно индексу I2 проводилась по рекомендациям Кокрановского сообщества, согласно которому I2=0-40% соответствует незначительной гетерогенности; 30-60% — умеренной гетерогенности; 50-90% — значительной гетерогенности; 75-100% — высокой гетерогенности. В качестве исходных значений для метаанализа показателей выживаемости использовались значения нескорректированного (полученного для однофакторной модели, unadjusted) и скорректированного (полученного для многофакторной модели, adjusted) ОР, определенного для изменения ГПД ЛЖ и МД ЛЖ на 1% и 10 мс, соответственно. Оценка публикационного смещения проводилась с помощью теста Эггера. Эффект считался статистически значимым при p<0,05.
Результаты
Результаты поиска литературы
В результате поиска по ключевым словам в базе данных PubMed, Google Scholar и Embase всего найдено 314 публикаций. Число публикаций после удаления дубликатов составило 302. После анализа заголовков и их аннотаций поставленной цели соответствовали 37 публикаций. Наиболее частыми причинами исключения статей были несоответствие поставленной цели, отсутствие заданных данных, а также исключались обзорные статьи, обсуждения, тезисы и доклады. Полнотекстовый скрининг прошли 20 публикаций. В трех исследованиях не были представлены данные сравнительного анализа показателей деформации миокарда ЛЖ у пациентов с развитием событий и без них, или результаты регрессионного анализа Кокса с данными ОР, в связи с чем данные исследования были исключены из нашего анализа [9-11]. В одном исследовании показатели ГПД ЛЖ и МД ЛЖ представлены в виде бинарных данных с определением диагностического порога отсечения (cut-off), что не позволило нам включить данное исследование для объединенного анализа непрерывных данных [12]. В одном исследовании были представлены крайне гетерогенные группы пациентов, которое помимо ишемической и неишемической дилатационной кардиомиопатии, включало пациентов с гипертрофической кардиомиопатией и саркаидозом сердца, в связи с чем данное исследование было также исключено из нашего анализа [13]. Таким образом, окончательно в наш обзор было включено 12 исследований, процесс отбора релевантных исследований показан на рисунке 1.

Рис. 1. Блок-схема отбора включенных в обзор исследований.
Общая характеристика исследований
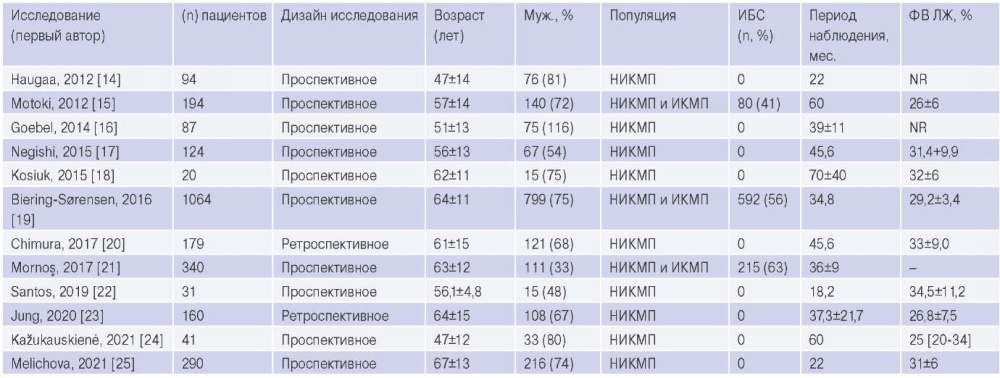
Общее количество пациентов с СН со сниженной ФВ ЛЖ, вызванной ишемической или неишемической кардиомиопатией, включенных в данный анализ, составило — 2624. Всем пациентам проводилась оценка ГПД и/или МД миокарда ЛЖ по данным STE. Средний возраст пациентов составил 57,9 года. Средняя продолжительность периода наблюдения составила 40,8 мес. Данные о дизайне исследования, исходных характеристиках пациентов обобщены в таблице 1.
Таблица 1
Синопсис исследований, включенных в систематический обзор

Сокращения: ИБС — ишемическая болезнь сердца, ИКМП — ишемическая кардиомиопатия, НИКМП — неишемическая кардиомиопатия, ФВ ЛЖ — фракция выброса левого желудочка, NR — not reported.
Эхокардиографические данные
Эхокардиограмму получали на ультразвуковых системах экспертного класса (General Electric, Philips, Siemens и Toshiba). В большинстве исследований (8 публикаций) постобработка данных проводилась на рабочих станциях EchoPAC (GE), в 1 исследовании TomTec (TomTec Imaging Systems) [19], в 1 исследовании Syngo Dynamics 9.0 software (Siemens) [15], и в 1 исследовании 2DST software (Toshiba Medical Systems) [20]. Деформация миокарда ЛЖ оценивалась с помощью 2D технологии STE. Основные характеристики эхокардиографического оборудования и программного обеспечения представлены в таблице 2.
Таблица 2
Характеристика (спецификация) ультразвукового оборудования, примененного в исследованиях

Сокращения: УЗ — ультразвуковой, NR — not reported.
Конечные точки и неблагоприятные исходы
Основными конечными точками в исследованиях, где проводилась оценка ГПД и/или МД ЛЖ, являлись «аритмическая» конечная точка (5 исследований) [14][18][19][21][25], большие сердечно-сосудистые неблагоприятные события (MACE — Major adverse cardiovascular events) (5 исследований) [15][16][20][22][24] и обратное ремоделирование ЛЖ (1 исследование) [23].
«Аритмическая» конечная точка включала различные события (устойчивая желудочковая тахикардия, фибрилляция желудочков, мотивированные срабатывания имплантируемого кардиовертера-дефибриллятора, ВСС). В большинстве включенных исследований была представлена комбинированная конечная точка, включающая кардиоваскулярную смертность, трансплантацию сердца, госпитализацию по поводу декомпенсации СН или имплантацию устройств механической поддержки ЛЖ. Совокупность указанных событий мы рассчитывали, как большие MACE, с целью проведения дальнейшего метаанализа. В большинстве исследований, включенных в наш анализ, были представлены данные ГПД ЛЖ [14-17][19-25], в трех исследованиях [14][16][21], кроме того, представлены показатели МД ЛЖ, и в одном исследовании [18] проводилась только оценка значений МД ЛЖ. В таблице 3 представлены основные значения показателей ГПД и МД ЛЖ, а также данные о конечных точках и количестве событий в каждой группе. В таблице 4 и 5 представлены данные ОР развития соответствующих конечных точек, полученные в результате унивариантного и многофакторного регрессионного анализа по методу Кокса при включении в качестве предикторов значений ГПД ЛЖ и/или МД ЛЖ в виде непрерывных переменных. Исследования, где был доступен аналогичный оценочный критерий (изменение ГПД ЛЖ и МД ЛЖ на 1% и 10 мс, соответственно), в зависимости от конечной точки были объединены для метаанализа.
Таблица 3
Показатели деформации и МД ЛЖ, включенных в систематический обзор публикаций

Сокращения: ВСС — внезапная сердечная смерть, ГПД — глобальная продольная деформация, ЖТ — желудочковая тахикардия, ИКД — имплантируемый кардиовертер-дефибриллятор, ЛЖ — левый желудочек, МД — механическая дисперсия, СН — сердечная недостаточность, ФЖ — фибрилляция желудочков.
Таблица 4
Оцениваемое изменение ГПД и МД ЛЖ, а также соответствующее ему ОР по данным унивариантного регрессионного анализа по методу Кокса

Сокращения: ДИ — доверительный интервал, ГПД — глобальная продольная деформация, ЛЖ — левый желудочек, МД — механическая дисперсия, ОР — отношение рисков, MACE — сердечно-сосудистые неблагоприятные события, SE — стандартная ошибка.
Таблица 5
Оцениваемое изменение ГПД и МД ЛЖ, а также соответствующее ему ОР по данным многофакторного регрессионного анализа по методу Кокса

Сокращения: АМКР — антагонисты минералокортикоидных рецепторов, БЛНПГ — блокада левой ножки пучка Гиса, БРА — блокаторы рецепторов ангиотензина II, ГПД — глобальная продольная деформация, ГЦД — глобальная циркулярная деформация, ДИ — доверительный интервал, иАПФ — ингибиторы ангиотензинпревращающего фермента, КДО — конечный диастолический объем, КДР — конечный диастолический размер, КСР — конечный систолический размер, ЛЖ — левый желудочек, ЛП — левое предсердие, МД — механическая дисперсия, ОР — отношение рисков, СРТ-Д — синхронизирующая сердечная терапия-дефибриллятор, ФВ — фракция выброса, ФК — функциональный класс, BNP — B-type natriuretic peptide, MACE — сердечно-сосудистые неблагоприятные события, NYHA — New York Heart Association, SE — стандартная ошибка, SD — standard deviation.
«Аритмическая» конечная точка
Средние значения показателей ГПД ЛЖ в зависимости от развития «аритмической» конечной точки были представлены в пяти исследованиях. Нами был выполнен метаанализ разности средних значений ГПД ЛЖ у пациентов c развитием «аритмической» конечной точки и без таковой (рис. 2). Как следует из рисунка 2, пациенты с желудочковыми аритмиями (ЖА) имели более худшие показатели ГПД ЛЖ по сравнению с пациентами без достижения аритмической конечной точки, так средневзвешенная разница значений ГПД ЛЖ составила — 3,12% (95% доверительный интервал (ДИ): -5,13; -1,11%), данные различия были статистически значимыми (р=0,002). При оценке теста Эггера получен статистически незначимый результат, t=1,37; df=3,0; p=0,26.

Рис. 2. Результаты метаанализа разности средних значений ГПД ЛЖ в группе с ЖА и без ЖА.
Примечание: зеленые квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер зеленых квадратов соответствует весу исследований), черные отрезки — 95% ДИ, черный ромб отражает средневзвешенное значение разности средних значений ГПД.
Сокращения: ГПД — глобальная продольная деформация, ДИ — доверительный интервал, ЖА — желудочковые аритмии.
Был выполнен также метаанализ разности средних значений МД ЛЖ у пациентов c развитием «аритмической» конечной точки и без таковой (рис. 3). Как следует из рисунка 3, пациенты с развитием аритмической конечной точки имели более высокие показатели МД ЛЖ по сравнению с пациентами без достижения аритмической конечной точки, так средневзвешенная разница значений МД ЛЖ составила — 33,69 мс (95% ДИ: -41,32; -26,05), данные различия были статистически значимыми (р<0,0001). При оценке теста Эггера также получен статистически незначимый результат, t=1,08; df=1,0; p=0,48.

Рис. 3. Результаты метаанализа разности средних значений МД ЛЖ в группе с ЖА и без ЖА.
Примечание: зеленые квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер зеленых квадратов соответствует весу исследований), черные отрезки — 95% ДИ, черный ромб отражает средневзвешенное значение разности средних значений МД.
Сокращения: ДИ — доверительный интервал, ЖА — желудочковые аритмии, МД — механическая дисперсия.
Данные унивариантного анализа изменения рисков развития «аритмической» конечной точки при использовании в качестве предиктора непрерывных оценок значения ГПД ЛЖ были представлены в трех исследованиях [14][17][21]. Данные исследования были сопоставимыми в связи с использованием одинакового критерия оценки предиктора (изменения на 1%), что позволило провести метаанализ этих публикаций. Количество развития «аритмической» точки в данных исследованиях составило 96 (17,2% от 558 пациентов), средний период наблюдения составил 29,8 мес. По результатам объединенного анализа ухудшение ГПД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки (ОР: 1,17 на каждый 1% ухудшения ГПД ЛЖ; 95% ДИ: 1,07-1,27; p=0,0005) (рис. 4). При оценке теста Эггера также получен статистически незначимый результат, t=0,63; df=2,0; p=0,59.

Рис. 4. Результаты метаанализа нескорректированного ОР достижения «аритмической» конечной точки при ухудшении ГПД ЛЖ на 1%.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Данные унивариантного анализа изменения рисков развития «аритмической» конечной точки при использовании в качестве педиктора непрерывных оценок значения МД ЛЖ были представлены лишь в двух исследованиях [14][21]. Данные исследования были сопоставимыми в связи с использованием одинакового критерия оценки предиктора (изменения на 10 мс), что позволило провести метаанализ этих публикаций. Количество развития «аритмической» точки в данных исследованиях составило 60 (13,8% от 434 пациентов), средний период наблюдения составил 29 мес. По результатам объединенного анализа увеличение МД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки (ОР: 1,29 на каждый 10 мс увеличения МД ЛЖ; 95% ДИ: 1,14-1,47; p<0,0001) (рис. 5).

Рис. 5. Результаты метаанализа нескорректированного ОР достижения «аритмической» конечной точки при увеличении МД ЛЖ на 10 мс.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Данные многофакторного анализа изменения рисков развития «аритмической» конечной точки при использовании в качестве предиктора непрерывных оценок значения ГПД ЛЖ были представлены в четырех исследованиях [14][17][21][25]. Данные исследования были сопоставимыми в связи с использованием одинакового критерия оценки предиктора (изменения на 1%), что позволило провести метаанализ этих публикаций. Количество развития «аритмической» точки в данных исследованиях составило 128 (15,1% от 848 пациентов), средний период наблюдения составил 31,4 мес. По результатам объединенного анализа ухудшение ГПД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки (скорректированное ОР: 1,10 на каждый 1% ухудшение ГПД ЛЖ; 95% ДИ: 1,01-1,19; p=0,03) (рис. 6). При оценке теста Эггера был получен статистически незначимый результат, t=2,82; df=2,0; p=0,106.

Рис. 6. Результаты метаанализа скорректированного ОР достижения «аритмической» конечной точки при ухудшении ГПД ЛЖ на 1%.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Данные многофакторного анализа изменения рисков развития «аритмической» конечной точки при использовании в качестве предиктора непрерывных оценок значения МД ЛЖ были представлены в трех исследованиях [14][21][25]. Данные исследования были сопоставимыми в связи с использованием одинакового критерия оценки предиктора (изменения на 10 мс), что позволило провести метаанализ этих публикаций. Количество развития «аритмической» точки в данных исследованиях составило 92 (12,7% от 724 пациентов), средний период наблюдения составил 26,6 мес. По результатам объединенного анализа увеличение МД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки (скорректированное ОР: 1,18 на каждый 10 мс увеличения МД ЛЖ; 95% ДИ: 1,08-1,29; p=0,0002) (рис. 7).

Рис. 7. Результаты метаанализа скорректированного ОР достижения «аритмической» конечной точки при увеличении МД ЛЖ на 10 мс.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Большие сердечно-сосудистые неблагоприятные события
Средние значения показателей ГПД ЛЖ в зависимости от развития MACE были представлены в 5 исследованиях. Нами был выполнен метаанализ разности средних значений ГПД ЛЖ у пациентов c развитием MACE и без развития MACE (рис. 8). Пациенты с MACE имели более худшие показатели ГПД ЛЖ по сравнению с пациентами без развития MACE, так средневзвешенная разница значений ГПД ЛЖ составила — 3,15% (95% ДИ: -4,27; -2,03%), данные различия были статистически значимыми (р<0,0001).

Рис. 8. Результаты метаанализа разности средних значений ГПД ЛЖ в группе с развитием MACE и без развития MACE.
Примечание: зеленые квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер зеленых квадратов соответствует весу исследований), черные отрезки — 95% ДИ, черный ромб отражает средневзвешенное значение разности средних значений ГПД ЛЖ.
Сокращения: ДИ — доверительный интервал, ЖА — желудочковые аритмии, ГПД ЛЖ — глобальная продольная деформация левого желудочка, MACE — сердечно-сосудистые неблагоприятные события.
Унивариантный анализ изменения рисков больших сердечно-сосудистых неблагоприятных событий для непрерывных оценок ГПД ЛЖ был представлен в четырех исследованиях [15][20][22][24] (табл. 4). В данных исследованиях был доступен аналогичный оценочный критерий (изменение ГПД ЛЖ на 1%), что позволило объединить их в метаанализе. В данных исследованиях конечная точка в виде больших сердечно-сосудистых неблагоприятных событий была достигнута у 144 пациентов (31,7% от 454). Средний период наблюдения составил 45,7 мес. По результатам проведенного анализа статистически значимой связи между ухудшением ГПД ЛЖ и развитием MACE не было выявлено (ОР: 1,17 на каждый 1% ухудшения ГПД ЛЖ; 95% ДИ: 0,96-1,41; p=0,11) (рис. 9). При оценке теста Эггера получен статистически незначимый результат, t=0,48; df=2,0; p=0,67. Отметим, что полученные результаты метаанализа были связаны с включением исследования Santos 2019 [22], где были представлены противоречивые данные, так по данным однофакторного анализа показано, ухудшение значений ГПД ЛЖ ассоциировано с уменьшением развития MACE (ОР: 0,879; 95% ДИ: 0,784-0,985; р=0,026). В то же время, по данным многофакторного анализа, ухудшение ГПД ЛЖ было ассоциировано с увеличением риска развития MACE (скорректированное ОР: 1,365; 95% ДИ: 1,106-1,686; р=0,003).

Рис. 9. Результаты метаанализа нескорректированного ОР достижения MACE при ухудшении ГПД ЛЖ на 1%.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
В связи с чем нами было исключено исследование Santos, 2019 [22] из дальнейшего метаанализа. В исследованиях, которые впоследствии были объединены [15][20][24], конечная точка в виде больших сердечно-сосудистых неблагоприятных событий была достигнута у 138 пациентов (33,3% от 414). Средний период наблюдения составил 55,0 мес. Метаанализ показал, что ухудшение ГПД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития MACE (нескорректированное ОР: 1,27 на каждый 1% ухудшения ГПД ЛЖ; 95% ДИ: 1,11-1,46; p=0,0008) (рис. 10). При оценке теста Эггера получен статистически незначимый результат, t=5,8; df=1,0; p=0,11.
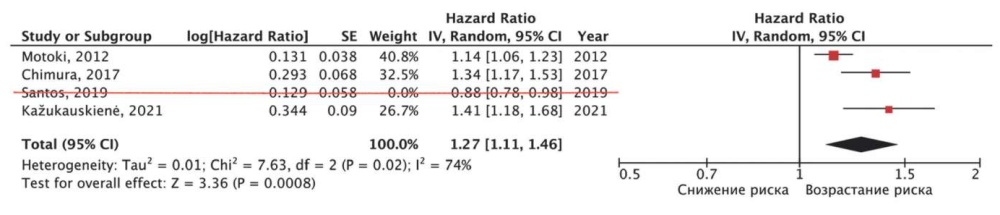
Рис. 10. Результаты метаанализа нескорректированного ОР достижения MACE при ухудшении ГПД ЛЖ на 1% (при исключении исследования Santos, 2019).
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Данные многофакторного анализа изменения рисков развития MACE при использовании в качестве предиктора непрерывных оценок значения ГПД ЛЖ были представлены в четырех исследованиях [15][20][22][24]. Данные исследования были сопоставимыми в связи с использованием одинакового критерия оценки предиктора (изменения на 1%), что позволило провести метаанализ этих публикаций. В данных исследованиях конечная точка в виде больших сердечно-сосудистых неблагоприятных событий была достигнута у 144 пациентов (31,7% от 454). Средний период наблюдения составил 45,7 мес. По результатам объединенного анализа ухудшение ГПД ЛЖ было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития MACE (скорректированное ОР: 1,22 на каждый 1% ухудшения ГПД ЛЖ; 95% ДИ: 1,11-1,33; p<0,0001) (рис. 11). При оценке теста Эггера для ГПД ЛЖ также получен статистически незначимый результат, t=1,73; df=2,0; p=0,22.

Рис. 11. Результаты метаанализа скорректированного ОР достижения MACE при ухудшении ГПД ЛЖ на 1%.
Примечание: красные квадраты показывают взвешенный размер эффекта для каждого конкретного исследования (размер красных квадратов соответствует весу исследований), красные отрезки — 95% ДИ, чёрный ромб отражает средневзвешенное значение ОР.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Обсуждение
На данный момент современные стратегии стратификации риска пациентов с хронической СН с сохранной ФВ, вызванной ишемической или неишемической кардиомиопатией, далеки от совершенства, по-прежнему существует клиническая необходимость в выявлении новых маркеров, помогающих в стратификации риска. ФВ ЛЖ представляет собой глобальную оценку систолической функции ЛЖ, которая не всегда связана с повреждениями миокарда и электрофизиологическими нарушениями, лежащими в основе электрической нестабильности миокарда, что подчеркивает необходимость использования других дополнительных параметров для стратификации риска.
На момент написания данной работы опубликованных метаанализов в отношении прогностической роли ГПД ЛЖ у пациентов с ишемической и неишемической кардиомиопатией нам найти не удалось.
В нашей работе было показано, что пациенты с развитием ЖА и MACE имели статистически значимо более худшие показатели ГПД ЛЖ по сравнению с пациентами без развития конечных точек. Кроме того, ГПД ЛЖ показала себя в качестве независимого предиктора развития неблагоприятных аритмических событий и MACE. Так, по результатам объединенного анализа показано, что ухудшение ГПД ЛЖ на каждый 1% было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки и MACE на 10% и 22%, соответственно.
Как отмечалось, МД ЛЖ является маркером замедленной и неоднородной проводимости в миокарде и может быть использована в качестве предиктора развития ЖА. В недавнем метаанализе Kawakami H, et al. [26] с участием 3198 пациентов было показано, что пациенты с развитием ЖА, имели более высокие показатели МД ЛЖ, по сравнению с пациентами без развития ЖА, так средневзвешенная разница значений МД ЛЖ составила — 20,3 мс (95% ДИ: 27,3-13,2; p<0,01). По результатам метаанализа увеличение МД ЛЖ на каждые 10 мс было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития ЖА (скорректированное ОР: 1,19; 95% ДИ: 1,09-1,29; p<0,01). Более того, прогностическая ценность МД ЛЖ была выше, чем оценка ФВ ЛЖ или ГПД ЛЖ. Следует также отметить, что в данный метаанализ была включена смешанная популяция пациентов как с сохранной, так и сниженной ФВ ЛЖ, и большинство пациентов переносили ИМ в анамнезе.
В нашей работе в группе пациентов с ишемической и неишемической кардиомиопатией было показано, что пациенты с развитием ЖА имели статистически значимо более высокие показатели МД ЛЖ по сравнению с пациентами без развития аритмической конечной точки. МД ЛЖ также показала себя в качестве независимого предиктора развития ЖА. По результатам объединенного анализа увеличение МД ЛЖ на каждые 10 мс было ассоциировано со статистически значимым возрастанием средневзвешенного риска развития «аритмической» конечной точки на 18%. Таким образом, оценка ГПД ЛЖ и МД ЛЖ по данным STE может использоваться как эффективный инструмент для стратификации риска у пациентов с ХСНнФВ.
Ограничения исследования. Во-первых, в наш систематический обзор и метаанализ включено небольшое количество исследований, кроме того, как и в случае любого метаанализа обсервационных исследований, различия в критериях включения и конечных точках являются потенциальными источниками неоднородности исследований. Учитывая ограниченное количество исследований и пациентов, на данный момент нам не удалось провести метаанализ отдельно для групп с ишемической и неишемической дилатационной кардиомиопатией, поскольку в некоторые исследования включена смешанная популяция пациентов, как с ишемической, так и неишемической кардиомиопатией, и не представлены данные анализа подгрупп. Во-вторых, мы включали в анализ данные ОР, полученные для ГПД ЛЖ и/или МД ЛЖ, как по данным унивариантного регрессионного анализа, так и данные многофакторного регрессионного анализа Кокса в виде скорректированных значение ОР. Однако в последнем случае в многофакторный анализ в различных исследованиях кроме показателей ГПД ЛЖ и/или МД ЛЖ включались различные ковариаты (возраст, пол, ФВ ЛЖ, конечный диастолический объем ЛЖ, ГПД и др.). В-третьих, несмотря на то, что был доступен аналогичный оценочный критерий (изменение ГПД ЛЖ и МД ЛЖ на 1% и 10 мс, соответственно), который позволил в зависимости от конечной точки исследования объединить их в метаанализе, необходимо помнить, для оценки деформации миокарда крайне важное значение имеет качество эхокардиографической визуализации и соответствующих настроек визуализации (например, частота кадров от 50 до 70 кадров/с). Кроме того, необходимо отметить, в исследованиях оценка эхокардиографических показателей проводилась с использованием различных аппаратов и программных обеспечений, используемых для постобработки данных, а также различными операторами.
Заключение
Оценка ГПД ЛЖ и МД ЛЖ с использованием STE обеспечивает важной дополнительной прогностической информацией у пациентов с ишемической и неишемической кардиомиопатией. Необходимы проспективные многоцентровые исследования с участием большой популяции пациентов и более длительным периодом наблюдения для валидизации полученных результатов и оценки возможности внедрения в практику для принятия клинических решений.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Голухова Е.З., Булаева Н.И., Мрикаев Д.В., Александрова С.А., Бердибеков Б.Ш. Прогностическая роль продольной деформации и механической дисперсии левого желудочка по данным спекл-трекинг эхокардиографии у пациентов с ишемической и неишемической кардиомиопатией: систематическии? обзор и метаанализ. Российский кардиологический журнал. 2022;27(3S):5034. https://doi.org/10.15829/1560-4071-2022-5034
Скопировать