Особенности портокавального кровотока у пациентов с легочной артериальной гипертензией
Аннотация
Цель. Провести сравнительный анализ ультразвуковой допплерографии портокавального кровотока с клинико-функциональным и гемодинамическим статусом пациентов с легочной артериальной гипертензией (ЛАГ).
Материал и методы. В исследование включены 42 пациента, с установленным диагнозом ЛАГ, госпитализированных в отдел легочной гипертензии (ЛГ) и заболеваний сердца ФГБУ «НМИЦ кардиологии им. акад. Е.И. Чазова» Минздрава России в период с 2022 по 2024гг. Диагноз устанавливался в соответствии с алгоритмом, предложенным в евразийских (2023) и российских рекомендациях по диагностике и лечению ЛГ (2024г)
Результаты. Согласно полученным данным венозных кривых портокавального кровотока, для пациентов подгруппы низкого риска обеих групп ЛАГ характерен только сдвиг А-волны на комплекс QRS без пульсации портального кровотока. В подгруппе высокого риска у всех пациентов с идиопатической ЛГ выявлена пульсация портального кровотока >50% и превышение высоты А-волны кавального кровотока над волной S. Среди пациентов промежуточного риска обеих групп и высокого риска группы с ЛГ, ассоциированной с системной склеродермией, встречаются исследуемые с равными А и S волнами и небольшой пульсацией портального кровотока, однако данный результат характерен не для всех пациентов этих подгрупп.
Заключение. Полученные результаты подтверждают наличие корреляции между выраженностью венозного застоя и степенью риска у пациентов с ЛАГ. Результаты также указывают на возможность неинвазивной оценки центрального венозного давления и портокавального градиента давления по показателям портокавальной гемодинамики у пациентов с недостаточностью правого желудочка.
Легочная гипертензия (ЛГ) — гемодинамическое и патофизиологическое состояние, которое характеризуется повышением среднего давления в легочной артерии (ДЛА) >20 мм рт.ст. в покое, измеренного при чрезвенозной катетеризации правых отделов сердца (КПОС). Нормальные значения ДЛА в покое — среднее ДЛА (срДЛА) ≤20 мм рт.ст. [1].
ЛГ может быть разделена на пять основных категорий: легочная артериальная гипертензия (ЛАГ), ЛГ вследствие патологии левых отделов сердца, ЛГ при заболеваниях легких и/или гипоксии, ЛГ из-за обструкций легочной артерии и ЛГ с неясными и/или многофакторными механизмами [2].
Наиболее распространенной формой ЛАГ является идиопатическая ЛАГ (ИЛАГ), за которой следует ЛАГ, связанная с заболеванием соединительной ткани (СтЗСТ-ЛАГ).
Среди подтипов, связанных с заболеванием соединительной ткани, системная склеродермия (ССк), системная красная волчанка, смешанное заболевание соединительной ткани, синдром Шегрена и ревматоидный артрит могут вызвать ЛАГ, хотя ССк составляет ~75% случаев СтЗСТ-ЛАГ [2]. ЛАГ поражает от 3 до 13% больных с СтЗСТ и является главной причиной их смерти. У таких пациентов отмечается самое тяжелое течение ЛГ и наиболее быстрое наступление летального исхода из всех подгрупп [3].
К сожалению, диагноз ЛАГ, практически любой этиологии, до сих пор остается поздно верифицируемым, что приводит к отсрочке в назначении лечения и прогрессированию сердечной недостаточности. Венозный застой в системе нижней полой вены (НПВ) один из ключевых элементов правожелудочковой дисфункции сердца. Прогрессирование застойных явлений приводит к нарушению работы органов и в результате к полиорганной недостаточности. Прямое измерение центрального венозного давления (ЦВД) инвазивным способом, хотя и остается золотым стандартом оценки венозного застоя, имеет существенные ограничения в повседневном использовании. Поэтому неинвазивная оценка состояния НПВ в комплексе с сосудами печени как элементов, соединяющих сосуды большого круга кровообращения с НПВ и правым предсердием (ПП), предоставляющая возможность определить наличие и степень венозного застоя, особенно ценна в клинической практике.
Ультразвуковая допплерография — это современный метод диагностики, позволяющий оценить состояние портокавального кровотока. При импульсно-волновой допплерографии, синхронизированной с электрокардиограммой (ЭКГ), можно четко проследить связь между сердечным циклом и фазами венозной кривой. В норме кавальная венозная кривая включает 4 зубца: волна A — отражает сокращение предсердий, которое происходит в конце диастолы, регистрируется после зубца P на ЭКГ; волна S — самая высокая по скорости антеградная волна, формирующаяся при сокращении правого желудочка (ПЖ), совпадает с интервалом S-T; волна V — появляется в начале расслабления ПЖ, когда трикуспидальный клапан (ТК) еще закрыт; а давление в печеночных венах (ПВ) возрастает, и эта волна соответствует зубцу T; волна D — антеградная волна, регистрируемая при открытии ТК, после зубца T. Говоря про воротную вену, в норме её допплеровский спектр непрерывный с незначительными колебаниями, связанными с актом дыхания и не зависит от ритма сердечной деятельности [4][5].
Целью нашей работы было провести допплерографию портокавального кровотока у пациентов с ИЛАГ и СтЗСТ-ЛАГ и сопоставить её результаты с гемодинамическим и функциональным статусом пациентов этих групп.
Материалы и методы
В ходе нашего исследования проанализированы данные 42 пациентов, которые были разделены на 2 равные группы, согласно генезу ЛАГ, пациенты с ИЛАГ и с ЛГ, ассоциированной с ССк. Медиана возраста всех пациентов 49 лет. Каждому пациенту выполнено комплексное обследование, включающие лабораторные исследования, эхокардиографию и КПОС. Для оценки функционального статуса проведен тест 6-минутной ходьбы (ТШХ). Согласно клиническим рекомендациям с целью исключения ассоциированных форм ЛГ осуществлено ультразвуковое исследование органов брюшной полости с прицельным исключением портальной гипертензии. В ходе этого исследования также проводилась оценка венозных кривых портокавального кровотока. Ультразвуковое исследование выполнено на аппарате Canon Aplio a550, конвексным датчиком с частотой 3,5 МГц в В-режиме с дуплексным сканированием, синхронизированной с ЭКГ.
Стратификация риска летальности в течение 1 года производилась согласно шкале оценки риска, предложенной в европейских рекомендациях ESC/ERS 2022г, евразийских (2023г) и российских рекомендациях по лечению ЛГ (2024г) [1][6][7].
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации.
Статистический анализ проводился с использованием программы StatTech v. 4.8.2 (разработчик — ООО «Статтех», Россия). Количественные показатели, выборочное распределение которых соответствовало нормальному, описывались с помощью средних арифметических величин и стандартных отклонений. Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение двух групп по количественному показателю, распределение которого в каждой из групп соответствовало нормальному, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента. Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью точного критерия Фишера (при значениях минимального ожидаемого явления <10). В качестве количественной меры эффекта при сравнении относительных показателей рассчитывалось отношение шансов с 95% доверительным интервалом. В случае нулевых значений числа наблюдений в ячейках таблицы сопряженности расчет отношения шансов выполнялся с поправкой Холдейн-Энскомб. Различия считались статистически значимыми при p<0,05.
Результаты
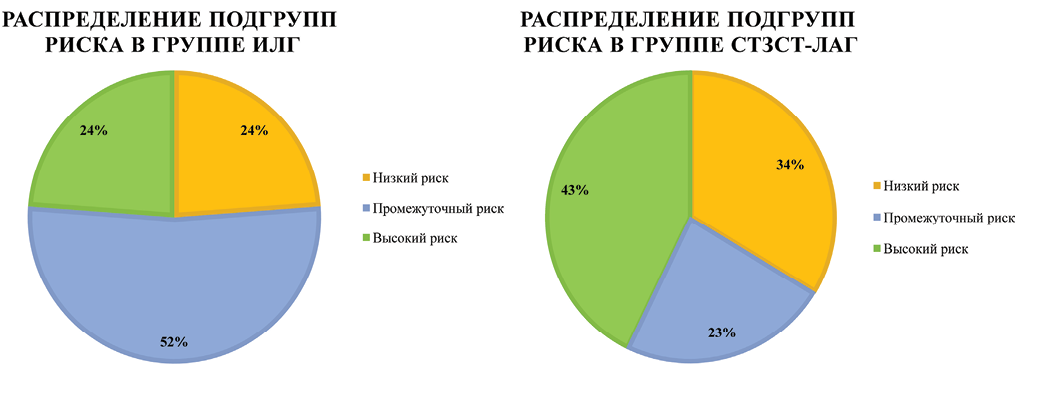
В группах ИЛАГ и СтЗСТ-ЛАГ все исследуемые были разделены на три подгруппы согласно шкале риска летальности пациентов с ЛАГ по российским клиническим рекомендациям от 2024г. В группе ИЛАГ соотношение по риску распределилось следующим образом: 5 пациентов (23,8%) в подгруппах низкого и высокого риска и 11 пациентов (52,4%) промежуточного риска (рис. 1). Среди пациентов с СтЗСТ-ЛАГ: 7 пациентов (33,3%) низкого риска, 5 пациентов (23,8%) промежуточного риска и 9 (42,9%) пациентов высокого риска (рис. 2).
При сравнении пациентов низкого риска, в группе ИЛАГ пациенты были моложе 31±8,2 лет vs 55,9±11,3 лет у пациентов с ССк. Анализ гендерного состава выявил различия между группами: доля женщин в группе ИЛАГ достигала 60%, в то время как группа ССтЗ-ЛГ была представлена только лицами женского пола. Несмотря на более молодой возраст, у исследуемых с ИЛАГ ряд показателей по данным эхокардиографии имели более высокие значения, у них больше размеры ПП и уровень систолического ДЛА (СДЛА), а показатель амплитуды систолического движения кольца ТК (TAPSE) несколько ниже среднего значения пациентов с СтЗСТ-ЛАГ, однако у 28,6% пациентов с СтЗСТ-ЛАГ выявлено наличие перикардиального выпота, который не отмечен в группе ИЛАГ, размеры НПВ у пациентов обеих групп 1,9±0,4 см, что соответствует норме, снижение коллабирования ни у одного пациента низкого риска не зафиксировано. При анализе результатов КПОС группа ИЛАГ также имела более высокий уровень срДЛА 63,0±22,2 мм рт.ст. vs 39,6±15,5 мм рт.ст. во второй группе, а также более низкий сердечный индекс 2,6±0,6 л/мин*м2, vs 2,8±0,5 л/мин*м2 у пациентов с СтЗСТ-ЛА Г. Скорее всего разница в возрасте сказывалась и на функцио-нальном статусе пациентов, в группе ИЛАГ средняя дистанция ТШХ 510,8±60,4 метров, у пациентов с СтЗСТ-ЛАГ 422,3±70,7 метров (табл. 1).
Помимо ключевых критериев, оцениваемых у пациентов с ЛАГ, был проведен анализ допплерограмм кавального (КК) и портального кровотока (ПК). Выявлено, что для всех пациентов с ЛАГ характерен сдвиг А-волны КК на комплекс QRS, что cвязано с дилатацией ПП и трикуспидальной регургитацией (ТР). Таким образом, А-волна, которая в норме образовывалась за счет ретроградного тока крови во время систолы предсердий, приходится на систолу желудочков. Также согласно изменениям А-волны, удалось выделить три типа изменений венозной кривой КК: амплитуда A-волны<S-волны, что соответствует норме, A=S и A>S. Изменения ПК соответствовали известным критериям: от монофазной кривой до наличия небольшой пульсации или >50%.
У всех пациентов подгруппы низкого риска помимо характерного сдвига А-волны, других значимых изменений и пульсации ПК не выявлено, что коррелирует с нормальным уровнем ЦВД по косвенным критериям данных эхокардиографии и уровню давления в ПП по результатам КПОС (рис. 3).
При этом в подгруппе низкого риска зафиксировано такое явление, как демпфирование, когда венозная кривая ПВ становится монофазной. Данный феномен кривой выявлен у 4 пациенток (19%) в группе СтЗСТ-ЛАГ и у 1 пациентки (4,8%) среди ИЛАГ. У этой группы пациентов не было зарегистрировано ни случаев клинически диагностированных патологий печени, ни отклонений в стандартных печеночных пробах.
В подгруппе промежуточного риска пациенты с СтЗСТ-ЛАГ также были старше пациентов с ИЛАГ, средний возраст первых 66,2±16,5 лет, вторых 42,6±11,2 лет. Анализ гендерного распределения выявил преобладание женщин в обеих подгруппах. Показатель прогрессирования сердечной недостаточности — N-концевой промозговой натрийуретический пептид, у пациентов с ССк был более, чем в 2 раза выше, чем у пациентов с ИЛАГ, 2140,9±3097,2 пкг/мл и 941,4±588,6 пкг/мл, соответственно. Однако в группе ИЛАГ были выше средние площадь ПП и СДЛА, но плевральный выпот был выявлен только у одного пациента в группе СтЗСТ-ЛА Г. Средние размеры НПВ в обеих группах соответствовали норме, коллабирование было снижено в 27,3% случаев у ИЛАГ и 20% у пациентов СтЗСТ-ЛА Г. По результатам КПОС, у пациентов с ССк было выше давление в ПП 10±7,6 мм рт.ст. и 6,6±2,1 у ИЛАГ, но ниже уровень срДЛА и ниже сатурация венозной крови. Дистанция в ТШХ в каждой из групп соответствовала II функциональному классу (табл. 2).
При оценке допплерограмм портокавального кровотока наиболее вариабельные параметры были зарегистрированы в подгруппе промежуточного риска. В группе ИЛАГ у 6 пациентов выявлен только сдвиг А-волны КК без пульсации ПК. У 3 пациенток A-волна равна S-волне с пульсацией ПК не более 50% и у 2 выявлено превышение размеров А-волны над волной S с пульсацией ПК >50% (табл. 3).
В группе СтЗСТ-ЛАГ у 2 пациентов не выявлено значимых изменений портокавального кровотока, у 1 пациентки A=S с небольшой пульсацией ПК и 2 пациентки, у которых высота А-волны превышала высоту S, а также отмечалась ПК >50% (табл. 3).
Пациенты с ИЛАГ в подгруппе высокого риска также моложе, чем в группе СтЗСТ-ЛАГ 47±3,9 лет и 59,2±11,1 лет, соответственно. Исследуемые в обеих подгруппах только женщины. Для пациентов с СтЗСТ-ЛАГ характерен более высокий уровень N-концевого промозгового натрийуретического пептида и общего билирубина. В целом в подгруппе высокого риска выше уровень общего билирубина, что скорее всего связано с венозным застоем по большому кругу кровообращения при нормальном уровне печеночных трансаминаз. У пациентов с ИЛАГ в этой подгруппе выявлены более высокий уровень СДЛА 102,2±24,8 мм рт.ст. и низкий показатель TAPSE 1,2±0,3, 93±15,6 мм рт.ст. и 1,7±0,3, соответственно в группе СтЗСТ-ЛАГ. Однако у большей части пациентов с СтЗСТ-ЛАГ зафиксировано наличие перикардиального выпота 77,8% пациентов, по сравнению с 60% в группе ИЛАГ. Также в обеих группах отмечается расширение НПВ и снижение её коллабирования. Оно снижено у 40% пациентов с ИЛАГ и у 66,7% пациентов с СтЗСТ-ЛАГ. Данные отклонения соответствуют повышению уровня ЦВД. Что также подтверждает высокий уровень давления в ПП в обеих группах, у пациентов с ИЛАГ 13,3±7,9 мм рт.ст. и 11,8±3,7 мм рт.ст. у пациентов с СтЗСТ-ЛАГ (табл. 4).
При оценке венозных кривых портокавального кровотока у всех пациентов высокого риска в группе ИЛАГ выявлена пульсация ПК 50-100%, А-волна КК больше волны S. Группа СтЗСТ-ЛАГ более неоднородна, только у 5 (55,6%) пациенток выявлена пульсация ПК и высота А-волны превышала высоту S-волны. У 3 пациенток отсутствовала пульсация ПК и был выявлен только сдвиг А-волны и у 1 пациентки выявлена пульсация ПК ~50% с одинаковыми размерами А и S-волн при оценке кавальной венозной кривой (табл. 5).
Также 17 пациентам с ИЛАГ и 13 пациентам с СтЗСТ-ЛАГ была выполнена двумерная сдвиговолновая эластография 2D SWE (рис. 4). Оценка результатов эластической жесткости печени (ЭЖП) проведена на основе экспертного мнения о том, что при венозном застое измерение отражает жесткость (ткани) печени, а не фиброз [8]. У пациентов с СтЗСТ-ЛАГ в подгруппах промежуточного и высокого риска выше уровень ЭЖП (7,0±0,7 кПа и 8,0±1,8 кПа), чем у пациентов с ИЛАГ (6,5±0,5 кПа и 7,4±1 кПа).

Рис. 1. Распределение подгрупп риска в группе ИЛАГ.
Рис. 2. Распределение подгрупп риска в группе СтЗСТ-ЛАГ.
Таблица 1
Показатели пациентов подгруппы низкого риска
| Показатель | Пациенты с ИЛАГ (n=5) | Пациенты с СтЗСТ-ЛАГ (n=7) | p* |
| Возраст (годы) | 31±8,2 | 55,9±11,3 | 0,002 |
| Женщины (%) | 60% | 100% | 0,152 |
| NT-proBNP (пкг/мл) | 470,2±320,4 | 491,5±550,6 | 0,941 |
| Общий билирубин (ммоль/л) | 18,8±9,2 | 11,7±4,9 | 0,138 |
| Площадь ПП (см2) | 19,1±4,8 | 17,5±4,0 | 0,556 |
| TAPSE | 1,6±0,3 | 2,0±0,3 | 0,035 |
| СДЛА (мм рт.ст.) | 70,2±17,3 | 58,1±18,9 | 0,288 |
| Перикардиальный выпот (%) | 0% | 28,6% | 0,470 |
| Размер НПВ (см) | 1,9±0,4 | 1,9±0,4 | 0,546 |
| Давление в ПП (мм рт.ст.) | 3,2±2,9 | 4,6±2,4 | 0,392 |
| срДЛА (мм рт.ст.) | 63,0±22,2 | 39,6±15,5 | 0,055 |
| SvO2 (%) | 71,0±4,9 | 70,3±3,6 | 0,773 |
| СИ (л/мин*м2) | 2,6±0,6 | 2,8±0,5 | 0,649 |
| Дистанция ТШХ (м) | 510,8±60,4 | 422,3±70,7 | 0,047 |
Примечание: * — различия показателей статистически значимы (p<0,05).
Сокращения: ИЛАГ — идиопатическая легочная гипертензия, НПВ — нижняя полая вена, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, СИ — сердечный индекс, СтЗСТ-ЛАГ — легочная гипертензия, ассоциированная с системной склеродермией, срДЛА — среднее давление в легочной артерии, ТШХ — тест 6-минутной ходьбы, NT-proBNP — N-концевой промозговой натрийуретический пептид, TAPSE — амплитуда систолического движения кольца трикуспидального клапана.

Рис. 3. Портокавальный кровоток пациент низкого риска с ИЛАГ.
Таблица 2
Показатели пациентов подгрупп промежуточного риска
| Показатель | ИЛАГ (n=11) | СтЗСТ-ЛАГ (n=5) | p* |
| Возраст (лет) | 42,6±11,2 | 66,2±16,5 | 0,005 |
| Женщины (%) | 77,8% | 100% | 1,000 |
| NT-proBNP (пкг/мл) | 941,4±588,6 | 2140,9±3097,2 | 0,215 |
| Билирубин общий (ммоль/л) | 23,3±12,2 | 18,2±4,9 | 0,389 |
| Площадь ПП (см2) | 23,6±4,9 | 21,4±2,7 | 0,359 |
| TAPSE | 1,6±0,3 | 1,5±0,2 | 0,620 |
| СДЛА (мм рт.ст.) | 94,9±25,8 | 70,2±15,1 | 0,069 |
| Перикардиальный выпот (%) | 0% | 20% | 0,312 |
| Размер НПВ (см) | 2,1±0,3 | 2,0±0,2 | 0,797 |
| Коллабирование НПВ <50% | 27,3% | 20% | 1,000 |
| Давление в ПП (мм рт.ст.) | 6,6±2,1 | 10±7,6 | 0,173 |
| срДЛА (мм рт.ст.) | 66,2±20,9 | 49,6±8,9 | 0,115 |
| SvO2 (%) | 63,3±7,2 | 57,8±7,8 | 0,192 |
| СИ (л/мин*м2) | 1,9±0,4 | 1,8±0,4 | 0,384 |
| Дистанция ТШХ (м) | 358,4±84,9 | 325±158,5 | 0,611 |
| Ширина QRS (мм) | 96,7±12,5 | 96±9,6 | 0,910 |
Примечание: * — различия показателей статистически значимы (p<0,05).
Сокращения: ИЛАГ — идиопатическая легочная гипертензия, НПВ — нижняя полая вена, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, СИ — сердечный индекс, СтЗСТ-ЛАГ — легочная гипертензия, ассоциированная с системной склеродермией, срДЛА — среднее давление в легочной артерии, ТШХ — тест 6-минутной ходьбы, NT-proBNP — N-концевой промозговой натрийуретический пептид, TAPSE — амплитуда систолического движения кольца трикуспидального клапана.
Таблица 3
Портокавальный кровоток у пациентов промежуточного риска
| Показатель | Категории | Группа ЛАГ | p | |
| ИЛАГ | Системная склеродермия | |||
| Кавальный кровоток | A>S | 3 (27,3%) | 2 (40%) | 1,000 |
| A=S | 2 (18,2) | 1 (20%) | ||
| A<S | 6 (54,5%) | 2 (40%) | ||
| Портальный кровоток | <50% | 10 (90,9%) | 3 (60%) | 0,214 |
| >50% | 1 (9,1%) | 2 (40%) | ||
Сокращения: ИЛАГ — идиопатическая легочная гипертензия, ЛАГ — легочная артериальная гипертензия.
Таблица 4
Показатели пациентов подгруппы высокого риска
| Показатель | Пациенты с ИЛАГ (n=5) | Пациенты с СтЗСТ-ЛАГ (n=9) | p* |
| Возраст (годы) | 47±3,9 | 59,2±11,1 | 0,037 |
| Женщины (%) | 100% | 100% | – |
| NT-proBNP (пкг/мл) | 3469,5±144,7 | 4960±2925,2 | 0,342 |
| Общий билирубин (ммоль/л) | 32,3±12,9 | 43,2±27 | 0,419 |
| Площадь ПП (см2) | 26,1±3,9 | 27,4±4,6 | 0,594 |
| TAPSE | 1,2±0,3 | 1,7±0,3 | 0,593 |
| СДЛА (мм рт.ст.) | 102,2±24,8 | 93±15,6 | 0,405 |
| Перикардиальный выпот (%) | 60% | 77,8% | 0,58 |
| Размер НПВ (см) | 2,5±0,2 | 2,2±0,4 | 0,180 |
| Коллабирование НПВ <50% | 40% | 66,7% | 0,580 |
| Давление в ПП (мм рт.ст.) | 13,3±7,9 | 11,8±3,7 | 0,710 |
| срДЛА (мм рт.ст.) | 69,3±12,2 | 61,3±10,5 | 0,305 |
| SvO2 (%) | 59,8±4,9 | 58,7±10 | 0,848 |
| СИ (л/мин*м2) | 1,7±0,3 | 1,9±0,3 | 0,292 |
| Дистанция ТШХ (м) | 313,3±156,9 | 205,8±111 | 0,294 |
| Ширина QRS (мм) | 93,6 (11,9) | 94,3 (13,5) | 0,931 |
Примечание: * — различия показателей статистически значимы (p<0,05).
Сокращения: ИЛАГ — идиопатическая легочная гипертензия, НПВ — нижняя полая вена, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, СИ — сердечный индекс, СтЗСТ-ЛАГ — легочная гипертензия, ассоциированная с системной склеродермией, срДЛА — среднее давление в легочной артерии, ТШХ — тест 6-минутной ходьбы, NT-proBNP — N-концевой промозговой натрийуретический пептид, TAPSE — амплитуда систолического движения кольца трикуспидального клапана.
Таблица 5
Портокавальный кровоток у пациентов подгруппы высокого риска
| Показатель | Категории | Группа ЛАГ | p | |
| ИЛАГ | СтЗСТ-ЛАГ | |||
| Кавальный кровоток | A<S | 0 (0%) | 3 (33,3%) | 0,221 |
| A=S | 1 (11%) | |||
| A>S | 5 (100%) | 5 (55,6%) | ||
| Портальный кровоток | <50% | 0 (0%) | 3 (33,3%) | 1,000 |
| >50% | 5 (100%) | 6 (66,7%) | ||
Сокращения: ИЛАГ — идиопатическая легочная гипертензия, ЛАГ — легочная артериальная гипертензия, СтЗСТ-ЛАГ — легочная гипертензия, ассоциированная с системной склеродермией.

Рис. 4. Портокавальный кровоток пациента высокого риска с СтЗСТ-ЛАГ.
Обсуждение
Изменения гемодинамики, возникающие в правых камерах сердца при ЛГ, влекут за собой и изменения в портокавальной кровотоке. В систолу при увеличении давления в ПП происходит реверсивный ток крови в НПВ. На спектре волн ПВ это выглядит как ретроградная А-волна. Китайские исследователи Sun DD, et al. получили увеличение А-волны у пациентов с ЛГ, ассоциированной с врожденными пороками. Поскольку у пациентов с ЛГ обычно повышено конечное диастолическое давление ПЖ, ПП должно сокращаться с большей силой, чтобы наполнить кровью ПЖ. Это приводит к увеличению давления в ПП и усилению ретроградного кровотока в полые вены. Кроме того, длительная перегрузка давлением приводит к гипертрофии ПЖ, расслабление которого может уменьшиться во время ранней диастолы, что ограничивает быстрое наполнение ПП. Затем ПП расширяется во время поздней диастолы за счет увеличения емкости. Компенсаторное сокращение волокон миокарда ПП усиливалось за счет эффекта Франка-Старлинга, что увеличивало скорость венозного рефлюкса и делало волну А более высокой [9].
Что касается длительности А-волны и смещения её на комплекс QRS, ввиду сохранения высокого давления в полости ПП даже во время систолического закрытия ТК, кровь продолжает возвращаться в ПВ в течение более длительного времени, чем через ТК, что и приводит к увеличению длительности А-волны в ПВ [9, 10].
В давнем исследовании, проведенном японской командой, Sakoda S, et al., также подтверждено, что волна А была увеличена в случаях ЛГ, а скорость А-волны в ПВ коррелировала с СДЛА1.
Считается, что изменение формы, высоты и направления S-волны связано с ТР. Во время систолы сокращаются не только стенки ПЖ, которые проталкивают кровь в его выходной тракт, но также происходит движение кольца ТК к верхушке сердца. Эти действия создают относительное отрицательное давление в ПП, вызывая антеградный отток крови из печени в сердце во время S-зубца. В нормальном сердце наибольшее количество антеградного кровотока наблюдается во время этой фазы. Легкая степень ТР не оказывает заметного влияния на допплеровский профиль ПВ, в то время как умеренная ТР может вызвать ослабление систолической формы волны. Во время систолы трикуспидальное кольцо также движется к верхушке сердца, как обычно. Однако из-за ТР кровь вытесняется ретроградно в предсердие, НПВ и печень (а также в выходной тракт ПЖ). Это дает уменьшенную или даже ретроградную S-волну [8][11]. Установлено, что нормальная венозная кривая ПВ становится монофазной у пациентов с циррозом печени или внутри печеночно-портальной гипертензией. Что описывается, как демпфирование венозной кривой [12]. Sun DD, et al. в своей работе сообщают о двух пациентах из группы ЛАГ, у которых при допплерографии ПВ наблюдалась монофазная допплеровская волна без фазы ретроградного потока. Среди них не было пациентов с циррозом, что было определено с помощью серологического анализа и ультразвукового исследования. Исследователи предположили, что монофазная волна отражала повышенную жесткость паренхимы печени вокруг ПВ и сниженную податливость ПВ [9].
Также обнаружена связь между задержкой конечного вдоха и притуплением венозных кривых ПВ. Это притупление может произойти из-за комбинации аспирационного эффекта, улучшающего наполнение ПЖ и, возможно, повышенного внутрибрюшного давления, если пациент непреднамеренно выполняет маневр Вальсальвы [13]. Однако мы предполагаем, что такие ситуации маловероятны, ввиду возможности проследить за актом дыхания пациента во время проведения исследования и при необходимости дать пациенту более четкие инструкции.
В норме кровь по воротной вене течёт с постоянной скоростью в направлении печени, поэтому ПК имеет монофазный или слабопульсирующий характер. При ТР повышенное давление из ПП передаётся ретроградно через печёночные вены в портальную систему, что приводит к характерным изменениям кровотока. Во время систолы желудочков регургитация вызывает снижение портального потока и возникает патологическая пульсация на венозной кривой ПК, а при превышении систолического реверсивного давления над антеградным развивается реверсивное направление потока (рис. 3). Установлено, что эти изменения могут косвенно свидетельствовать о повышении транспеченочного градиента давления, т.е. о застойной портальной гипертензии, обусловленной правожелудочковой недостаточностью, ЛГ и ТР [4].
Согласно полученным данным, венозные кривые портокавального кровотока демонстрировали наибольшую неоднородность у пациентов подгруппы СтЗСТ-ЛАГ, относящихся к категориям промежуточного и высокого риска, также у этих пациентов выявлен больший уровень ЭЖП, чем в группе ИЛАГ. Это явление может быть обусловлено патогенетическими особенностями ССк — редкого заболевания соединительной ткани, для которого характерно сочетание аутоиммунных механизмов с выраженными сосудистыми нарушениями, прогрессирующим фиброзом кожи и внутренних органов и значительной вариабельностью возможных исходов. Точное определение фенотипов ЛГ у пациентов с ССк по-прежнему представляет сложность в клинической практике. Вероятно, это связано с многообразием и возможным переплетением патогенетических механизмов ЛГ при ССк. В частности, развитие ЛГ может быть обусловлено васкулопатией легочных артерий, интерстициальным фиброзом легких, поражением сердца или изменениями, напоминающими венозную окклюзионную болезнь легких. Однако у отдельных пациентов бывает трудно выделить единственный ведущий механизм, поскольку зачастую эти факторы сочетаются в различных пропорциях, формируя клиническую картину заболевания [14].
В клинической практике печень и ее микрососудистая структура не входят в число целей ССк. Тем не менее у пациентов с ССк может редко присутствовать аутоиммунное поражение печени, в основном состоящее из первичного билиарного холангита. В испанском реестре, состоящем из 1572 пациентов с ССк, было зарегистрировано 118 (7,5%) случаев гепато-билиарных расстройств: биларный холангит был основной причиной более чем в половине случаев, в то время как аутоиммунный гепатит составлял 16% этой группы; и только у 7 пациентов были обнаружены гепато-билиарные аномалии, связанные с самой ССк. Интерес представляют антиэндотелиальные антитела, выявленные у некоторых пациентов с идиопатической портальной гипертензией, которые повреждают эндотелиальные клетки портальных сосудов и создают плотные отложения эластических волокон вокруг периферических разветвлений вен печени. Антиэндотелиальные антитела также были обнаружены у значительного процента пациентов с ССк, что напрямую коррелировало с повреждением сосудов и эндотелия, посредством антителозависимого клеточного апоптоза, который стимулировал микрососуды к высвобождению провоспалительных и профибротических цитокинов [15].
Заключение
Таким образом, сопоставление данных венозных кривых портокавального кровотока и критериев оценки риска у пациентов с ЛАГ, выявило корреляцию между пульсацией ПК, увеличением высоты А-волны КК и степенью риска. Выявленная взаимосвязь представляет значительный клинический интерес, поскольку может служить основанием совершенствования терапевтических подходов и улучшения показателей качества жизни пациентов. К тому же она демонстрируют перспективность использования характеристик портокавального кровотока для неинвазивной оценки повышения ЦВД и транспеченочного градиента у пациентов с правожелудочковой сердечной недостаточностью для прогнозирования висцеральной дисфункции.
Тем не менее у пациентов подгруппы СтЗСТ-ЛАГ были получены разнородные результаты, что подчеркивает важность проведения дополнительных исследований для создания детализированной классификации степеней венозного застоя с учетом специфики различных подгрупп ЛАГ.
1 Sakoda S, Mitsunami K, Kinoshita M. Evaluation of hepatic venous flow patterns using a pulsed Doppler technique. J Cardiol. 1990;20(1):193-208. [Japanese].
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Барковская М.К., Кушнир В.В., Мартынюк Т.В. Особенности портокавального кровотока у пациентов с легочной артериальной гипертензией. Российский кардиологический журнал. 2025;30(2S):6443. https://doi.org/10.15829/1560-4071-2025-6443. EDN: BHKPSI
Скопировать