Новые концепции в вариабельности артериального давления
Аннотация
В обзоре литературы последних лет рассмотрены новые концепции в вариабельности артериального давления (ВАД), их возможное клиническое значение. По нашему мнению, перспективны два подхода, в которых патофизиологические процессы, лежащие в основе, рассматриваются как в виде простой линейной модели, так и в виде более сложной, нелинейной. При этом оба подхода имеют конкретное практическое воплощение: первый — в виде шкалы, второй — в виде новых показателей ВАД. Шкала предназначена для оценки выраженности так называемого системного гемодинамического атеротромботического синдрома, являющегося результатом накапливающегося в течение длительного времени синергетического взаимодействия поражения сосудов и «гемодинамического стресса», а новые показатели описывают меру сложности ВАД «от удара к удару», отражающей сохранность регуляторных механизмов. Анализ литературы позволил нам также предположить возможные пути совершенствования указанных концепций.
Вот уже несколько десятилетий вариабельность артериального давления (ВАД) привлекает внимание исследователей в области артериальной гипертензии (АГ). Результаты их работы подкрепляют представление о том, что ВАД является отдельным фактором риска сердечно-сосудистой и общей смертности, коронарной болезни, сердечной недостаточности (СН), конечной стадии хронической болезни почек, инсультов и деменции [1-3].
Ценный материал об этом, опубликованный в последние годы, стимулировал возникновение нового Консенсуса, посвященного этой, сравнительно узкой области «гипертензиологии». Примечательно, что авторы не дают четкого определения понятия ВАД, ограничиваясь «количественным» указанием. «Более специфические определения основаны на продолжительности наблюдения: очень краткосрочная (very-short-term) ВАД (от сокращения к сокращению и даже в пределах одного сокращения (within beat), краткосрочная (в течение 24-х часов, от изменений артериального давления (АД) в течение нескольких минут до циркадных колебаний и величины утреннего подъема АД), среднесрочная (в течение нескольких дней), долгосрочная (изменения в течение недель, месяцев, сезонные колебания, а также ВАД в пределах нескольких визитов в клинику) [3]. Согласно консенсусу, «сверхдолгосрочные» (в течение нескольких лет) колебания АД отражают, скорее, процесс старения организма и не относятся к ВАД.
Надо отметить, что в отечественной литературе ВАД определяют как «множественные отклонения от систематического тренда АД» [4] или применительно к 24-х часовому профилю, — «отклонения от суточного ритма АД» [5]. При таком подходе некоторые описанные в консенсусе параметры — циркадные изменения АД (specific patterns), а также минимальные и максимальные значения АД за определенный период и их соотношения (instability), к ВАД не относятся.
Однако материалы консенсуса убедительно подтверждают то, что представления о ВАД (как в «узком», так и в более широком понимании термина) не являются чем-то устоявшимся, а претерпевают не только количественные, но и качественные изменения, что выразилось в появлении новых концепций, в определённой степени переосмысливающих клиническое значение ВАД [6][7].
В настоящем обзоре мы рассмотрели два новых перспективных подхода, в которых патофизиологические процессы, лежащие в основе, рассматриваются как в виде простой линейной модели, так и в виде более сложной, нелинейной. Первая концепция названа авторами «системным гемодинамическим атеротромботическим синдромом» (СГАТС). Он, по их мнению, является результатом накапливающегося в течение длительного времени синергетического взаимодействия поражения сосудов и «гемодинамического стресса», связанного с ВАД. Вторая концепция предполагает соответствие сохранности регуляторных механизмов, ответственных за АД, мере сложности «очень краткосрочной» ВАД — вариабельности «от удара к удару» (ВУУ), выражающейся в показателях, связанных с энтропией.
Краткая сравнительная характеристика концепций представлена в таблице 1. Разделение на две концепции может показаться несколько искусственным с клинических позиций, но может быть оправдано с методических: оба подхода имеют конкретное практическое воплощение, первый — в виде шкалы, второй — в виде новых показателей вариабельности.
Таблица 1
Методологические отличия рассмотренных концепций
|
Характеристика |
СГАТС |
Нелинейная модель |
|
Вид вариабельности (по классификации ESH) |
от краткосрочной до сезонной |
очень краткосрочная, «от удара к удару» |
|
Период, за который анализируется АД |
от суток до лет, прерывистые измерения. Дополнительную информацию имеет «траектория» АД в течение жизни |
сотни ударов сердца подряд |
|
Функциональная область («домен») показателей ВАД |
дисперсия, временна́я область, циркадный профиль |
область сложности (рис. 1) |
|
Учёт сосудистых гемодинамических показателей |
да |
нет |
Сокращения: АД — артериальное давление, ВАД — вариабельность артериального давления, СГАТС — системный атеротромботический синдром, ESH — European Society of Hypertension.
Концепция системного гемодинамического атеротромботического синдрома
Концепция СГАТС развита из предложенной ранее Kazuomi Kario гипотезы резонанса, приводящего к выраженному острому повышению АД [8], и поддержана затем крупными исследователями из США и Японии [6]. Концепция описывает порочный круг сосудистых заболеваний и «гемодинамического стресса», влияющих друг на друга синергически. Kario К, et al. предположили, что оценка ВАД, выражающей «гемодинамический стресс», в сочетании с диагностикой поражения артерий могли бы быть основой для раннего вмешательства при АГ, что уменьшило бы её прогрессирование, и, соответственно, количество сердечно-сосудистых событий в дальнейшем.
Описание «порочного круга» в СГАТС является синтезом современных представлений о ВАД и о гемодинамических явлениях [3][9][10]. Согласно авторам концепции, влияния, запускающие развитие разнообразных клинических видов СГАТС, в основном механистические. К ним относятся увеличение постнагрузки на левый желудочек (ЛЖ), усиление напряжения сдвига в артериях и повреждение атеросклеротической бляшки при критичном повышении АД [11]. Хронически повышенная постнагрузка способствует гипертрофии и диастолической дисфункции ЛЖ, связана с повышенным риском СН, в т. ч. острой. К другим влияниям относятся артериосклероз и следующая за ним потеря способности крупных артерий гасить гидродинамическую энергию, что ведёт к широкому спектру нарушений в мелких артериях: от микроциркуляторных заболеваний, таких как хроническая болезнь почек, микроваскулярная стенокардия, до церебральных кровоизлияний и инфарктов или повреждений афферентных артериол клубочков юкстамедуллярных нефронов. Однако к СГАТС относятся не только артериосклероз при АГ или естественном процессе старения, но и атеросклероз, инициированный повреждением эндотелия на фоне метаболических изменений, с возникновением бляшек; а также, кроме коронарной болезни сердца, инсультов, СН, и другие болезни артерий: расслоения, аневризмы аорты [6]. Заболевания артерий усиливают «гемодинамический стресс» через нейрогуморальные звенья, включающие изменения барорефлекса [8][11].
Краеугольным камнем концепции СГАТС является гипотеза «резонанса». Авторы описывают ВАД в разных временны́х интервалах: от краткосрочных до годовых (сезонных). Так, одним из примеров «резонанса» является увеличение реактивности АД зимой [12]. Как одну из форм ВАД рассматривают также отличающиеся формы пульсовой волны при каждом сердечном сокращении, что согласуется с современными преставлениями о так называемом «форм-факторе» волн [13]. Вследствие ремоделирования мелких артерий и изменений барорефлекса выраженность каждой ВАД увеличивается, и предполагается, что «резонанс» любой формы ВАД с каждым годом может с возрастающей вероятностью генерировать большие динамические «всплески» АД, которые, в свою очередь, ускоряют или даже вызывают наступление сердечно-сосудистых событий [8].
Конечно, применение термина «резонанс» достаточно условно; тем не менее оно вполне пригодно для того, чтобы показать, что происходит не простое суммирование колебаний, а их усиление. Синергетическое взаимодействие накапливающейся сосудистой патологии и АД, имеющего «всплески» по причине вышеописанного «резонанса», определило и принцип оценки тяжести СГАТС, с использованием недавно предложенной шкалы (табл. 2) [14]. Как видно из таблицы 2, компонентами шкалы СГАТС являются оценка АД и оценка сосудов. Вес, присвоенный каждому компоненту двух оценок, основан на относительных рисках, определенных с использованием существующей литературы. Чтобы отразить синергетическое взаимодействие, для расчета тяжести СГАТС суммарные баллы, выражающие вес компонентов, не суммируются, а умножаются.
Таблица 2
Шкала СГАТС
|
Компонент |
Баллы |
|
А. Оценка АД |
Всего 10 баллов |
|
1. Офисное АД |
Максимум 2 балла |
|
Офисное САД ≥140 мм рт.ст. |
1 балл |
|
Офисная ВАДсист↑e |
1 балл |
|
2. Домашнее АД |
Максимум 3 балла |
|
Домашнее САД↑ (утром или вечером ≥135 мм рт.ст. или ночьюa ≥120 мм рт.ст. |
2 балла |
|
Домашняя ВАДсист↑f |
1 балл |
|
3. СМАДb |
Максимум 3 балла |
|
Амбулаторное САД↑ (дневное/утреннее ≥135 мм рт.ст., ночноеa ≥120 мм рт.ст. или 24-часовое ≥130 мм рт.ст.) |
2 балла |
|
Амбулаторная ВАДсист↑g |
1 балл |
|
4. Суточный профильc |
Максимум 2 балла |
|
Ночной подъём |
2 балла |
|
Экстремальное ночное снижение или утренний подъём↑ |
1 балл |
|
5. Мерцательная аритмия |
5 балловd |
|
B. Сосудистая оценка |
Всего 10 баллов |
|
1. ССЗh |
Максимум 5 баллов |
|
Одно сердечно-сосудистое заболевание |
2 балла |
|
Два ССЗ |
4 балла |
|
Три и более ССЗ |
5 баллов |
|
2. Бессимптомные ССЗ |
Максимум 3 балла |
|
Одна аномальная находка |
1 балл |
|
Две аномальных находки |
2 балла |
|
Три и более аномальных результата |
3 балла |
|
3. Микрососудистые заболевания |
Максимум 2 балла |
|
ХБП, связанная с диабетом (альбуминурия, рСКФ <60 мл/мин/1,73 м²)/ретинопатия мелких артерий |
2 балла |
Примечания: таблица воспроизводится с любезного разрешения Кazuomi Kario.
Показатели АД и сосудистых показателей рассчитываются отдельно, каждый из которых может иметь оценку от 0 до 10 баллов. Эти баллы затем умножаются для расчета тяжести СГАТС (0-100). Для диагностики СГАТС требуется оценка ≥5 баллов, при этом тяжесть СГАТС увеличивается параллельно со значением шкалы.
а — САД в ночное время можно измерить с помощью СМАД или домашнего мониторинга АД; b — если СМАД не выполняется, общий балл по СМАД и суточной вариации равен 1; c — суточные колебания оцениваются с помощью СМАД; d — при наличии мерцательной аритмии (оценка =5) баллы ВАДсист и суточного профиля равны 0; e — определяется как максимальное САД ≥180 мм рт.ст., стандартное отклонение от визита к визиту [SD] ≥20 мм рт.ст., ортостатическое изменение (увеличение или снижение) ≥20 мм рт.ст. или сезонные колебания (САД зимой минус САД летом) <0 мм рт.ст. или ≥20 мм рт.ст.; f — определяется как максимальное утреннее/вечернее САД ≥180 мм рт.ст., максимальное ночное САД ≥160 мм рт.ст., утренне-вечерняя разница ≥20 мм рт.ст., или межсуточный коэффициент вариации ≥6,1%, или сезонная вариация (САД зимой минус САД летом) <0 мм рт.ст. или ≥9,1 мм рт.ст.; g — определяется как максимальное дневное САД ≥180 мм рт.ст., максимальное ночное САД ≥160 мм рт.ст. или средневзвешенное САД ≥20 мм рт.ст.; h — ССЗ = инсульт, ишемическая болезнь сердца, сердечная недостаточность, аортальный стеноз, когнитивная дисфункция или заболевание периферических артерий/расслоение аорты; i — оценка бессимптомного ССЗ — это количество аномальных результатов, основанных на следующих четырех тестах: Тест 1 (пульсовое давление) — офисное, домашнее или амбулаторное пульсовое давление ≥70 мм рт.ст.; Тест 2 (ЛПИ/каротидная бляшка) — лодыжечно-плечевой индекс <0,9 или ≥1,3 (или межплечевая разница САД ≥15 мм рт.ст.) или наличие каротидной бляшки (максимальная толщина интима-медиа N 1,1 мм); Тест 3 (артериальная жесткость) — сердечно-лодыжечный сосудистый индекс (CAVI) ≥9 (или скорость плече-лодыжечной пульсовой волны ≥18 м/с, или скорость каротидно-феморальной пульсовой волны ≥10 м/с); Тест 4 — патологические изменения со стороны сердца (гипертрофия левого желудочка, определяемая на электрокардиографии или эхокардиографии, или уровень N-концевого промозгового натрийуретического пептида ≥125 пг/мл). Другие специфические аномалии, такие как опосредованное потоком расширение плечевой артерии <4%, пиковая систолическая скорость почечной артерии ≥220 см/с, поражение белого вещества, бессимптомный церебральный инфаркт или микрокровоизлияния, оцениваемые с помощью магнитно-резонансной томографии головного мозга, объединяются в один балл, если был обнаружен положительный результат (Тест 5). Однако они необязательны и не всегда необходимы.
Сокращения: АД — артериальное давление, ВАДсист — вариабельность систолического артериального давления, ЛПИ — лодыжечно-плечевой индекс, рСКФ — расчетная скорость клубочковой фильтрации, САД — систолическое артериальное давление, СМАД — суточное мониторирование артериального давления, ССЗ — сердечно-сосудистые заболевания, ХБП — хроническая болезнь почек.
Имея практическое воплощение, новая концепция ВАД обладает также потенциалом для дальнейшего развития, и при глубоком анализе концепции СГАТС можно предложить пути её совершенствования.
Так, например, поздняя систолическая постнагрузка на ЛЖ, как одно из проявлений сосудистого компонента СГАТС, в работах Kario К, et al. объясняется уменьшенным временем прохождения «отраженных» пульсовых волн по жёсткой аорте и попаданием их в систолу желудочка. Можно отметить, что понятием «отражённых» волн до сих пор оперирует ряд научных коллективов, объясняя поражение органов-мишеней [15]. Однако гипотеза «отражений» пульсовых волн критиковалась уже довольно давно [16], и выглядит слабой по сравнению с гипотезой, описывающей входной импеданс и резервуарное давление в аорте и крупных артериях [17][18]. Не исключено, что дальнейшая работа в этом направлении сможет привести к уточнению раздела «сосудистая оценка» шкалы СГАТС при помощи показателей, например, ультразвуковых, которые чётко отражали бы постнагрузку ЛЖ.
Возможно, повысить практическую ценность шкалы удастся с помощью модификации, учитывающей применение дополнительных показателей домашнего мониторирования АД (ДМАД), получивших существенное развитие в последнее время. В недавнем масштабном исследовании обнаружилось, что показатели ВАД (не использованные в таблице 2) при ДМАД имеют превосходство в прогнозировании сердечно-сосудистого риска по сравнению с ВАД при суточном мониторировании АД [19]. Хорошая воспроизводимость показателей ДМАД, наличие целевых значений домашнего АД [20], простота расчёта ВАД [21] и, кроме этого, очень важная для практики возможность оперативного подбора терапии, а также возрастание приверженности пациентов к лечению [22], являются дополнительными аргументами, которые могут быть использованы в работе по методологическому совершенствованию шкалы. Весьма перспективно также ночное ДМАД [20].
Усовершенствовать подход можно также выбирая сосудистые показатели с более высокой диагностической ценностью. Так, авторы предлагают использовать лодыжечно-плечевой индекс (ЛПИ), который вносит вклад в шкалу как в случае его низких значений (<0,9), так и высоких (>1,3). Однако известно, что высокий ЛПИ не считается подходящим инструментом для диагностики, а исследования, которые сделали выводы на основе ЛПИ >1,3, скорее всего, неправильно оценивали обнаруженные эффекты [23]. Крупными научными сообществами в таких случаях рекомендуется использовать метод, основанный на обычной плоскостной рентгенографии стопы в двух проекциях [24]. Ещё одним предлагаемым сосудистым показателем является CAVI [25], определение которого относится к так называемым «прокси»-методам оценки жёсткости аорты. Приставка «прокси» обозначает, что, кроме аорты, являющейся зоной интереса, волны дополнительно проходят ещё и другие участки сосудистого русла, и вследствие большого расстояния от точек измерения до аорты это приводит к «неоднозначной интерпретации пройденного волной пути вдоль эластичных и мышечных артерий, и поэтому практически невозможно эффективное согласование полученных значений с реальной жесткостью аорты» [26]. Вместо таких «прокси»-методов, научные сообщества рекомендуют использовать магнитно-резонансную томографию или, по крайней мере, методы с более близким к аорте расположением точек и расчётом каротидно-феморальной скорости пульсовой волны [27].
Таким образом, как шкала, так и концепция СГАТС в целом весьма перспективны, их развитие может быть связано с усовершенствованием теории и, в большей степени, с выбором наиболее диагностически и/или клинически ценных методик.
Концепция нелинейного взаимодействия пато- и физиологических влияний
Автор концепции СГАТС раскрывает систему патофизиологических взаимодействий через понимание подкомпонентов этой системы. Как известно, полностью описать и понять какую-либо систему с помощью разложения на подкомпоненты возможно лишь в том случае, если она линейная (а именно, не имеет информационной неопределённости или непредсказуемости). Нелинейные же системы таким свойством не обладают по причине «конструктивного» или «деструктивного» взаимодействия между этими подкомпонентами, что делает, в частности, возможными непредвиденные эффекты, когда небольшие изменения на «входе» могут вызвать серьезные изменения на «выходе» (так называемый «эффект бабочки»). В последние годы развилось также и более сложное понимание, чем в концепции СГАТС, происхождения и характеристик спонтанных изменений АД, относящихся именно к области «сложности», что выразилось в появлении новых, так называемых нелинейных показателей, пришедших к нам из теории информации, среди инструментов которой есть и оценка неопределённости.
Давно известно, что ВУУ связана с постоянной модуляцией сосудистого тонуса нейрогуморальными влияниями, например, симпатическими и парасимпатическими, меняющимися в ответ на барорецепторные и кардиореспираторные рефлексы. В ВУУ вовлечены ренин-ангиотензиновая система, катехоламины, эндотелин-1 и оксид азота, и даже, косвенным образом, инсулин [28]. Эндотелиально-зависимый синтез оксида азота влияет на АД с частотой, аналогичной респираторным процессам [29], а миогенный ответ сосудов на повышенное перфузионное давление вызывает возмущения в виде очень низкочастотных колебаний [10][30].
Благодаря этой постоянной модуляции, оценка ВУУ может иметь независимую способность различать патологические изменения даже при состояниях, в которых средние значения АД идентичны, а также фиксировать детали и тонкости, которые могут быть упущены при периодических измерениях АД [7].
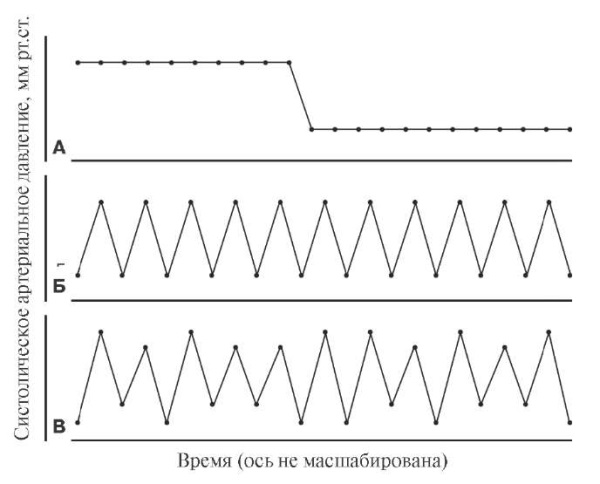
Современный анализ ВУУ позволяет надежно проводить количественную её оценку с использованием как линейных, так и нелинейных параметров [31]. К линейным параметрам относятся уже давно известные показатели двух категорий. К первой категории относятся параметры, которые рассчитываются как функция средних уровней и не учитывают временной ряд значений АД (рис. 1, пример А); к этим параметрам относятся стандартное отклонение, коэффициент дисперсии и вариабельность, независимая от среднего [3]. Индексы второй категории (средняя реальная вариабельность, остаточная последовательная разность и последовательная дисперсия) учитывают временной порядок точек данных АД (рис. 1, пример Б) и рассчитываются на основе линейной функции времени. Многочисленные работы отмечают связь линейных показателей ВУУ со структурой и функцией артерий, цереброваскулярными событиями, вегетативным контролем, метаболическими нарушениями [1-4][32][33].

Рис. 1. Примеры ВАД в виде упрощённых схем.
Примечание: линейные параметры ВАД, не учитывающие временной ряд, демонстрируют одинаковое значения в примерах А, Б и В; линейные параметры ВАД, относящиеся ко временно́й области, отличаются в примерах А и Б, но могут быть одинаковы в примерах Б и В; нелинейные параметры ВАД (относящиеся к области сложности) отличаются во всех примерах. Примеры А и Б адаптированы из [34]. См. также объяснения в тексте.
Нелинейные индексы учитывают и временну́ю структуру и организацию серии измерений (рис. 1, примет В). Эти параметры основаны на постулате о том, что неустойчивое поведение биологических систем происходит из-за конкурентных и, что важно, нелинейных взаимодействий сердечно-сосудистых влияний, поступающих в систему из множества подкомпонентов.
Нелинейные параметры включают вычисление энтропии (En) и анализ флуктуаций без тренда (АФБТ) [3][31]. Под энтропией имеется в виду информационная энтропия как мера неопределённости какой-либо системы, либо как мера скорости производства информации. К вычислениям энтропии первоначально относилась аппроксимационная энтропия (ApEn) [35], затем, чтобы преодолеть её недостатки, включающие зависимость от длины записи, разработан расчёт выборочной энтропии (SamEn) [36], а в последующем и энтропии, «измеряемых в нескольких шкалах» (Multiscale entropy, MSE) [37]. Имеются сообщения об использовании так называемой энтропии компрессии (CompEn) для изучения ВАД [38]. Необходимо отметить, что сложность отражает степень надежности или устойчивости механизмов контроля АД и снижается с возрастом или с наличием патологии [7].
В противоположность этому, корреляции между подкомпонентами временны́х рядов ВУУ при АФБТ, наоборот, повышаются. Корреляционный анализ дает количественную оценку самоподобия этих рядов, являющегося результатом вклада ее фрактальных сосудистых подсетей, а также нервных и гуморальных путей в регуляцию кровотока и установление гомеостаза [39]. Временной ряд называется самоподобным, если его можно разделить на подкомпоненты, колебания которых статистически подобны общей динамике глобальной системы. АФБТ обладает способностью обнаруживать долгосрочные корреляции в нерегулярном внешнем тренде. В таком анализе показатель отражает как бы «шероховатость» данного временного ряда, так что большее значение указывает на более сглаженный набор данных с более высокой степенью корреляции [40].
Возрастает количество публикаций, оценивающих значение нелинейных параметров ВУУ в клинике. Так, есть сведения об изучении совместно с традиционными оценками влияния показателей сложности (En и АФТБ) в предоперационной ВУУ на периоперационный риск у пациентов при плановом аортокоронарном шунтировании. Между MSE ДАД и оценками риска смертности и заболеваемости по клинической шкале общества торакальных хирургов присутствовала значительная обратная связь [31]. При изучении связей между вегетативной дисфункцией, вызывающей потерю гемодинамической адаптивности к стрессорам, влияющим на физиологические резервы, и сложностью АД, у ослабленных пациентов была значительно более низкая MSE по сравнению с пациентами без дисфункции. Изучение сложности АД было способно предсказать продолжительность пребывания в отделении интенсивной терапии в степени, сравнимой со шкалой риска общества торакальных хирургов [41]. Кроме исследований в клинике с оценками различных сердечно-сосудистых рисков, имеется также ряд публикаций, указывающий на хорошие диагностические характеристики нелинейных показателей ВУУ при использовании их у пациентов с ожирением, сахарным диабетом 1 типа, при различных терапевтических вмешательствах [7].
Следует также отметить исследование возможных механизмов, лежащих в основе вегетативных расстройств, в которых продемонстрирована способность параметров сложности различать эффекторы динамики АД в ответ на запрокидывание головы вверх и на решение арифметических задач в уме. Обнаружено, что при запрокидывании головы сложность снижается, что можно объяснить повышенным симпатическим тонусом, непосредственно влияющим на резистивные артерии в отрыве от других систем, т. е. сердечной и дыхательной. Однако при наличии психического стресса условная энтропия как систолического АД, так и диастолического АД увеличивается и зависит от участия высших отделов мозга в регуляции АД [42].
Анализ литературы показывает, что перспективы развития нелинейной модели и соответствующих показателей ВАД хорошо определены научным медицинским сообществом. Нелинейные показатели оценивались в клинике с использованием безманжеточных методов измерения АД. Эти методы до недавнего времени были не стандартизированы и представляли собой широкую и разнородную группу техник, которые могли иметь известные потенциальные проблемы с точностью, связанные, например, с необходимостью индивидуальной калибровки и стабильностью этих измерений после калибровки [43]. Это ограничение было преодолено недавно принятыми основополагающими стандартами для валидации необходимых устройств 1 [44]. Таким образом, ближайшие перспективы концепции заключаются в накоплении стандартизированных эпидемиологических и в первую очередь клинических данных валидированными должным образом устройствами, а также в обобщении полученного опыта.
Нерешенные проблемы и перспективы
Как показывает анализ литературы, большинство источников не противоречат друг другу, и это является аргументом для учета ВАД в современном ведении больных АГ. К сожалению, остаётся актуальным, в т. ч. и для отечественной медицины, применение аппаратуры хорошего качества, т. к. в противном случае значения ВАД могут быть сильно переоценены [45]. Сильное влияние на оценку ВАД может оказать «ручное» редактирование записей, что делает полученные результаты слабо воспроизводимыми. Ещё одним «минусом» является отсутствие взаимозаменяемости индексов: например, краткосрочная, среднесрочная и долгосрочная ВАД могут быть связаны с исходами в одинаковой степени, но слабо коррелировать между собой [46].
Среди многих вопросов, обсуждаемых экспертами в настоящее время, важное значение имеет так называемая «добавочная прогностическая ценность». Не до конца решён вопрос, достаточна ли дополнительная прогностическая ценность ВАД для того, чтобы сделать её клинически полезным маркером сердечно-сосудистого риска. Поэтому полезные практические указания, предложенные в последнем консенсусом документе, пока практически не нашли отражения в современных клинических рекомендациях по АГ [47]. Однако самые современные публикации [1][48] дают надежду, что это — дело недалёкого будущего.
Заключение
При рассмотрении двух новых патофизиологических концепций мы можем убедиться, что различные типы колебаний АД могут раскрывать различные механизмы контроля деятельности сердечно-сосудистой системы. Это подтверждает заявления в новом консенсусе специалистов по ВАД о том, что данное явление представляет собой не «физиологический шум», который необходимо удалить для точной оценки уровней АД, а является ценным источником сердечно-сосудистой информации.
Несомненным «плюсом» в согласительном документе европейских экспертов по ВАД является попытка создать ориентиры для практического использования показателей ВАД. В частности, при повышенной ВАД рекомендуется предпочтительное применение антигипертензивных препаратов длительного действия (в т. ч. в составе комбинированной терапии) для достижения более равномерного эффекта и во избежание ятрогенного повышения ВАД. При отсутствии клинических показаний для выбора других конкретных классов препаратов, рекомендованы блокаторы кальциевых каналов длительного действия и диуретики (препараты с доказанным позитивным эффектом в отношении ВАД). Предложены примерные пороговые значения для основных показателей ВАД. Превышение этих значений потенциально означает принадлежность пациента к группе более высокого риска ССЗ.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Non-invasive sphygmomanometers — Part 3: Clinical investigation of con¬tinuous automated measurement type [Internet]. International Organization for Standardization (ISO) 81060-3:2022. [Accessed 19 July 2023] Available from: https://www.iso.org/standard/71161.html.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Горбунов В.М., Посохов И.Н. Новые концепции в вариабельности артериального давления. Российский кардиологический журнал. 2024;29(2S):5827. https://doi.org/10.15829/1560-4071-2024-5827. EDN: GPHOIF
Скопировать