Легочная гипертензия у пациентов с сердечной недостаточностью с сохраненной фракцией выброса
Аннотация
Легочная гипертензия (ЛГ), развивающаяся на фоне сердечной недостаточности с сохранённой фракцией выброса (СНсФВ), является распространённым и прогностически неблагоприятным состоянием. В обзоре рассматриваются эпидемиология, патогенез, подтипы ЛГ, а также ключевые биомаркеры и гемодинамические показатели, влияющие на прогноз. Особое внимание уделено роли правожелудочковой дисфункции и сосудистого ремоделирования при комбинированной ЛГ. Представлены диагностические алгоритмы, отражающие сложности дифференциальной диагностики между легочной артериальной гипертензией и ЛГ-СНсФВ. Обзор подчёркивает важность раннего выявления и персонифицированного подхода к пациентам с ЛГ-СНсФВ.
Легочная гипертензия (ЛГ) — это гемодинамическое и патофизиологическое состояние, при котором среднее давление в лёгочной артерии превышает 20 мм рт.ст. в покое, согласно данным катетеризации правых отделов сердца (КПОС) [1].
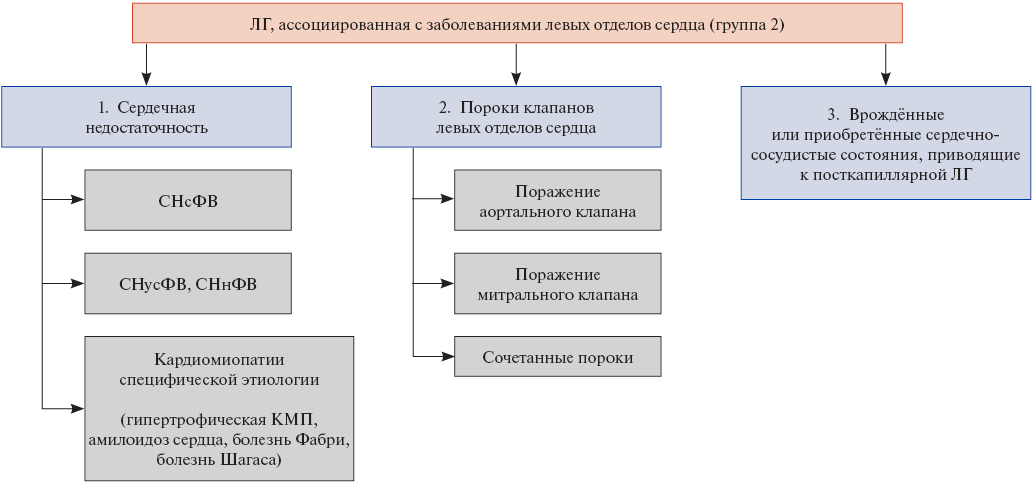
Наиболее частой причиной повышения давления в малом круге кровообращения является патология левых отделов сердца. По данным эпидемиологических исследований, на её долю приходится от 65% до 80% всех случаев ЛГ [2]. Согласно обновлённой клинической классификации ЛГ, принятой на VII Всемирном симпозиуме по легочной гипертензии, данное состояние отнесено ко II группе — ЛГ, ассоциированной с заболеваниями левых отделов сердца [3]. В свою очередь, ЛГ, ассоциированная с заболеваниями левых отделов сердца, также классифицируется на подтипы (рис. 1).
ЛГ развивается как при хронической сердечной недостаточности (ХСН) со сниженной фракцией выброса (ФВ) (СНнФВ), так и при ХСН с сохранённой ФВ (СНсФВ), причём значительно чаще встречается при последней [4].
Во II группе ЛГ выделяют два гемодинамических подтипа: изолированную посткапиллярную ЛГ (ипк-ЛГ), характеризующуюся лёгочным сосудистым сопротивлением (ЛСС) ≤2 ед. Вуда, и комбинированную пост- и прекапиллярную ЛГ (кпк-ЛГ), при которой ЛСС превышает 2 ед. Вуда. Эти формы дифференцируются на основе гемодинамических показателей, прежде всего по величине сосудистого сопротивления. Комбинированный подтип (кпк-ЛГ) ассоциируется с более выраженной симптоматикой и неблагоприятным прогнозом по сравнению с изолированной формой (ипк-ЛГ) [5][6].
За последние десятилетия наблюдается устойчивый рост распространённости СНсФВ, особенно среди пожилых пациентов [7], а также у лиц с ожирением, артериальной гипертензией, сахарным диабетом 2 типа и хронической болезнью почек [8][9]. При этом ЛГ, развивающаяся на фоне СНсФВ (ЛГ-СНсФВ), остаётся недостаточно изученной. Отсутствие стандартизированных диагностических алгоритмов, противоречивые подходы к интерпретации результатов обследования, низкая чувствительность неинвазивных методов и фрагментарное понимание патофизиологических механизмов затрудняют своевременное выявление и точную стратификацию риска у этой категории пациентов. Тем не менее, с учётом высокой распространённости СНсФВ и негативного прогностического значения ЛГ, особенно её комбинированного подтипа, особую значимость приобретает ранняя диагностика и лечение.
Целью обзора является систематизировать современные данные и охарактеризовать клинические и патофизиологические особенности ЛГ у пациентов с СНсФВ.
Методология исследования
Методология научного поиска заключалась в анализе публикаций, посвящённых ЛГ у пациентов с ЛГ-СНсФВ. Были проанализированы результаты клинических и обсервационных исследований, обзоров и метаанализов, опубликованных за последние 10 лет. Поиск проводился в научных электронных базах данных и поисковых системах, включая Google Scholar, PubMed, elibrary.ru, КиберЛенинка, Embase и Web of Science. Для поиска использовались следующие ключевые слова на русском и английском языках: лёгочная гипертензия (pulmonary hypertension), сердечная недостаточность (СН) с сохранённой фракцией выброса (heart failure with preserved ejection fraction, HFpEF), дисфункция правого желудочка (ПЖ) (RV dysfunction) и прекапиллярная/посткапиллярная ЛГ (precapillary/postcapillary PH).
Результаты
Распространенность ЛГ-СНсФВ
Распространённость ЛГ-СНсФВ варьирует в зависимости от исследовательской методологии, используемых диагностических критериев и популяционных различий. Исторически сложилось так, что именно систолическая дисфункция левого желудочка (ЛЖ) и клапанные нарушения были в значительной степени связаны с возникновением ЛГ. Однако в последнее время СНсФВ все чаще признается в качестве ведущей причины. Согласно данным исследований, в которых диагноз ЛГ устанавливался с помощью КПОС, её распространённость среди пациентов с ХСН составляет от 33% до 68%, а в подгруппе больных СНсФВ этот показатель достигает 50-80% [1, 10]. В странах Азии, Африки и Австралии частота ЛГ составляет от 20% до 40%, а в Японии она достигает 42% среди пациентов с СНсФВ [11]. Несмотря на положительную тенденцию к улучшению выживаемости у пациентов с СНнФВ, аналогичного прогресса у больных с СНсФВ не наблюдается. По оценкам, смертность среди пациентов с ЛГ-СНсФВ составляет 23,6% в течение первого года и достигает 48,2% в течение 5 лет [7][12][13].
В Российской Федерации эпидемиологические данные по ЛГ, ассоциированной с СНсФВ, крайне ограничены. Однако известно, что за последние 20 лет распространённость ХСН в популяции увеличилась с 6,1% до 8,2%, что эквивалентно примерно 3,1 млн человек (по данным на 2019г) [8][9]. При этом доля СНсФВ составляет ~50% всех случаев СН и продолжает расти приблизительно на 1% ежегодно. Типичный профиль пациента с СНсФВ и ЛГ включает пожилой возраст, женский пол и наличие таких коморбидных состояний, как ожирение, артериальная гипертензия, сахарный диабет 2 типа и хроническая болезнь почек. Учитывая международные данные, свидетельствующие о наличии ЛГ у 36-83% пациентов с СНсФВ, можно предположить значительный рост числа ЛГ-СНсФВ и в российской популяции.
Патогенез ЛГ-СНсФВ и роль биомаркеров
Патофизиология ЛГ-СНсФВ является многофакторной и мультисистемной. Развитие ЛГ можно рассмотреть как непрерывный процесс, который начинается еще у бессимптомных пациентов с нормальным внутрисердечным давлением в состоянии покоя и появлении ЛГ при физических нагрузках, первоначально представляя собой ипк-ЛГ, которая может прогрессировать до тяжелой комбинированной кпк-ЛГ. кпк-ЛГ заключается в более обширном ремоделировании легочных сосудов, чем ипк-ЛГ, и может спровоцировать дисфункцию ПЖ (ДПЖ). Патогенез развития ЛГ-СНсФВ схематично изображен на рисунке 2.
Основной причиной ЛГ-СНсФВ является нарушение расслабления и наполнения ЛЖ, что приводит к передаче повышенного давления на левое предсердие (ЛП), усиленная насосная активность предсердий становится важным компенсаторным механизмом, обеспечивающим их опорожнение. Гемодинамический каскад развивается при истощении компенсаторных возможностей, что приводит к повышению давления в венозной, капиллярной и артериальной системах, прогрессирующему повышению давления в ЛП, увеличению постнагрузки ПЖ. Последующее развитие ДПЖ и правожелудочковой недостаточности приводит к бивентрикулярной декомпенсации, что делает клиническое состояние критическим [6].
При ипк-ЛГ среднее давление в легочной артерии повышается исключительно за счет пассивной передачи повышенного давления наполнения от левых отделов сердца в малый круг кровообращения. Длительное и постепенное увеличение давления приводит к истинному ремоделированию капилляров и мелких артерий, со временем поражаются средние и более крупные артерии (развивается кпк-ЛГ). Последние теории предполагают роль биомеханических воздействий на сосуды: длительное растяжение и напряжение стенки сосудов формирует биологические сигналы, что называют механотрансдукцией. Биологические сигналы управляют ремоделированием сосудов, включая гипертрофию, гиперплазию, апоптоз, синтез и деградацию внеклеточного матрикса. Ремоделирование заключается в снижении эластичности сосудов за счет изменения цитоскелета и увеличения толщины интимы, что было выявлено в тканях легочных вен человека, и это является ключевым гистологическим признаком ЛГ, ассоциированной с патологией левых отделов сердца [14]. В процесс вовлечен каскад гормональной и цитотоксической активации, поддержание хронического воспаления, повышение уровня эндотелина-1 (ЭТ-1) и снижение уровня оксида азота (II) (NO), расширяющего сосуды, приводят к ремоделированию ЛП, что знаменует переход к кпк-ЛГ, при этом регресс ремоделирования сомнителен [15].
Интересно, что характеристики кпк-ЛГ больше напоминают легочную артериальную гипертензию (ЛАГ), чем ипк-ЛГ, однако легочные венулы (в которых происходит сужение просвета с утолщением неоинтимы и гипертрофией медии) более активно участвуют в ремоделировании сосудов при кпк-ЛГ, чем при ЛАГ. В отличие от патологических изменений, которые происходят при ЛАГ, при ЛГ 2-й группы не наблюдается истинных плексиформных поражений.
Несмотря на адаптивную компенсаторную гипертрофию и повышенную сократительную способность ПЖ, в конечном итоге развивается его систолическая дисфункция из-за значимой постнагрузки. Последствия недостаточности ПЖ включают повышение центрального венозного давления и застой в системе кровообращения, которые приводят к множеству системных нарушений, повышающих заболеваемость и смертность [15].
Несмотря на прогресс в понимании патофизиологии заболевания, основные молекулярные механизмы остаются в значительной степени неизвестными. Поскольку СНсФВ и ЛГ признаны мультиорганными и системными заболеваниями, поиск значимых экстракардиопульмональных биомаркеров может помочь получить новое представление об этом заболевании, поиске новых возможностей по борьбе с ним.
Одними из самых широкодоступных и используемых биомаркеров являются натрийуретический пептид типа В (BNP) и N-концевой промозговой натрийуретический пептид (NT-proBNP). Их уровни обычно повышены при СН. Верхняя граница нормы для BNP составляет 35 пг/мл, а для NT-proBNP — 125 пг/мл [16]. При этом уровень натрийуретических пептидов может быть повышен у пожилых людей, при фибрилляции предсердий и почечной недостаточности без СН или быть непропорционально низким у пожилых людей, пациентов с ожирением. Повышенный уровень BNP коррелирует с уровнем систолического давления в легочной артерии у пациентов с ЛГ II группы. Однако это не позволяет отличить прекапиллярную ЛГ от посткапиллярной, поскольку натрийуретические пептиды могут быть повышены при обоих состояниях [8].
Повышенные уровни интерлейкина-1β в плазме крови, ЭТ-1, фактора роста эндотелия сосудов D, лептина и адипонектина, β2-микроглобулина, а также снижение уровня микроРНК-206 в сыворотке крови были связаны с выраженностью ЛГ при СНсФВ [9]. Однако их полезность для характеристики и определения методов лечения заболеваний, вызванных ЛГ-СНсФВ, остается неясной.
Несмотря на то, что снижение активности NO является давней парадигмой в патогенезе ЛГ-СНсФВ, клиническая значимость этого механизма требует дальнейшего изучения, недавние испытания препаратов, нацеленных на недостаточную передачу сигналов NO, не улучшили симптомы или исходы, что требует дальнейшего изучения [17].
ЭТ-1 является предиктором госпитализации, отдаленной смертности и более выраженным ремоделированием ЛА у пациентов с ЛГ-СНсФВ. У пациентов с ЛГ-СНсФВ отмечается снижение уровней вазодилатирующего простациклина (PGI2), усиление синтеза вазоконстрикторного тромбоксана A2, эти изменения особенно выражены на стадии перехода от ипк-ЛГ к кпк-ЛГ [18].
Среди наиболее значимых воспалительных медиаторов отмечается интерлейкин-6, который вместе с другими провоспалительными цитокинами формирует хронический низкоинтенсивный провоспалительный фон, характерный для пациентов с метаболическим синдромом, ожирением и диабетом 2 типа — основными коморбидностями при СНсФВ [19].
Дополнительным патогенетическим механизмом выступает нарушение липидного обмена, в частности, дисбаланс между противовоспалительными метаболитами омега-3 жирных кислот (например, марезин-1, резольвины) и провоспалительными производными арахидоновой кислоты [20].
Ведутся исследования по множеству других биомаркеров. Идентификация этих маркеров открывает перспективы для ранней диагностики, стратификации риска и разработки таргетной терапии, ориентированной на молекулярные механизмы заболевания. Однако важный нерешенный вопрос заключается в том, почему у части пациентов с СНсФВ развивается только ипк-ЛГ, а кпк-ЛГ или не развивается вообще [21].
Диагностический алгоритм для ЛГ-СНсФВ
Пациенты с ЛГ на фоне СНсФВ представляют особый интерес в плане диагностики, поскольку у них может формироваться прекапиллярный компонент с пограничными значениями давления заклинивания в легочной артерии (ДЗЛА), что создаёт гемодинамический перекрёст между ЛАГ (группа 1) и ЛГ, ассоциированной с заболеваниями левых отделов сердца (группа 2). Данные европейского регистра COMPERA свидетельствуют о существовании «атипичного» фенотипа таких пациентов, которые по клиническим и гемодинамическим характеристикам не укладываются строго в одну из двух категорий, что ставит под сомнение традиционную классификацию и подчёркивает необходимость более гибкого подхода к диагностике и лечению ЛГ в контексте СНсФВ [22]. Далее представлен диагностический алгоритм для ЛГ-СНсФВ с изменениями, который был предложен рабочей группой по неартериальной ЛГ на IV Всемирном симпозиуме по ЛГ (рис. 3).
Пациенты с симптомами СН и нормальной ФВ ЛЖ, у которых по данным эхокардиографии выявлена ЛГ, должны быть стратифицированы по вероятности наличия СНсФВ. У лиц пожилого возраста с характерным клиническим профилем (артериальная гипертензия, сахарный диабет 2 типа, ожирение, гипертрофия ЛЖ, увеличение ЛП, повышенные уровни натрийуретических пептидов и рентгенологические признаки венозного застоя) высока вероятность ЛГ-СНсФВ. У таких пациентов диагностического подтверждения, как правило, не требуется. В случае неясной клинической картины (средний возраст, нормальный уровень BNP, удовлетворительная физическая переносимость, отсутствие выраженной гипертензии и признаков СН), для уточнения гемодинамического фенотипа рекомендуется проведение КПОС. При этом ключевыми параметрами являются ДЗЛА и ЛСС: ДЗЛА ≥15 мм рт.ст. и ЛСС <2 ед. Вуда указывают на ипк-ЛГ; ДЗЛА повышение обоих параметров — на кпк-ЛГ. У больных с повышенным ДЗЛА и ЛСС ≥2 может применяться фармакологическая проба с нитроглицерином для оценки обратимости: снижение ДЗЛА при неизменном ЛСС подтверждает СНсФВ, тогда как снижение обоих показателей — наличие комбинированного варианта (ЛАГ и СНсФВ). Алгоритм также подчёркивает, что у пациентов молодого возраста без коморбидностей и с признаками типичной ЛАГ необходимо исключать другие причины ЛГ, включая наследственные и лекарственно-обусловленные формы. Таким образом, интеграция клинической оценки с КПОС позволяет более точно классифицировать подтипы ЛГ-СНсФВ и оптимизировать лечебную тактику.
Предполагаемые предикторы неблагоприятного прогноза при ЛГ-СНсФВ
- Наличие кпк-ЛГ
Хотя ипк-ЛГ является наиболее распространённой формой ЛГ у пациентов с СНсФВ, кпк-ЛГ считается более тяжёлым и прогностически неблагоприятным фенотипом. В исследовании Assad TR, et al. (2016) были проанализированы данные 2817 пациентов с ЛГ, из которых 13% имели кпк-ЛГ, 52% — ипк-ЛГ, а 20% — ЛАГ. Пациенты с кпк-ЛГ были в среднем моложе, но при этом у них отмечалось более выраженное поражение легочного сосудистого русла, сходное с таковым при ЛАГ. Генетический анализ выявил 75 общих экзонных однонуклеотидных полиморфизмов между кпк-ЛГ и ЛАГ, вовлечённых в регуляцию клеточной структуры, внеклеточного матрикса и иммунной функции; экспрессия этих генов в легких была на 32% выше, чем в других тканях. Несмотря на это, после поправки на сопутствующие факторы риск смерти у пациентов с кпк-ЛГ не отличался статистически значимо от пациентов с ипк-ЛГ (hazard ratio (HR) =1,14; 95% доверительный интервал: 0,96-1,35; p=0,15), если подтип ЛГ классифицировался по диастолическому градиенту давления — разности между диастолическим давлением в легочной артерии и давлением заклинивания легочных капилляров; значение >7 мм рт.ст. при этом ранее рассматривалось как критерий кпк-ЛГ. Авторы пришли к выводу, что кпк-ЛГ может быть отдельным, тяжёлым фенотипом ЛГ, обладающим молекулярным сходством с ЛАГ и потенциально отличающимся по патогенезу от ипк-ЛГ [24]. В исследовании Omote К, et al. (2022) проводился сравнительный анализ гемодинамических и клинических параметров между подтипами кпк-ЛГ и ипк-ЛГ у пациентов с СНсФВ. Было показано, что у пациентов с кпк-ЛГ выявляются выраженные признаки лёгочного сосудистого ремоделирования, воспаления и вазоконстрикции, сходные с изменениями, наблюдаемыми при идиопатической ЛГ. Кроме того, у этих пациентов была выявлена рассогласованность между насосной функцией ПЖ и сопротивлением в лёгочной артерии, что ведёт к ухудшению лёгочной перфузии и ограниченной доставке кислорода в условиях физической нагрузки. Также отмечалось значительное снижение аэробной адаптации, обусловленное ограниченной способностью сосудов к расширению, гипоксемией и снижением диффузионной способности лёгких. Авторы подчёркивают, что кпк-ЛГ при СНсФВ представляет собой самостоятельный патофизиологический фенотип, характеризующийся выраженным поражением легочного сосудистого русла и неблагоприятным прогнозом. Учитывая наличие выраженного лёгочного сосудистого ремоделирования, воспаления и вазоконстрикции у пациентов с кпк-ЛГ на фоне СНсФВ, авторы подчёркивают необходимость разработки терапевтических подходов, направленных на поражение сосудистого русла малого круга кровообращения, в дополнение к стандартному лечению СН [25].
- ДПЖ
У пациентов с ЛГ-СНсФВ ассоциировано с развитием ДПЖ и существенно ухудшает клинический прогноз. В исследовании Damy Т, et al. (2012), охватившем 1547 амбулаторных больных с ХСН, у значительной части пациентов с СНсФВ была выявлена сниженная систолическая функция ПЖ, определяемая по амплитуде систолического движения кольца трикуспидального клапана (tricuspid annular plane systolic excursion — TAPSE). TAPSE <15,9 мм, зафиксированный у 20% больных с СНсФВ, оказался значимо ассоциирован с увеличением риска смерти за 5 лет наблюдения на 34%, а в многофакторной модели сниженный TAPSE, наряду с увеличением индекса объёма правого предсердия и NT-proBNP, достоверно предсказывал неблагоприятные исходы [26].
Исследование Mohammed SF, et al. (2014) подтвердило эти данные в когорте из 562 пациентов с СНсФВ, продемонстрировав, что наличие ДПЖ, включая TAPSE <15 мм, коррелировало с более тяжёлой ЛГ, выраженной регургитацией на трикуспидальном клапане, увеличенными размерами ПЖ, снижением сердечного индекса и более высокой частотой госпитализаций. Пациенты с ДПЖ были подвержены повышенному риску общей (HR =1,35) и сердечно-сосудистой смерти (HR =1,85), а также частоты госпитализаций по поводу ХСН (HR =1,81). Особенно важным предиктором прогноза оказалось сочетание ДПЖ и систолического давления в легочной артерии >47 мм рт.ст. [27].
Работа Burke MA, et al. (2014) усилила фокус на ДПЖ у пациентов с ЛГ-СНсФВ. В когорте из 419 пациентов с СНсФВ выявлено, что ремоделирование ПЖ, выражающееся в утолщении его стенки, наблюдалось у 35% и ассоциировалось с ухудшением прогноза (HR =1,37; 95% доверительный интервал: 1,16-1,61; p<0,001), вне зависимости от ФВ ЛЖ. Наряду с этим, у 28% пациентов было отмечено снижение TAPSE, а у 15% — снижение фракции изменения площади ПЖ (ФИППЖ), что указывает на высокую распространённость систолической ДПЖ у больных СНсФВ с сопутствующей ЛГ. Именно толщина стенки ПЖ и её прогрессирующее увеличение в условиях хронической перегрузки давлением, характерной для ЛГ, оказались наиболее значимыми маркерами неблагоприятного течения СНсФВ [28].
Таким образом, у пациентов с СНсФВ наличие даже умеренной ЛГ усиливает отрицательное влияние на правожелудочковую функцию, усиливает взаимосвязь с систолической недостаточностью ПЖ, а также значительно повышает риск госпитализаций и смертности. Эти данные подчёркивают необходимость рутинной оценки давления в лёгочной артерии, структурного и функционального состояния ПЖ (включая TAPSE, ФИППЖ и толщину стенки) при стратификации риска у пациентов с СНсФВ и ЛГ.

Рис. 1. Классификация ЛГ, ассоциированной с заболеваниями левых отделов сердца.
Сокращения: КМП — кардиомиопатия, ЛГ — лёгочная гипертензия, СНнФВ — сердечная недостаточность с низкой фракцией выброса, СНсФВ — сердечная недостаточность с сохранённой фракцией выброса, СНунФВ — сердечная недостаточность с умеренно сниженной фракцией выброса.

Рис. 2. Патогенез ЛГ-СНсФВ.
Сокращения: ДЗЛА — давления заклинивания в легочной артерии, ипк-ЛГ — изолированная посткапиллярная лёгочная гипертензия, кпк-ЛГ — комбинированная лёгочная гипертензия, ЛЖ — левый желудочек, ЛСС — легочное сосудистое сопротивление, СНсФВ — сердечная недостаточность с сохраненной фракцией выброса, срДЛА — среднее давление в легочной артерии.

Рис. 3. Диагностический алгоритм для ЛГ-СНсФВ (с изменениями), адаптирован из [23].
Сокращения: АГ — артериальная гипертензия, ГЛЖ — гипертрофия левого желудочка, ДЗЛА — давление заклинивания в лёгочной артерии, ИБС — ишемическая болезнь сердца, КПОС — катетеризация правых отделов сердца, ЛАГ — лёгочная артериальная гипертензия, ЛГ — лёгочная гипертензия, ЛЖ — левый желудочек, ЛП — левое предсердие, ЛСС — лёгочное сосудистое сопротивление, СД — сахарный диабет, СН — сердечная недостаточность, СНсФВ — сердечная недостаточность с сохранённой фракцией выброса, ФВ — фракция выброса, ХСН — хроническая сердечная недостаточность, ЭхоКГ — эхокардиография, BNP — натрийуретический пептид типа В, Е/е’ — отношение максимальной скорости раннего диастолического наполнения левого желудочка (пик Е) к максимальной скорости движения фиброзного кольца митрального клапана в раннюю диастолу на уровне межжелудочковой перегородки (е’), см/с.
Заключение
ЛГ, развивающаяся на фоне СНсФВ, представляет собой гетерогенное клинико-гемодинамическое состояние с высокой распространённостью и неблагоприятным прогнозом. Наиболее тяжелым фенотипом считается комбинированная форма ЛГ, характеризующаяся выраженным ремоделированием сосудистого русла лёгких, воспалением и перегрузкой ПЖ давлением. Наличие ЛГ у пациентов с СНсФВ ассоциировано с увеличением смертности, частоты госпитализаций и снижением толерантности к физическим нагрузкам, особенно при наличии признаков правожелудочковой дисфункции. Прогностическую значимость имеют такие параметры, как TAPSE, ФИППЖ, систолическое давление в легочной артерии, уровень натрийуретических пептидов и показатели гемодинамики по данным КПОС. Современные алгоритмы диагностики подчеркивают важность комплексной оценки у пациентов с подозрением на ЛГ-СНсФВ.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Яфарова А.А., Филиппов К.Г., Джиоева О.Н., Драпкина О.М. Легочная гипертензия у пациентов с сердечной недостаточностью с сохраненной фракцией выброса (обзор литературы). Российский кардиологический журнал. 2025;30(2S):6457. https://doi.org/10.15829/1560-4071-2025-6457. EDN: FCITGY
Скопировать