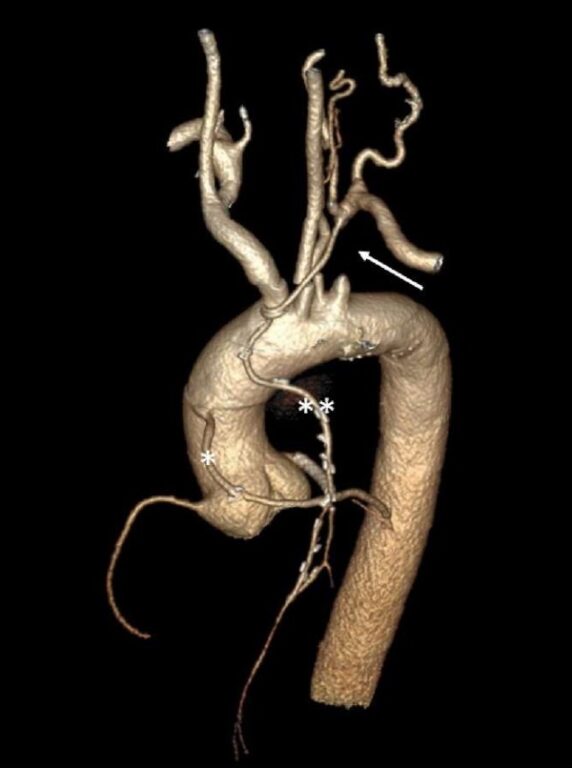
Кардиомиопатия такоцубо. Обзор данных литературы: клиническая картина, алгоритм диагностики, лечение, прогноз. Часть II
Аннотация
В обзоре представлены современные данные по проблеме кардиомиопатии такоцубо: информация о клинических проявлениях заболевания, алгоритме обследования и подходах к лечению, а также возможных осложнениях и прогнозе.
Кардиомиопатия такоцубо (КТ) представляет собой форму острой и, как правило, обратимой сердечной недостаточности, провоцируемой у большинства пациентов различными стрессовыми факторами, протекающей с транзиторной дисфункцией преимущественно левого желудочка (ЛЖ), клинически и электрокардиографически напоминающей острый коронарный синдром (ОКС).
Целью настоящего обзора является анализ современных исследований, касающихся клинического течения КТ и методов ее диагностики, а также о принципах лечения и профилактике заболевания, выполненных за последнее десятилетие.
Материал и методы
Мы провели систематический поиск в базе данных PubMed по следующим ключевым словам: «stress cardiomyopathy», «cardiomyopathy takotsubo», «broken heart syndrome», «apical ballooning syndrome», «takotsubo syndrome», «transient apical ballooning syndrome» за период с 1 января 2010г по 1 января 2022г. По результатам поиска было проанализировано 170 источников литературы: согласительные документы, метаанализы, обзоры литературы, статьи, клинические случаи.
В первой части обзора по данной проблеме в основном обсуждались критерии диагностики и патогенетические механизмы КТ. Во второй части будет представлена информация о клинических проявлениях заболевания, алгоритме обследования и подходах к лечению.
Клиническая картина
Клинические проявления КТ напоминают картину ОКС или острой левожелудочковой недостаточности. По данным регистров самыми частыми симптомами заболевания являются: боль в грудной клетке (67,9-75,9%) и одышка (46,9-51,8%) [1-3]. Реже встречаются такие симптомы, как сердцебиение (11-12%), обморок (7,7-8,9%), тошнота/рвота (14-49,5%) [1][4]. Некоторые авторы описывают дебют заболевания в виде остановки кровообращения на фоне жизнеугрожающих нарушений ритма [3]. У многих больных имеются симптомы тревоги, могут наблюдаться неврологические и психические нарушения [3][5]. При вторичной КТ в клинической картине присутствуют симптомы основного заболевания, спровоцировавшего развитие КТ [5].
Методы диагностики при КТ
Электрокардиография (ЭКГ)
ЭКГ в остром периоде заболевания изменена у большинства больных. Наиболее часто регистрируются инверсия зубца T (у 41-91% пациентов), удлинение интервала QT (38-97%), подъем сегмента ST (встречается у 35-56%), депрессия сегмента ST (наблюдается у 8-19,1%) [4-6]; реже выявляется блокада левой ножки пучка Гиса (0-5% больных) [5][7][8], патологический зубец Q (15-22%) [2][6][7].
Следует отметить, что у 14% больных с КТ не находят изменений ЭКГ, объяснения этому факту пока не найдено [9].
Подъем сегмента ST, причем амплитуда элевации обычно меньше, чем при инфаркте миокарда (ИМ) с подъемом сегмента ST (ИМпST) [10], преимущественно выявляется в прекардиальных отведениях V2-V5 и отведениях от конечностей II и aVR, тогда как при переднем ИМпST подъем сегмента ST обнаруживается чаще в прекардиальных отведениях V1-V4 и отведениях от конечностей I и aVL; повышение сегмента ST только в отведениях II, III, aVF считается не характерным для КТ [11]. В последние годы было предложено несколько ЭКГ критериев, которые с высокой чувствительностью и специфичностью позволяют отличить КТ от переднего ИМпST [11]. Так, подъем сегмента ST в отведении aVR при отсутствии его подъема в отведении V1 позволял дифференцировать КТ от ИМпST с чувствительностью 73%, специфичностью 84% [12]. Стойкая элевация сегмента ST через 72 часа после поступления обнаруживается у 19% пациентов и прогнозирует риск развития внутрибольничных осложнений [3][5][13].
Инверсия зубца Т в основном встречается в прекардиальных отведениях, нарастает в течение нескольких дней с последующим постепенным разрешением в сроки от нескольких дней до недель [8][11]. Зубцы T, как правило, более глубокие и распространенные по сравнению с пациентами с ИМ [5][14]. У больных с поздним обращением эти признаки могут быть единственными обнаруживаемыми изменениями ЭКГ и, следовательно, важными для диагностики. Считается, что инверсия зубца T связана с наличием отека миокарда и может сохраняться в течение нескольких месяцев даже после восстановления сократительной способности ЛЖ, оставляя «электрофизиологический след» перенесенной КТ [11][15].
Удлинение интервала QT — частый признак КТ [5][11], менее характерный для больных ИМ, может сохраняться от нескольких дней до недель. Патологические зубцы Q при КТ встречаются реже, чем при переднем ИМпST (15% vs 69%) [11]. При КТ, как и при переднем ИМпST, зубцы Q могут возникать в острой фазе, но быстро регрессировать с восстановлением зубца R, что соответствует «электрическому оглушению» [7][11].
Биомаркеры
По сравнению с ИМпST пациенты с КТ обычно имеют более низкие пиковые значения тропонинов Т/I и уровни креатинфосфокиназы-MB из-за отсутствия некроза миокарда [1][5]. Кроме того, для КТ характерно несоответствие между степенью повышения биомаркера и выраженностью дисфункции миокарда [5][16]. Высокий уровень тропонина при поступлении является предиктором худшего исхода в стационаре [11]. Следует отметить, что при КТ, развивающемся на фоне новой коронавирусной инфекции (COVID-19), отмечены более высокие значения тропонина, чем у больных, не переносящих эту инфекцию [17][18].
Вместе с тем КТ часто связана со значительным увеличением в плазме уровней натрийуретического пептида B-типа (BNP) и N-концевой фрагмент проBNP, достигая пика примерно через 24-48 ч после появления симптомов [11]. Предполагается, что высокие уровни этих гормонов могут быть вызваны главным образом интенсивным отеком миокарда, а не растяжением камер сердца [19].
Показано, что на основании возраста, пола, наличия психических расстройств в анамнезе, данных фракции выброса (ФВ) ЛЖ и соотношения уровней BNP/тропонин I при поступлении можно дифференцировать КТ и ИМпST с чувствительностью 92% и специфичностью 77% [5][20].
Помимо приведенных биомаркеров, в последнее время предложено несколько новых показателей для дифференциальной диагностики КТ и ИМпST [5][21]. Например, копептин (С-концевой провазопрессин), который сам по себе не помогает отличить КТ от ИМпST [5], однако соотношение копептин/N-концевой фрагмент проBNP позволяет различать КТ и ИМпST [5][22].
Как уже говорилось выше, у пациентов с КТ при поступлении повышены уровни интерлейкина (IL)6 в плазме, но они ниже в сравнении с пациентами с ИМпST, тогда как уровни IL-7 повышены более существенно [5]. Уровни IL-6, IL-2, IL-4 и IL-10 были достоверно выше во время острой фазы КТ, чем при ИМпST [5][23].
Коронарная ангиография и вентрикулография
Несмотря на то, что коронароангиография (КАГ) не подтверждает диагноз КТ, она имеет важное диагностическое значение для обнаружения тромбоза коронарных артерий и ОКС [5][24]. Как ранее указывалось, в настоящее время ишемическая болезнь сердца (ИБС) и атеросклеротическое поражение коронарных артерий не исключают КТ, тем более что возраст пациентов с данным заболеванием является фактором риска ИБС. 23% из 1016 пациентов с КТ имели сопутствующую обструктивную ИБС, а 41% — необструктивную форму ИБС [5][25]. Важно помнить, что зона нарушения сократимости миокарда при КТ в отличие от ИМ всегда выходит за рамки бассейна одной коронарной артерии [11].
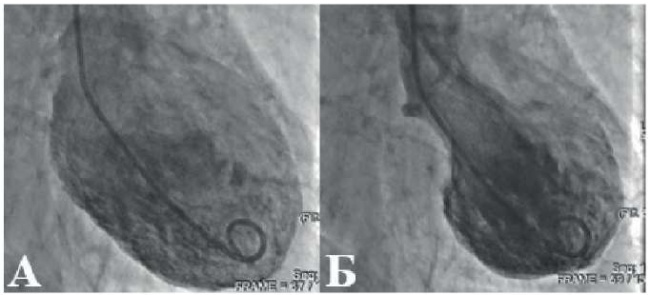
Иногда для проведения дифференциального диагноза КТ и ИМ без обструкции коронарных артерий (ИМБОКА) требуются методы внутрисосудистой визуализации, такие как внутрисосудистое ультразвуковое исследование и оптическая когерентная томография, с помощью которых можно обнаружить такие причины ИМ, как разрыв или эрозия небольшой атеросклеротической бляшки, а также — спонтанную диссекцию коронарной артерии [5, 26, 27]. Надежным методом диагностики при КТ является вентрикулография, визуализирующая нарушение сократимости миокарда с типичной для КТ картиной (рис. 1, 2). Примерно 33% пациентов с характерным апикальным баллонированием имеют феномен «апикального соска» — небольшой участок с сохраненной сократимостью на верхушке ЛЖ, что позволяет отличить КТ от переднего ИМпST, при котором этот признак не определяется [5][28]. Вентрикулография может выявить обструкцию выходного тракта (ВТ) ЛЖ, встречающуюся примерно у 20% пациентов с КТ. Поэтому при проведении вентрикулографии рекомендуется гемодинамическая оценка градиента давления в ВТ ЛЖ, а также оценка конечного диастолического давления в ЛЖ [11].

Рис. 1. Вентрикулография у пациента с типичной (апикальной) формой КТ. A — ЛЖ в диастоле; Б — ЛЖ в систоле. Собственные данные.

Рис. 2. Вентрикулография у пациента со среднежелудочковой формой КТ: A — ЛЖ в диастоле; Б — ЛЖ в систоле. Определяются два локальных участка гипокинезии передней и нижней стенок ЛЖ. Собственные данные.
Компьютерная томографическая ангиография (КТА)
У пациентов, которым не может быть выполнена КАГ, неинвазивная КТА является подходящей альтернативой, особенно у стабильных пациентов с низкой вероятностью ОКС, при подозрении на рецидив КТ, а также в тех случаях, когда пациент поступил в подострую фазу заболевания. КТА предоставляет информацию как об анатомии коронарной артерии, так и о региональном сокращении ЛЖ [11].
Эхокардиография (ЭхоКГ)
ЭхоКГ — наиболее часто используемый метод диагностики при выявлении КТ [5][11]. С помощью ЭхоКГ можно идентифицировать различные варианты нарушения сократимости ЛЖ при КТ, которые были указаны в 1 части обзора (рис. 3). Во время рецидива заболевания, как указывалось, паттерн нарушений сократимости ЛЖ может меняться [11].

Рис. 3. ЭхоКГ у пациента с типичной (апикальной) формой КТ (четырехкамерный вид): A — диастола ЛЖ; Б — систола ЛЖ. Собственные данные.
Дополнительным способом для дифференциальной диагностики КТ и ИМ может быть оценка индекса сферичности ЛЖ. Это простой, быстрый и воспроизводимый показатель для оценки геометрических изменений, который потенциально может использоваться в качестве еще одного количественного параметра в дополнение к стандартным диагностическим критериям [29].
Обычно сократимость ЛЖ по данным рутинного ЭхоКГ полностью восстанавливается через 4-8 нед. [11], в то время как нарушения глобальной продольной и циркулярной деформации, выявленные при помощи speckle tracking ЭхоКГ, как сообщается, сохраняются в течение нескольких месяцев после острой фазы КТ [5][30][31]. Таким образом, оценка ФВ ЛЖ как единственного маркера функционального улучшения сократимости не является оптимальной, т.к. имеется более чувствительный метод, способствующий более детальной оценке восстановления сократимости ЛЖ — speckle tracking ЭхоКГ [32]. Остаточные нарушения сократимости могут быть обусловлены изменением ориентации волокон на фоне ремоделирования миокарда при КТ, однако вопрос о ценности этого диагностического метода требует дальнейшего изучения на больших выборках пациентов.
Магнитно-резонансная томография сердца (МРТ)
Как уже упоминалось, бывает довольно трудно дифференцировать КТ с ИМБОКА, а также с миокардитом, протекающим под маской ИМ. В таких случаях на помощь приходит МРТ с контрастированием гадолинием. По мнению европейских и американских экспертов, этот метод при КТ является «золотым стандартом» [11][33-35]. Он позволяет выполнить качественную и количественную оценку сократимости ЛЖ и правого желудочка, их объемов, оценить наличие перикардиального и плеврального выпота, тромбов и, что особенно важно, выявить признаки повреждения миокарда, характерные для ИМ, миокардита, КТ и других кардиомиопатий [5][11].
Недавно были установлены конкретные МРТ-критерии для диагноза КТ во время острой фазы заболевания, которые включают комбинацию типичных нарушений сократимости стенки ЛЖ, отек и отсутствие ишемического и поствоспалительного некроза миокарда по результатам оценки позднего накопления гадолиния [5][11]. У большинства пациентов с КТ присутствует отек миокарда в областях с аномальной систолической функцией, связанный в первую очередь с процессами воспаления, возможно — транзиторной ишемии миокарда [5][11].
Новым инструментом для количественного анализа региональной деформации ЛЖ считается методика speckle tracking МРТ, позволяющая количественно оценить деформацию всех камер сердца [5][36]. Имеется информация, что нарушение глобальной продольной деформации по данным МРТ может служить прогностическим фактором, определяющим исход при КТ [5][37]. Более того, нарушение вращательной механики и периферическая диссинхрония были идентифицированы как характерные особенности МРТ при КТ [5][37].
МРТ следует использовать в острой фазе КТ, когда затруднительно получить оптимальные ЭхоКГ изображения или когда подозревается другой диагноз, например миокардит или ИМ, требующий иной терапевтической стратегии [5][24]. В последующем в течение 2 мес. также рекомендовано выполнять МРТ сердца для подтверждения диагноза КТ [5][11][24][34][38].
Другие методы исследования
Определенную диагностическую ценность, по данным литературы, при КТ имеют позитронная эмиссионная томография миокарда и перфузионная сцинтиграфия миокарда. Однако имеющиеся данные по результатам сцинтиграфии носят противоречивый характер. Исследования с помощью позитронной томографии сердца — немногочисленны [11].
Диагностический алгоритм при КТ
Дифференциальная диагностика КТ и ОКС часто затруднена из-за сходства клинической картины, изменений ЭКГ, реакции сердечных биомаркеров [5][11]. Основными диагностическими инструментами в таком случае выступают ЭхоКГ, КАГ и вентрикулография, а также — МРТ [11]. В 2018г комитетом экспертов Европейского общества кардиологов был предложен диагностический алгоритм у пациентов с болями в грудной клетке для исключения КТ (рис. 4).

Рис. 4. Диагностический алгоритм для подтверждения/исключения КТ (адаптировано из [11]).
Сокращения: ВОЛЖ — выходной отдел левого желудочка, ИБС — ишемическая болезнь сердца, КТ — кардиомиопатия такоцубо, ЛЖ — левый желудочек, МРТ — магнитно-резонансная томография, МСКТ — мультиспиральная компьютерная томография, ОКС — острый коронарный синдром, ПЖ — правый желудочек, ПНА — передняя нисходящая артерия, СОЭ — скорость оседания эритроцитов, СРБ — С-реактивный белок, ЭКГ — электрокардиография, ЭхоКГ — эхокардиография.
При этом, если у больного отсутствует элевация сегмента ST, предлагается использовать шкалу стратификации риска КТ InterTAK (табл. 1). Согласно полученным баллам, по данной шкале определяется степень вероятности КТ.
Таблица 1
Шкала стратификации риска КТ InterTAK

Примечание: адаптировано из [11].
Сокращение: ЭКГ — электрокардиография.
Пациенты с итоговым значением в 30 баллов имеют прогнозируемую вероятность развития КТ <1%, лица с 50 баллами — 18%, а пациенты, у которых >70 баллов — >90%.
Лечение
В настоящее время нет рандомизированных клинических исследований, касающихся лечения пациентов с КТ, поэтому все рекомендации по ведению больных с данной патологией имеют класс доказательности «С» и основаны на клиническом опыте врачей и мнении экспертов [11].
Тактика ведения больного зависит от конкретной клинической ситуации и стратификации риска развития осложнений. Так, согласно шкале GEIST, разработанной по результатам международного многоцентрового регистра (учитывается пол, ФВ ЛЖ, наличие в анамнезе неврологических нарушений, поражение правого желудочка), в зависимости от набранных баллов пациентов с КТ подразделяют на пациентов с низким, средним и высоким риском внутрибольничных осложнений (табл. 2) [39].
Таблица 2
Шкала риска внутрибольничных осложнений GEIST у больных с КТ

Примечания: * — значения от 0,15 до 0,7; адаптировано из [39].
Сокращения: ЛЖ — левый желудочек, ФВ — фракция выброса.
На догоспитальном этапе и начальном стационарном этапе, пока диагноз ОКС не исключен, пациенты, как правило, получают такую же терапию, как при ОКС, включая антиагреганты и антикоагулянты в рекомендованных дозировках, статины, ингибиторы ангиотензинпревращающего фермента (иАПФ)/ блокаторы рецепторов ангиотензина II (БРА) с целью восстановления функции ЛЖ, диуретики, нитраты и антиаритмические средства при наличии показаний. При подозрении на КТ в случае необходимости инотропной поддержки следует предпочесть использование левосимендана и механическую поддержку кровообращения и дыхания [11][40].
Окончательно не решен вопрос об эффективности бета-адреноблокаторов (ББ) при КТ. Несмотря на то, что ББ логично рассматривать как патогенетическую терапию при данном заболевании, фактически не было получено данных, подтверждающих их пользу как в острой фазе заболевания, так и в долгосрочной перспективе [40][41]. Причины этого факта остаются непонятными.
Осложнения КТ в острый период и их лечение
Кардиогенный шок (КШ) при КТ по данным литературы развивается в 6-20% случаев [39][40][42]. Лечение КШ при КТ является сложной задачей, потому что обычные подходы, а именно — рутинное использование вазопрессоров и инотропных средств, могут быть потенциально опасными [11][40]. У пациентов с КТ, получающих катехоламины внутривенно, по данным литературы, нередко наблюдаются серьезные нарушения кровообращения и сердечной функции, более неблагоприятные исходы в стационаре и более высокие показатели долгосрочной смертности по сравнению с пациентами, не получающими такой фармакологической поддержки [40][43]. В качестве альтернативы классическим инотропам предлагается использовать левосимендан — некатехоламинергический инотропный препарат, однако его следует использовать у пациентов с нарушенной систолической функцией при систолическом артериальном давлении ?90 мм рт.ст. и при отсутствии обструкцию ВТ ЛЖ, которая встречается при КТ. При обструкции ВТ ЛЖ и артериальном давлении >90 мм рт.ст. следует рассмотреть вопрос о назначении ?1-селективных ББ с коротким периодом полувыведения (рис. 5) [40][44].

Рис. 5. Подходы к лечению острых осложнений при КТ (адаптировано из [40]).
Сокращения: АВ — атриовентрикулярный, ВЭКС — временная электрокардиостимуляция, НИВЛ — неинвазивная вентиляция легких, ОВТЛЖ — обструкция выходного тракта левого желудочка, ОКС — острый коронарный синдром, ОСН — острая сердечная недостаточность, САД — систолическое артериальное давление, ФВ — фракция выброса, ЭКС — электрокардиостимуляция.
Механическая поддержка кровообращения (экстракорпоральная мембранная оксигенация и внутриаортальная баллонная контрпульсация) также используется у пациентов с КТ и КШ.
Аритмии возникают в острой фазе КТ у 8,1-10% пациентов [40][45][46]. Фибрилляция предсердий возникает в 4,7% случаев, дисфункция синусового узла — в 1,3%, а атриовентрикулярная блокада — в 2,9%, что, скорее всего, связано с нейро-вегетативным дисбалансом, катехоламиновым стрессом [11]. Данные регистра GEIST показывают, что наиболее частыми нарушениями ритма являются желудочковые аритмии и полная атриовентрикулярная блокада [40][47]. Неотложное лечение желудочковой тахикардии включает фармакологический подход с применением сульфата магния и/или ?1-блокатора короткого действия, а также — электроимпульсную терапию. Следует отметить, что из-за высокой распространенности удлиненного интервала QT у пациентов с КТ во время острой фазы [6][40], необходимость использования амиодарона или соталола оценивается в каждом конкретном случае индивидуально. При наличии желудочковой тахикардии torsade de pointes, связанной с удлинением интервала QT, также применяют сульфат магния, ?1-блокатор короткого действия и электроимпульсную терапию. Стойкая атриовентрикулярная блокада высокой степени требует имплантации кардиостимулятора (рис. 5) [40][48].
Среди больных с КТ часто встречается аритмогенная внезапная остановка кровообращения, поэтому Американская кардиологическая ассоциация включила КТ в число потенциальных показаний для носимых кардиовертер-дефибрилляторов [45]. Следует отметить, что остановка кровообращения чаще встречалась у пациентов с КТ при физическом, а не эмоциональном триггере, развивается, как правило, при поступлении, но может возникнуть в течение всей острой фазы [45].
Кардиоэмболические осложнения при КТ возникают у 0,8-4% пациентов и связаны с образованием тромба в полости ЛЖ [11][40][49]. Период повышенного риска тромбообразования в ЛЖ составляет ~2 нед. после начала заболевания. Пациентам с признаками наличия тромбов в ЛЖ во время госпитализации, по мнению экспертов, следует назначать пероральные антикоагулянты на срок до 3-х мес. до полного разрешения тромбоза [40][49][50]. Вопрос о том, какие препараты являются эффективными в этих случаях не изучен. Назначаются как антагонисты витамина К, так и прямые пероральные антикоагулянты [49].
Ряд исследователей предлагают назначать антикоагулянты больным с КТ профилактически на срок до 3 мес. при следующих условиях: типичный (апикальный) вариант КТ, ФВ ЛЖ ?30%, имеется другое сердечно-сосудистое заболевание в анамнезе, повышен уровень С-реактивного белка, уровень тропонина-I >10 нг/мл и количество лейкоцитов при поступлении >10?103 клеток/мкл [40][49][51]. Считается, что при апикальном баллонировании без признаков внутрисердечного тромбоза и повышенного уровня тропонина при поступлении показания для профилактического назначения антикоагулянтов отсутствуют [40][49]. Пациенты со средне-желудочковым или базальным типами КТ и нормальным уровнем тропонина также не нуждаются в профилактическом приеме антикоагулянтов [40][49][50].
Лечение КТ после выписки
Подходом первой линии является «управление» стрессовыми ситуациями и сопутствующими заболеваниями, которые могут спровоцировать рецидив заболевания [11][40][52].
Что касается иАПФ/БРА, ББ, то в настоящее время данные по эффективности этих препаратов в отдаленном периоде заболевания у больных с КТ довольно противоречивы [40][53]. В одном из крупнейших регистров пациентов с КТ продемонстрировали, что использование иАПФ/БРА связано с улучшением выживаемости через 1 год, однако не было получено никаких доказательств улучшения выживаемости при использовании ББ [1]. Также, согласно метаанализу, в который было включено 1664 пациента с КТ (средний период наблюдения 24,5 мес.), применение иАПФ/БРА, в отличии от ББ, снижало риск рецидива в отдаленном периоде [54]. В свою очередь, лечение ББ было связано с более низким риском рецидива или смерти, в то время как значимой связи улучшения прогноза с использованием иАПФ/БРА не наблюдалось [55]. Однако результаты наблюдательного регистра (RETAKO) показали, что пациенты, перенесшие КШ и выписанные с назначением ББ, имели более низкую годовую смертность от всех причин по сравнению с теми, кто не получал ББ [40][42].
Статины и ацетилсалициловая кислота (АСК) показаны при наличии у пациента атеросклероза коронарных артерий [11]. Вместе с тем недавние исследования на большой популяции пациентов с КТ показали, что АСК и статины не влияют на краткосрочный или долгосрочный прогноз (до 5 лет) при КТ [41][56][57]. Частота тяжелых сердечно-сосудистых событий среди пациентов, получавших АСК, существенно не отличалась по сравнению с пациентами, не леченными АСК [40][57], но кровотечения встречались достоверно чаще [56].
В настоящее время также нет убедительных доказательств об эффективности какой-то терапии в отношении предупреждения рецидивов заболевания [40][41].
Таким образом, для оценки эффективности медикаментозного лечения при КТ необходимы рандомизированные клинические исследования.
Прогноз при КТ
Хотя КТ чаще описывается как доброкачественное заболевание, жизнеугрожающие осложнения в острый период были описаны у 20,4-45% пациентов, включая, как указывалось, такие как отек легких, КШ, фибрилляция желудочков [1][4][39][40][42]. КШ во время госпитализации является одним из наиболее сильных предикторов краткосрочного и долгосрочного исхода. У пациентов с КШ в 5 раз выше риск смерти от всех причин в отдаленном периоде [42]. Клинические факторы, в значительной степени связанные с КШ, включали мужской пол, более низкую ФВ ЛЖ при обращении, более длинные интервалы QTc, наличие градиента ВТ ЛЖ и физический триггер [40][42].
Уровень госпитальной летальности по данным литературы колеблется от 1 до 8,7% [11][39][40] и по некоторым результатам был сопоставим с летальностью среди пациентов с ИМпST [58]. Отдаленная летальность пациентов, перенесших КТ, как следует из литературы, составляет ~5,6% пациентов в год, а частота основных сердечно-сосудистых событий — 9,9% [11]. Среди пациентов, включенных в регистр InterTak, в течение первых 30 дней после поступления частота серьезных сердечных и цереброваскулярных событий составила 7,1%, включая смерть, инсульт [1][40]. Внезапная сердечная смерть развивается примерно у 2% и нередко связана с рецидивом КТ [46].
Рецидив КТ встречается, по одним данным, у 11,4% пациентов в течение 4 лет после первого обращения [58], по другим, в 4,7-5% при наблюдении на протяжении 10 лет [40][59]. Большинство рецидивов было зарегистрировано в первые 5 лет после эпизода индексной КТ [40]. В целом у пациентов с КТ отдаленные результаты сопоставимы с пациентами, перенесшими ОКС, соответствующего возраста и пола [60].
Одним из основных предикторов долгосрочного прогноза является характер запускающего стрессорного механизма. При КТ, вызванной физическими триггерами, наблюдается более высокая смертность в краткосрочной и долгосрочной перспективе, чем при КТ, вызванной эмоциональным стрессом [61].
Заключение
КТ становится все более актуальной проблемой не только в кардиологии, но и при другой патологии внутренних органов. Статистика о распространенности КТ растет параллельно с повышением осведомленности врачей о данном заболевании. В настоящее время продолжается изучение патогенетических механизмов заболевания, подходов к его профилактике и лечению.
На наш взгляд, представляется важным создание национального регистра КТ, который поможет ответить на ряд нерешенных при этой патологии вопросов.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Болдуева С.А., Евдокимов Д.С. Кардиомиопатия такоцубо. Обзор данных литературы: клиническая картина, алгоритм диагностики, лечение, прогноз. Часть II. Российский кардиологический журнал. 2022;27(3S):4994. https://doi.org/10.15829/1560-4071-2022-4994
Скопировать