Эпидемиология, факторы риска развития и принципы диагностики хронической тромбоэмболической легочной гипертензии: данные регистра
Аннотация
Цель. Провести анализ эпидемиологии, факторов риска и исходных клинических данных пациентов, включенных в регистр пациентов с хронической тромбоэмболической легочной гипертензией (ХТЭЛГ).
Материал и методы. В проспективное наблюдательное одноцентровое исследование включено 286 пациентов (женщины 51% (n=148)) с впервые установленным диагнозом ХТЭЛГ и пролеченных в ФГБУ «НМИЦ им. В. А. Алмазова» в период с 01.01.2014 по 31.12.2023. Диагноз ХТЭЛГ верифицировали согласно критериям Европейского общества кардиологов от 2015г и клиническим рекомендациям Минздрава России. С целью оценки эффективности работы мультидисциплинарной «команды ХТЭЛГ» больные были разделены на две подгруппы в зависимости от времени верификации диагноза ХТЭЛГ: группа 1 (n=147) включала пациентов, обследованных и пролеченных в период с 01.01.2014 по 31.12.2018; группа 2 (n=139) — в период с 01.01.2019 по 31.12.2023.
Результаты. Средний возраст пациентов на момент постановки диагноза был 56 [43; 66] лет, большинство имели продвинутую стадию заболевания (III функциональный класс (ФК), n=176, 62%), а время от дебюта симптомов до постановки диагноза составило 2,6 [1,4; 4,6] года. 40,7% пациентов были жителями Санкт-Петербурга, распространенность заболевания в Санкт-Петербурге на конец 2023г составила 21,1 случая на 1 млн. человек. Отмечен рост заболеваемости ХТЭЛГ в Санкт-Петербурге с 1,56 до 2,86 случая на 1 млн. населения. Верифицированный эпизод тромбоэмболии легочной артерии в анамнезе зафиксирован в 71% (n=204) пациентов, в половине случаев он носил массивный характер. Анализ факторов риска ХТЭЛГ продемонстрировал высокую распространенность антифосфолипидного синдрома (11%) и спленэктомии (5%), а также выявил такие вероятные факторы риска, как крупная артериовенозная мальформация и крупная миома матки. При сравнении клинико-лабораторных характеристик двух групп в зависимости от периода включения, пациенты группы 1 отличались наличием более выраженного ремоделирования и дисфункции правых камер сердца по данным эхокардиографии (площадь правого предсердия, соотношение правого желудочка к левому желудочку, диаметр легочной артерии, ударный объем левого желудочка), и в группе 2 более высокими значениями N-концевого промозгового натрийуретического пептида (1512,0 [511,5; 2702,0] vs 816,5 [197,0; 2235,5], р=0,004). При этом отличий по показателям гемодинамики малого круга кровообращения и срокам верификации диагноза получено не было. При этом в группе 2 чаще выявлялись пациенты ХТЭЛГ ФК I (9% vs 1%, р=0,041). Отличий по числу пациентов с эмпирически назначенной специфической терапией легочной артериальной гипертензии не установлено.
Заключение. Продемонстрирована низкая заболеваемость ХТЭЛГ, а также длительные сроки постановки диагноза, ассоциированные с более выраженными изменениями гемодинамики малого круга кровообращения при сравнении с зарубежными регистрами. Обозначена позитивная тенденция в виде увеличения среди вновь выявленных больных пациентов с более низким ФК и менее выраженным ремоделированием правых камер сердца, что, вероятно, является следствием совершенствования системы маршрутизации пациентов с синдромом легочной гипертензии.
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) представляет собой редкий вариант прекапиллярной легочной гипертензии (ЛГ), характеризующейся стойкой посттромбоэмболической обструкцией ветвей легочных артерий (ЛА) в сочетании с вторичными изменениями микроциркуляторного русла, что приводит к прогрессирующему повышению легочного сосудистого сопротивления (ЛСС) и в итоге к развитию правожелудочковой сердечной недостаточности [1, 2]. ХТЭЛГ является одним из немногих вариантов ЛГ с потенциально возможной нормализацией гемодинамики малого круга кровообращения на фоне хирургического или эндоваскулярного лечения и полным обратным ремоделированием правых камер сердца, а также восстановлением исходного функционального статуса пациентов. Именно поэтому актуальной задачей остается раннее выявление ХТЭЛГ, которая имеет неспецифические клинические проявления, дебютирующие только на фоне продвинутых стадий заболевания.
Эпидемиологические данные о ХТЭЛГ остаются ограниченными, что во многом связано с недостаточной выявляемостью заболевания. По данным регистров США, Европы и Канады, общая заболеваемость ХТЭЛГ варьирует от 0,9 до 39,0 случаев на 1 млн. взрослого населения в зависимости от периода наблюдения, снижаясь до 3,1-6,0 на 1 млн. общей популяции населения в национальных регистровых исследованиях [3-5]. Распространенность ХТЭЛГ также значительно варьирует от 5 до 30 случаев на 1 млн. населения, что, вероятно, зависит от организации маршрутизации и наблюдения за пациентами с тромбоэмболией ЛА (ТЭЛА) и ХТЭЛГ, а также связано с особенностями (этническая принадлежность), численностью анализируемой выборки и способом расчета. Так, в Китае распространенность ХТЭЛГ составляет ~85 случаев на 1 млн. госпитализированных пациентов и снижается до 6,74 случаев на 1 млн. взрослого населения [6]. Распространённость ХТЭЛГ в Испании и Швеции схожа и составляет ~22,5 случаев на 1 млн. населения, характеризуя в целом регистры ХТЭЛГ экономически развитых Европейских стран [7], снижаясь до 16,5 случаев на 1 млн. населения в Латвии [8]. В Российской Федерации (РФ) данные о распространенности ХТЭЛГ отсутствуют и ограничены результатами регистра, включающего отдельные центры/отдельные регионы нашей страны, на основании которых нельзя полноценно судить о распространенности ХТЭЛГ в России [9]. При этом последний международный регистр пациентов с ХТЭЛГ, включивший 1009 пациентов и характеризующий клиническую практику США, Европы (включая Россию) и Японии, приводит ту же усредненную цифру по распространенности — от 3 до 30 случаев на 1 млн. человек [10].
Возможное решение проблемы ранней диагностики ХТЭЛГ лежит в организации системы наблюдения за пациентами после эпизода острой ТЭЛА. Частота развития ХТЭЛГ после верифицированного тромбоза ЛА значительно варьирует в различных исследованиях от 0,57% до 9,1%. Так, по данным крупного проспективного наблюдательного исследования FOCUS, включившего 1098 пациентов, перенесших ТЭЛА, частота формирования посттромбоэмболического синдрома достигала 16%, при этом ХТЭЛГ подтверждена только в 2,3% случаев [11]. По данным японского многоцентрового наблюдательного исследования COMMAND VTE Registry-2, включившего 2787 пациентов с острой ТЭЛА, кумулятивная частота трансформации в ХТЭЛГ за период трехлетнего наблюдения также составила 2,3% [12]. По результатам работы Klok FA, et al., проанализировавших данные 772 пациентов, перенесших ТЭЛА, с длитель- ностью наблюдения 1,5 года, процент развития ХТЭЛГ составил 2,8%, при этом среди пациентов с ТЭЛА низкого риска тридцатидневной летальности частота трансформации в ХТЭЛГ составила всего 0,38% (95% доверительный интервал (ДИ): 0-1,5%), а у пациентов с ТЭЛА высокого риска — 10% (95% ДИ: 6,5-15%) [13]. Эти существенные отличия подчеркивают важность правильной стратификации риска пациентов с ТЭЛА и четкого определения группы риска, для которой скрининг может быть оправдан. К факторам риска развития ХТЭЛГ на сегодняшний день относятся: протромботические состояния (прежде всего антифосфолипидный синдром (АФС)) и повышение уровня фактора свертывания VIII и активности фактора Виллебранта, наследственные тромбофилии; такие состояния, как спленэктомия, хронические воспалительные заболевания, вентрикулоатриальные шунты, активный инфекционный процесс и активное онкологическое заболевание; рецидивирующее течение ТЭЛА, массивность тромботического поражения ЛА, а также отсроченная диагностика и идиопатический характер тромбоза ЛА [2][14][15]. При этом важно отметить, что до 25-40% пациентов с ХТЭЛГ не имеют документированного анамнеза острой ТЭЛА, что указывает на возможность бессимптомного/малосимптомного течения первичного тромбоэмболического эпизода или развития заболевания по альтернативным механизмам.
Помимо эпидемиологических данных и факторов риска развития заболевания проведение наблюдательных и регистровых исследований помогает выявить изменения в стратегии оказания медицинской помощи, оценить реальную возможность внедрения современных методов обследования и лечения пациентов с ХТЭЛГ, а также проанализировать их эффективность и безопасность. Целью настоящей работы был анализ эпидемиологии, факторов риска и исходных клинических данных пациентов, включенных в регистр пациентов с ХТЭЛГ.
Материал и методы
В проспективное наблюдательное одноцентровое исследование включено 286 пациентов (женщины 51% (n=148)) с впервые установленным диагнозом ХТЭЛГ и пролеченных в ФГБУ «НМИЦ им. В. А. Алмазова» в период с 01.01.2014 по 01.01.20241. Для оценки гемодинамических показателей малого круга кровообращения выполнялась катетеризация правых камер сердца с использованием термодилюционного баллонного катетера 7F Свана-Ганца (B. Braun Melsungen AG, Германия) с определением и расчетом показателей среднего давления в ЛА (срДЛА), давления заклинивания капилляров легких, сердечного индекса, ЛСС. Диагноз ХТЭЛГ верифицировали согласно критериям Европейского общества кардиологов от 2015г и клиническим рекомендациям Минздрава России «Легочная гипертензия, в том числе хроническая тромбоэмболическая легочная гипертензия» от 2020г (срДЛА >25 мм рт.ст., давление заклинивания ЛА <15 мм рт.ст., ЛСС >3 ед. Вуда) [16][17]. Морфофункциональная оценка сердца выполнялась с помощью эхокардиографического исследования (ЭхоКГ) на аппарате VIVID 7 Dimension (General Electric, США) в соответствии с текущими на тот период времени рекомендациями Американского общества эхокардиографии [18]. Для оценки толерантности к физической нагрузке выполнялся тест с 6-минутной ходьбой согласно рекомендациям Американского торакального общества [19]. Комплексное исследование функции внешнего дыхания с определением стандартных и динамических показателей вентиляции и статических объемов легких выполняли на аппарате VIASYS Healthcare Hoechberg (Германия). Кардиопульмональное нагрузочное тестирование проводили на велоэргометре с одновременной оценкой газообмена методом breath-by-breath (анализ каждого дыхательного цикла в режиме реального времени) с помощью системы Oxycon Pro.
Всем включенным в исследование выполняли клинический анализ крови (Sysmex XNL-350, Sysmex, Япония), оценивали уровень N-концевого промозгового натрийуретического пептида (NT-proBNP) в качестве лабораторного маркера сердечной недостаточности электрохемилюминесцентным методом с помощью стандартного набора Elecsys (Roche Diagnostic GmbH, Германия) на анализаторе Cobas (Cobas 2000, Roche Diagnostics, США). Все исследования были выполнены до назначения ЛАГ-специфической терапии и проведения хирургического/эндоваскулярного лечения. С учетом необходимости приема антикоагулянтов пациентами с ХТЭЛГ обследование на АФС включало оценку уровня критериальных антител к кардиолипину (IgM, IgG) и антител к b2-гликопротеину- I-типа в рамках первого скрининга и далее с интервалом 12 нед., в случае приема прямых оральных антикоагулянтов полный второй скрининг (включающий оценку волчаночного антикоагулянта), в случае применения варфарина — только определение уровня критериальных антител к кардиолипину (IgM, IgG) и антител к b2-гликопротеину-I-типа. Для постановки диагноза АФС были использованы Сиднеевские критерии АФС [20]. Полиморфные варианты генов факторов свертывания и фибринолитической системы крови (FV Leiden: 1691 G>A (Arg506Gln), FII (протромбин): 20210 G>A, FI (фибриноген): -455 G>A, FVII: G>A (Arg353Gln), FXIII: G>T (Arg353Gln), SERPINE1 (PAI-1): -675 5G>4G) изучались методом полимеразной цепной реакции в режиме реального времени с помощью набора «Кардиогенетика тромбофилия» (ДНК-технологии, Россия).
С целью оценки эффективности работы мультидисциплинарной «команды ХТЭЛГ», созданной на базе центра ЛГ в ФГБУ «НМИЦ им В. А. Алмазова», включенные в исследование больные были разделены на две подгруппы в зависимости от времени верификации диагноза ХТЭЛГ: группа 1 (n=147) включала пациентов, обследованных и пролеченных в период с 01.01.2014 по 31.12.2018; группа 2 (n=139) — в период с 01.01.2019 по 31.12.2023. Следует отметить, что в течение первого анализируемого периода (с 01.01.2014 по 31.12.2018; группа 1) в мультидисциплинарную «команду ХТЭЛГ» входили два кардиолога-специалиста по легочной артериальной гипертензии (ЛАГ), один врач по рентгенэндоваскулярным диагностике и лечению и один кардиохирург, имеющий опыт выполнения операций на аорте и трансплантации сердца. Ко второму анализируемому периоду (с 01.01.2019 по 31.12.2023; группа 2) команда расширилась за счет присоединения опытного врача лучевой диагностики, второго опытного кардиохирурга и второго врача по рентгенэндоваскулярным диагностике и лечению, а также трех специалистов функциональной диагностики, выполняющих расширенный протокол ЭхоКГ и кардиопульмонального нагрузочного тестирования. Развитие мультидисциплинарной «команды ХТЭЛГ», помимо увеличения личного опыта в работе с данными пациентами сопровождалось расширением интервенционных возможностей и, в частности, внедрением с 2016г метода баллонной ангиопластики ЛА с постепенным увеличение числа выполненных процедур.
Исследование выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования одобрен локальным этическим комитетом (выписка № 12-20 от 21 декабря 2020г). До включения в исследование у всех участников было получено письменное информированное согласие.
Статистическая обработка данных проводилась в SPSS Statistic. Для проверки нормальности распределения применялся тест Шапиро-Уилка. Количественные данные с ненормальным распределением представлены в виде медианы, 25-й и 75-й процентилей (Me [Q1; Q3]). Для сравнения двух независимых групп применялся тест Манна-Уитни. Анализ качественных данных проводился с использованием критерия Фишера. Для оценки взаимосвязи между количественными переменными использовался коэффициент ранговой корреляции Спирмена. Различия считали значимыми при p<0,05.
Результаты
Клиническая характеристика пациентов
Средний возраст в обследованной группе (n=286) на момент включения составил 56 [ 43; 66] лет, индекс массы тела 27,3 [ 24,4; 31,1] кг/м2, при этом ожирение (значение индекса массы тела >30 кг/м2) встречалось только у 19% (n=55) пациентов. Среди сопутствующей патологии лидирующие позиции занимала артериальная гипертензия (36%, n=103) и патология желудочно-кишечного тракта (26%, n=74). Большинство пациентов имели продвинутую стадию заболевания на момент диагностики ХТЭЛГ (III функционального класса (ФК), n=176, 62%) и следующие жалобы: одышку при физической нагрузке (92%) и/или одышку в покое (21%), отёки (41%), дискомфорт в груди (29%), утомляемость (31%), головокружение (28%), кашель (22,1%, кровохарканье — 3,1%), пресинкопальные состояния (10,7%), потери сознания — 8,7%. Среднее время от дебюта симптомов до постановки диагноза составило 2,6 [ 1,4; 4,6] года.
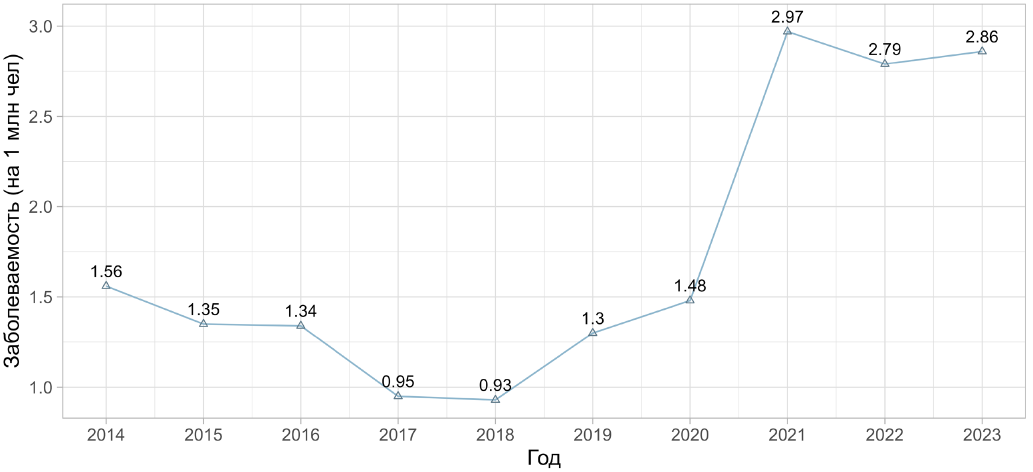
Следует отметить, что большинство больных — 59,3% (n=170) были направлены для дообследования из региональных лечебных учреждений, при этом существенную роль в маршрутизации оказала система телемедицинского консультирования, которая начала функционировать в «НМИЦ им В. А. Алмазова» с 2019г. 40,7% пациентов были жителями Санкт-Петербурга, что, с одной стороны, упрощало динамическое наблюдение за больными, а с другой, давало возможность рассчитать ряд эпидемиологических показателей. За период с 01.01.2014 по 01.01.2024 включительно в Санкт-Петербурге диагностировано 118 случаев ХТЭЛГ (рис. 1). Распространенность заболевания в Санкт-Петербурге на конец 2023г составляла 21,1 случая на 1 млн. человек, исходя из общей численности населения на 01.01.2024г — 5597763 человека по данным Федеральной службы государственной статистики2. Отмечен рост заболеваемости ХТЭЛГ в Санкт-Петербурге за анализируемый период времени (рис. 1).
Факторы риска развития ХТЭЛГ
Характеристика эпизода острого тромбоза ЛА
На основании ретроспективного анализа медицинской документации и опроса пациентов показано, что тромбоз глубоких вен, ассоциированный с эпизодом острой ТЭЛА, встречался в 59% (n=169) случаев, верифицированная по данным компьютерной ангиопульмонографии ТЭЛА — в 71% (n=204), при этом массивный тромбоз ЛА (вовлечение главных и долевых ветвей ЛА в тромботическое поражение) был отмечен у 50% (n=101), а признаки перегрузки давлением правых камер по данным ЭхоКГ встречались у 31% (n=63). Такие традиционные транзиторные факторы риска острого эпизода ТЭЛА, как хирургическая операция (абдоминальная хирургия и ортопедические операции), встречались в 2,8% (n=8), прием оральных контрацептивов у 3,5% (n=10), онкологическое заболевание — 2% (n=5). В связи с тем, что большинство пациентов не были обследованы в полном объеме для уточнения причины исходного эпизода венозного тромбоза, ретроспективно оценить истинную частоту традиционных факторов риска развития тромбоза ЛА не представлялось возможным, поэтому в ряде случаев эпизод ТЭЛА расценивался как идиопатический (неспровоцированный). Оценка такого признанного фактора риска трансформации в ХТЭЛГ, как рецидивирующий характер течения ТЭЛА, также была затруднена в связи с отсутствием архива данных компьютерной ангиопульмонографии и высокой вероятностью того, что в ряде случаев врачами на местах в качестве рецидива ТЭЛА воспринималась декомпенсация явлений правожелудочковой сердечной недостаточности у больного с предсуществующей ХТЭЛГ.
Протромботические состояния как фактор риска трансформации в ХТЭЛГ
На наличие АФС было обследовано 91% пациентов (n=260) с ХТЭЛГ, у 5% (n=15) больных в анамнезе было указание на положительный тест на волчаночный антикоагулянт, что при отсутствии информации об условиях забора крови (наличие приема антикоагулянтов на момент выполнение анализа) делало эти результаты не интерпретируемыми и требовало полноценного обследования для исключения АФС с интервалом 12 нед., что было выполнено в ходе наблюдения. У 6% (n=17) обследованных имелось в анамнезе указание на отрицательные антитела к кардиолипинам (IgG, IgM) и b2-гликопротеину I типа, в случае этих больных полный скрининг выполнялся однократно в рамках стационарного этапа обследования на фоне пропуска одного подкожного введения низкомолекулярного гепарина. В результате дообследования у 11% (n=31) пациентов был подтвержден диагноз АФС, при этом в 7 случаях он носил вторичный характер на фоне верифицированной системной красной волчанки.
Генетическое тестирование выполнено у 70% (n=200) пациентов с ХТЭЛГ. Выявлен один случай гомозиготного носительства мутации гена протромбина FII (20210 G>A), а также один случай сочетания гетерозиготного носительства мутации гена FV (1691 G>A) и FII (20210 G>A), которые можно отнести к наследственным тромбофилиям высокого тромботического риска (табл. 1). Всем пациентам на этапе верификации диагноза ХТЭЛГ и оценки операбельности выполнялась оценка активности антитромбина-3, дефицитных состояний не было выявлено, среднее значение активности антитромбина-3 составило 92% [ 83,3; 100,0]. Дефицит протеинов С и S рутинно не оценивался с учетом необходимости применения антикоагулянтной терапии. Наличие не нулевой группы крови отмечено у 82% (n=235) и было ассоциировано с повышением концентрации фактора Виллебранта в плазме крови (201 [ 67; 243] vs 87 [ 51; 189]%, p=0,003).
Спленэктомия
В анамнезе спленэктомия выполнена у 5% (n=14) пациентов: в 6 случаях селезенка удалялась по причине острой травмы, в остальных — в рамках лечения наследственного сфероцитоза. При этом в двух случаях при дообследовании в рамках верификации диагноза ХТЭЛГ наследственный сфероцитоз был исключен и диагностирована талассемия.
Лимфопролиферативные заболевания
В нашем исследовании зарегистрировано 5 пациентов (1,7%) с миелопролиферативными заболеваниями: 1 пациент с эссенциальным тромбоцитозом, 4 пациента с истинной полицитемией (JAK2+).
Миома матки и сосудистые мальформации
Согласно нашим наблюдениям отдельной группой риска развития острой ТЭЛА с последующей трансформацией в ХТЭЛГ могут рассматриваться пациентки с гигантскими миомами матки (размер миомы >16 нед.), составившие в нашем исследовании 2,4% (n=7). Аномальные маточные кровотечения приводили у этих женщин к тяжёлой железодефицитной анемии и гемической гипоксии — самостоятельным факторам риска венозного тромбоза, которые в совокупности со сдавлением крупной миомой сосудов малого таза реализовывались в исходный эпизод острого тромбоза ЛА. При этом объём и длительность антикоагулянтной терапии снижались на фоне рецидивов маточных кровотечений, что, несомненно, ограничивало реканализацию острых тромбоэмболов и приводило к их хронизации. В дальнейшем формирование синдрома ЛГ и клиники правожелудочковой недостаточности становилось причиной отказа в выполнении гистерэктомии этим пациенткам, замыкая тем самым причинно-следственные взаимосвязи этих трех нозологий.
Особой группой в нашем исследовании были пациенты с сосудистыми аномалиями — крупными артерио-венозными мальформациями согласно классификации сосудистых аномалий3: 2 пациента с синдром Клиппеля-Треноне-Вебера с локализацией мальформации на верхней конечности и мягких тканях спины с деформацией позвоночника и костей верхнего пояса конечностей; 1 пациент с синдром Паркс-Вебера-Рубашова и формированием выраженных варикозных изменений вен нижних конечностей с явлениями флеботромбоза, тромбоза подвздошных вен и глубоких вен нижних конечностей с развитием выраженного посттромбофлебитического синдрома. Во всех случаях наличие крупных артерио-венозных мальформаций осложнилось рецидивирующим течением тромбоза ЛА с постепенной трансформацией в ХТЭЛГ и дополнительной хронической объемной перегрузкой правого желудочка за счет артерио-венозного шунтирования крови [21][22].
Аутовоспалительные и аутоиммунные заболевания
Доказанным фактором риска развития ХТЭЛГ за счет системного воспаления и вероятной транзиторной бактериемии являются воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит), диагностированные у 5% (n=14) пациентов нашей группы. Обсуждается связь формирования ХТЭЛГ у пациентов, имеющих клинически значимую ревматологическую патологию. В нашей когорте эти пациенты представлены семью пациентами с системной красной волчанкой и вторичным АФС, четырьмя больными с ревматоидным артритом и двумя случаями верифицированного диагноза системной склеродермии. Аутоиммунный тиреоидит с явлениями гипотиреоза, требующего заместительной терапии, констатирован у 5% (n=13) пациентов. Временная связь начала неспецифической клиники ХТЭЛГ с перенесением новой коронавирусной инфекции (<3 мес. между верифицированным эпизодом коронавирусной инфекции и синдромом одышки) отмечена в 4% (n=11) случаев.
Внутрисердечные имплантированные устройства
У 4 пациентов (1%) был установлен постоянный электрокардиостимулятор на момент постановки диагноза ХТЭЛГ.
Медикаментозная терапия на момент постановки диагноза ХТЭЛГ
На момент верификации диагноза и оценки операбельности пациентов с ХТЭЛГ большинство в качестве антикоагулянтной терапии получали варфарин — 61% (n=174), 39% (n=112) — прямые оральные антикоагулянты (препараты c анти-Ха активностью), дезагреганты в рамках комбинированной антитромботической терапии ишемической болезни сердца получали 7% больных. Петлевые диуретики и антагонисты альдостерона получали 74% пациентов. ЛАГ-специфическая терапия была назначена эмпирически по месту жительства в 16% случаев (n=45), при этом только у 14 пациентов на основании выполненной в регионе катетеризации камер сердца.
Клиническая характеристика пациентов, включенных в регистр, в зависимости от временного периода
При сравнении клинико-лабораторных характеристик двух групп больных, отражающих рутинную клиническую практику ведения пациентов ХТЭЛГ в разные временные периоды внутри одного учреждения, следует отметить, что не выявлено различий по возрастно-половому составу, спектру сопутствующей патологии и факторов риска (табл. 2). Пациенты группы 1 (период с 01.01.2014 по 31.12.2018) отличались наличием достоверно более выраженного ремоделирования и дисфункции правых камер сердца по данным ЭхоКГ, и в группе 2 более высокими значениями NT-proBNP (1512,0 [511,5; 2702,0] vs 816,5 [197,0; 2235,5], р=0,004) (период с 01.01.2019 по 31.12.2023). При этом отличий по показателям гемодинамики малого круга кровообращения получено не было. Не отличались также и сроки верификации диагноза, однако в группе 2 достоверно чаще выявлялись пациенты ХТЭЛГ ФК I (по Всемирной организации здравоохранения) (табл. 2). Важно отметить, что у пациентов 2 группы назначение варфарина регистрировалось достоверно реже по сравнению с группой 1 (71 vs 50%, p=0,003). Отличий по числу пациентов с эмпирически назначенной ЛАГ-специфической терапией не установлено.

Рис. 1. Динамика заболеваемости ХТЭЛГ на 1 млн. населения в г. Санкт-Петербург по годам в период с 01.01.2014 по 31.12.2023.
Таблица 1
Частоты встречаемости полиморфизмов генов факторов свертывания крови и фибринолитической системы
| Ген и мутация | Гомозиготное носительство, n, % | Гетерозиготное носительство, n, % | Отсутствие полиморфизма, n, % |
| FV Leiden: 1691 G>A (Arg506Gln), n=199 | 0 | 14 (7%) | 185 (93%) |
| FII (протромбин): 20210 G>A, n=199 | 1 (1%) | 16 (8%) | 182 (91%) |
| FI (фибриноген): -455 G>A, n=102 | 1 (1%) | 41 (40%) | 60 (59%) |
| FVII: G>A (Arg353Gln), n=101 | 1 (1%) | 19 (19%) | 81 (80%) |
| FXIII: G>T (Arg353Gln), n=101 | 9 (9%) | 30 (30%) | 62 (61%) |
| SERPINE1 (PAI-1): -675 5G>4G, n=108 | 28 (26%) | 51 (47%) | 29 (27%) |
Таблица 2
Клиническая характеристика включенных в исследование пациентов в зависимости от периода постановки диагноза
| Показатель | Группа 1 (n=147)
(01.01.2014-31.12.2018) Ме [Q1; Q3]# |
Группа 2 (n=139)
(01.01.2019-31.12.2023) Ме [Q1; Q3]# |
Р |
| Возраст на момент включения, годы | 60,0 [ 47,0; 71,0] | 59,0 [ 45,0; 70,0] | 0,554 |
| Время до постановки диагноза, годы | 2,7 [ 1,1; 4,9] | 2,6 [ 1,5; 4,5] | 0,813 |
| Женский пол, % | 50% (n=73) | 53% (n=73) | 0,638 |
| ФК I/II/III/IV, % | 1/21/68/10 | 9/19/55/9 | 0,111
pI-I=0,041* pI-I=0,171 pI-I=0,061 pI-I=0,876 |
| Дистанция в ТШХ, м | 300,0 [ 200,0; 407,0] | 320,0 [ 216,0; 390,0] | 0,066 |
| Наличие синкопальных состояний, % | 33 [ 26; 41] | 22 [ 16; 30] | 0,063 |
| Наличие отеков, % | 75 (51%) | 70 (50%) | 0,906 |
| NT-proBNP, пг/мл | 1512,0 [ 511,5; 2702,0] | 816,5 [ 197,0; 2235,5] | 0,004* |
| Данные эхокардиографического исследования | |||
| Размер ЛП в продольной оси, мм | 40,0 [ 36,3; 44,0] | 41,0 [ 36,0; 44,0] | 0,896 |
| иОЛП, мл/м2 | 30,0 [ 24,0; 35,0] | 31,0 [ 25,0; 36,0] | 0,420 |
| ИММЛЖ, г/м2 | 85,0 [ 69,3; 100,8] | 78,0 [ 66,0; 95,5] | 0,235 |
| КДР ЛЖ, мм | 43,0 [ 38,0; 47,0] | 44,00 [ 40,0; 48,0] | 0,411 |
| ФВ ЛЖ, % | 62,0 [ 58,0; 66,0] | 63,0 [ 58,0; 67,0] | 0,181 |
| УО ЛЖ, мл | 46,0 [ 36,0; 58,0] | 53,0 [ 45,5; 63,3] | 0,002* |
| Степени диастолической дисфункции ЛЖ 0/I/II/III, % | 32/62/3/3 | 29/64/5/2 | 0,871 |
| Диаметр ЛА, мм | 31,0 [ 28,0; 34,0] | 29,0 [ 26,0; 33,0] | 0,005* |
| Площадь ПП, см2 | 28,0 [ 23,0; 33,5] | 26,0 [ 21,0; 32,0] | 0,019* |
| ПЖ базальный размер, мм | 50,5 [ 45,0; 57,0] | 50,0 [ 44,0; 55,5] | 0,162 |
| ПЖ/ЛЖ | 1,26 [ 1,10; 1,44] | 1,14 [ 0,94; 1,37] | 0,003* |
| TAPSE, мм | 15,5 [ 13,0; 18,0] | 16,0 [ 13,0; 20,0] | 0,131 |
| TAV’S, см/сек | 10,0 [ 8,0; 11,0] | 10,0 [ 9,0; 11,0] | 0,166 |
| FAC, % | 28,5 [ 24,0; 33,0] | 30,0 [ 22,3; 34,0] | 0,761 |
| РСДЛА, мм рт.ст. | 90,5 [ 77,3; 105,0] | 85,0 [ 70,0; 100,0] | 0,017* |
| Свободная стенка ПЖ, мм | 6,0 [ 5,0; 7,0] | 5,0 [ 5,0; 6,0] | <0,001* |
| Диаметр НПВ, мм | 22,0 [ 20,0; 25,5] | 22,0 [ 19,0; 25,0] | 0,383 |
| Данные катетеризации правых камер сердца | |||
| срДЛА, мм рт.ст. | 54,0 [ 45,0; 61,2] | 52,0 [ 40,5; 61,0] | 0,248 |
| ДЗЛК, мм рт.ст. | 14,0 [ 10,0; 15,5] | 13,0 [ 11,5; 14,0] | 0,851 |
| ЦВД, мм рт.ст. | 13,0 [ 10,0; 17,0] | 13,0 [ 9,0; 18,0] | 0,798 |
| СИ, л/мин*м2 | 2,01 [ 1,74; 2,50] | 2,03 [ 1,69; 2,42] | 0,467 |
| ЛСС, дин*с*см-5 | 886,0 [ 594,8; 1160,0] | 880,5 [ 500,0; 1143,0] | 0,702 |
| SatO2, % | 92,0 [ 89,0; 95,0] | 92,2 [ 89,2; 95,0] | 0,983 |
| SvO2, % | 60,0 [ 55,0; 65,2] | 60,0 [ 53,0; 66,0] | 0,872 |
| Данные спирографии | |||
| ОФВ1, %Д | 96,0 [ 85,0; 106,3] | 91,0 [ 81,5; 105,0] | 0,203 |
| ЖЕЛ, %Д | 101,0 [ 90,0; 112,0] | 97,0 [ 87,0; 115,8] | 0,252 |
| ОФВ1/ЖЕЛ | 78,0 [ 73,0; 84,3] | 78,0 [ 71,0; 85,0] | 0,752 |
| Данные кардио-респираторного нагрузочного тестирования | |||
| VO2peak, %Д (норма >85%) | 56,0 [ 43,8; 68,0] | 51,5 [ 38,0; 64,0] | 0,116 |
| VO2 на АП, %Д (норма >85%) | 45,0 [ 36,0; 60,0] | 44,5 [ 30,0; 58,0] | 0,177 |
| VO2/HR, %Д (норма >85%) | 60,0 [ 49,0; 75,0] | 64,5 [ 48,0; 74,0] | 0,962 |
| VE/VCO2 (норма <34) | 55,0 [ 48,0; 62,0] | 57,0 [ 47,1; 67,1] | 0,523 |
Примечание: * — статистически значимый уровень р<0,05, # — данные представлены в виде медианы и интерквартильного размаха,
Сокращения: АП — аппарат, ДЗЛК — давление заклинивания в легочных капиллярах, ЖЕЛ — жизненная емкость легких, ИММЛЖ — индекс массы миокарда левого желудочка, иОЛП — индекс объема левого предсердия, КДР — конечный диастолический размер, ЛА — легочная артерия, ЛЖ — левый желудочек, ЛП — левое предсердие, ЛСС — легочное сосудистое сопротивление, НПВ — нижняя полая вена, ОФВ1 — объем форсированного выдоха за 1 секунду, ПЖ — правый желудочек, ПП — правое предсердие, ПЖ/ЛЖ — отношение базальных размеров правого и левого желудочков, РСДЛА — расчетное систолическое давление в легочной артерии, СВ — сердечный выброс, СИ — сердечный индекс, срДЛА — среднее давление в легочной артерии, ТШХ — тест с шестиминутной ходьбой, ЦВД — центральное венозное давление, УО — ударный объем, ФВ — фракция выброса, ФК — функциональный класс, FAC — процент изменения площади правого желудочка в одном сердечном цикле, NT-proBNP — N-концевой промозговой натрийуретический пептид, SatO2 — сатурация артериальной крови, SpO2peak — сатурация кислорода на пике ФН, SvO2 — насыщение кислородом смешанной венозной крови, TAPSE — амплитуда движения латеральной части фиброзного кольца трикуспидального клапана, TAV’S — скорость движения латеральной части фиброзного кольца трикуспидального клапана, VE/VCO2 — вентиляторный эквивалент по CO2, VO2peak — пиковое потребление кислорода, выраженное в процентах от должной, VO2/HR peak — кислородный пульс.
Обсуждение
Расчет таких показателей, как заболеваемость и распространенность, крайне важен для долгосрочного планирования работы системы здравоохранения, и он должен максимально быть приближен к реальности. В случае ХТЭЛГ хорошим примером может служить система, внедренная в Великобритании и Швеции, когда все пациенты с верифицированным диагнозом ЛАГ и ХТЭЛГ направляются в несколько экспертных центров, которые ежегодно подвергаются аудиту и предоставляют данные больных для обобщающего анализа центральным органом управления здравоохранением. Вероятно, поэтому данные этих стран по распространенности ХТЭЛГ находятся в одном диапазоне и достаточно велики: 25,8 на 1 млн. населения для Швеции4 и 38,4 на 1 млн. населения для Великобритании5. При отсутствии централизованного сбора таких данных результаты локальных регистров менее репрезентативны и показатели распространенности могут быть заниженными. Также крайне важны критерии включения пациента в регистр. В случае с ХТЭЛГ — это прежде всего верификация на основании выполнения катетеризации правых камер сердца, которая рутинно выполняется в европейских и американских центрах ЛГ и менее доступна странах Ближнего Востока, Африки и Восточной Азии. Так, согласно данным Öngen HG, et al., проанализировавших 212 пациентов с ХТЭЛГ, включенных в период с 2016 по 2017гг в странах региона EMEA (Europe, the Middle East and Africa), в 11% случаев не была выполнена инвазивная оценка гемодинамики малого круга кровообращения. Следует отметить, что 42% пациентов, включенных в этот регистр, были больными из РФ, представленными 8 исследовательскими центрами. Всем им была выполнена оценка гемодинамики малого круга кровообращения, что косвенно свидетельствует о положительном сдвиге в развитии программы помощи пациентам с ЛГ в России [23]. В 2021г были опубликованы данные Российского регистра пациентов с ЛГ, включившего данные 404 пациентов с ХТЭЛГ из 15 центров ЛГ за период с 2012 по 2020гг, при этом 32,2% пациентов (n=130) были жителями Москвы [9]. Исходя из средней численности населения в Москве (12,3 млн. человек) и в РФ (144,6 млн. человек) в обозначенный период времени получаем следующие цифры распространенности ХТЭЛГ: 10,5 случаев на 1 млн. населения для Москвы и 2,3 случая на 1 млн. населения для РФ. Распространенность заболевания в России в соответствии с представленными данными, несомненно, занижена, т.к. в обозначенном регистре представлены не все экспертные центры страны в силу того, что он является прежде всего научной инициативой коллектива авторов, а не административной нормой учета данной редкой патологии. При этом данные по распространенности пациентов с ХТЭЛГ в Москве (10,5 случаев на 1 млн. человек за 8 лет) вполне сопоставимы с полученной нами цифрой для Санкт-Петербурга (21,5 на 1 млн. человек за 10 лет), а имеющиеся различия можно объяснить большим временным периодом включения в нашем исследовании. Зафиксированный нами прирост ежегодной заболеваемости ХТЭЛГ в Санкт-Петербурге с 1,56 случаев до 2,86 случаев на 1 млн. населения (рис. 1), на наш взгляд, является позитивным результатом создания и внедрения отечественных клинических рекомендаций по данной теме, повышения информированности врачей, а также увеличения опыта и мощности нашего экспертного центра ЛГ. Полученный нами уровень заболеваемости сопоставим с данными испанского регистра REHAP (Spanish Registry of Pulmonary Arterial Hypertension), включившего за период 2007-2008гг 167 пациентов ХТЭЛГ и показавшего заболеваемость 3,2 случая на 1 млн. населения [24], однако значимо ниже более современных данных немецкого, французского и британского регистров, фиксирующих значение ежегодной заболеваемости около 5-6 случаев на 1 млн. населения [4][25]. Для дополнительного подтверждения представлений о недостаточной выявляемости ХТЭЛГ целесообразно рассчитать потенциальное число пациентов с ХТЭЛГ за 10 лет, исходя из численности населения Санкт-Петербурга, которая в среднем за период 2014-2024гг составляла 5362678 человек (согласно данным Росстата). Используя данные по распространенности ТЭЛА (40-70 случаев на 100 тыс. населения в год) и взяв для расчетов нижнее значение, а также предположив, исходя из результатов эпидемиологических исследований, что в среднем 81,2% пациентов переживают эпизод тромбоза ЛА [25], получаем 17363 пациентов с ТЭЛА за десятилетний период в Санкт-Петербурге. Взяв за частоту трансформации в ХТЭЛГ значение 2,3%, полученное в последних наблюдательных исследованиях [11][26], получаем минимальное число вновь выявленных больных за 10 лет — 399 пациентов, что в 3,4 раза выше полученного нами значения (n=118). Помимо эпидемиологических данных в случае ХТЭЛГ крайне важным показателем является среднее время от начала симптомов до верификации диагноза. В этом аспекте наши данные (2,6 года) согласуются с результатами референтных центров г. Москвы (2,4 года) и китайских коллег (2 года), но значительно превышают сроки, продемонстрированные в многоцентровом европейском регистре — 1,18 года (n=679 за период с 02.2007 по 01.2009; 26 европейских центров и 1 центр в Канаде), американском регистре — 0,83 года (n=803 за период с 04.2015 по 03.2018) и международном регистре ХТЭЛГ — 1,25 года (n=1009 за период с 02.2015 по 02.2016; 34 центра в США, Европе и Японии). Эти результаты открывают дополнительное направление для развития отечественных центров ЛГ, прежде всего связанное с организацией системы наблюдения за пациентами, перенесшими ТЭЛА.
Сопоставляя клинико-анамнестические данные на момент постановки диагноза пациентов нашего регистра с наиболее крупными зарубежными исследованиями, были отмечены ряд схожих характеристик, а именно аналогичный гендерный состав: 51,5% женщин в нашем исследовании, 49,9% в регистре [27][28] и 52% в международном регистре пациентов с ХТЭЛГ, опубликованном в 2024г [10]. При этом пациенты нашего регистра были несколько моложе: средний возраст составлял 60 лет против 63 лет в выше приведенных регистрах. Состояние большинства больных регистра НМИЦ им. В. А. Алмазова (62%) на момент постановки диагноза соответствовало III ФК (по Всемирной организации здравоохранения), что было сопоставимо с данными (68,6%) европейского регистра ХТЭЛГ [27] и 61% в международном регистре [10]. В российском регистре был отмечен более молодой возраст пациентов (57 лет) и меньшая доля пациентов с III ФК (56%) [9]. Сравнивая исходные показатели, характеризующие тяжесть пациентов на момент постановки диагноза, следует отметить, что наши пациенты имели более выраженные нарушения гемодинамики малого круга кровообращения при сравнении с международным регистром: срДЛА 53 [40; 61] vs 44 [35; 52] мм рт.ст., сердечный индекс 2,0 [ 1,6; 2,5] vs 2,2 [ 1,8; 2,7] л/мин×м2, ЛСС 871 (483-1116) дин×с×см-5 vs 643 (453-912) дин×с×см-5 [10]. При этом наши результаты согласуются с данными московских коллег и исследователями из ФГБУ «НМИЦ им. акад. Е. Н. Мешалкина» Минздрава России, продемонстрировавших следующие исходные показатели гемодинамики малого круга: срДЛА 51 мм рт.ст. и 49 мм рт.ст. и ЛСС 2008 дин×с×см-5 и 871 дин×с×см-5, соответственно [9][29]. Важными тенденциями, продемонстрированными в нашем исследовании, является увеличение числа больных с ХТЭЛГ I ФК на момент постановки диагноза с 1% в течение первых 5 лет работы центра (группа 1) до 9% в более поздний период (группа 2). Кроме этого, пациенты второй группы (временной интервал 2019-2023гг) имели менее выраженные изменения правых камер сердца по эхокардиографическим данным в сочетании с меньшими значениями NT-proBNP. На наш взгляд, эта динамика косвенно подтверждает важность формирования системы маршрутизации пациентов с ЛАГ/ХТЭЛГ в РФ, появление региональных центров ЛГ и формирование экспертных центров ХТЭЛГ с всеми современными возможностями диагностики и лечения этих пациентов.
Дополнительной возможностью улучшения диагностики и лечения пациентов с ХТЭЛГ является уточнение группы риска трансформации в ХТЭЛГ, прежде всего на основании выделения факторов риска. В нашем регистре у большинства больных (71%) в анамнезе был верифицированный эпизод ТЭЛА, в половине случаев с вовлечением главных и долевых ветвей, а у 30% пациентов имелась перегрузка правых камер сердца, расцениваемая как указание на повышение расчетного систолического давления в ЛА и/или расширение правых камер сердца по данным ЭхоКГ выписного эпикриза за период ТЭЛА. Эти результаты согласуются с результатами зарубежных и отечественных наблюдательных исследований: частота исходного эпизода ТЭЛА составляла 78,1% в европейском регистре и 72,4% в российском регистре пациентов с ХТЭЛГ. При этом важно подчеркнуть, что ретроспективный сбор данных об исходном эпизоде ТЭЛА в рамках регистра делает не точным частоту и значимость факторов риска и требует отдельных наблюдательных исследований у пациентов с перенесенным тромбозом ЛА. В ходе одной из таких работ Klok FA, et al. проанализировали данные 772 пациентов, перенесших ТЭЛА с частотой развития ХТЭЛГ 2,8%. Были выделены 6 факторов, ассоциированных с развитием ХТЭЛГ, 3 из которых непосредственно характеризовали перенесенную ТЭЛА: отсроченная диагностика >2 нед. (отношение рисков (ОР) 7,9 (95% ДИ: 3,3-19)), идиопатический характер тромбоза (ОР 20 (95% ДИ: 2,7->100)), дисфункция правого желудочка по данным компьютерной томографии или ЭхоКГ (ОР 4,1 (95% ДИ: 1,4-12)). Эти же факторы риска развития ХТЭЛГ наравне с системной гипоксемией (ОР 2,5 (95% ДИ: 3,3-19)) и нормальным значением Д-димера (ОР 0,96 (95% ДИ: 0,91-0,99)) были получены в крупном проспективном исследовании японских коллег COMMAND VTE Registry-2, включившего 2787 пациентов с ТЭЛА с частотой формирования ХТЭЛГ — 2,3% [12]. Быстрая реперфузия легких (системный тромболизис или эмболэктомия) при ТЭЛА являлась одной из «протективных» в отношении развития ХТЭЛГ. Уточнение/подтверждение влияния этого фактора представляется крайне важным в свете сегодняшнего развития транскатетерных методов лечения ТЭЛА. Подобный подход планируется и в текущем исследовании HI-PIETO по изучению эффективности ультразвукового тромболизиса у пациентов с ТЭЛА промежуточно-высокого риска [30].
При анализе традиционных факторов, ассоциированных с развитием ХТЭЛГ, в особую группу следует выделить протромботические состояния крови и прежде всего АФС, зафиксированный в нашем исследовании у 11% пациентов, и число обследованных на это состояние (n=260), при этом в 7 случаях АФС носил вторичный характер на фоне подтвержденного диагноза системной красной волчанки. Эти результаты согласуются с данными европейского регистра — 10,1%, при меньшем охвате пациентов обследованием (только 63% включенных в регистр пациентов), несколько ниже распространенности, продемонстрированной московскими коллегами — 15,3% [9] и значимо выше данных немецкого регистра пациентов с ХТЭЛГ, где АФС выявлен у 4,3% больных [31]. Расхождения, вероятно, связаны с отличиями локальных протоколов обследования пациентов с ХТЭЛГ и необходимостью приема антикоагулянтных препаратов, затрудняющей полноценное обследование. На наследственные тромбофилии в нашем исследовании были обследованы 70% (n=200) пациентов, при этом мутации, ассоциированные с высоким тромботическим риском, выявлены в 1% случаев (гомозиготное носительство FII (протромбин): 20210 G>A), гетерозиготное носительство мутаций FV Leiden: 1691 G>A (Arg506Gln) у 7% пациентов, а гетерозиготное носительство мутаций FII (протромбин): 20210 G>A встречалось у 8% пациентов. Эти данные сложно сопоставлять с результатами других регистров, т.к. под термином тромбофилия исследователями могут подразумеваться различные состояния. Так, в исследовании московских коллег продемонстрирована высокая частота детектированной тромбофилии — 33,6%, под которой, вероятно, подразумевали наличие различных полиморфных вариантов генов коагуло-фибринолитической системы [9]. В европейском регистре для мутации гена FV Лейдена получена частота 7,7%, для мутации гена FII — 3,5% [27], в немецком регистре наследственные тромбофилии встречались в 8,2% случаев [31], что в большей степени согласуется с нашими данными. Следует подчеркнуть, что в наблюдательных исследованиях не подтверждена ассоциация наследственных тромбофилий с формированием ХТЭЛГ, именно поэтому скрининг на эти состояния не регламентирован текущими клиническими рекомендациями [1][2]. Тогда как выявление АФС принципиально меняет подход к выбору антикоагулянтной терапии в пользу варфарина.
Спленэктомия, встречавшаяся в нашем исследовании у 5% (n=14) пациентов, на сегодняшний день рассматривается в качестве отдельного фактора риска формирования ХТЭЛГ за счет формирования вторично тромбоцитоза и тромбинемии на фоне сохраняющейся дисфункции эритроцитов, что также относит этот фактор к протромботическим состояниям крови [32][33]. Крайне важно, что в 80% случаев (n=8) показанием для удаления селезенки был наследственный сфероцитоз, сам по себе увеличивающий вероятность формирования дистального варианта ХТЭЛГ. Эти результаты согласуются с данными российского и европейского регистров, где спленэктомия встречалась в 3,7% и 3,4% случаев, соответственно [9].
Следует отметить низкую встречаемость в нашей группе такого фактора риска, как онкологическое заболевание в анамнезе: 2% vs 12,7% в европейском регистре, что, вероятно, объясняется дополнительным увеличением длительности постановки диагноза ХТЭЛГ на фоне тяжелой, конкурирующей патологии. В нашем исследовании у 1,7% пациентов с выявленными лимфопролиферативными заболеваниями среди причин развития ХТЭЛГ прежде всего рассматривается истинная полицитемия и эссенциальный тромбоцитоз, ассоциированные с мутацией в гене JAK2 (95% для истинной полицитемии и 50% для эссенциального тромбоцитоза). Эти заболевания характеризуются протромботическим статусом крови за счет высокого уровня гематокрита, повышения вязкости крови и дисфункции тромбоцитов, а также высокого содержания лейкоцитов и воспалительных цитокинов [34], что приводит к венозным тромбозам, включая синдром Бадда-Киари, тромбоз глубоких вен или ТЭЛА с частой трансформацией в ХТЭЛГ [35]. У 5% больных нашего регистра зарегистрированы воспалительные заболевания кишечника, являющиеся независимым фактором риска хронизации тромботического поражения ЛА. Весьма велико число выявленных больных с системными заболеваниями соединительной ткани (5%, n=14), скрининг на которые заложен в обязательный алгоритм обследования пациента с ЛГ. В качестве отдельного фактора риска ХТЭЛГ нами предложено рассматривать крупные миомы матки, ассоциированные с анемией и связанными с ней системной гипоксемией, активацией системы гемостаза, а также ограничениями в приеме антикоагулянтов.
Таким образом, текущие показатели распространённости ХТЭЛГ существенно отличаются от прогнозируемых, что свидетельствует о недостаточной информированности врачей о проблеме ЛГ и необходимости оптимизации принципов наблюдения больных после эпизода ТЭЛА, а также проведение проспективных исследований для уточнения критериев группы риска развития ХТЭЛГ. Появление в последние годы в анализируемом регистре пациентов с ХТЭЛГ низкого ФК с менее выраженными признаками ремоделирования камер сердца свидетельствует об эффективности ранее предложенной и внедренной системы скрининга и маршрутизации ЛАГ и ХТЭЛГ, важным звеном которой является взаимодействие региональных центров ЛГ с федеральным экспертным центром [36].
Заключение
Анализ регистра пациентов с ХТЭЛГ ФГБУ «НМИЦ им. В. А. Алмазова» продемонстрировал длительные сроки постановки диагноза, ассоциированные с более выраженными изменениями гемодинамики малого круга кровообращения при сравнении с зарубежными регистрами. При этом обозначен позитивный тренд в виде увеличения среди вновь выявленных больных пациентов с более низким ФК и менее выраженным ремоделированием правых камер сердца, что, вероятно, является следствием повышения информированности врачей и совершенствования системы маршрутизации пациентов, прописанной в клинических рекомендациях Минздрава России.
1 Регистр пациентов с хронической тромбоэмболической легочной гипертензией. Симакова М. А., Марукян Н. B., Рыжков А. В., Карпова Д. В., Моисеева О. М. Свидетельство о регистрации базы данных RU 2018620437 от 14.03.2018. Заявка № 2018620083 от 16.01.2018. [Электронный ресурс]. URL: https://elibrary.ru/project_cteph.
2 Численность населения Санкт-Петербурга по состоянию на 1 января 2023 года: статистический бюллетень / Петростат. — [Электронный ресурс]. — URL: https://78.rosstat.gov.ru/storage/mediabank/%D0%A7%D0 %B8%D1%81%D0%BB.%D0%A1%D0%9F%D0%B1%20%D0%BD%D0%B0%2001.01.2023.pdf.
3 Международное общество по изучению сосудистых аномалий (ISSVA). ISSVA Classification of Vascular Anomalies [Электронный ресурс]/International Society for the Study of Vascular Anomalies. 2025. Режим доступа: https://www.issva.org/classification.
4 SPAHR: Svenska PAH & CTEPH registret [Электронный ресурс]. Orphanet. Режим доступа: https://www.orpha.net/en/research-trials/registry/226932? name=&mode=&country=.
5 National Pulmonary Hypertension Audit [Электронный ресурс] / NHS Digital. 2025. Режим доступа: https://digital.nhs.uk/data-and-information/clinical-audits-and-registries/national-pulmonary-hypertension-audit.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Симакова М.А., Осадчий А.М., Алексеева Д.В., Марукян Н.В., Гончарова Н.С., Маликов К.Н., Грабик М.А., Злобина И.С., Березина А.В., Гордеев М.Л., Моисеева О.М. Эпидемиология, факторы риска развития и принципы диагностики хронической тромбоэмболической легочной гипертензии: данные регистра. Российский кардиологический журнал. 2025;30(2S):6571. https://doi.org/10.15829/1560-4071-2025-6571. EDN: OXQCOV
Скопировать