Связка Маршалла и ее роль в нарушениях ритма сердца
Аннотация
Связка Маршалла, являясь рудиментарной структурой, играет ключевую роль в аритмогенезе из-за сочетания сохранившихся в ней мышечных волокон с патологическим автоматизмом и плотной вегетативной иннервации. Её элиминация приводит к увеличению эффективности интервенционного лечения персистирующей фибрилляции предсердий, а также профилактирует развитие послеоперационной фибрилляции предсердий и желудочковых аритмий.
В 1850г Джон Маршалл опубликовал первое описание рудиментарной складки в перикарде, состоящей из фиброзных волокон, мелких сосудов и нервных окончаний, заключенных в жировую ткань [1]. Данное анатомическое образование получило название связка Маршалла. В её структуре проходит косая вена Маршалла, впадающая в коронарный синус (КС). Связка расположена по диагонали над ушком левого предсердия (ЛП) и кпереди от левых легочных вен (ЛВ). Долгое время ей не уделялось особого внимания, пока исследователи Scherlag BJ, et al. (1972) не выдвинули гипотезу о том, что содержащиеся в ней мышечные волокна (пучки Маршалла) представляют собой конечный сегмент межпредсердного проводящего пути в сердце собаки [2]. Связка Маршалла имеет эмбриологическое происхождение от левой общей кардинальной вены и левого рога венозного синуса. В процессе развития сердца эти структуры подвергаются инволюции и не исчезают полностью, а превращаются в рудиментарный тяж. Связка у взрослого содержит остатки мышечных волокон, нервных сплетений и косую вену Маршалла.
Связка Маршалла играет ключевую роль в возникновении аритмий благодаря сохранившимся в её толще мышечным волокнам, способным к самостоятельной электрической активности. Она иннервирована вегетативными нервными ганглиями, что делает её источником эктопических импульсов, запускающих фибрилляцию предсердий (ФП) [3]. Анатомически связка служит проводником между КС и ЛП, создавая пути для циркуляции патологических импульсов. Именно поэтому в последнее возрастает интерес к связке Маршалла, она становится мишенью лечения и профилактики различных нарушений ритма сердца.
Цель обзора состоит в систематизации и обобщении современных научных данных о морфофункциональных особенностях связки Маршалла, ее роли в патогенезе аритмий, в частности ФП, а также достоинствах и ограничениях современных методов диагностики и терапии, включая интервенционные подходы. Особое внимание уделяется взаимодействию анатомо-гистологических и электрофизиологических характеристик связки с механизмами аритмогенеза, а также анализу экспериментальных и клинических исследований, направленных на оптимизацию лечения пациентов с нарушениями ритма сердца с вовлечением связки Маршалла.
Анатомия и гистология связки Маршалла
Связка Маршалла формируется в процессе эмбриогенеза как результат инволюции левой общей кардинальной вены и левого рога венозного синуса, которые в ранних стадиях развития сердца выполняют ключевую роль в венозном оттоке плода. В ходе нормального морфогенеза эти сосудистые структуры редуцируются и трансформируются в тонкий фиброзно-мышечный тяж, сохраняющийся у взрослого человека в виде связки Маршалла. Несмотря на редукцию, в составе связки сохраняется косая вена Маршалла, а также остатки мышечных волокон и обширная вегетативная иннервация, что обусловливает её функциональную значимость в электрофизиологии сердца. Этот эмбриологический процесс объясняет рудиментарный характер связки, а также её анатомическую вариабельность и потенциальную роль в аритмогенезе.
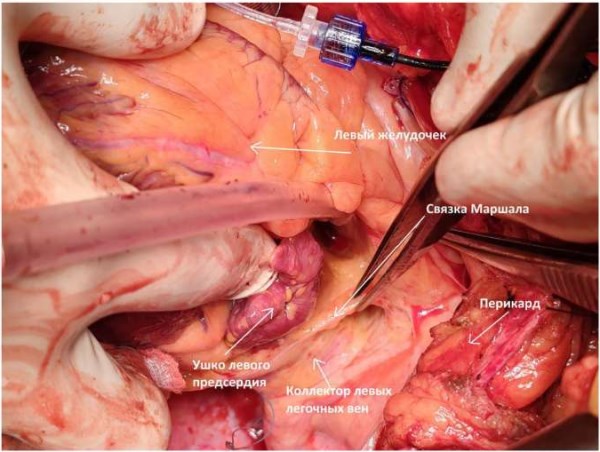
Анатомически связка Маршалла располагается на заднебоковой поверхности ЛП, занимая важное положение в сложной анатомической области. Она проходит косо в складке перикарда, отделяющей ЛП от левого лёгкого (рис. 1).

Рис. 1. Топографическое расположение связки Маршалла (из личного архива авторов).
Связка проходит в непосредственной близости от устьев левых лёгочных вен, располагаясь кпереди и латеральнее них, за ушком ЛП, и образует естественную границу между ушком ЛП и ЛВ.
Топография связки Маршалла отличается тесными взаимоотношениями с ключевыми сердечными структурами. Спереди от неё находится ушко ЛП, сзади — тело предсердия и устья левых лёгочных вен, снизу — атриовентрикулярная борозда с проходящими в ней коронарной артерией и венозным синусом. В самой толще связки заключены рудиментарная косая вена, мышечные волокна, нервные ганглии и жировая ткань [4][5].
Такое расположение делает связку Маршалла важным анатомическим ориентиром при выполнении катетерных аблаций и объясняет её значимую роль в возникновении аритмий (рис. 2) [3].

Рис. 2. Схематическое изображение топографии связки Маршалла по отношению к прилегающим структурам.
Гистологическая архитектоника связки Маршалла представляет собой сложный конгломерат разнородных тканей, интегрированных в единую структуру. Ее можно назвать сложным нейро-мышечно-сосудистым комплексом. Основу связки составляет плотная волокнистая соединительная ткань, образующая непрерывный каркас из коллагеновых и эластических волокон. Этот фиброзный матрикс служит механической опорой для других элементов и является продолжением эпикардиальных слоев (рис. 3 А, Б, В).
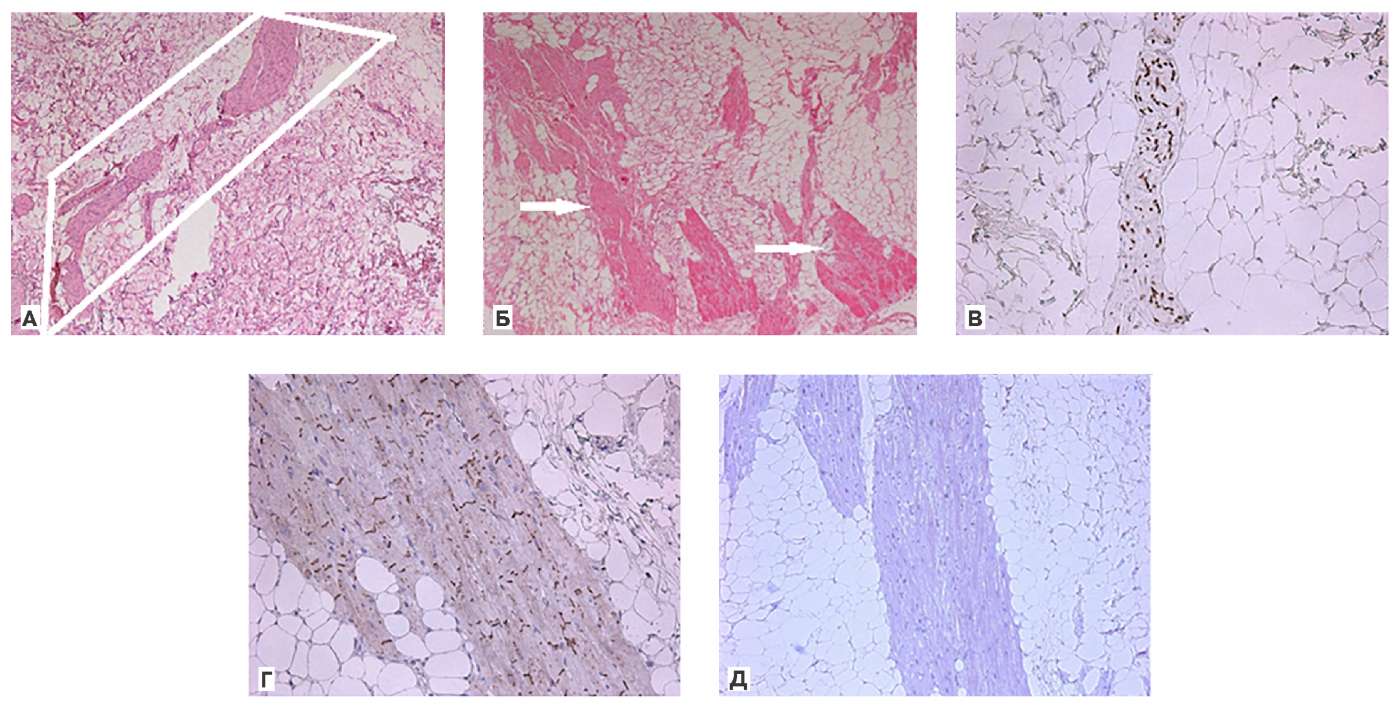
Рис. 3. Два варианта гистологического строения связки Маршалла (А, Б, В) и иммуногистохимическое исследование мышечного пучка связки Маршалла (Г, Д). А — связка представлена нервными волокнами (обведены трапецией), окруженными жировой тканью. Мышечных пучков и фиброзной ткани нет; Б — связка представлена мышечными пучками (указаны стрелками), жировой тканью и нервными волокнами, окраска гематоксилином и эозином, ×50; В — мелкие нервные волокна второго варианта с экспрессией SOX10 (коричневое окрашивание ядер), ×200; Г — экспрессия коннексина 43 (коричневое окрашивание) на вставочных дисках кардиомиоцитов рабочего миокарда; Д — отсутствие экспрессии HCN4 на кардиомиоцитах мышечного пучка, ×200.
В толще этого соединительнотканного остова заключены поперечнополосатые кардиомиоциты, формирующие анатомическое образование известное как пучок Маршалла. Мышечные волокна демонстрируют значительную гистологическую вариабельность: среди типичных рабочих кардиомиоцитов встречаются клетки, морфологически сходные с элементами проводящей системы. Эти специализированные миоциты часто образуют выраженный мышечный футляр вокруг косой вены Маршалла и устанавливают непосредственные электрические контакты с миокардом прилегающих структур [3].
Центральное положение в гистологической организации занимает косая вена Маршалла, чей просвет выстлан типичным эндотелием. Стенка сосуда подвергается возрастной фиброзной трансформации с элементами гиалиноза, что отражает её рудиментарный статус. Особый интерес представляет богатая нервная ткань, представленная многочисленными ганглиями вегетативной нервной системы и разветвлёнными нервными сплетениями. Эти нейрональные скопления включают как холинергические, так и адренергические нейроны, устанавливающие тесные контакты с мышечными элементами [6][7].
Вся эта сложная структура погружена в адипозную ткань, которая не только выполняет механическую и трофическую функции, но и участвует в паракринной регуляции. Такая гистологическая организация превращает связку Маршалла в уникальный нейро-мышечно-сосудистый комплекс, способный генерировать и поддерживать патологическую электрическую активность.
Анатомия связки Маршалла демонстрирует значительную вариабельность между разными пациентами, что отражается в её макроскопической структуре, гистологическом составе и функциональной значимости. Наличие и выраженность данной структуры варьируют в популяции — у части пациентов связка представлена хорошо развитым фиброзно-мышечным тяжом с сохранёнными мышечными волокнами, в то время как у других может наблюдаться её полная редукция или фрагментация.
Критически важным аспектом вариабельности является сохранность мышечного компонента — пучка Маршалла. Именно наличие функционирующих кардиомиоцитов, способных к автоматизму и формированию электрических связей с миокардом предсердий, определяет аритмогенный потенциал структуры. Степень сохранности просвета косой вены Маршалла также вариабельна: у большинства взрослых происходит её облитерация, но возможны случаи частичной проходимости [3].
Топографические взаимоотношения, включая точки фиксации к КС и ЛП, могут иметь индивидуальные особенности, что важно учитывать при интервенционных вмешательствах. Нервный компонент связки, представленный вегетативными ганглиями, также отличается изменчивой плотностью и организацией.
Эта анатомо-функциональная гетерогенность объясняет, почему связка Маршалла играет ключевую роль в патогенезе ФП лишь у определенной группы пациентов, что диктует необходимость персонализированного подхода к её электрофизиологической оценке и аблации [8].
Связка Маршалла анатомически тесно связана не только с ЛП, но и с миокардом левого желудочка (ЛЖ). Функциональная взаимосвязь обусловлена наличием в составе связки остаточных кардиомиоцитов и богатой вегетативной иннервации, которые обеспечивают симпатические и парасимпатические влияния на желудочковый миокард. Исследования показали, что связка Маршалла может выступать как симпатический проводящий путь между левым звездчатым ганглием и миокардом ЛЖ, что может свидетельствовать о её роли в патогенезе желудочковых аритмий, особенно в остром периоде инфаркта миокарда (ИМ) [6][9]. Таким образом, нейро-кардиальные связи связки Маршалла представляют собой важный компонент регуляции электрической стабильности ЛЖ и являются перспективной мишенью для антиаритмической терапии.
Электрофизиологические свойства связки Маршалла
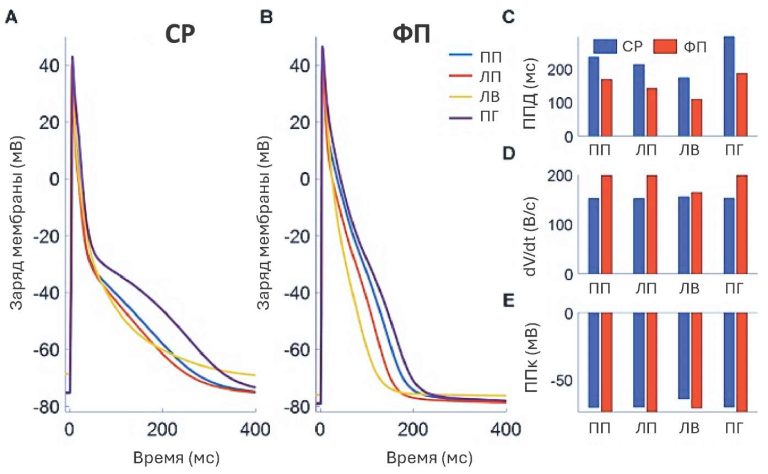
Кардиомиоциты, сохранившиеся в структуре связки Маршалла, обладают уникальными электрофизиологическими свойствами, которые обусловливают их высокий аритмогенный потенциал. Эти клетки демонстрируют способность к патологическому автоматизму и триггерной активности, что делает их источником эктопических импульсов, инициирующих и поддерживающих ФП.
Автоматизм клеток пучка Маршалла проявляется в их способности к спонтанной диастолической деполяризации [10]. В отличие от специализированных клеток синоатриального узла, этот автоматизм является патологическим и возникает в условиях изменения электрофизиологической среды — при активации вегетативной нервной системы, ишемии или растяжении ткани. Мембрана этих кардиомиоцитов обладает особым набором ионных каналов, включая кальциевые каналы T-типа и funny-каналы, которые обеспечивают медленный диастолический подъем потенциала действия до порога активации быстрых натриевых каналов. Этот механизм позволяет им функционировать как эктопические водители ритма, конкурируя с синусовым узлом.
Триггерная активность представляет собой другой важный механизм аритмогенности. Она возникает вследствие нарушения кальциевого гомеостаза в клетках, что приводит к появлению осцилляторных колебаний мембранного потенциала — ранних и поздних постдеполяризаций. Ранние постдеполяризации развиваются во время фазы плато потенциала действия и связаны с реактивацией кальциевых каналов L-типа на фоне удлиненного рефрактерного периода. Поздние постдеполяризации возникают после завершения реполяризации и обусловлены спонтанным выбросом кальция из саркоплазматического ретикулума через рианодиновые рецепторы. При достижении критической амплитуды эти осцилляции могут инициировать возникновение потенциала действия [11].
Особую значимость этим механизмам придает тесная интеграция кардиомиоцитов связки Маршалла с вегетативной нервной системой [12]. Парасимпатическая стимуляция приводит к укорочению эффективного рефрактерного периода и увеличению дисперсии реполяризации, создавая субстрат для re-entry. Симпатическая активация усиливает кальциевую нагрузку клеток, повышая вероятность возникновения триггерной активности. Это нейро-кардиальное взаимодействие превращает связку Маршалла в мощный аритмогенный узел, способный отвечать на изменения вегетативного тонуса генерацией патологических импульсов [13].
Клиническое значение этих механизмов подтверждается эффективностью целевой аблации области связки Маршалла у пациентов с персистирующей ФП, особенно в случаях, когда конвенциональной изоляции ЛВ оказывается недостаточно [14].
Роль связки Маршалла в аритмогенезе
Учитывая усиление позиций контроля ритма при ФП [15], целесообразно рассмотреть роль связки Маршалла в триггерной активности и поддержании ФП.
В инициации ФП ключевую роль играет способность кардиомиоцитов связки генерировать эктопическую активность [16]. Благодаря сохраненным мышечным волокнам, обладающим свойствами автоматизма, эта структура может выступать источником частых преждевременных предсердных сокращений. Эктопические импульсы, возникающие особенно часто на фоне повышенного вегетативного тонуса, способны запускать ФП при попадании в уязвимый период реполяризации [17]. Важным механизмом является фокальный высокочастотный разряд, при котором клетки связки генерируют очень частые импульсы, непосредственно инициирующие волны re-entry в ЛП [18].
Молекулярным механизмом триггерной активности является нарушение кальциевого гомеостаза в кардиомиоцитах связки. Повышенная плотность рианодиновых рецепторов типа 2 способствует спонтанному высвобождению кальция из саркоплазматического ретикулума, вызывая поздние постдеполяризации. Эти события при достижении порогового уровня инициируют эктопические импульсы, запускающие ФП [19].
В поддержании ФП участвуют несколько взаимосвязанных механизмов. Связка Маршалла служит стабильным источником постоянной триггерной активности, которая непрерывно «подпитывает» аритмию. Через свои мышечные соединения с КС и ЛП она создает дополнительные пути для проведения импульсов, содействующие формированию и поддержанию множественных волн re-entry. Богатая вегетативная иннервация структуры модулирует электрофизиологические свойства прилегающего миокарда, увеличивая дисперсию реполяризации и создавая аритмогенный субстрат.
Особое значение имеет способность связки Маршалла выступать в качестве драйвера ФП. При картировании во время процедуры аблации нередко выявляется, что именно эта зона является источником фрагментированной активности, которая поддерживает ФП [20]. Этот механизм особенно характерен для персистирующих и длительно-персистирующих форм ФП, где традиционная изоляции ЛВ может оказаться недостаточно эффективной без воздействия на область связки Маршалла [20].
Экспериментальные исследования на животных моделях предоставили фундаментальные доказательства аритмогенного потенциала связки Маршалла. В одной из основополагающих работ Scherlag BJ, et al. (2005) на собачьих моделях была продемонстрирована возможность индукции ФП электрической стимуляцией зоны связки Маршалла. Исследование выявило наличие специализированных мышечных волокон, способных к проведению импульсов со скоростью значительно медленнее, чем в миокарде предсердий. Эта гетерогенность проведения создает идеальные условия для формирования re-entry [21].
В исследовании Aidonidis I, et al. (2009) на свиных моделях было показано, что инъекция ацетилхолина в область связки Маршалла вызывала устойчивую ФП в 2 раза чаще, чем его инъекция в другие участки ЛП [22].
При ФП у собак, индуцированной постоянной стимуляцией, источником быстрой электрической активности являются связка Маршалла и ЛВ. Механизм, в результате которого ЛП активируется быстрее и имеет большее количество волн возбуждения, чем правое, может быть связан с тем, что ЛП анатомически ближе к этим участкам с патологически быстрой проводимостью [23].
Экспериментальные исследования продемонстрировали значительную роль связки Маршалла в патогенезе желудочковых аритмий, особенно в условиях острого ИМ. На моделях животных установлено, что симпатическая иннервация связки служит проводящим путем между левым звездчатым ганглием и желудочками, способствуя возникновению и поддержанию желудочковой тахикардии и фибрилляции. Аблация дистальной части связки Маршалла приводила к значительному снижению частоты желудочковых аритмий, что подтверждает её функциональную связь с нейро-кардиальной регуляцией желудочкового миокарда [9]. Эти данные указывают на потенциал связки Маршалла как мишени для профилактики опасных для жизни желудочковых нарушений ритма в острый период инфаркта.
Клинические исследования подтвердили значимость этих находок. В рандомизированном клиническом исследовании VENUS [23] (n=343) добавление спиртовой аблации вены Маршалла к стандартной катетерной аблации значимо повышало эффективность лечения персистирующей ФП по сравнению с только изоляцией ЛВ.
Анализ по принципу намерения лечить (intention-to-treat) показал увеличение частоты успеха (свобода от аритмии >30 с после одной процедуры) с 38,0% до 49,2% (отношение рисков (ОР) 0,63; 95% доверительный интервал (ДИ): 0,41-0,97; p=0,037). В анализе по протоколу различие было еще более выраженным (51,6% успеха, ОР 0,57; 95% ДИ: 0,37-0,90; p=0,015). В группе спиртовой аблации также были достигнуты вторичные конечные точки: бремя ФП, необходимость в повторных процедурах и общий успех после повторных вмешательств [24].
В работе Báez-Escudero JL, et al. (2012) спиртовая аблация вены Маршалла также продемонстрировала эффективность в лечение перимитрального трепетания предсердий [25].
В ходе рандомизированного клинического исследования с участием 430 пациентов частичная кардиальная денервация (пересечение связки Маршалла) продемонстрировала значительное снижение частоты возникновения послеоперационной ФП после коронарного шунтирования (18,1% в группе вмешательства vs 31,6% в контрольной группе; ОР 0,57 (95% ДИ: 0,41-0,81); P=0,001), что было дополнительно подтверждено анализом выживаемости (ОР 0,53 (95% ДИ: 0,36-0,79); P=0,002). Процедура не была сопряжена с дополнительными рисками и привела к снижению послеоперационных медицинских расходов, что позволяет рассматривать её в качестве эффективного варианта профилактики послеоперационной ФП в кардиохирургической практике [26].
Связка Маршалла играет значительную роль в патогенезе не только ФП, но и других наджелудочковых аритмий, в частности предсердных тахикардий и трепетания предсердий. Её анатомические и электрофизиологические особенности создают уникальный субстрат для возникновения и поддержания этих нарушений ритма.
Активность связки Маршалла может проявляться в виде фокальных предсердных тахикардий, характеризующихся регулярной и частой эктопической активностью [16]. Эти тахикардии часто имеют характерные особенности на поверхностной электрокардиограмме, включая определенную морфологию зубца P и специфическую ось предсердной деполяризации. Механизм таких аритмий обычно связан с патологическим автоматизмом кардиомиоцитов связки или триггерной активностью на фоне нарушения кальциевого гомеостаза.
При трепетании предсердий связка Маршалла может выступать критическим истмусом macro-re-entry. Её мышечные соединения с КС и ЛП создают пути проведения, способствующие формированию и поддержанию циркуляции волны возбуждения. Особое значение имеет возможность связки участвовать в перимитральном трепетании, где она может создавать зону медленного проведения [27].
Симпатическая денервация связки Маршалла оказывает протективный эффект в отношении в т.ч. желудочковых аритмий, индуцированных острым ИМ. Результаты исследований показали, что дистальная часть связки Маршалла может служить симпатическим проводящим путем между левым звездчатым ганглием и желудочками [11][13]. Антиаритмический эффект аблации дистальной части связки, вероятно, связан с прерыванием симпатической нервной связи между левым звездчатым ганглием и желудочками. Таким образом, аблация связки Маршалла может рассматриваться как альтернативный метод профилактики жизнеугрожающих аритмий у пациентов с высоким риском их развития в остром периоде ИМ [28].
Вегетативная иннервация связки значительно влияет на её аритмогенный потенциал. Активация парасимпатических нервных окончаний может приводить к замедлению деполяризации и увеличению дисперсии реполяризации в прилегающих участках миокарда, создавая благоприятные условия для возникновения re-entry. Симпатическая стимуляция, в свою очередь, усиливает автоматизм и триггерную активность кардиомиоцитов связки [6].
Таким образом, связка Маршалла вносит существенный вклад в структурное и электрическое ремоделирование предсердий, выступая катализатором фиброза и электрической нестабильности. Сохранившиеся в её структуре кардиомиоциты демонстрируют патологический автоматизм и триггерную активность, что приводит к постоянной патологической активности миокарда предсердий, которая, в свою очередь, запускает процесс фиброзирования. Параллельно, богатая вегетативная иннервация связки модулирует электрофизиологические свойства прилегающих тканей: парасимпатическая стимуляция через ацетилхолин-зависимые калиевые каналы укорачивает эффективный рефрактерный период, а симпатическая активация усиливает кальциевую перегрузку клеток, что совместно увеличивает дисперсию реполяризации и создает субстрат для re-entry [3][29]. Этот порочный круг, при котором электрическая нестабильность приводит к фиброзу, а фиброз усугубляет электрическую нестабильность в проведении импульсов и создание зон медленного проведения, делает связку Маршалла ключевым элементом в прогрессировании ФП от пароксизмальной к персистирующей форме.
Денервация связки Маршалла использована для профилактики желудочковых тахиаритмий у пациентов с высоким риском их развития в исследовании NEUROPREVENT-VT. В рамках одноцентрового рандомизированного контролируемого исследования пациенты с показаниями к аортокоронарному шунтированию распределяются на группы с выполнением стандартного лечения с дополнительной денервацией связки Маршалла или без неё. Основными целевыми показателями являются частота и тяжесть желудочковых аритмий, развитие послеоперационной ФП, а также оценка безопасности процедуры. Результаты данного исследования позволят уточнить роль нейро-модифицирующих вмешательств на уровне связки Маршалла в профилактике аритмий у пациентов с ишемической кардиомиопатией.
Методы исследования связки Маршалла
Диагностика аритмий, связанных со связкой Маршалла, требует комплексного электрофизиологического исследования с использованием современных методов картирования. Высокочастотная стимуляция и фармакологические пробы способствуют выявлению триггерной активности, в то время как эндо-эпикардиальное картирование позволяет идентифицировать участие связки в циклах re-entry.
Электрофизиологические исследования играют ключевую роль в выявлении и характеристике аритмогенной активности связки Маршалла, сочетая методы точного картирования и стимуляционных проб. Современное трехмерное электрокардиографическое картирование позволяет идентифицировать фокальные источники патологической активности в области связки с точной пространственной локализацией, определяя зоны наиболее ранней активации и фрагментированных электрограмм (рис. 4). Специфические стимуляционные протоколы, включая программированную и сверхчастую стимуляции из различных участков предсердий, провоцируют проявление латентной триггерной активности, в то время как фармакологические тесты с изопротеренолом и аденозином помогают выявить вегетативно-опосредованные аритмии. Важным диагностическим приемом является высокочастотная стимуляция из КС, позволяющая активировать мышечные волокна связки Маршалла и оценить их участие в поддержании аритмии. Интрапроцедурное использование диагностических катетеров с малым межэлектродным расстоянием, особенно применение многоконтактного картирования [30], обеспечивает регистрацию высокочастотных потенциалов пучка Маршалла, а комбинация эндо- и эпикардиального подходов позволяет полностью охарактеризовать сложные механизмы re-entry, связанные с этой структурой.
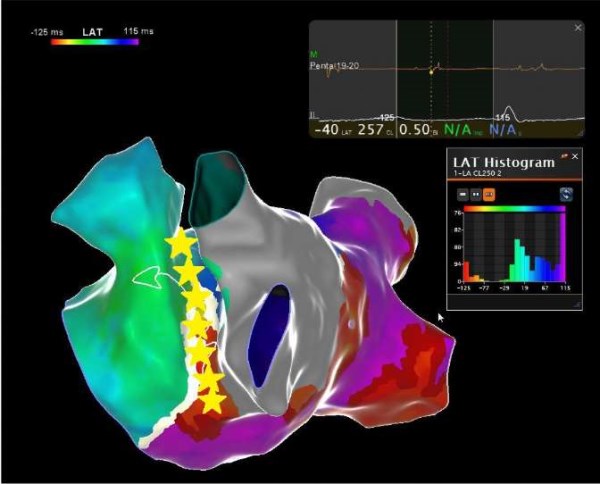
Рис. 4. Схематическое изображение связки Маршалла (желтые звездочки) при картировании в трехмерной навигационной системе Carto 3, Biosense Webster.
Визуализация связки Маршалла представляет значительные трудности из-за её малого размера и сложного анатомического расположения, однако современные методы визуализации позволяют косвенно оценить её структуру и выявить связанные с ней патологические изменения. Чреспищеводная эхокардиография иногда визуализирует связку как линейную структуру между ЛП и левой верхней ЛВ, но её чувствительность остается ограниченной. При этом при спиртовой аблации часто применяется интракардиальная эхокардиография. Наличие повышенной локальной эхогенности миокарда в области гребня и стабильного эхогенного потока (echogenic streaming) в ЛП, регистрируемых при интракардиальной эхокардиографии во время инфузии этанола в устье вены Маршалла, свидетельствует об увеличении объема ткани, подвергнутой аблации, в этой зоне. Компьютерная томография с контрастированием обеспечивает более детальную анатомическую оценку, позволяя идентифицировать фиброзно-жировую ткань связки и её взаимоотношения с КС и ушком ЛП, что особенно важно для планирования интервенционных процедур [31]. Магнитно-резонансная томография с отсроченным контрастированием имеет особую ценность для оценки степени фиброза в области связки Маршалла, который коррелирует с её аритмогенным потенциалом и может служить предиктором эффективности аблации. Селективная ангиография вены Маршалла, хотя и технически сложная, обеспечивает прямую визуализацию сосудистого компонента связки и используется в ходе процедуры спиртовой аблации для подтверждения правильного положения катетера и распределения этанола [32]. Комбинация этих методов позволяет комплексно оценить анатомические особенности связки Маршалла и их влияние на электрофизиологию предсердий, что имеет критическое значение для выбора оптимальной стратегии лечения пациентов с ФП [33].
Гистологические и иммуногистохимические методы исследования детально характеризуют тканевый состав и молекулярные особенности связки Маршалла. Стандартное гистологическое окрашивание гематоксилин-эозином позволяет визуализировать сложную архитектонику связки, включая фиброзную строму, сохранившиеся пучки кардиомиоцитов, жировую ткань и элементы нервной системы (рис. 3 Г, Д). Иммуногистохимические исследования с использованием антител к коннексину-43 демонстрируют нарушение экспрессии и нарушение распределения щелевых контактов в кардиомиоцитах связки, что объясняет замедление проведения импульсов. Анализ с маркерами вегетативной нервной системы (тирозин-гидроксилаза для симпатических и ChAT для парасимпатических волокон) демонстрирует обильную иннервацию связки с образованием сложных нейро-кардиальных взаимодействий [12]. Критически важным является определение экспрессии ионных каналов с помощью антител к HCN4 и Cav3.1, что подтверждает наличие пейсмейкерных свойств у клеток пучка Маршалла. Современные методы иммунофлюоресценции позволяют одновременно оценивать несколько маркеров в одной ткани, выявляя пространственные взаимоотношения между разными типами клеток и нервными окончаниями, что значительно углубляет наше понимание патофизиологических механизмов аритмогенеза, связанных с этой уникальной структурой.
Клиническое значение и терапевтические подходы
Аблация связки Маршалла представляет собой воздействие на аритмогенный субстрат в этой зоне с целью устранения триггеров ФП, особенно при персистирующих ее формах. Процедура выполняется во время электрофизиологического исследования с использованием либо стандартной радиочастотной энергии, либо метода спиртовой аблации, при котором в просвет вены Маршалла селективно вводится этанол, приводящий к химической деструкции прилегающих мышечных и нервных тканей. Основной мишенью аблации являются мышечные волокна пучка Маршалла, сохранившие способность к патологическому автоматизму и триггерной активности, а также вегетативные ганглии, модулирующие электрофизиологические свойства окружающего миокарда [3][13][15][34]. Критерием успешной аблации служит полное устранение регистрируемой электрической активности в области связки и невозможность индукции аритмии при программированной стимуляции.
Поводом к аблации связки Маршалла могут быть персистирующая и длительно-персистирующая формы ФП при документально подтвержденной триггерной активности из этой области, выявленной во время электрофизиологического исследования. Дополнительным указанием на целесообразность аблации связки служат рецидивы аритмии после ранее выполненной изоляции ЛВ, когда другие потенциальные источники аритмогенеза уже элиминированы. Процедура также может быть рассмотрена у пациентов с частыми симптомными предсердными тахикардиями, исходящими из связки Маршалла.
Радиочастотная аблация выполняется с использованием орошаемого аблационного катетера. Строится трехмерная электромагнитная навигационная карта ЛП и выполняется серия точечных воздействий вокруг устья вены Маршалла и по ходу связки. Критерием эффективности является исчезновение локальных потенциалов и невозможность индукции аритмии при программированной стимуляции. Основной сложностью при этой технике является необходимость точного позиционирования катетера.
Криоаблация применяется реже, но может быть эффективной при наличии специальных криобаллонов, адаптированных для воздействия на область КС. Метод предполагает создание зоны контролируемого некроза через замораживание ткани до температур от -50 °C до -60 °C. Преимуществом криоэнергии является лучшая стабильность катетера, длительность воздействия и потенциально более предсказуемые размеры зоны некроза.
Спиртовая аблация представляет собой технику, при которой в просвет вены Маршалла селективно вводится 98% этанол через специальный катетер. Химическое воздействие приводит к деструкции не только мышечных волокон, но и вегетативных ганглиев, значимо снижая аритмогенный потенциал зоны. Наибольшая эффективность как раз отмечается у пациентов с документально подтвержденной триггерной активностью из этой области и при спиртовой аблации, которая обеспечивает полную электрическую изоляцию зоны [35].
Выбор конкретной техники зависит от опыта оператора, доступного оборудования и индивидуальных анатомических особенностей пациента. Комбинированные подходы, включающие последовательное применение разных источников энергии, чаще показывают наилучшие результаты при сложных случаях.
Осложнения процедуры включают несколько потенциальных рисков, связанных с анатомической близостью к важным структурам. Наиболее серьезным является повреждение огибающей артерии, проходящей вблизи зоны аблации, что может привести к ИМ. Тампонада сердца возможна при перфорации стенки предсердия или КС при манипуляциях катетером. Дисфункция диафрагмального нерва возникает при распространении энергии на область его прохождения, но это осложнение обычно преходящее. Стеноз КС является редким, но серьезным осложнением, особенно при агрессивном радиочастотном воздействии в его устье. При спиртовой аблации существует риск распространения спирта в полость перикарда с последующим развитием констриктивного перикардита [3].
Заключение
Связка Маршалла является ключевым аритмогенным субстратом из-за сочетания сохранившихся мышечных волокон с патологическим автоматизмом и вегетативной иннервацией, что обусловливает её роль в инициации и поддержании тахиаритмий через механизмы фокальной триггерной активности и re-entry. Аблация связки значимо повышает эффективность лечения персистирующей ФП, в частности при использовании спиртовой аблации, а также предупреждает развитие послеоперационной ФП и желудочковых аритмий.
Отношения и деятельность. Работа выполнена с использованием ресурсов Центра коллективного пользования «Центр доклинических и трансляционных исследований» на базе ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России».
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Гасымова Н.З., Коробченко Л.Е., Старикова А.В., Исмаил-заде И.К., Иванов И.Ю., Митрофанова Л.Б., Михайлов Е.Н. Связка Маршалла и ее роль в нарушениях ритма сердца (обзор). Российский кардиологический журнал. 2025;30(4S):6594. https://doi.org/10.15829/1560-4071-2025-6594. EDN: GXYSWE
Скопировать