Клинико-морфологическое исследование миокарда при фибрилляции предсердий в разные волны COVID-19 и постковидном периоде
Аннотация
Цель. Морфологический поиск аритмогенного субстрата новой коронавирусной инфекции (COVID-19) при фибрилляции предсердий (ФП).
Материал и методы. В исследование включены 312 пациентов с подтверждённой COVID-19: 274 умерших в острую фазу инфекции и 38 пациентов постострого периода, перенёсших заболевание и потребовавших проведения эндомиокардиальной биопсии для диагностики сердечно-сосудистой патологии. Морфологическое исследование включало гистологический и иммуногистохимический анализ с количественной морфометрией (CD3, CD68, HLA-DR, VEGF, MHC I, Ang1, C1q, spike SARS-CoV-2, VP1 энтеровирусов) и статистическую обработку данных с построением моделей логистической регрессии и расчётом отношения шансов для предикторов ФП.
Результаты. В острой фазе COVID-19 наличие ФП ассоциировалось с ишемическими микротромбозами (отношение шансов (ОШ) 3,89) и очаговыми некрозами (ОШ 2,62) на фоне предшествующей гипертрофии кардиомиоцитов (ОШ 4,17). Среди клинических факторов наиболее значимыми были сахарный диабет, хроническая сердечная недостаточность и лимфопения. Построенная модель продемонстрировала высокую точность (ROC-AUC 0,944). В постостром периоде ФП ассоциировалась преимущественно с дилатационной кардиомиопатией (ОШ 2,16) и миокардитом с экспрессией VP1 энтеровирусов в кардиомиоцитах, сосудистой стенке и воспалительном инфильтрате во всех случаях, персистирующей экспрессией spike SARS-CoV-2 в макрофагах. При этом низкая сосудистая экспрессия Ang1 и VEGF, а также умеренная макрофагальная инфильтрация чаще встречались у пациентов без ФП (ROC-AUC 0,942).
Заключение. Сочетание инфекции с коморбидной кардиальной патологией и системным воспалением с развитием ишемических некрозов миокарда повышает риск ФП в остром периоде. В постостром периоде патогенез ФП обусловлен неполной репарацией миокарда с макрофагальной инфильтрацией и персистенцией вируса.
Пандемия новой коронавирусной инфекции (COVID-19), вызванная вирусом SARS-CoV-2, первоначально рассматривалась преимущественно как заболевание респираторного тракта. Однако накопленные данные убедительно свидетельствуют о том, что COVID-19 оказывает системное воздействие, поражая сердечно-сосудистую систему и способствуя развитию различных форм аритмий. Уже первые клинические наблюдения выявляли электрокардиографические изменения в острой фазе заболевания, которые, помимо признаков перегрузки правых отделов сердца вследствие пневмонии [1], включали нарушения ритма и проводимости, ишемические изменения сегмента ST, а также появление временных комплексов SIQIIITIII [2][3].
Более поздние исследования с применением методов магнитно-резонансной томографии показали наличие структурного повреждения миокарда у пациентов как в острую фазу COVID-19 [4][5], так и в постостром периоде [6], что подтверждает потенциальную кардиотропность SARS-CoV-2. Эти данные были дополнены исследованиями динамических электрокардиограмм, выявившими выраженное снижение вариабельности сердечного ритма, увеличение числа предсердных и желудочковых экстрасистол, эпизодов предсердной тахикардии, а также персистирующее удлинение интервала QTc даже после перенесённой COVID-19 [7][8].
Особый интерес в последние годы вызывает развитие фибрилляции предсердий (ФП) у пациентов с COVID-19. Согласно метаанализу Rathore SS, et al., объединённая распространённость впервые возникшей ФП (NOAF) у данной категории пациентов составила 7,8% (95% доверительный интервал (ДИ): 6,54-9,32%), при этом риск тяжёлого течения COVID-19 у больных с NOAF был значительно выше, чем у пациентов без аритмий (отношение шансов (ОШ) 4,78; 95% ДИ: 3,75-6,09) [9]. Другие исследования показали, что тяжёлая форма COVID-19 ассоциирована с 3,851-кратным увеличением риска нарушений предсердной электрической активности, а среди независимых предикторов развития аритмии выделены выраженное поражение лёгких по данным компьютерной томографии (КТ), курение и артериальная гипертензия [10].
Таким образом, накопленные данные позволяют утверждать, что COVID-19 способна индуцировать нарушения ритма преимущественно за счёт системного воздействия на миокард. В этой связи развитие ФП у пациентов с COVID-19 имеет патогенетические параллели с ФП, возникающей при инфекциях и сепсисе. Известно, что в условиях сепсиса факторами риска NOAF являются как предшествующие сердечно-сосудистые заболевания (например, ишемическая болезнь сердца (ИБС), клапанные пороки, сердечная недостаточность (СН)), так и острые триггеры, включая применение вазопрессоров, системное воспаление, катетеризацию правых отделов сердца и выраженные гемодинамические нарушения [11]. Если ранее ФП при инфекциях рассматривалась как обратимое и относительно «доброкачественное» явление, то новые крупные исследования демонстрируют её высокую склонность к рецидивированию и необходимость более тщательной стратификации риска [12].
Таким образом, COVID-19, подобно другим системным инфекционным процессам, способна инициировать ФП, сочетая воздействие воспаления, электрофизиологических нарушений и структурных изменений миокарда.
Цель: поиск механизмов формирования аритмогенного субстрата на фоне COVID-19 и выявление связи ФП с COVID-19.
Материал и методы
Исследование выполнено на клинико-морфологическом материале, полученном от пациентов с подтверждённой COVID-19, находившихся в острой и постострой фазах. Всего проанализированы образцы миокарда 312 пациентов, включая 274 умерших в острой фазе COVID-19 и 38 пациентов постострого периода, перенёсших заболевание и впоследствии обследованных по поводу клинически значимой сердечной патологии.
Пациенты с острой фазой COVID-19. В группу острой фазы включено 274 пациента, умерших в период первых трех волн пандемии COVID-19. У всех обследованных инфекция SARS-CoV-2 была подтверждена методом количественной полимеразной цепной реакции с обратной транскрипцией по мазкам из носоглотки при жизни и/или по аутопсийным образцам (трахея, бронхи, лёгкие). Для анализа использовался диагностический набор SARS-CoV-2/SARS-CoV Reagent Kit (ООО «ДНК-Технология», Москва, Россия; серия F2912S-2М) на амплификаторе CFX96 Touch (Bio-Rad, США).
Пациенты были распределены по 3 эпидемическим волнам в зависимости от циркулировавших вариантов SARS-CoV-2:
- I волна (апрель — июль 2020г) — 77 пациентов (34 женщины, 43 мужчины; медиана возраста 71 [ 66; 76] лет), доминирующая вирусная линия B.1;
- II волна (декабрь 2020 — февраль 2021г) — 119 пациентов (63 женщины, 56 мужчины; медиана возраста 74 [ 71; 80] лет), доминирующие вирусные линии B.1.397, B.1.317, вариант Alpha VOC (B.1.1.7) и AT.1;
- III волна (июнь — август 2021г) — 78 пациентов (48 женщин, 30 мужчин; медиана возраста 72 [ 68; 76] лет), доминирующий вариант Delta (B.1.617.2).
Всем пациентам при жизни выполнялось клинико-лабораторное обследование, включающее КТ органов грудной клетки (Somatom Definition 128 Siemens), измерение уровней С-реактивного белка (СРБ), показателей клинического анализа крови, прокальцитонина, D-димера, ферритина, тропонина I, а также электрокардиографическое и эхокардиографическое исследование.
Пациенты с постострой фазой COVID-19. В группу постострого периода включено 38 пациентов, перенёсших лабораторно подтверждённую COVID-19 и впоследствии предъявивших жалобы на кардиальные симптомы, потребовавшие проведения диагностической эндомиокардиальной биопсии (ЭМБ).
Критерии включения: перенесённая инфекция SARS-CoV-2, подтверждённая методом полимеразной цепной реакции с обратной транскрипцией; развитие или усиление клинических проявлений со стороны сердечно-сосудистой системы (боли в груди, СН, аритмии, синкопальные состояния); выполнение ЭМБ с получением материала достаточного объёма для морфологического и иммуногистохимического анализа.
Критерии невключения: выявление саркоидоза сердца, гранулематозного или гнойного миокардита; наличие другой установленной причины миокардиального повреждения (ИБС, токсическое воздействие, системные васкулиты); неудовлетворительное качество биоптата.
Для всех включенных в исследование пациентов оценивались клинические характеристики (возраст, пол, коморбидность), степень поражения лёгких по данным КТ, временной интервал от COVID-19 до ЭМБ, наличие нарушений ритма и проводимости, фракция выброса (ФВ) левого желудочка (ЛЖ) и показатель продольного движения трикуспидального кольца.
Гистологическое исследование. Гистологический анализ проводился на парафиновых срезах толщиной 2-4 мкм, окрашенных гематоксилином и эозином по стандартной методике. Аутопсийный материал включал фрагменты свободной стенки желудочков, межжелудочковой перегородки и предсердий, материал ЭМБ был получен из межжелудочковой перегородки. Для всех пациентов оценивались выраженность воспалительной инфильтрации, характер её клеточного состава, дистрофические и некротические изменения кардиомиоцитов, признаки интерстициального фиброза и микроангиопатии.
Иммуногистохимическое исследование. Иммуногистохимическое исследование проводилась по стандартной методике на парафиновых срезах с использованием панели антител: CD3, CD68, Ang1, VEGF, HLA-DR, MHC I, C1q, spike SARS-CoV-2, VP1 энтеровирусов для пациентов с признаками воспалительного поражения миокарда по данным стандартной гистологии (n=52).
Морфометрия и статистический анализ. Для морфометрического анализа все образцы были оцифрованы с помощью гистологического сканера Aperio AT2 (Leica Biosystems, Калифорния, США) при 20-кратном увеличении объектива. Обработка полученных цифровых изображений осуществлялась с помощью программного обеспечения Aperio ImageScope версии 12.4 (Leica Biosystems Imaging, Калифорния, США). Подсчитывалось среднее количество клеток воспалительного инфильтрата (всего и по субпопуляциям CD3⁺, CD68⁺) на 1 мм². Выраженность экспрессии иммуногистохимических маркеров HLA-DR, Ang1, VEGF, MHC I, spike SARS-CoV-2 оценивалась полуколичественно по четырёхбалльной шкале:
1 — единичные клетки или сосуды;
2 — экспрессия до 1/3 площади препарата;
3 — экспрессия в 1/2-2/3 площади;
4 — диффузная экспрессия.
Диагноз миокардита устанавливался при наличии ≥14 лейкоцитов/мм² (включая ≤4 моноцита/мм²) и ≥7 CD3⁺ Т-лимфоцитов/мм², согласно критериям Европейского общества кардиологов.
Статистический анализ полученных данных проводился с использованием библиотек NumPy, SciPy, Pandas и Matplotlib на языке программирования Python (v. 3.13). В качестве теста на нормальность использовался тест Колмогорова-Смирнова. Нормально распределенные значения были представлены в виде средних значений с ДИ, а значения, чье распределение было отличным от нормального, были представлены в виде медиан и 25-го и 75-го процентилей. При сравнении результатов между группами использовались t-критерий Стьюдента или непараметрический U-критерий Манна-Уитни. Различия считались статистически значимыми при p<0,05. Для сравнения частот встречаемости данных в группах использовался точный тест Фишера. При проведении корреляционного анализа использовался критерий Спирмена, оценка значимости выявленных корреляций производилась в соответствии со шкалой Чеддока.
Для выявления факторов, ассоциированных с развитием ФП, был проведён анализ клинико-лабораторных и морфологических параметров с применением метода логистической регрессии. В качестве зависимой переменной рассматривалось наличие эпизодов ФП, независимыми переменными — демографические, клинические, биохимические и морфометрические показатели. Перед построением модели данные были разделены на обучающую и тестовую выборки в соотношении 70:30 с сохранением стратификации по наличию или отсутствию миокардита. Количественные признаки стандартизировались методом Z-преобразования с использованием StandardScaler (scikit-learn). Обучение проводилось с использованием модели логистической регрессии (C=1,0, solver=liblinear, max_iter=1000). Качество модели оценивалось по показателям accuracy, ROC-AUC, а также по матрице ошибок и отчёту классификации (classification report). Для количественной оценки влияния отдельных факторов рассчитывались коэффициенты регрессии и отношения шансов (ОШ) (odds ratio=e^β). Наиболее значимыми предикторами считались признаки с наибольшими абсолютными значениями коэффициентов. Для повышения надёжности результатов и проверки устойчивости модели проводилась перекрёстная проверка (k-fold cross-validation, k=5) и bootstrap-анализ распределения коэффициентов. Визуализация вклада факторов и направленности их влияния выполнена с использованием библиотек matplotlib и seaborn, а также с использованием модуля shap.
Исследование выполнено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации (2013). Протокол одобрен Локальным этическим комитетом ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России (протокол № 1131-22 от 28.11.2022). Для всех пациентов, чьи данные могут быть потенциально идентифицируемы, было получено письменное информированное согласие на участие в исследовании.
Результаты
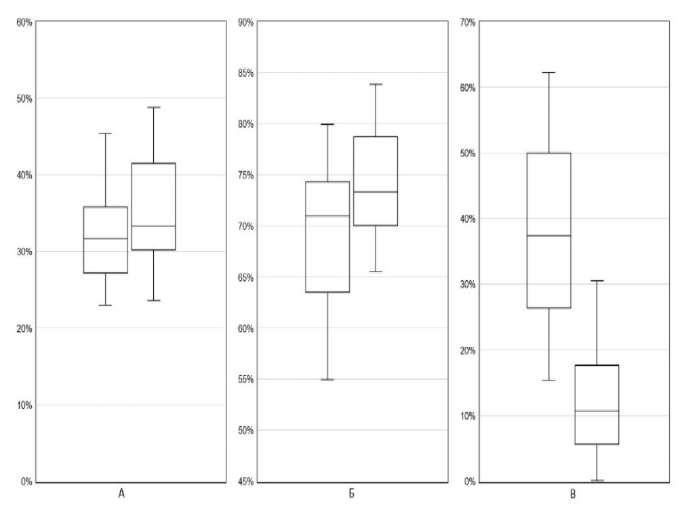
При сравнении умерших пациентов в остром периоде COVID-19 в зависимости от наличия ФП статистически значимых различий по волне пандемии, полу, длительности симптомов до госпитализации, частоте инвазивной вентиляции и воспалительным маркерам (СРБ, прокальцитонин, ферритин, D-димер, тропонин I) выявлено не было (p>0,05). Показатели %SpO2 и объема поражения лёгких по КТ также не различались между группами.
Пациенты с ФП были значимо старше по сравнению с пациентами без данного нарушения ритма (77,5 [ 68,0; 83,0] лет vs 71,0 [ 59,0; 81,0] лет, p<0,001). Также у них наблюдалась более выраженная лимфопения (0,7 [ 0,54; 0,93] vs 0,8 [ 0,55; 1,12] ×10⁹/л, p=0,045) и более низкие значения ФВ ЛЖ (59,0 [ 50,0; 59,0]% vs 59,0 [ 57,0; 63,0]%, p<0,001).
По данным электрокардиографии, у пациентов с ФП чаще встречалась атриовентрикулярная блокада II степени (p=0,018), тогда как другие блокады и формы экстрасистолии не имели статистически значимых различий.
Анализ сопутствующей патологии показал, что артериальная гипертензия с ремоделированием миокарда, хроническая СН (ХСН), ИБС, сахарный диабет (СД), а также цереброваскулярные заболевания значимо чаще встречались у пациентов с ФП (все p<0,01). Частота острого повреждения почек, онкологической патологии и острого инфаркта миокарда не различалась между группами.
Гистологический диагноз миокардита в остром периоде был сопоставим в обеих группах (5,6% без ФП vs 4,5% при ФП, p=0,901), указывая на отсутствие прямой связи между наличием аритмии и воспалительным поражением миокарда на этой стадии заболевания.
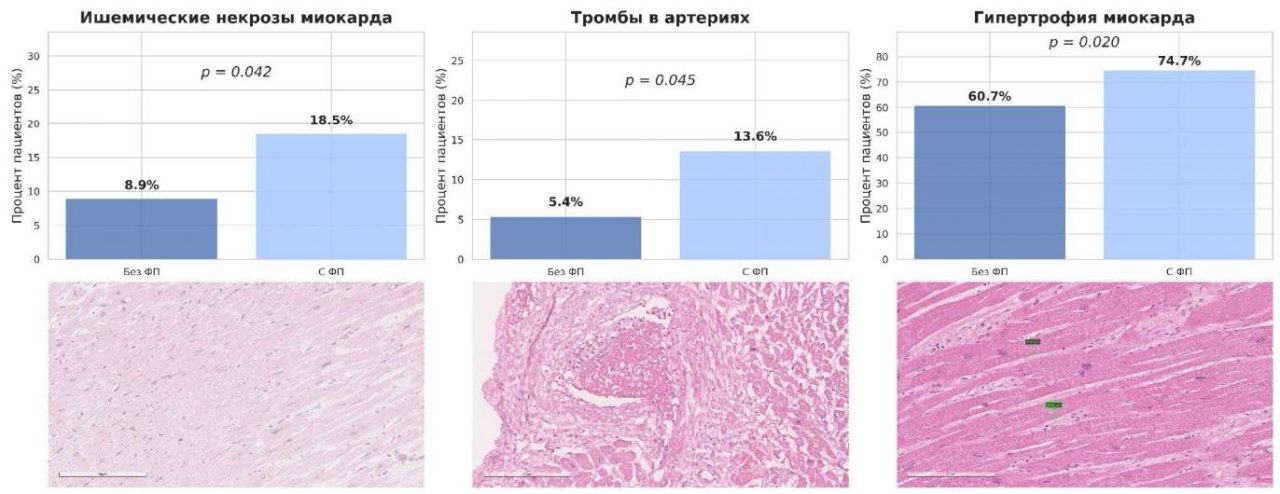
При морфологической оценке миокарда наличие ФП ассоциировалось с более выраженными ишемически-некротическими изменениями. Так, фокусы некроза миокарда выявлялись достоверно чаще у пациентов с ФП (30 (19%) vs 10 (9%), p=0,042). Тромбы в артериях миокарда также регистрировались значимо чаще при наличии ФП (22 (14%) vs 6 (5%), p=0,045). Гипертрофия кардиомиоцитов встречалась у большинства пациентов с ФП (121 (75%) vs 68 (61%) у пациентов без ФП, p=0,020), что, вероятно, отражает более выраженные хронические структурные изменения миокарда (рис. 1). Макрофагальная инфильтрация миокарда чаще регистрировалась при ФП (48 (30%) vs 26 (23%)), однако статистическая значимость не была достигнута (p=0,300). Частота остальных морфологических изменений в миокарде, включая наличие периваскулярных крупных полиморфных клеток, геморрагических некрозов, тромбов на эндокарде, васкулита, очагового плазматического пропитывания, липоматоза, заместительного кардиосклероза не демонстрировали достоверных различий между группами.

Рис. 1. Морфологические изменения в миокарде в остром периоде COVID-19 в связи с наличием и отсутствием ФП.
Сокращение: ФП — фибрилляция предсердий.
Для выявления факторов, ассоциированных с развитием ФП, была построена модель логистической регрессии. При валидации по схеме 5-fold cross-validation модель достигла ROC-AUC 0,934±0,026, а на независимом тестовом наборе — ROC-AUC 0,944 и точность 87,9%, что указывает на устойчивость предсказательной способности и высокую чувствительность к выявлению клинико-морфологических паттернов, связанных с развитием аритмии.
Анализ важности признаков с использованием ОШ показал, что гипертрофия кардиомиоцитов, выявляемая при морфологическом исследовании, ассоциировалась с наиболее выраженным увеличением вероятности ФП (ОШ 4,17). Наличие тромбов в интрамиокардиальных артериях и очагов некроза также являлись ключевыми морфологическими маркерами аритмогенного субстрата (ОШ 3,89 и ОШ 2,62, соответственно), отражая вклад ишемии и локального повреждения тканей на фоне острой COVID-19. Среди клинико-функциональных параметров наибольший вклад вносили СД с увеличением шансов ФП на 49,8%, а также ХСН, повышавшая риск ФП на 31,2%. Более умеренное влияние оказывали низкие значения ФВ ЛЖ и более старший возраст, которые сопровождались ростом риска ФП на 11,2% и 6,6%, соответственно. Интересно, что повышение уровня лимфоцитов имело протективный эффект: увеличение показателя на 1 стандартное отклонение (0,3*10⁹/л) снижало шансы развития ФП на 40,5%, что может отражать связь выраженной лимфопении и более тяжёлого течения заболевания с системным воспалительным ответом и миокардиальным повреждением (рис. 2).

Рис. 2. Наиболее значимые признаки, влияющие на развитие ФП в остром периоде COVID-19 (SHAP (Аддитивные объяснения Шепли)).
Сокращение: ХСН — хроническая сердечная недостаточность.
В группе постострой COVID-19 ЭМБ у пациентов была взята после 3 нед. — 17 мес. от последнего положительного мазка полимеразной цепной реакции из носоглотки на SARS-CoV-2 с медианным значением в 4 [ 2; 8] мес.
У пациентов с ФП отмечалась тенденция к более низким значениям ФВ ЛЖ (24,0 vs 29,0%), однако статистическая разница достигнута не была. У пациентов с ФП чаще наблюдался морфофенотип дилатационной кардиомиопатии, более высокая частота признаков ХСН до перенесённой COVID-19, однако различия также не достигли уровня значимости. Показатели системного воспаления (СРБ, D-димер, лейкоциты, лимфоциты) также не различались между группами.
В группе пациентов без ФП гистологический диагноз миокардита выставлен в 14 (47%) случаях, тогда как у пациентов с ФП — в 6 (75%). Тем не менее различия не достигли статистической значимости (p=0,362), что, возможно, обусловлено малым объемом выборки. По данным иммуногистохимического исследования, уровни инфильтрации CD3+ Т-лимфоцитами и CD68+ макрофагами были сопоставимы в обеих группах, что указывает на отсутствие выраженного усиления клеточного воспаления при наличии ФП. Более того, в отличие от острого периода COVID-19, плотность инфильтрации CD68+ макрофагами в миокарде пациентов с ФП имела тенденцию к снижению по сравнению с пациентами без ФП (9,0 (4,1; 13,9) vs 11,7 (9,8; 13,5), p=0,266). Экспрессия HLA-DR и MHC I оставалась умеренно повышенной у всех пациентов, что свидетельствует о персистирующей активации иммунного ответа независимо от наличия ФП. Активация комплемента (C1q) и сосудистые маркеры повреждения (VEGF, Ang1) не различались между группами, хотя у пациентов с ФП отмечалась тенденция к более значимой сосудистой экспрессии VEGF, что может отражать более выраженную эндотелиальную дисфункцию при нарушениях ритма. Экспрессия spike SARS-CoV-2 в воспалительном инфильтрате и в эндотелии была сопоставима между пациентами с наличием и отсутствием ФП (1,0 [ 1,0; 2,0] балл vs 1,0 [ 0,0; 1,0] балл для воспалительного инфильтрата и 1,0 [ 1,0; 2,0] балл vs 1,0 [ 1,0; 2,0] балл для эндотелия) (рис. 3). SARS-CoV-2 spike protein в кардиомиоцитах не был выявлен ни в одном случае, тогда как VP1 энтеровирусов выявлялся в кардиомиоцитах, клетках сосудистых стенок и воспалительном инфильтрате во всех случаях миокардита.
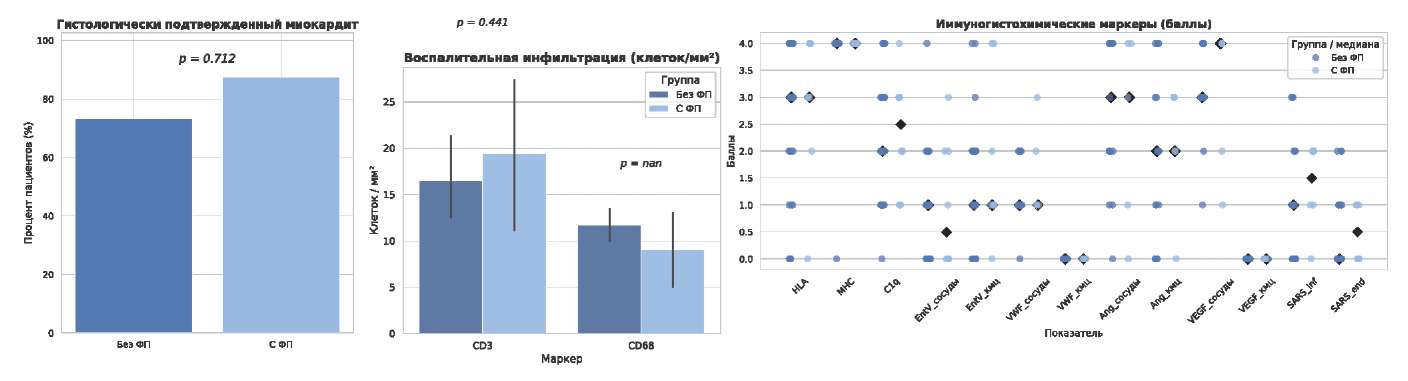
Рис. 3. Морфологические изменения у пациентов в постостром периоде COVID-19 в зависимости от наличия ФП.
Сокращение: ФП — фибрилляция предсердий.
Для выявления клинико-морфологических факторов, ассоциированных с ФП в постостром периоде COVID-19, была также построена модель логистической регрессии. При валидации по схеме 5-fold cross-validation модель продемонстрировала ROC-AUC 0,817±0,260, а на независимом тестовом наборе — ROC-AUC 0,942 при точности 89,5%.
Интересно, что наличие ХСН до COVID-19, являвшееся значимым фактором риска в остром периоде, в последующем демонстрировало обратную ассоциацию с персистированием аритмии (ОШ 0,49). Наиболее выраженную ассоциацию с ФП в постковидном периоде имел морфофенотип дилатационной кардиомиопатии, наличие которого увеличивало вероятность нарушения ритма более чем вдвое (ОШ 2,16). Экспрессия spike-белка SARS-CoV-2 в воспалительном инфильтрате также сохраняла значимое влияние (ОШ 1,46), в то время как наличие гистологического диагноза миокардита сопровождалось ростом шансов развития ФП на 44,9%. Низкая экспрессия VEGF и Ang1 в сосудах была ассоциирована с уменьшением вероятности развития ФП на 17,0% и 58,6%, а снижение количества CD68+ макрофагов — со снижением вероятности ФП на 25,9% (рис. 4, 5).
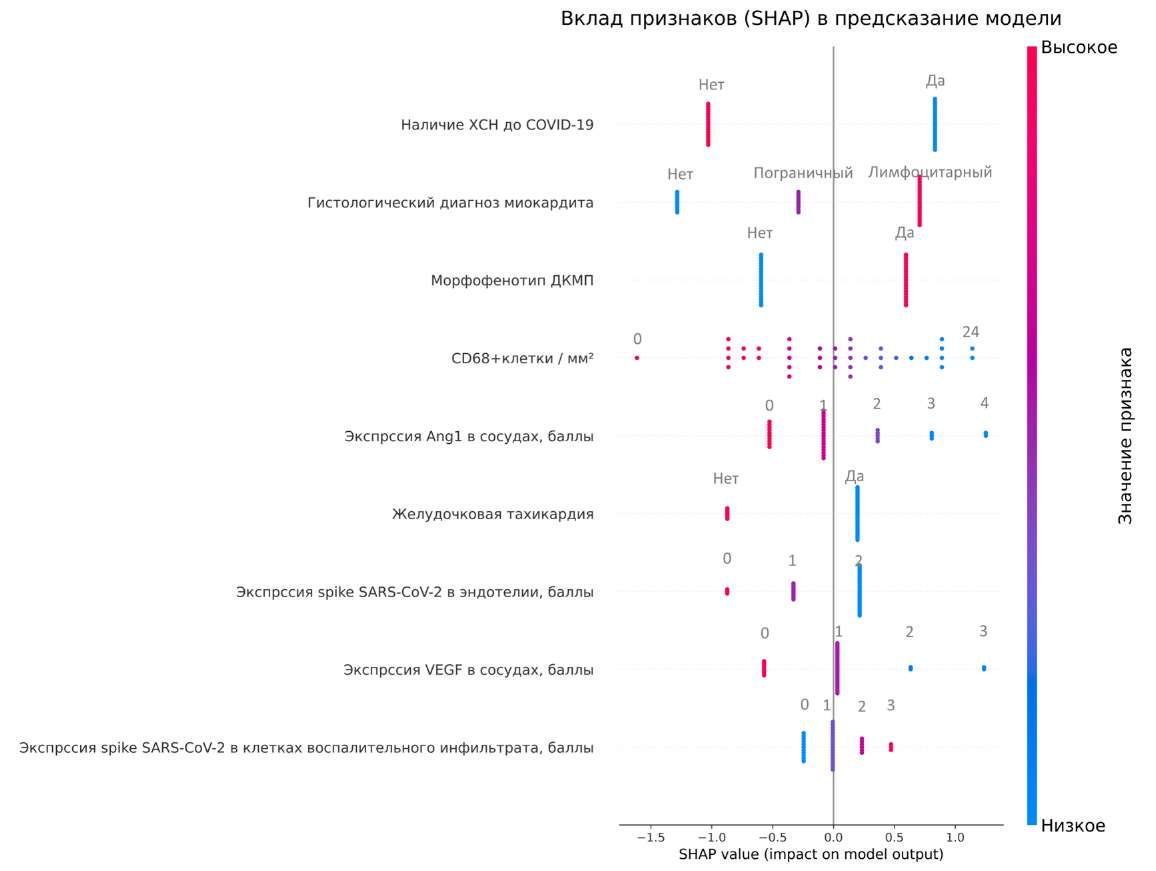
Рис. 4. Наиболее значимые признаки, влияющие на развитие ФП в постостром периоде COVID-19 (SHAP (Аддитивные объяснения Шепли) analysis).
Сокращения: ДКМП — дилатационная кардиомиопатия, ХСН — хроническая сердечная недостаточность, COVID-19 — новая коронавирусная инфекция.

Рис. 5. Морфологические признаки, влияющие на развитие ФП.
Примечание: А — активный лимфоцитарный миокардит, окраска гематоксилин-эозин; B — CD68+ макрофаги в миокарде; С — Ang1 на эндотелии сосудов; D — SARS-CoV-2 в эндотелии сосудов и макрофагах (коричневое окрашивание), ×400.
Для 1 пациента в постостром периоде с гистологически подтвержденным миокардитом и клиникой ХСН высокого функционального класса мы провели дополнительное иммуногистохимическое исследование с антителами к TMS1/ASC и NLRP3 для подтверждения потенциальной роли аутовоспаления и пироптоза в патогенезе симптомов постострого периода. Анализ выявил интенсивную цитоплазматическую экспрессию TMS1/ASC преимущественно в макрофагах воспалительного инфильтрата, а также очаговую экспрессию компонента инфламмасомы NLRP3 в отдельных макрофагах (рис. 6), что подтверждает активацию путей врождённого иммунного ответа в миокарде на данном этапе заболевания.
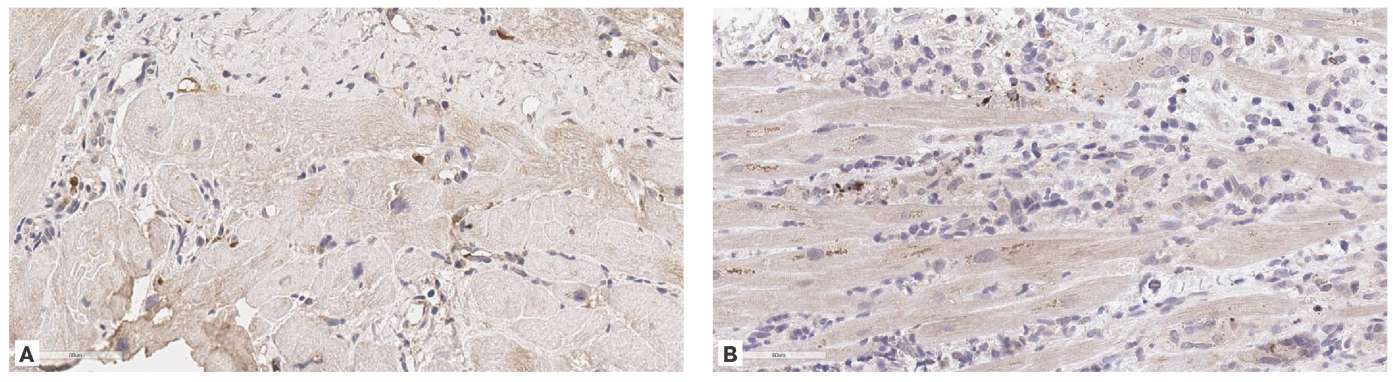
Рис. 6. Иммуногистохимическое исследование миокарда пациента в постостром периоде COVID-19, увеличение 400.
Примечание: A — иммуноокрашивание TMS1/ASC: цитоплазматическая экспрессия в меньшей части макрофагов воспалительного инфильтрата; B — иммуноокрашивание NLRP3: цитоплазматическая гранулярная экспрессия в единичных клетках воспалительного инфильтрата.
Обсуждение
COVID-19 формирует гетерогенный аритмогенный субстрат, характеристики которого варьируют в зависимости от временной фазы заболевания. В острой фазе преобладает ишемический механизм развития ФП, в основе которого лежит дисэндотелиоз с возникновением микротромбов и некрозов миокарда [13].
Важным дополнительным электрофизиологическим механизмом развития ФП в остром периоде может являться дисфункция коннексинов. Экспериментальные и клинические исследования демонстрируют, что при воспалении и перегрузке давлением происходит гипофосфорилирование Cx43 и его перераспределение с щелевых контактов на латеральные мембраны кардиомиоцитов [14]. Это перераспределение приводит к потере электрической непрерывности и фрагментации волн деполяризации. Сходные изменения межклеточных соединений описаны при ХСН и фиброзе миокарда [15-17], что позволяет рассматривать острую COVID-19 как дополнительный фактор дестабилизации проводящей системы на фоне уже имеющегося ремоделирования у пациентов с сопутствующей патологией, включая гипертрофию ЛЖ, СД, ИБС и ХСН.
Дополнительным механизмом аритмогенеза может также быть нарушение кальциевого гомеостаза. В исследовании Kanuri SH, et al. продемонстрировано, что SARS-CoV-2 воздействует на ключевые регуляторы кальциевого обмена — рианодиновые рецепторы (RyR), кальциевую АТФазау саркоэндоплазматического ретикулума (SERCA) и фосфоламбан (PLB), приводя к избыточному высвобождению кальция и его внутриклеточной аккумуляции. Кроме того, вирус может активировать внутренние деполяризующие токи (ICaL, INa) и одновременно подавлять реполяризующие (Ito, IKs, IKr), создавая дополнительный аритмогенный фон [18].
В постостром периоде COVID-19 ассоциация ФП с дилатационной кардиомиопатией и миокардитом с экспрессией энтеровирусов во всех случаях в нашей когорте может отражать особенности выборки. Тем не менее выявленные корреляции с интенсивностью CD68+ инфильтрации миокарда, экспрессией маркеров ангиогенеза и сохранением spike-белка SARS-CoV-2 в клетках воспалительного инфильтрата свидетельствуют о потенциальной роли персистирующего вирус-индуцированного воспаления в формировании аритмогенного субстрата. Эти данные позволяют предположить существование адаптивного механизма развития ФП у данной категории пациентов, опосредованного хронической иммунной активацией и процессами тканевой реорганизации. Также в ряде исследований было показано, что именно увеличение количества макрофагов в миокарде является отличительной чертой постострого периода вкупе с продолжающейся репарацией миокарда от последствий острого периода COVID-19 [19].
Считается, что цитокиновый дисбаланс, характерный для острого периода COVID-19, играет ключевую роль в формировании аритмогенного субстрата. Повышение уровня ангиотензина [20] инициирует паракринно-аутокринную активацию фибробластов, что приводит к избыточному синтезу коллагена, ремоделированию межклеточного матрикса и нарушению электрической однородности миокарда [14]. Вероятно, именно этот механизм обусловливает более высокий риск развития аритмий у пациентов с выраженной экспрессией Ang1, выявленной в нашем исследовании. Дополнительным фактором, поддерживающим аритмогенные изменения, может выступать персистенция вирусных антигенов в миокарде. Показано, что длительное присутствие патогенов, включая SARS-CoV-2, способствует хроническому воспалению и формированию устойчивого аритмогенного субстрата, резистентного к стандартной терапии и катетерной аблации [21]. Аналогичные явления описаны и при тяжёлом кризе гуморального отторжения трансплантата, сопровождающемся персистенцией антигенов SARS-CoV-2 [22][23]. Эти данные подтверждают гипотезу о потенцирующем влиянии коронавирусной инфекции как в остром, так и в постостром периодах на развитие нарушений ритма и проводимости, в основе которых лежит сочетание воспаления, фиброза и электрической дезорганизации миокарда.
С другой стороны, в соответствии с классической концепцией «atrial fibrillation begets atrial fibrillation» [24], даже кратковременные эпизоды ФП, возникающие на фоне острого периода инфекции, могут индуцировать рефрактерные изменения, укорочение длины волны и формирование зон re-entry. Этот эффект, в условиях сохраняющейся персистирующей экспрессии spike-белка и структурного дисбаланса коллагенового матрикса, может объяснять прогрессирование от пароксизмальной ФП в острой фазе к длительно персистирующей и постоянной форме на поздних этапах заболевания.
Полученные данные об экспрессии белков инфламмасомы NLRP3 и, в особенности, адаптерной молекулы TMS1/ASC в макрофагах воспалительного инфильтрата 1 пациента в постостром периоде, позволяют выдвинуть осторожное предположение о возможной роли активации инфламмасомы и пироптоза в патогенезе персистирующего повреждения миокарда. Полученные данные указывают на потенциально перспективное направление для будущих исследований [25]. Вероятный патогенетический механизм может заключаться в том, что персистенция антигенов SARS-CoV-2 инициирует хроническую активацию инфламмасомы NLRP3, что приводит к постоянному высвобождению провоспалительных цитокинов (таких как IL-1β и IL-18) через механизм пироптоза, тем самым поддерживая воспаление и дисфункцию миокарда даже после элиминации вируса. Подтверждение этой гипотезы на больших когортах пациентов может открыть новые перспективы для таргетной противовоспалительной терапии.
Таким образом, COVID-19 обладает возможностями многоуровневого воздействия на сердечно-сосудистую систему — от молекулярных нарушений ионного гомеостаза клеток до структурного ремоделирования миокарда. Наличие коморбидной сердечно-сосудистой патологии в сочетании с системным воспалительным ответом представляет собой значимый фактор риска развития ФП как в остром, так и в постостром периоде инфекции.
Особого внимания заслуживает необходимость раннего начала антиаритмической терапии именно в остром периоде заболевания. Промедление с восстановлением синусового ритма для таких пациентов может привести к усугублению морфологических изменений в миокарде и прогрессированию ФП до устойчивых форм, при которых вероятность успешного восстановления и поддержания синусового ритма существенно снижается.
Заключение
Проведенное исследование демонстрирует, что патогенез ФП на фоне COVID-19 имеет различные механизмы в остром и постостром периоде.
В остром периоде развитие ФП обусловлено преимущественно преморбидным фоном пациента. Ключевыми факторами риска являются наличие исходной сердечно-сосудистой патологии (ИБС, ХСН, СД), сопровождающейся ремоделированием миокарда и снижением ФВ ЛЖ, а также пожилой возраст. На этом фоне острая COVID-19, вызывая нарушение микроциркуляции, приводит к тромбозам интрамиокардиальных артерий и некрозам кардиомиоцитов, которые и служат непосредственным морфологическим субстратом для возникновения аритмии у большинства пациентов.
В постостром периоде патогенез ФП обусловлен неполной репарацией миокарда с макрофагальной инфильтрацией и персистенцией вируса.
Отношения и деятельность. Исследование выполнено за счёт и в рамках гранта «Изучение патогенеза миокардитов и перикардитов с позиции аутовоспаления и аутоиммунитета», руководитель НИР: Мячикова В. Ю. Номер гранта: 25-25-00337.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Макаров И.А., Гарькина C.В., Силкин М.С., Митрофанова Л.Б. Клинико-морфологическое исследование миокарда при фибрилляции предсердий в разные волны COVID-19 и постковидном периоде. Российский кардиологический журнал. 2025;30(4S):6705. https://doi.org/10.15829/1560-4071-2025-6705. EDN: DRYPMX
Скопировать