Успешное лечение пациентки с синдромом компрессии ствола левой коронарной артерии на фоне легочной артериальной гипертензии при ВИЧ-инфекции
Аннотация
Вирус иммунодефицита человека (ВИЧ) характеризуется медленным и последовательным поражением иммунной системы. За последние годы оно продемонстрировало рост заболеваемости в среднем на 10% в год. Однако в эпоху антиретровирусной терапии продолжительность жизни данной когорты пациентов увеличилась, в связи с чем акцент внимания сместился на осложнения, в т.ч. сердечно-сосудистые. В статье рассматривается клинический случай развития у пациентки с легочной артериальной гипертензией (ЛАГ) на фоне ВИЧ-инфекции редкого, тяжелого осложнения — синдрома компрессии ствола левой коронарной артерии дилатированным легочным стволом, с описанием успешного эндоваскулярного лечения, а также подбора ЛАГ-специфической терапии.
Легочная артериальная гипертензия (ЛАГ), ассоциированная с инфекцией вируса иммунодефицита человека (ВИЧ) — одна из редких форм легочной гипертензии (ЛГ) (0,4% по данным Национального регистра). Патогенез ЛАГ-ВИЧ в настоящее время требует более детального исследования, однако в литературе имеются данные о влиянии ВИЧ-связанных белков, таких как Tat, Nef, gp120, на развитие эндотелиальной дисфункции независимо от стадии ВИЧ-инфекции [1-7].
Говоря о синдроме сдавления ствола левой коронарной артерии (ЛКА) расширенным стволом легочной артерии (ЛА), необходимо отметить отсутствие достаточного количества описанных клинических случаев данного синдрома у пациентов с ЛАГ-ВИЧ. Частота его встречаемости среди других форм ЛГ также доподлинно неизвестна, тем не менее существуют данные о развитии вышеупомянутого синдрома у пациентов с идиопатической ЛГ, у больных ЛГ с врожденным пороком сердца, в частности при синдроме Эйзенменгера [8-11].
ЛАГ является тяжелым осложнением ВИЧ-инфекции и вносит свой, независимый от основного заболевания вклад в смертность данной группы пациентов. Формирование на ее фоне не менее грозного патофизиологического состояния — синдрома сдавления ЛКА дилатированным легочным стволом — может послужить причиной внезапной сердечной смерти. К сожалению, ныне не разработан общепринятый алгоритм ведения обсуждаемой категории пациентов. Что же касается хирургической тактики лечения, имеются отдельные, немногочисленные описания случаев эндоваскулярного лечения синдрома сдавления ствола ЛКА расширенным стволом ЛА. В качестве наглядного примера представляем клинический случай успешной транслюминальной баллонной ангиопластики со стентированием ствола ЛКА, на фоне подобранной ЛАГ-специфической терапии.
Описание клинического случая
Пациентка М., 40 лет, поступила в НМИЦК им. акад. Е. И. Чазова с жалобами на одышку и боль давящего характера в области грудной клетки при ходьбе на дистанцию менее 100 метров в обычном темпе, а также на общую слабость. Из анамнеза было известно, что пациентка впервые отметила появление одышки при подъеме по лестнице на несколько этажей в 2018г. Вскоре также стала отмечать появление отеков нижних конечностей, синкопальные состояния. В связи с чем была обследована по месту жительства, где была выявлена ЛГ, недостаточность трикуспидального клапана. Учитывая наличие анамнестических данных о повышении температуры тела до 39,0 C на догоспитальном этапе, клиническая картина была расценена как следствие перенесенного инфекционного эндокардита. Была назначена медикаментозная терапия (в т.ч. силденафил 60 мг/сут.), на фоне которой отметила улучшение самочувствия в виде уменьшения выраженности одышки и разрешения отечного синдрома. Больная была выписана в удовлетворительном состоянии.
В анамнезе у пациентки имеются сведения о наличии сопутствующих хронических вирусных инфекций: В 2004г диагностированы хронический гепатит C, а также ВИЧ-инфекция, в связи с чем проводилась этиотропная противовирусная терапия (лопинавир + ритонавир 200 мг + 50 мг 2 раза/сут., ламивудин — 300 мг 2 раза/сут., тенофовир — 300 мг 2 раза/сут.)
В феврале больная 2025г поступила в ФГБУ «НМИЦК им. акад. Е. И. Чазова» Минздрава России с ухудшением состояния.
Пациентка на фоне проведенной противовирусной терапии являлась реконвалесцентом (РНК гепатита С отрицательна с 04.2024), по поводу ВИЧ-инфекции также была достигнута стадия ремиссии на фоне антиретровирусной терапии (АРВТ) (РНК ВИЧ — 200 коп/мл, CD4-508 кл/мкл (23%) от 12.2024).
Лекарственная терапия на момент поступления в Кардиоцентр: ивабрадин — 2,5 мг 2 раза/сут., торасемида — 5 мг 1 раз/сут., силденафил — 20 мг 3 раза/сут., лопинавир + ритонавир 200 мг + 50 мг 2 раза/сут., ламивудин — 300 мг 2 раза/сут., тенофовир — 300 мг 2 раза/сут.
Состояние пациентки средней тяжести. Был проведен комплекс исследований, в данной статье отображены значимые результаты, которые позволили поставить окончательный диагноз.
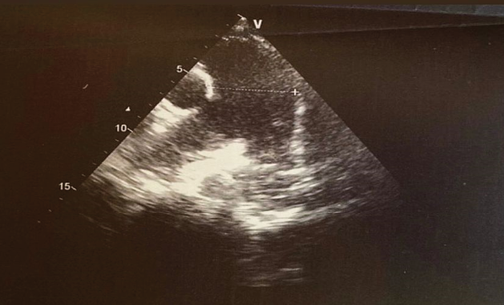
По данным эхокардиографии (ЭхоКГ) (табл. 1) обращало на себя внимание значимое расширение ствола ЛА (рис. 1), а также признаки высокой ЛГ.
Рентгенография органов грудной клетки: легочный рисунок видоизменен: периферический сосудистый рисунок обеднен. Нарушение легочной гемодинамики: артериальная ЛГ, значительно выраженная: резко расширен и выбухает ствол ЛА, увеличен коэффициент Мура — 42% (N 22-30%), увеличена выпуклость (высота) легочного сегмента — 12 мм (N 0-1мм).
- Корни легких: структурны, расширены: нисходящая ветвь правой ЛА — 20 мм, (N <15 мм (ж)); левая ЛА — 33 мм (N <24 мм).
- Сердце ротировано, расширено в поперечнике, выбухает легочный ствол. Кардиоторокальный индекс 62% (N ≤50%).
- Правопредсердный коэффициент 38% (N <30%).
Заключение: Изменения соответствуют высокой ЛАГ. Значительное расширение ствола ЛА. Кардиомегалия. Увеличение правых отделов сердца. Расширены верхняя полая и непарная вены.
Тест шестиминутной ходьбы не проводился, в связи с возникновением болей за грудиной при прохождении менее 100 метров.
Биохимический анализ крови на уровень N-концевого промозгового натрийуретического пептида 3 469,0 пг/мл.
Учитывая признаки высокой ЛГ, значительное расширение ствола ЛА по данным ЭхоКГ, а также жалобы пациентки на загрудинные боли ангинозного характера, была проведена чрезвенозная катетеризация правых отделов сердца и коронароангиография.
Результаты катетеризации (метод расчета: Фик):
- Систолическое давление в ЛА: 96 мм рт.ст.;
- Среднее давление в ЛА: 65 мм рт.ст.;
- Давление заклинивания в ЛА: 10 мм рт.ст.;
- SpO2артериальной крови: 98%;
- SvO2в ЛА: 56%;
- Сердечный выброс: 4,38 л/мин;
- Сердечный индекс: 2,88 л/мин/м2;
- Соотношение легочного кровотока к системному кровотоку (Qp/Qs): 1.0;
- Легочное сосудистое сопротивление: 19,6 Ед. Вуда.
По данным коронароангиографии была выявлена компрессия ствола ЛКА, суживающая просвет сосуда на 90% (рис. 2).
Таблица 1
ЭхоКГ данные
|
Правое предсердие |
Площадь =29 cм2 (N <18 см2) |
|
Правый желудочек |
• Передне-задний размер =3,9 см (N до 3,0 см) • Базальный размер =5,1 см (N до 4,2 см) • TAPSE =1,4 см (N ≥1,7 см) • Фракционное изменение площади =26% (N ≥35%) • Толщина передней стенки: 0,6 см (N <0,5 см) |
|
Межжелудочковая перегородка |
Движение парадоксальное (обусловленное перегрузкой правого желудочка) |
|
Легочная артерия |
Расширена • Ствол =3,2 см (N <2,7 см) • Правая ветвь =2,5 см (N до 1,5 см) • Левая ветвь =2,5 см (N до 1,5 см) |
|
Нижняя полая вена |
Расширена, 2,2/0,6 см (N=1,2-2,2 см). Коллабирует: >50% |
|
Систолическое давление в легочной артерии |
103 мм рт.ст. (N до 30 мм рт.ст.) |
|
Среднее давление в легочной артерии |
65 мм рт.ст. (N до 20 мм рт.ст.) |
|
Давление заклинивания легочной артерии |
11 мм рт.ст. (N до 15 мм рт.ст.) |
|
Максимальный систолический градиент на трикуспидальном клапане |
95 мм рт.ст. |
|
Клапанный аппарат (особенности) |
Признаки недостаточности: • Митрального: 1-2 ст. • Трикуспидального: 3 ст.; vena contracta =0,81 см; несколько эксцентричная струя, направлена под септальную створку • Лёгочного: 2 ст. |

Рис. 1. Признаки расширения ствола ЛА по данным ЭхоКГ.

Рис. 2. Компрессия ствола ЛКА, суживающая просвет сосуда на 90%.

Рис. 3. Данные ВСУЗИ.

Рис. 4. Данные МРК.

Рис. 5. Повторные данные ВСУЗИ.

Рис. 6. Данные ангиографии после эндоваскулярного лечения.

Рис. 7. Данные МРК после эндоваскулярного лечения.
Лечение
Больной в рамках ЛАГ-специфической терапии по жизненным показаниям был инициирован прием мацитентана 10 мг 1 раз/сут. [1]. Переносимость препарата удовлетворительная. Учитывая клиническую симптоматику и наличие гемодинамически значимого эксцентричного стеноза ствола ЛКА, принято решение о проведении транслюминальной баллонной ангиопластики со стентированием ствола ЛКА. С целью оценки протяженности поражения и определения оптимального размера стента было выполнено внутрисосудистое ультразвуковое исследование (ВСУЗИ). По данным ВСУЗИ минимальная площадь просвета в стволе ЛКА составила 5,35 мм2 (рис. 3).
Затем с целью верификации ишемии было выполнено исследование моментального резерва кровотока (МРК), по результатам которого в стволе ЛКА был выявлен градиент давления, МРК за местом стеноза составил 0,72, что подтверждает наличие ишемии (рис. 4).
Далее в место стеноза был установлен стент Resolute 4×12 мм, давлением до 20 атм., с достижением оптимального результата по данным ВСУЗИ — минимальная площадь раскрытия стента 12,76 мм2, что соответствует 100% раскрытию относительно референсного диаметра (рис. 5, 6).
Эндоваскулярное лечение прошло без осложнений. В качестве дезагрегантной терапии была назначена комбинированная терапия ацетилсалициловой кислотой 100 мг/сут., клопидогрелом 75 мг/сут. (рекомендована отмена через полгода). Прием препаратов не сопровождался нежелательными явлениями. Пациентка была выписана в удовлетворительном состоянии. Со слов, отметила улучшение клинического состояния.
Для контроля результатов стентирования было выполнено повторное МРК, по результатам которого, также удалось достичь оптимального результата МРК =0,96 (рис. 7).
Был рекомендован контроль уровня аланинаминотрансферазы, аспартатаминотрансферазы, общего билирубина, общего анализа крови 1 раз в 3 мес., а также динамическое наблюдение кардиологом и инфекционистом по месту жительства.
Обсуждение
ВИЧ-инфекция обладает высокой заболеваемостью и является большой угрозой для здоровья человечества. По данным Объединённой программы Организации Объединённых Наций по вирусу иммунодефицита человека/синдрому приобретенного иммунного дефицита человека (ЮНЭЙДС) в 2022г составило 39 млн (33,1-45,7 млн) человек. В настоящее время наблюдается увеличение продолжительности жизни данной группы пациентов, ввиду внедрения в клиническую практику АРВТ. В связи с чем фокус внимания сместился на осложнения, возникающие при данной патологии [2].
ЛГ у пациентов с ВИЧ встречается в 0,5% случаев, значимо увеличивая риск смертности. Однако стоит отметить, что истинная распространенность ЛГ у больных с ВИЧ может быть выше, т.к. в большую часть исследований не включались бессимптомные больные [12][13].
Синдром сдавления ствола ЛКА расширенным стволом ЛА впервые был описан Corday в 1957г [14][15]. С тех пор, к сожалению, так и не разработан алгоритм диагностики и выбора тактики лечения, в т.ч. хирургического.
Mehta NJ, et al. (2000) в своем обзоре 131 случая ЛАГ-ВИЧ описали частоту возникновения у пациентов с ЛАГ на фоне ВИЧ-инфекции жалоб на боль в груди, которая составила 7%, а также на одышку — 85% случаев [16][17]. Учитывая их неспецифичность (могут возникать как за счет гипертрофии правого желудочка, приводящей к ишемии миокарда, так и при ишемической болезни сердца, и при компрессии ствола ЛКА аневризмой ствола ЛА и т.д.), необходимо проводить дифференциальный диагноз, не забывая о таком редко встречающимся синдроме, как сдавление ствола ЛКА расширенным стволом ЛА, которое может привести к жизнеугрожающим последствиям [18][19], в т.ч. к внезапной сердечной смерти.
В результатах работы Galie N, et al. (2017) распространенность упомянутого синдрома у больных ЛАГ с клиникой стенокардии достигала порядка 50%. У 121 из 765 пациентов (16%) отмечались жалобы на боли за грудиной, среди них у 94 больных (78%) было обнаружено сдавление ствола ЛКА дилатированным стволом ЛА (по данным мультиспиральной компьютерной коронароангиографии (МСКТ)) [20-22]. К предикторам развития многие авторы относят диаметр ствола ЛА >40 мм [22][23]. Vaseghi M, et al. (2010) обнаружили, что пациенты с ЛГ низкого роста были более предрасположены к коронарной компрессии. В их серии наблюдений средний рост пациентов составлял 160 см (диапазон: 154-167 см). Предположительно коронарная компрессия связана с диаметром средостения [24]. Наша пациентка, рост которой составляет 152 см, также невысокого роста.
Данные неинвазивной диагностики (ЭхоКГ, МСКТ) могут позволить заподозрить синдром сдавления ствола ЛА, однако «золотым стандартом» для окончательной его диагностики является коронароангиография. Отдельно стоит отметить особенности диагностики стеноза ствола ЛКА при сужении просвета сосуда в связи с наличием атеросклеротической бляшки и при синдроме ствола ЛКА. При обследовании нормальной коронарной артерии с использованием ВСУЗИ обычно наблюдается характерное трехслойное изображение стенки сосуда, состоящее из адвентиции, медии и интимы, в то время как при атеросклеротическом поражении артерии внутри стенки сосуда визуализируются фиброзные, липидные или кальциевые включения, дифференцируемые между собой в зависимости от эхогенности [25]. Таким образом, при синдроме сдавления ствола ЛКА по данным ВСУЗИ наблюдается неизмененная структура коронарной артерии, однако внутренний просвет сужен за счет внешнего сдавления.
Решение о выборе тактики хирургического лечения должно быть коллегиальным, с учетом жалоб пациента, данных ЭхоКГ, холтеровского мониторирования, ангиографической картины с применением ВСУЗИ. Рассматривая данный вопрос в фокусе пациентов с ВИЧ-инфекцией, необходимо учитывать часто встречающуюся тромбоцитопению, а также лекарственное взаимодействие дезагрегантов с антиретровирусными препаратами, в частности ритонавиром [26].
В доступной литературе описаны случаи успешного эндоваскулярного лечения [8][14][15][21][27-31]. Отдельно стоит отметить, что применялись как голометаллические стенты (BMS), так и стенты с лекарственным покрытием (DES). Результаты разных авторов весьма противоречивы. Так, Ikegami R, et al. (2018) описали клинический случай успешной имплантации стента BMS больной с синдромом Эйзенмегера с последующим наблюдением в течение 6 мес. без нежелательных явлений [20]. Однако по данным Galiè N, et al. (2017), наблюдавших пациентов в течение 9 мес. после эндоваскулярного лечения, частота рестенозов отмечалась в 11% случаев [22]. Ряд авторов описывают сопоставимые результаты без признаков рестеноза стента, как при использовании BMS, так и DES стентов [11][18][19][23][24][27-30][32-34]. Наиболее длительным было трехгодичное наблюдение [20].
Таким образом, при выявлении у пациента с ЛАГ-ВИЧ клиники стенокардии, а также при обнаружении методами неинвазивного исследования (ЭхоКГ, МСКТ) расширения ствола ЛА диаметром >40 мм, стоит рассмотреть возможность проведения коронароангиографии для исключения редкого, но тяжелого осложнения — синдрома сдавления ствола ЛКА расширенным стволом ЛА.
Дальнейшая тактика хирургического лечения должна определяться в экспертном центре с учетом оперативных и геморрагических рисков, а также лекарственного взаимодействия дезагрегантов с АРВТ.
Заключение
ЛАГ является грозным осложнением ВИЧ-инфекции, на фоне которой, в связи с расширением легочного ствола, может встречаться редкий, жизнеопасный синдром сдавления ствола коронарной артерии дилатированным легочным стволом. В связи с отсутствием четких рекомендаций по тактике обследования и лечения данной категории больных, а также с учетом серьезных последствий, к которым он способен привести (в т.ч. к внезапной сердечной смерти), необходимо проведение дальнейших исследований с целью выработки единого алгоритма. На сегодняшний день возможно предположить, что коронароангиография с возможностью проведения ВСУЗИ может служить «золотым стандартом» диагностики в данном случае. Вопрос о применении метода хирургического лечения остаётся открытым, однако чрескожное коронарное вмешательство со стентированием может быть рассмотрено в качестве возможного и оптимального способа реваскуляризации миокарда. Следует подчеркнуть, что дилатация легочного ствола возникает, вероятней всего, при тяжелой, длительно текущей ЛГ, в связи с чем ранняя диагностика ЛАГ и своевременное инициирование ЛАГ-специфической терапии является важным компонентом не только в лечении ЛГ, но и в профилактике развития синдрома сдавления ЛКА.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Читанава В.Л., Гришин Н.С., Мартынюк Т.В., Меркулов Е.В., Терещенко А.С. Успешное лечение пациентки с синдромом компрессии ствола левой коронарной артерии на фоне легочной артериальной гипертензии при ВИЧ-инфекции. Клинический случай. Российский кардиологический журнал. 2025;30(2S):6451. https://doi.org/10.15829/1560-4071-2025-6451. EDN: OUFCEY
Скопировать







dutasteride tamsulosin tab
dutasteride tamsulosin tab
sémaglutide oral posologie
sémaglutide oral posologie
semaglutid köpa online
semaglutid köpa online