Хроническая тромбоэмболическая болезнь легких: status artium
Аннотация
Концепция хронической тромбоэмболической болезни легких (ХТЭБЛ) появилась в последние годы для описания пациентов со стойкими тромботическими поражениями легочных сосудов при наличии клинических симптомов, но отсутствии легочной гипертензии (ЛГ) в состоянии покоя. В зарубежной литературе ХТЭБЛ является всеобъемлющим термином, объединяющим всех симптомных пациентов с наличием посттромбоэмболического поражения легочных артерий по данным МСКТ-ангиопульмонографии и/или наличием дефектов перфузии при вентиляционно-перфузионной сцинтиграфии легких при отсутствии вентиляционных дефектов независимо от наличия ЛГ в покое. Российские эксперты сохранили исторический термин хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) для пациентов с ЛГ в покое. В данном обзоре мы рассмотрим ключевые положения о диагностике и лечении больных ХТЭБЛ без ЛГ.
Эпидемиология
Точные эпидемиологические данные о распространенности тромбоэмболии легочной артерии (ТЭЛА) в Российской Федерации отсутствуют. Ежегодно в развитых странах Европы и Северной Америки регистрируется от 39 до 115 новых случаев ТЭЛА и 53-115 случаев тромбозов глубоких вен на 100 тыс. взрослого населения [1].
Распространенность остаточного тромбоза через 6 мес. после ТЭЛА составляет от 16% до 69%. Вентиляционно-перфузионная сцинтиграфия имеет более высокую чувствительность, чем компьютерная томографическая (КТ) ангиография, для выявления стойкого легочного тромбоза, и поэтому считается методом первой линии в диагностике [2].
Определенная совокупность факторов может способствовать сохранению тромбоза легочной артерии (ЛА). Так, в ряде исследований описаны независимые предикторы остаточного тромбоза после неспровоцированной острой ТЭЛА после 6 мес. лечения антикоагулянтами [3-6], включая возраст старше 65 лет, курение и хронические респираторные заболевания [7, 8]. Повышенные уровни фактора VIII сосудистая обструкция (>25%) при остром эпизоде ТЭЛА также являются предикторами сохранения тромбоза [9][10].
Несколько исследований показывают, что ряд пациентов сообщают об ухудшении или сохранении исходной одышки в течение периода от 6 мес. до 3 лет после острого эпизода ТЭЛА. По данным Klok F, et al., более трети пациентов сообщают об ухудшении одышки через 3,5 года после острой ТЭЛА, и до 76% из них сообщают о появлении или ухудшении одышки после эпизода ТЭЛА [11]. Sanchez O, et al. [9] обнаружили, что у 30% пациентов наблюдались постоянные дефекты перфузии после ТЭЛА, что было связано с прогрессированием одышки и уменьшением дистанции, пройденной во время теста с 6-минутной ходьбой, а также с увеличением давления в ЛА (ДЛА), оцененного по данным эхокардиографии.
Хроническая тромбоэмболическая болезнь легких (ХТЭБЛ) как звено континуума от ТЭЛА к хронической тромбоэмболической легочной гипертензии (ХТЭЛГ)?
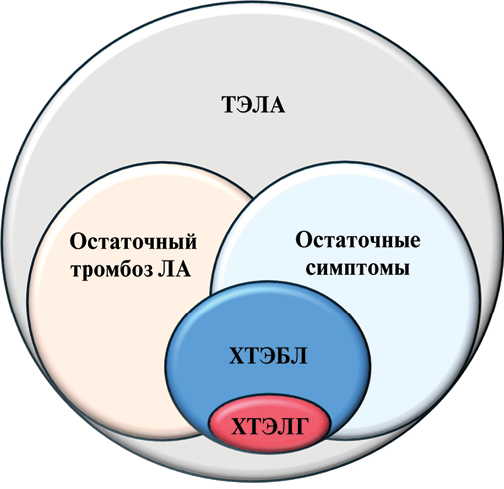
Спектр последствий ТЭЛА варьируется от стойкого бессимптомного тромбоза ЛА до ХТЭЛГ (рис. 1).
ХТЭЛГ, наиболее серьезное осложнение ТЭЛА, характеризуется обструктивным ремоделированием ЛА вследствие ТЭЛА, сопровождающимся развитием легочной гипертензии (ЛГ). Совокупная заболеваемость ХТЭЛГ составляет 0,1-9,1% в течение первых 2 лет после эпизода симптомной ТЭЛА [3-5]. Хотя и ежегодная заболеваемость ХТЭЛГ неизвестна, некоторые данные по распространенности указывают на то, что это заболевание может возникать у 5 человек на миллион населения в год. При дифференциальной диагностике ХТЭЛГ следует исключать другие возможные варианты обструкции ЛА, такие как саркома ЛА, эмболия опухолевыми клетками, паразитические (эхинококкозные кисты), эмболии инородными телами, врожденные или приобретенные стенозы ЛА.
Однако определение ХТЭЛГ не включает подгруппу пациентов, у которых есть жалобы на одышку при нагрузке и/или функциональные ограничения, которых у них не было до ТЭЛА, и у которых есть остаточный тромбоз, но нормальное ДЛА в состоянии покоя [1]. У этих пациентов облитерация, вызванная постоянным тромбозом, считается причиной легочной сосудис- той дисфункции, которая проявляется в первую очередь как непереносимость физических нагрузок [12]. Патофизиологический механизм этой дисфункции, ее клинические и терапевтические последствия, а также факторы риска, определяющие неспособность разрешения тромба, недостаточно изучены и в настоящее время изучаются. Рекомендации ESC/ERS 2022г декларируют снижение порога для определения ЛГ до среднего давления в ЛА (срДЛА) >20 мм рт.ст. (с легочным сосудистым сопротивлением (ЛСС) >3 ед. Вуда) [13], а это означает, что у пациентов, ранее диа- гностированных с ХТЭБЛ, теперь может быть диагностирована ХТЭЛГ. В работе Held M, et al. определение ЛГ по уровню срДЛА >20 мм рт.ст. вместо ≥25 мм рт.ст. приводит к относительному увеличению частоты диагностики ХТЭЛГ на 23,5%. Также следует отметить, что большая часть литературы по проблеме ХТЭЛГ, включая алгоритмы лечения, основана на предыдущих гемодинамических определениях [14].
В любом случае, у пациентов с ХТЭБЛ наблюдаются симптомы и ограниченная толерантность к физической нагрузке, обусловленные дисфункцией легочных сосудов. Она проявляется во время физических нагрузок, поэтому диагностические тесты, проводимые в состоянии покоя, часто находятся в пределах нормы, поскольку им не хватает чувствительности для выявления легочной васкулопатии. Однако изменения во время нагрузки у пациентов с ХТЭБЛ достаточно схожи с изменениями, которые наблюдаются у пациентов с ХТЭЛГ [15][16].
Соответственно, ХТЭБЛ — это состояние, которое возникает в результате персистенции тромбов в легочном сосудистом русле, что приводит к легочной васкулопатии, которая ограничивает растяжимость легочного сосудистого русла и приводит к неэффективности вентиляции во время физических нагрузок. Таким образом, основанием для диагноза ХТЭБЛ служит, с одной стороны, наличие остаточного тромбоза в ЛА, и, с другой стороны, должна быть подтверждена дисфункция легочных сосудов в виде неэффективности вентиляции по данным эргоспирометрии [17]. Эргоспирометрия демонстрирует модель сердечно-сосудистого ограничения толерантности к физической нагрузке (снижение пикового потребления O2, ранний анаэробный порог, сниженный кислородный пульс), сопровождающуюся признаками неэффективности вентиляции из-за сосудистой облитерации (повышенный наклон VE/VCO2, повышенный эквивалент CO2 и сниженный PETCO2 на анаэробном пороге). При сравнении пациентов с ХТЭЛГ и ХТЭБЛ — у пациентов с ХТЭЛГ наблюдалось повышение срДЛА >20 мм рт.ст. в состоянии покоя, тогда как срДЛА в покое было нормальным у пациентов с ХТЭБЛ. Однако при физической нагрузке срДЛА увеличивалось непропорционально сердечному выбросу при ХТЭБЛ. Также наблюдалось небольшое увеличение ЛСС при физической нагрузке вместо снижения, как у здоровых лиц [12]. Это может быть результатом патологической реакции сосудов малого круга кровообращения при физической нагрузке. Из-за хронической тромбоэмболической обструкции не происходит достаточного рекрутирования и расширения легочных сосудов при физической нагрузке, что приводит к повышению ДЛА при увеличении сердечного выброса. Это может быть причиной симптомов при физической нагрузке у таких пациентов.
При частоте возникновения 5,75% в течение 2 лет после ТЭЛА ХТЭБЛ, по-видимому, встречается так же часто, как и ХТЭЛГ с частотой 5,25% [14][15].
Данные мультиспиральной КТ могут помочь также в проведении дифференциальной диагностики пациентов с ХТЭБЛ и ХТЭЛГ. В работе Capone C, et al. [18] по данным мультиспиральной КТ у пациентов с ХТЭБЛ наблюдалась сосудистая обструкция, аналогичная таковой у пациентов с ХТЭЛГ, но без КТ-признаков ЛГ, мозаичных участков повышенной плотности легких и с меньшим распространением дефектов перфузии на йодной карте. Не было получено данных о поражении дистального русла у пациентов с ХТЭБЛ, что может быть одной из причин отсутствия ЛГ в покое у этих пациентов (рис. 2).
Более простые методы диагностики также могут быть полезны в дифференциальной диагностике этих двух состояний [19]. Так, в работе Блиновой Е. В. и др. [20] оценивались изменения электрической оси сердца (ЭОС) на вдохе у больных с ХТЭЛГ и ХТЭБЛ. В группе без ЛГ (срДЛА <20 мм рт.ст.) на вдохе во всех случаях происходило отклонение ЭОС правее исходного положения. В группе с ХТЭЛГ в 33 (48%) случаях на вдохе ЭОС смещалась правее исходного положения, а в 36 (52%) случаях — левее. Разница значений ЭОС на свободном дыхании и на вдохе имела достоверные прямые корреляционные связи умеренной силы с ДЛА и ЛСС. Для ответа на вопрос, можно ли с использованием значений ЭОС на свободном дыхании и ее изменений на вдохе разделить подгруппы с наличием и отсутствием ЛГ был проведен ROC-анализ. Результаты анализа показали, что с чувствительностью 62-65% и специфичностью 100% возможно разделение этих подгрупп.
После изменения уровня срДЛА для выявления ЛГ, в литературе до сих пор нет четких критериев для диагностики ХТЭБЛ и его выявления после ТЭЛА. На рисунке 3 представлен адаптированный под современное определение ЛГ, алгоритм наблюдения за пациентами после перенесенной ТЭЛА, для выявления ХТЭБЛ, предложенный Ramírez P, et al. в 2020г [1].
У симптомных пациентов с остаточным тромбозом, предпочтительно выявленным с помощью вентиляционно-перфузионной сцинтиграфии, следует выполнить эхокардиографию для получения информации о вероятности наличия ЛГ. Если вероятность высокая, следует выполнить катетеризацию правых отделов сердца; если низкая, необходимо провести эргоспирометрию. При выявлении картины ограниченной толерантности сердечно-сосудистой системы к физической нагрузке с критериями неэффективности вентиляции, целесообразно выполнить катетеризацию правых отделов сердца во время нагрузки. Диагноз ХТЭБЛ следует устанавливать в случаях с срДЛА <20 мм рт.ст. в покое или >30 мм рт.ст. наряду с ЛСС >3 ед. Вуда во время физической нагрузки.
Подходы к лечению ХТЭБЛ
Подходы к лечению пациентов с ХТЭБЛ в настоящее время четко не регламентированы. Исключение составляет антикоагулянтная терапия, которую пациенты с ХТЭБЛ должны принимать неопределенно долго, так же как и пациенты с ХТЭЛГ [4][5][13].
Остается неясным, являются ли пациенты с ХТЭБЛ отдельной нозологией или у них будет наблюдаться прогрессирование в сторону ХТЭЛГ, и может ли раннее оперативное/эндоваскулярное вмешательство предотвратить это прогрессирование. Однако недавнее исследование [21] проанализировало естественное течение ХТЭБЛ у 113 пациентов, не обнаружив существенного прогрессирования заболевания в течение медианного периода наблюдения в 37 мес., что позволяет предположить, что быстрое прогрессирование может не быть типичной особенностью в этой группе больных.
Согласно действующим рекомендациям, операция легочной тромбэндартерэктомии (ЛЭЭ) является стандартом лечения пациентов с ХТЭЛГ. Однако у пациентов с ХТЭБЛ данные ограничены. Исследование 2014г, проведенная ЛЭЭ у пациентов с ХТЭБЛ и имплантированным кава-фильтром, продемонстрировало снижение срДЛА с 21 до 18 мм рт.ст., увеличение теста шестиминутной ходьбы с 372 до 421 м, снижение ЛСС со 164 до 128 дин/с/см-5 и улучшение функционального класса [22]. Послеоперационные осложнения возникли у 40% пациентов (тампонада сердца, субдуральная гематома и др.). Два пациента умерли после выписки, что привело к смертности 5%. Исследование 2018г с участием 23 пациентов показало схожие результаты и характеристики выживаемости [23].
Баллонная легочная ангиопластика (БАП) ЛА продемонстрировала благоприятные эффекты в улучшении функционального состояния и физической работоспособности у пациентов с ХТЭБЛ в работе Kiko T, et al. [24]. В отличие от предыдущих работ [25-27], здесь была низкая частота осложнений БАП ЛА у пациентов с ХТЭБЛ, что обнадеживает. Однако данное исследование не показало существенных различий в прогнозе пациентов с ХТЭБЛ, которым была проведена и не проведена БАП ЛА. Таким образом, основной целью проведения БАП ЛА для пациентов с ХТЭБЛ может быть облегчение симптомов, а не улучшение прогноза.
Назначение специфической терапии легочной артериальной гипертензии у пациентов с ХТЭБЛ не рекомендовано с учетом отсутствия вовлеченности в патологический процесс дистального легочного русла и отсутствия точки приложения специфической терапии.
Реабилитация может быть полезной для всех симптомных пациентов, перенесших ТЭЛА, в т.ч. и для пациентов с ХТЭБЛ для повышения переносимости физических нагрузок. К сожалению, большинство исследований не различают пациентов с функциональными нарушениями после ТЭЛА, ХТЭБЛ и ХТЭЛГ, что затрудняет анализ результатов наблюдения. Исследование 27 пациентов (после ТЭЛА, но без ХТЭЛГ) продемонстрировало улучшение по опросникам оценки качества жизни и улучшение функционального состояния, уменьшения симптомов после 12-нед. программы реабилитации [28].

Рис. 1. Спектр осложнений, возникающих после ТЭЛА.
Сокращения: ЛА — легочная артерия, ТЭЛА — тромбоэмболия легочной артерии, ХТЭБЛ — хроническая тромбоэмболическая болезнь легких, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.

Рис. 2. Субтракционная КТ-ангиопульмонография. Перфузионные карты.
Примечание: йодные карты показывает большую степень дефектов перфузии (черные области) при ХТЭЛГ (Б), чем при ХТЭБЛ (А).

Рис. 3. Алгоритм диагностики ХТЭБЛ.
Сокращения: В/П сцинтиграфия легких — вентиляционно-перфузионная сцинтиграфия легких, ДЗЛА — давление заклинивания в легочной артерии, КПОС — катетеризация правых отделов сердца, ЛГ — легочная гипертензия, ЛСС — легочное сосудистое сопротивление, срДЛА — среднее давление в легочной артерии, ТЭЛА — тромбоэмболия легочной артерии, ХТЭБЛ — хроническая тромбоэмболическая болезнь легких, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Заключение
Стойкие тромботические поражения после перенесенной ТЭЛА отмечаются у 16-69% больных, по данным литературы. Клинический спектр, связанный с этими поражениями, широк и варьирует от бессимптомного течения с полным функциональным восстановлением до ХТЭЛГ. Термин «ХТЭБЛ» пока не стал отдельной нозологической единицей, он предложен для описания подгруппы пациентов с стойкими тромботическими поражениями, у которых есть симптомы при нагрузке и легочная сосудистая дисфункция, но нет ЛГ в покое.
В плане терапии эксперты сходятся во мнении о необходимости пожизненного приема антикоагулянтной терапии. В отношении ЛЭЭ в настоящее время отсутствуют данные, позволяющие оценить соотношение риска и пользы для данной группы пациентов, особенно учитывая, что сама операция является достаточно травматичной.
Проведение БАП ЛА должно решаться в индивидуальном порядке для улучшения переносимости физических нагрузок.
Требуются дополнительные исследования для уточнения диагностических критериев, оптимизации стратегий лечения и улучшения долгосрочных результатов.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Валиева З.С., Остраух А.В., Мартынюк Т.В. Хроническая тромбоэмболическая болезнь легких: status artium (обзор литературы). Российский кардиологический журнал. 2025;30(2S):6455. https://doi.org/10.15829/1560-4071-2025-6455. EDN: VPWTDH
Скопировать




semaglutide ozempic 0.25 mg
semaglutide ozempic 0.25 mg
finns semaglutid naturligt
finns semaglutid naturligt
sildenafil monitoring parameters
sildenafil monitoring parameters
doxycycline 100mg price at clicks
doxycycline 100mg price at clicks
doxycycline hyclate dosage for cats
doxycycline hyclate dosage for cats