Современный взгляд на фенотипы легочной гипертензии
Аннотация
За последние годы были достигнуты значительные успехи в понимании патогенеза различных типов легочной гипертензии (ЛГ), усовершенствованы диагностические подходы и лечебные алгоритмы. Рост распространенности ЛГ в мире связан с демографическими изменениями, в частности с увеличением доли пожилого населения и изменениями образа жизни. Прошедшие три десятилетия ознаменовались кардинальным изменением фенотипа пациентов с легочной артериальной гипертензией (ЛАГ), что связано с постарением населения и верификацией диагноза в более старшей возрастной группе с наличием обширной коморбидной патологии. Несмотря на свою относительную редкость, ЛАГ представляет собой значительную проблему для здравоохранения во всем мире, т.к. наблюдается рост заболеваемости и распространенности ЛАГ. В свою очередь, это может свидетельствовать о повышении осведомленности и своевременной диагностике заболевания, с чем связано и снижение глобальной смертности от ЛАГ.
В обзоре отражены современные подходы к классификации и фенотипированию пациентов с ЛГ, изложены мировые тенденции распространенности и прогноза заболевания, а также обсуждены новые тенденции в разработке персонифицированных подходов к лечению различных фенотипов пациентов с ЛАГ.
Легочная гипертензия (ЛГ) — гетерогенная группа заболеваний, приводящих к повышению легочного сосудистого сопротивления (ЛСС) и устойчивому повышению давления в легочной артерии (ДЛА), что отражается в выраженном структурно-функциональном нарушении правого желудочка (ПЖ) и неблагоприятном прогнозе пациентов.
Изучение ЛГ началось в 1865г с описания J. Klob сужения мелких легочных артерий (ЛА) и артериолосклероза при анализе аутопсийного материала. Спустя 26 лет E. Romberg на аутопсии описал склероз ЛА без патологии сердца и легких. Только в начале XXв A. Ayerza впервые клинически охарактеризовал болезнь молодого пациента с тяжелыми симптомами сердечной недостаточности (СН), цианозом и полицитемией, с быстрым наступлением смерти. Данная болезнь получила имя ее первооткрывателя. В настоящее время это заболевание, как и прежде является орфанным и называется идиопатическая легочная артериальная гипертензия (ИЛАГ) [1].
Прорыв в диагностике ЛГ случился в 1956г, когда W. Forssmann, первостепенно испытав на себе, совместно с американскими коллегами разработал метод катетеризации правых отделов сердца (КПОС). Данная разработка была удостоена Нобелевской премии и инициировала эру новых диагностических открытий [1].
На сегодняшний день ЛГ является глобальной про- блемой здравоохранения, поражая ~1% населения планеты. В возрастной группе 65 лет и старше ее распространенность достигает 10%, что связано с высокой частотой сердечно-легочной коморбидности у данной категории пациентов. Распространенность и заболеваемость ЛГ значительно варьируют в зависимости от клинической группы и типа заболевания. Ведущими причинами возникновения ЛГ по всему миру остаются патологии левых отделов сердца (до 80% всех пациентов с ЛГ) и заболевания легких. В очень редких случаях ЛГ представлена не как синдром, ассоциированный с различными заболеваниями сердца и сосудов или респираторной патологией, а как самоcтоятельная нозология (ИЛАГ). Независимо от этиологии, прогрессирование заболевания тесно связано с декомпенсацией ПЖ, что приводит к увеличению риска смерти [2-4].
Своевременная верификация ЛГ остается до сих пор сложной задачей из-за многоликих этиологических факторов, разнообразия фенотипов ЛГ и роста бремени сопутствующих заболеваний.
Представленная в национальных и зарубежных рекомендациях [2-4] классификация ЛГ основана на распределении пациентов на 5 групп в зависимости от этиологии заболевания:
- Так, к первой группе относится легочная артериальная гипертензия (ЛАГ), патофизиология которой представлена пролиферативной васкулопатией с поражением легочного артериального сосудистого русла. ЛАГ встречается среди всех групп ЛГ примерно у 11,4% [5].
- ЛГ, связанная с заболеваниями левых отделов сердца (группа 2, изолированная посткапиллярная или комбинированная пост-/прекапиллярная ЛГ) наблюдается у 48,7% пациентов среди всех групп с ЛГ [5]. Формирование группы 2 ЛГ основано на пассивной обратной передаче повышенного давления в левом предсердии в легочное венозное русло. ЛГ данной группы представлена различными фенотипами левожелудочковой СН на фоне ее систолической, диастолической дисфункции, приобретенной патологии клапанов сердца или кардиомиопатий. К тому же, характер коморбидного статуса (кардиоренальный или метаболический фенотип СН с сохранной фракцией выброса (ФВ) левого желудочка (ЛЖ), сопутствующие заболевания бронхолегочной системы) вносит особый вклад в утяжеление течения имеющейся посткапиллярной ЛГ и ее возможную трансформацию в комбинированную пост-/прекапиллярную ЛГ [6].
- К группе 3 относится ЛГ, связанная с паренхиматозными заболеваниями легких и/или гипоксией, формирование которой основано на гипоксической вазоконстрикции и облитерации сосудов легких. Данная группа наблюдается у 33,5% среди всех групп ЛГ [5].
- ЛГ вследствие обструкции ЛА, в т.ч. хроническая тромбоэмболическая ЛГ (группа 4), патогенез которой основывается на ограничении и перераспределении артериального легочного кровотока организованным тромботическим материалом, имеет место у 6,4% среди всех форм [5].
- Отсутствуют эпидемиологические данные о ЛГ группы 5, которая включает в себя гематологические заболевания, метаболические и системные нарушения, сложные врожденные пороки сердца и др. Это обусловлено многофакторным патогенезом имеющейся ЛГ у данной группы, что может характеризоваться в ряде случаев как прекапиллярным типом, так и посткапиллярным типом ЛГ [2-5].
В дальнейшем особое внимание представляется важным уделить пациентам с ЛАГ (группа 1), бремя которой неуклонно растет на фоне старения населения и увеличения числа сопутствующих болезней. Как следствие, кардинально меняется и ранее привычный фенотип пациентов с ЛАГ.
Динамика фенотипа пациентов с ЛАГ за последние 30 лет
В начале 1990-х годов для «фенотипа» пациентов с ЛАГ наблюдалась четкая закономерность: большинство пациентов были молодыми женщинами в возрасте от 20 до 50 лет, чаще всего без какой-либо сопутствующей сердечно-легочной патологии. Три десятилетия назад весьма редко встречались пациенты с верифицированным диагнозом ЛАГ и избыточной массой тела или с артериальной гипертензией (АГ) в анамнезе [7].
В 2010г в зарубежных регистрах средний возраст пациентов с ЛАГ уже составил 52,5 года [8]. Анализ европейского регистра COMPERA отмечает увеличение доли пациентов с ЛАГ старше 65 лет, которая достигает 64% при соотношении женщин и мужчин 2,3:1 [9].
Согласно анализу данных Российского регистра по проблеме ЛАГ за период с 2012 по 2019гг, отмечено, что 40,9% впервые выявленных случаев среди ЛАГ приходятся на ее идиопатическую форму [2][3][10]. Наиболее частыми причинами ассоциированных форм являются врожденные пороки сердца (простые системно-легочные шунты; 36,6%) и системные заболевания соединительной ткани (19,3%) [2][3][10]. При этом уникальный фенотип пациентов с ИЛАГ и наследственной формой ЛАГ с наличием положительного теста на вазореактивность имеет место только у 8,6% пациентов. Среди пациентов с ЛАГ 83% являются лицами женского пола [3]. Диагноз ЛАГ устанавливается в среднем возрасте 45,2 года, что выше, чем 38 лет назад, когда по данным регистра Национального института здоровья в США средний возраст пациента с ИЛАГ был ~35 лет [2][3][7][10].
Помимо увеличения числа пациентов с ЛАГ старших возрастных групп, на территории Российской Федерации также наблюдается рост сопутствующих сердечно-легочных заболеваний среди пациентов с ЛАГ, таких как АГ (до 42%), ожирение (до 38%), сахарный диабет 2 типа (СД) (14%), и ишемическая болезнь сердца (ИБС) (до 12%) [2][3][10].
Бремя ЛАГ в мире
За последние три десятилетия во всем мире наблюдается небольшой рост заболеваемости и распространенности ЛАГ, в то время как показатели количества лет с поправкой на инвалидность и смертность по причине ЛАГ снизились.
Распространенность и заболеваемость ЛАГ существенно варьируют в зависимости от социально-экономического уровня страны. В экономически развитых странах распространенность ЛАГ может достигать 55 случаев на 1 млн. человек, а заболеваемость — около 6 случаев на 1 млн. взрослого населения [4].
Несмотря на свою относительную редкость, ЛАГ представляет собой значительную проблему для здравоохранения во всем мире. При анализе глобального бремени ЛАГ в мире в 2021г число случаев ЛАГ составило 2,28 на 100 тыс. населения, заболеваемость выросла до 0,52 на 100 тыс., а уровень смертности от ЛАГ составил 0,27 случаев смерти на 100 тыс. населения [11]. На 2021г в мире было зарегистрировано 192 тыс. случаев ЛАГ, из них 62% у женщин и 38% у мужчин. Умерло по причине ЛАГ за 2021г — 22 тыс. человек [12].
При анализе периода с 1990 по 2021гг в глобальном масштабе темп роста распространенности ЛАГ составляет примерно 3,2% в год. Рост распространенности ЛАГ в мире связан с демографическими изменениями, в частности с увеличением доли пожилого населения и изменений образа жизни. Важно отметить, что наибольшая распространённость наблюдалась у лиц в возрасте 75-79 лет (7,99 на 100 тыс.), что связано с наличием кумулятивных факторов риска, ответственных за снижение эластичности сосудов и более выраженное ремоделирование легочного сосудистого русла (АГ, СД, ожирение, хроническая обструктивная болезнь легких и т.д.) [11-14].
Несмотря на более высокую распространенность ЛАГ среди женщин, смертность была одинаковой среди женщин и мужчин: 0,28 смертей от ЛАГ на 100 тыс. женщин (0,22-0,34) и 0,27 смертей от ЛАГ на 100 тыс. мужчин (0,21-0,33) в 2021г [11][12].
Половой парадокс при ЛАГ — более высокая распространенность среди женщин, но более высокая летальность среди мужчин — хорошо известен, но не полностью объяснен и может быть связан с половыми гормонами, поведением в отношении здоровья и различиями в адаптации ПЖ [15].
Однако в странах с высоким социально-экономическим индексом отмечается тенденция к снижению распространенности ЛАГ, что может быть связано с более эффективной диагностикой и лечением болезни, а также улучшением работы системы здравоохранения. В свою очередь, снижение глобальной смертности и бремени болезней свидетельствует об улучшении верификации диагноза и лечения ЛАГ. Рост заболеваемости и распространенности ЛАГ во всем мире может свидетельствовать также о повышении осведомленности и своевременной диагностике заболевания.
Среди 21-го региона мира в 2021г самые низкие стандартизированные по возрасту показатели распространенности ЛАГ были отмечены в Южной Азии: 1,71 на 100 тыс. населения. Напротив, самый высокий стандартизированный по возрасту показатель распространенности ЛАГ наблюдался в Западной Европе: 3,56 на 100 тыс. населения. В Восточной Европе стандартизированный по возрасту показатель распространенности ЛАГ составил от 2,4 до 3,1 на 100 тыс. населения [12].
Также к 2021г отмечается повышение распространенности правожелудочковой СН, связанной с ЛАГ, до 191808 случаев, а количество лет, прожитых с инвалидностью, — с 9788 до 17765 случаев. Хотя общий показатель количества прожитых лет с поправкой на инвалидность по причине ЛАГ снизился до 8,24 на 100 тыс. населения [11].
Сравнивая с данными 1990г, глобальная заболеваемость ЛАГ к 2021г увеличилась с 0,302 на 100 тыс. человек в 1990г до 0,329 на 100 тыс. человек в 2021г, при средней предполагаемой частоте заболеваний 0,27%. Распространенность заболевания также несколько увеличилась: с 1,56 на 100 тыс. человек в 1990г до 1,62 на 100 тыс. человек в 2021г. Напротив, показатель количества лет с поправкой на инвалидность, связанной с ЛАГ, снизился за тот же период с 5,30 на 100 тыс. человек в 1990г до 4,04 на 100 тыс. человек в 2021г. Аналогичным образом, глобальный показатель смертности от ЛАГ снизился с 0,0832 на 100 тыс. человек в 1990г до 0,0634 на 100 тыс. человек в 2021г, при средней продолжительности жизни — 0,89% [11][12][16].
Бремя ЛАГ сохраняется из-за старения и роста населения, несмотря на снижение стандартизированных по возрасту показателей. Дальнейшие меры должны учитывать региональные и демографические различия в заболеваемости ЛАГ. Глобальный анализ прогнозирует рост распространенности ЛГ до 2050г, обусловленный демографическими изменениями и ростом сопутствующих заболеваний [12][16].
Изменение гемодинамических критериев ЛГ: обоснование
Важно отметить, что анализ глобальной распространенности ЛАГ в мире на 2021г был сделан на момент существования не обновленных критериев ЛАГ: среднее давление в ЛА (срДЛА) ≥25 мм рт.ст. и ЛСС >3 ед. Вуда, что подразумевает вероятное занижение полученных показателей распространенности заболевания.
Впервые на 6-м всемирном конгрессе по ЛГ (2018г, Ницца) было предложено изменить гемодинамические критерии заболевания со снижением ранее привычных значений срДЛА с ≥25 мм рт.ст. до >20 мм рт.ст. и ЛСС с 3 ед. Вуда до 2 ед. Вуда [17]. И уже в 2022г в рекомендациях Европейского общества кардиологов [4], в 2023г в рекомендациях Евразийской ассоциации кардиологов [3] и с 2024г в национальных рекомендациях, одобренных Минздравом России [2], внесены изменения в гемодинамическое определение ЛГ. Так, согласно КПОС, обновленные критерии ЛАГ представлены в виде значения срДЛА >20 мм рт.ст., ЛСС >2 ед. Вуда и уровня давления заклинивания ЛА (ДЗЛА) ≤15 мм рт.ст., характеризующего прекапиллярный тип ЛГ. В свою очередь, пациентов с изолированной посткапиллярной ЛГ характеризует следующая гемодинамическая картина: срДЛА >20 мм рт.ст., ДЗЛА >15 мм рт.ст., а ЛСС ≤2 ед. Вуда. Тогда как повышение ЛСС >2 ед. Вуда при посткапиллярном типе ЛГ подразумевает присоединение прекапиллярного компонента и формирование комбинированной пост-/прекапиллярной ЛГ.
Изменения гемодинамических критериев ЛГ объясняются доказательствами, что даже умеренное увеличение ДЛА и ЛСС ассоциируется с ухудшением выживаемости и функционального состояния пациентов [18][19].
Так, результаты Великобританского исследования EVIDENCE-PAH демонстрируют, что новая гемодинамическая классификация ЛГ с понижением порогов для срДЛА и ЛСС выявляет значительное число пациентов с умеренным повышением этих показателей, у которых наблюдается ухудшение выживаемости независимо от наличия сопутствующих сердечно-легочных заболеваний [19]. У пациентов с умеренно повышенным срДЛА (21-24 мм рт.ст.) или умеренно повышенным ЛСС (>2, но ≤3 ед. Вуда) выживаемость была ниже, чем у пациентов с нормальным срДЛА (<21 мм рт.ст.) и нормальным ЛСС (≤2 ед. Вуда). Умеренное повышение срДЛА и умеренное повышение ЛСС являются независимыми предикторами выживаемости с поправкой на сопутствующие заболевания сердца и легких (отношение шансов (ОШ) 1,33, 95% доверительный интервал (ДИ): 1,01-1,75, p=0,042 и ОШ 1,4, 95% ДИ: 1,06-1,86, p=0,019, соответственно). При этом у 68,2% пациентов с умеренным повышением срДЛА имела место сопутствующая сердечно-легочная патология [19].
Очевидно, изменение гемодинамических критериев повлияло и на увеличение распространенности пациентов с ЛГ на фоне патологии левых камер сердца: на 10% изолированной посткапиллярной формы, а на 60% комбинированной пост-/прекапиллярной формы ЛГ [12][18].
Фенотипирование ЛАГ за пределами имеющейся клинической и гемодинамической классификации
За последние три десятилетия кардинально изменился «портрет» пациентов с ЛАГ. Первостепенно это связано с постарением населения и верификацией диагноза в более старшей возрастной группе, с обширной коморбидной патологией, включающей не только компоненты метаболического синдрома, но и сопутствующие сердечно-легочные заболевания [20][21]. Условия проживания, урбанизация, образ жизни, стрессогенные факторы являются одними из причин меняющегося портрета данных пациентов. В клинической практике каждый пациент с ЛГ является уникальным случаем, характеризующимся разнообразием не только этиологических факторов, но и коморбидным фоном, особенностей ремоделирования правых камер сердца и выраженности нарушения гемодинамики и ремоделирования легочного артериального сосудистого русла, что и является основными составляющими фенотипа пациента [21].
Именно поэтому считается, что для полноценного понимания течения заболевания и ответа на терапию нельзя ограничиваться только распределением пациентов на 5 групп в зависимости от имеющейся этиологической классификации ЛГ, как и распределением ЛГ по типам гемодинамики (превалирования пре- или посткапиллярного компонента). Так как этио- логическая составляющая ЛГ и характер нарушения гемодинамики малого круга кровообращения являются лишь одними из составляющих сложного и до сих пор динамически меняющегося фенотипа пациентов.
В работе профессора Hoeper MМ подчеркнута важность различий между гемодинамической классификацией и фенотипированием пациентов с ЛГ, ввиду ограничений использования такого показателя, как ДЗЛА в дифференциации форм заболевания. Подчеркивается важность клинико-патофизиологических фенотипов для более точного управления пациентами с ЛГ, что полностью соответствует современной тенденции персонификации терапии [22].
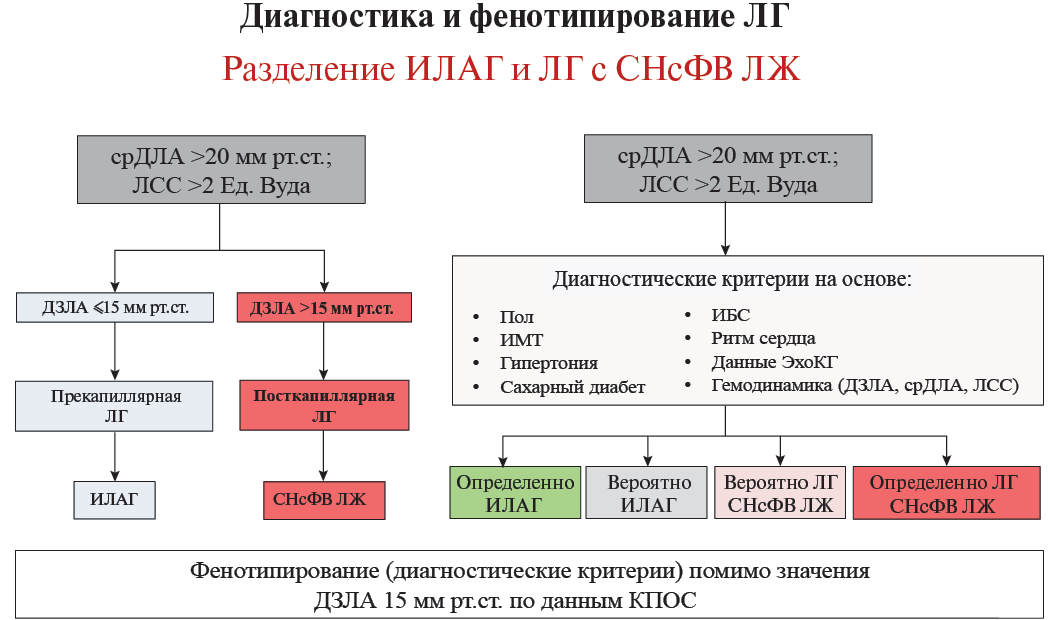
Такие сопутствующие заболевания, как ожирение, АГ, СД и ИБС, обычно связаны с поражением левых отделов сердца, особенно с СН с сохранной ФВ (СНсФВ) ЛЖ [6][22][23]. Поэтому на фоне меняющейся демографической ситуации, а также расширении коморбидного статуса пациентов с ЛГ с присоединением факторов кардиоваскулярного риска актуальным становится вопрос корректной дифференциальной диагностики ИЛАГ и ЛГ на фоне СНсФВ ЛЖ (рис. 1).

Рис. 1. Диагностика и фенотипирование ЛГ за пределами гемодинамических критериев (адаптировано из Hoeper MM [22]).
Сокращения: ДЗЛА — давление заклинивания легочной артерии, ИБС — ишемическая болезнь сердца, ИМТ — индекс массы тела, ИЛАГ — идиопатическая легочная артериальная гипертензия, КПОС — катетеризация правых отделов сердца, ЛГ — легочная гипертензия, ЛСС — легочное сосудистое сопротивление, СНсФВ ЛЖ — сердечная недостаточность с сохранной фракцией выброса левого желудочка, срДЛА — среднее давление в легочной артерии, ЭхоКГ — эхокардиография.
Пороговое значение ДЗЛА в 15 мм рт.ст., которое разграничивает прекапиллярную и посткапиллярную ЛГ, является краеугольным камнем современной диагностической классификации. По мнению профессора Hoeper MM, использование бинарного порогового значения ДЗЛА не учитывает динамическую природу ЛГ, особенно у пациентов с СНсФВ ЛЖ. Корректировка порогового значения или дальнейшая стандартизация измерений ДЗЛА сами по себе не решат эту проблему, как и использование водной нагрузки или оценки гемодинамики с физической нагрузкой [22]. Более того, важно не упускать из виду возможность некорректной оценки уровня ДЗЛА при инвазивной диагностике и получении его неистинного значения.
Rayner SG, et al. [24] предложили ввести «зону неопределенности» для значений ДЗЛА между 12 и 18 мм рт.ст. Значения <12 мм рт.ст. указывают на прекапиллярную ЛГ, тогда как значения >18 мм рт.ст. предполагают посткапиллярную ЛГ. Предполагается, что дополнительные клинические данные, включая анамнез, характер сопутствующей патологии, эхокардиографические (ЭхоКГ) данные с оценкой диастолической функции ЛЖ, должны быть определяющими при дифференциальном диагнозе ИЛАГ и СНсФВ ЛЖ, когда ДЗЛА попадает в диапазон «неопределенности». Однако установление зоны неопределенности также подразумевает области относительной уверенности (ДЗЛА <12 и >18 мм рт.ст.), но даже данный диапазон значений ДЗЛА может не быть абсолютно надежными [24].
Важно отметить, что при физических нагрузках, гипертонических кризах или при перегрузке жидкостью эпизодическое повышение ДЗЛА может приводит к ремоделированию сосудов легких и ЛГ. При этом на поздних стадиях ввиду тяжести ЛГ может быть ограничен легочный кровоток, что приводит к псевдонормализации ДЗЛА.
Рандомизированные клинические исследования не показали пользы ЛАГ-специфической терапии для пациентов с ЛГ и ДЗЛА >15 мм рт.ст. Однако данные для пациентов с ДЗЛА ≤15 мм рт.ст. и факторами риска заболеваний левых отделов сердца (при ЛАГ и сердечно-легочной коморбидности) остаются также менее однозначны, чем при ЛАГ без коморбидности [2-4]. До сих пор данный фенотип пациентов не изучался в рандомизированном контролированном исследовании как отдельная группа, и имеющиеся данные об эффективности/безопасности специфической терапии получены только в рамках ретроспективного анализа для больных с ЛАГ и 3 и более сердечно-легочными коморбидными состояниями. Следовательно, многие пожилые пациенты с заболеванием левых отделов сердца, но ДЗЛА ≤15 мм рт.ст., вероятно, неправильно классифицируются и лечатся как имеющие ИЛАГ с сердечно-легочной коморбидностью, несмотря на недостаточность доказательств пользы и потенциальных рисков терапии [25].
Профессор Hoeper MM предлагает в ряде случаев руководствоваться не именно гемодинамическим критерием ДЗЛА, а первоначально критериями, определяющими высокую вероятность СНсФВ ЛЖ, основываясь на клинических данных, наличии и характере коморбидных состояний, ЭхоКГ показателях, и рассматривать вариант диагноза ЛГ на фоне СНсФВ ЛЖ, даже если КПОС демонстрирует уровень ДЗЛА ≤15 мм рт.ст. (рис. 1) [22]. Критерии, на основании которых оценивается патология левых камер сердца как первостепенная причина имеющейся ЛГ у пациента, детально представлены в Национальных клинических рекомендациях по проблеме ЛГ [2].
Потенциально формирование комплексной системы оценки типа ЛГ, включающей фенотипические данные, такие как возраст, сопутствующие заболевания, данные ЭхоКГ и характера ремоделирования сердца, гемодинамику, включая ДЗЛА, могут совершенствовать имеющуюся классификацию и обеспечить корректную постановку диагноза, а, как следствие, персонифицированный и верный выбор тактики лечения.
Функция ПЖ как составляющая фенотипа пациента с ЛАГ
Предлагается еще один подход к фенотипированию пациентов с ЛГ с использованием оценки характера структурно-функциональных нарушений ПЖ в качестве зеркала тяжести состояния и прогрессирования заболевания.
По данным двумерной ЭхоКГ оценка таких параметров систолической функции ПЖ, как фракционное изменение площади ПЖ (отражающего радиальный компонент сокращения ПЖ) и систолической экскурсии кольца трикуспидального клапана — TAPSE (отражающую продольное смещение ПЖ от основания до верхушки) является неотъемлемой частью комплексного протокола ЭхоКГ для пациентов с ЛГ. Снижение показателя фракционного изменения площади ПЖ <35%, а величины TAPSE <1,7 см считается нарушением систолической функции ПЖ. Несмотря на имеющуюся сильную корреляцию величины TAPSE с значением ФВ ПЖ по данным магнитно-резонансной томографии (МРТ) сердца, имеется ряд ограничений в трактовке полученных значений данного параметра [26].
Сложная геометрия ПЖ и его ретростернальное расположение в принципе затрудняют достоверную визуализацию ПЖ. Более того, зависимость величины TAPSE от угла наклона и ориентации датчика, оценка только продольной, а не глобальной функции ПЖ при анализе величины TAPSE требуют расширения стандартного ЭхоКГ протокола с добавлением дополнительных параметров оценки глобальной функции ПЖ [26].
Согласно обновленным европейским и национальным рекомендациям по проблеме ЛГ, оценка TAPSE также представляется важным компонентом при анализе сердечно-сосудистого сопряжения (ССС) ПЖ/ЛА, представленного в виде отношения TAPSE к величине расчетного СДЛА. Величина TAPSE/рСДЛА <0,35 ассоциируется с увеличением риска смерти в 10 раз у пациентов с СН. Тогда как для пациентов с ЛАГ при уровне TAPSE/рСДЛА ≤0,32 риск летального исхода в течение года составляет как минимум 5-20% [2][27].
Оценка глобальной продольной деформации свободной стенки ПЖ, согласно ЭхоКГ, является параметром, более полно отражающим глобальную дисфункцию ПЖ. Значение данного параметра >20% отражает наличие дисфункции ПЖ, тогда как его величина >15% говорит о тяжелых нарушениях функции ПЖ [28]. Важно отметить, что данный показатель в меньшей степени зависит от угла наклона датчика и характера перегрузки ПЖ, и является более воспроизводимым, чем TAPSE, при этом он может выявлять субклиническую дисфункцию, имеет сильную корреляцию с ФВ ПЖ по данным МРТ сердца и имеет доказанную прогностическую ценность [29].
Использование трехмерной ЭхоКГ в оценке состояния ПЖ становится все более доступной методикой, используемой не только в рамках научных протоколов, но и в клинической практике. Ведь именно с помощью трехмерной ЭхоКГ возможна оценка геометрии и функции ПЖ (объемы, ФВ ПЖ, расчет сердечного выброса), а также морфологии трикуспидального клапана. Величина ФВ ПЖ по данным ЭхоКГ имеет сильную корреляцию с ФВ ПЖ по данным МРТ сердца. Значение ее <45% говорит о наличии дисфункции ПЖ [26].
С помощью трехмерной ЭхоКГ также возможна оценка такого показателя, как ССС ПЖ-ЛА. Поддержание нормального ССС улучшает механическую и метаболическую эффективность сердечно-сосудистой системы. Для оценки ССС ПЖ-ЛА с помощью трехмерной ЭхоКГ требуется анализ эффективной жесткости ЛА (представлена в виде формулы: (срДЛА — ДЗЛА)/ударный объем ПЖ), а также анализ конечно-систолической жесткости ПЖ (отношение срДЛА к конечно-систолическому объему ПЖ). Само ССС ПЖ/ЛА в дальнейшем рассчитывается как отношение эффективной жестокости ЛА к конечно-систолической жесткости ПЖ [30]. Данный маркер продемонстрировал себя в качестве важного диагностического компонента при оценке эффективности проводимой терапии для пациентов с ИЛАГ [31].
К ограничениям использования трехмерной ЭхоКГ относятся зависимость от хорошего качества изображения (до 25% случаев не поддаются оценке), регулярная частота сердечных сокращений, потребность в специальном дорогостоящем оборудовании и программном обеспечении, опыт врача, проводящего измерения и трактовку результатов.
Как по данным трансторакальной ЭхоКГ, так и по МРТ сердца оценка таких показателей, как глобальная продольная деформация ПЖ, ФВ ПЖ, сопряжение ПЖ-ЛА, и сердечный индекс, остается важной для определения тяжести ремоделирования сердца и динамического ответа на терапию.
Экспериментальные исследования подчеркивают важность глубокого фенотипирования ПЖ с помощью метода МРТ и машинного обучения для понимания компенсаторного и дезадаптивного ремоделирования ПЖ при ЛГ. Данный метод позволяет выделять группы пациентов с разной скоростью прогрессирования и риском СН [32]. Изучение по данным МРТ сердца таких маркеров, как усиление внеклеточного объема в точках прикрепления ПЖ и межжелудочковой перегородки может служить важными интегративными маркерами тяжести заболевания. Данные показатели одни из первых значимо реагируют на перегрузку ПЖ и служат МРТ-индикаторами адаптации и дезадаптации ПЖ, представляя значительный потенциал для оценки эффекта терапевтических вмешательств, направленных на улучшение функции ПЖ [32].
Выполнение МРТ сердца в динамике пациентам с ЛАГ может быть важным подспорьем в своевременном обнаружении субклинической дисфункции ПЖ даже у пациентов низкого риска летального исхода, что будет способствовать своевременной эскалации/оптимизации терапии, а, как следствие, достижению целей лечения [33][34].
Фенотипически обоснованные подходы к выбору ЛАГ-специфической терапии
Современные исследования указывают на значительное улучшение показателей выживаемости благодаря совершенствованию подходов к диагностике и лечению ЛАГ. Так, с момента верификации диагноза однолетняя выживаемость при ИЛАГ составляет 95,8%, а пятилетняя выживаемость пациентов с ИЛАГ достигает 86,8%, что значительно выше исторических данных (36% выживаемость за 5 лет наблюдения 1980-х гг) [35][36].
На территории Российской Федерации на сегодняшний день используются в клинической практике у пациентов с ЛАГ семь ЛАГ-специфических препаратов: ингибиторы фосфодиэстеразы типа 5 (силденафил, тадалафил), антагонисты эндотелиновых рецепторов (бозентан, мацитентан, амбризентан), стимулятор растворимой гуанилатциклазы (риоцигуат) и препараты, влияющие на путь простациклина (ингаляционный илопрост и пероральный селексипаг). Залогом успеха терапии пациента с ЛАГ является достижение низкого риска летального исхода (<5%) согласно шкале стратификации риска, представленной в современных национальных рекомендациях [2].
Несмотря на изменения гемодинамических критериев ЛАГ согласно обновленным национальным [2] и европейским рекомендациям [4] подход к инициации ЛАГ-специфической терапии для пациентов с ЛГ группы 1 (ЛАГ) первостепенно основан на присутствии значений срДЛА ≥25 мм рт.ст., ЛСС ≥3 ед. Вуда, и подтверждению прекапиллярного компонента ЛГ (ДЗЛА ≤15 мм рт.ст.) согласно данным КПОС. Это обусловлено наличием доказательной базы эффективности и безопасности ЛАГ-специфической терапии, основанной на предыдущих гемодинамических критериях диагноза.
Наличие фенотипических характеристик течения ЛАГ подразумевает использовать в каждом конкретном случае строгий персонифицированный подход к выбору тактики лечения и тщательному динамическому наблюдения за переносимостью терапии и ее эффектом [21].
Первым шагом при определении стратегии лечения является отнесение пациента к одной из пяти клинических групп и, как следствие, к одному из гемодинамических подтипов ЛГ. Ранее подход к выбору стратегии лечения большинства пациентов с ЛАГ определялся в зависимости от наличия или отсутствия положительной острой фармакологической пробы, и в дальнейшем выбор типа и объема ЛАГ-специфической терапии основывался на риске летального исхода на момент верификации диагноза и при динамическом наблюдении [37].
Современный подход к выбору тактики ЛАГ-специфического лечения основывается еще на одном из принципиально важных критериев — наличие или отсутствие сердечно-легочной коморбидности при ЛАГ. Особое внимание акцентируется на присутствии именно трех и более сердечно-легочных состояний повышенного риска наличия патологии левых камер сердца (которые способны скомпрометировать ЛЖ и возможное нарастание посткапиллярного компонента ЛГ). К таким состояниям относят: АГ, СД, ИБС, ожирение, фибрилляцию предсердий или наличие патологии легких в сочетании с диффузионной способностью легких по монооксиду углерода (DLCO) <45% [2-4].
Данные об эффективности и безопасности ЛАГ-специфической терапии у пожилых пациентов с ЛАГ и ≥3 сердечно-легочными коморбидностями получены только при проведении анализов ретроспективных регистров или post-hoc анализов проводимых рандомизированных клинических исследований, поэтому эффект и безопасность как начальной комбинированной, так и последовательной трехкомпонентной комбинированной терапии у данных пациентов изучена недостаточно [38].
Вне зависимости от риска летального исхода согласно современным рекомендациям на момент верификации диагноза данным пациентам назначается монотерапия представителем класса ингибиторов фосфодиэстеразы тип 5 или антагонистов эндотелиновых рецепторов, основываясь на ограниченных данных о комбинированной терапии в этой растущей популяции [2-4][14]. При динамическом наблюдении в зависимости от эффекта терапии и ее переносимости, динамики компенсации или декомпенсации сопутствующих состояний, подход к выбору типа и объема ЛАГ-специфической терапии у пациентов с ЛАГ и ≥3 сердечно-легочными коморбидностями определяется в индивидуальном порядке в стенах экспертного центра [2-4].
Важно отметить, что в принципе отнесение к той или иной группе ЛГ для ряда пациентов может быть проблематичным, поскольку до 40% пациентов имеют смешанную этиологию. Более того, опора на клинические характеристики и показатели малоэффективна для определения целей лечения и разработки новых препаратов для лечения ЛГ.
В исследовании Boucly А, et al. [39] продемонстрировано использование плазменного протеома для кластеризации пациентов с ЛГ вне зависимости от ее этиологии, выявляя новые молекулярные паттерны, которые коррелируют с клиническими фенотипами и прогнозом. Эти данные открывают новые горизонты в понимании индивидуальных механизмов заболевания и способствуют развитию таргетированных терапевтических подходов.
На сегодняшний день основное внимание высокопроизводительной протеомики плазмы (несколько тысяч циркулирующих белков, секретируемых из тканей) было уделено выявлению ключевых циркулирующих маркеров прогрессирования заболевания или ответа на лечение у пациентов именно с ЛАГ (группа 1). Предполагается, что углубленное молекулярное профилирование, применяемое к более широкой популяции пациентов с клиническим диагнозом ЛГ различных групп, является лучшим подходом к разработке таргетных методов лечения ЛГ. Профиль белков плазмы может помочь не только дифференцировать пациентов с ЛАГ от здоровых лиц, но и предоставить информацию для предсказания прогноза пациентов с ЛАГ, а также стать молекулярным инструментом для раскрытия патофизиологического разнообразия ЛГ.
Согласно исследованию Boucly А, et al., вне зависимости от клинической классификации ЛГ при протеомном профилировании было выделено 4 белковых кластера. В качестве доказательства принципа персонификации лечения, направленного на идентифицированные дисрегуляторные пути патогенеза ЛГ, были исследованы известные лекарственные мишени: пути тромбоцитарного фактора роста (PDGF) и трансформирующего фактора роста-β (TGF-β). Путь PDGF был повышен в кластере 3. Этот путь давно вовлечен в патогенез ЛГ из-за его роли в опосредованном ремоделировании сосудов и пролиферации гладкомышечных клеток ЛА. Путь PDGF остается активным интересом в качестве терапевтической мишени. Было показано, что пероральный иматиниб (ингибитор тирозинкиназы) улучшает гемодинамику и толерантность к физической нагрузке при ЛГ. Потенциально кластер 3 может быть использован для выявления подгруппы пациентов, у которых преимущества ингибирования тирозинкиназы перевешивают потенциальные побочные эффекты [39].
Аналогично, выявленное повышение активности пути TGF-β в кластере 1 может указывать на группу пациентов, которым, вероятно, будет эффективно назначение сотатерцепта — лигандная ловушка представителей семейства TGF-β (активна А и B, GFF-11). Генетические, а теперь и фармакологические исследования сотатерцепта подчеркивают важность пути TGF-β при ЛГ. Его нарушение регуляции связано с эндотелиальной дисфункцией, воспалением и фиброзом в легочных сосудах [40]. Считается, что сотатерцепт, полученный из рецептора активина типа IIA, восстанавливает баланс сигнала костного морфогенетического белка (BMP)-TGF-β при ЛГ [41]. Использование протеомного профилирования из кластера 1 может позволить персонифицировано использовать препарат для тех пациентов, у которых он потенциально будет эффективен [39].
Таким образом, лечение может быть направлено на конкретные молекулярные драйверы, нарушенные у каждого пациента, и улучшить баланс эффективности/побочных эффектов, присущий каждому препарату (рис. 2).

Рис. 2. Аспекты персонификации терапии на основании фенотипирования пациентов с ЛАГ.
Примечание: Терапия А, B, С — варианты подходов к специфической терапии в зависимости от фенотипа пациента на основании проведение комплексного фенотипирования с использованием клинических и инструментальных данных, биомаркеров крови и омиксного глубокого фенотипирования.
Сокращения: ЛАГ — легочная артериальная гипертензия, КПОС — катетеризация правых отделов сердца.
ДЗЛА является основным гемодинамическим показателем у пациентов с ЛГ, отражающим задействование венозного или артериального легочного сосудистого русла.
Протеомное профилирование также может идентифицировать пациентов, отнесенных к другим клиническим группам ЛГ (т.е. за пределами группы 1), у которых потенциально могут быть эффективны препараты, воздействующие на дисрегуляторные пути PDGF и TGF-β [39].
Дифференциальная экспрессия путей PDGF и TGF-β в протеомных кластерах знаменует собой новую эру персонализированной терапии ЛГ для каждого фенотипа пациентов.
При выборе характера ЛАГ-специфической терапии важно учитывать не только этиологический фактор развития ЛГ и ее гемодинамический тип, но и демографический и коморбидный статус пациента, статус курения или приема лекарственных средств, риски межлекарственных взаимодействий, возможности лекарственного обеспечения и потенциальную комплаентность пациента к терапии [21].
Таким образом, ЛГ остается значимой проблемой здравоохранения с возрастающей распространенностью. Современные изменения в классификации и диагностике, интеграция данных фенотипирования и молекулярного анализа способствуют лучшему пониманию патогенеза и совершенствованию подходов к разработке персонифицированной терапии.
Крайне важна в достижении целей лечения и улучшении прогноза пациентов с ЛГ эффективная организация медицинской помощи, которая может быть реализована только при обеспечении преемственности на всех уровнях здравоохранения. Для этого необходимы слаженная маршрутизация, быстрая диагностика, координация между региональными и федеральными экспертными центрами, а также подготовка специалистов, обладающих знаниями и опытом ведения пациентов с ЛГ [42]. Такой комплексный и системный подход способствует сокращению времени от верификации диагноза до инициации терапии, снижению числа госпитализаций и улучшению качества жизни пациентов с тяжелыми формами ЛГ в Российской Федерации.
Заключение
За последние три десятилетия заболеваемость ЛАГ возросла благодаря появлению современных диагностических инструментов и повышению осведомленности о заболевании. Рост распространенности ЛАГ связан с постарением населения с верификацией диагноза в более старшей возрастной группе, с обширной коморбидной патологией. В то же время смертность от ЛАГ снизилась благодаря достижениям в области медицинских технологий и ранней диагностики. В то время как страны с высоким уровнем дохода, обладающие развитыми системами здравоохранения, способны диагностировать и лечить ЛАГ на более ранних стадиях и более эффективно. В отличие от этого, страны с низким и средним уровнем дохода сталкиваются с такими проблемами, как задержка диагностики и нехватка ресурсов для лечения, что подчеркивает необходимость целенаправленных мер от здравоохранения для снижения глобального бремени ЛАГ.
Значимые изменения «портрета» пациентов с ЛАГ за тридцать лет подразумевают использование новых подходов к фенотипированию пациентов, основанных не только на оценке этиологии и характере гемодинамических нарушений, но и на особенностях ремоделирования сердца, демографических характеристиках и коморбидном статусе пациентов, а также омиксном фенотипировании. Комплексный анализ фенотипа пациента позволит разработать персонифицированные подходы к выбору терапии ЛГ, а, как следствие, улучшению прогноза пациентов и их качества жизни.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Ляпина И.Н. Современный взгляд на фенотипы легочной гипертензии (обзор литературы). Российский кардиологический журнал. 2025;30(2S):6701. https://doi.org/10.15829/1560-4071-2025-6701. EDN: IUHKND
Скопировать