Артериальная гипертензия при метаболическом синдроме
Аннотация
В статье проанализированы современные представления о патогенезе, диагностике и влиянии на прогноз артериальной гипертензии тела при метаболическом синдроме. Приведен обзор современных возможностей диагностики, немедикаментозной и медикаментозной терапии артериальной гипертензии, а также сердечно-сосудистых преимуществах препаратов, используемых для терапии артериальной гипертензии на фоне метаболического синдрома.
Диагностика и лечение артериальной гипертензии (АГ) у лиц с метаболическим синдромом (МС) проводится в соответствии с действующими клиническими рекомендациями [1], поэтому представляется целесообразным более подробно остановиться на важных особенностях коррекции повышенного артериального давления (АД) у этого фенотипа пациентов.
Эпидемиология
Существует положительная линейная корреляция между индексом массы тела (ИМТ) и риском развития гипертонии, которая прослеживается уже c подросткового возраста [2].
Повышение АД — один из наиболее часто встречающихся компонентов МС [3]. У лиц среднего возраста с избыточной массой тела вероятность развития АГ на 50% выше, чем у тех, кто имеет нормальный вес. По данным эпидемиологических исследований прибавка в весе на каждые 4,5 кг приводит к повышению систолического АД на 4,2-4,4 мм рт.ст. [4].
В исследовании Pressioni Arteriose Monitorate E Loro Associazioni (PAMELA) study АГ имела место более чем у 80% пациентов с МС, причем в этой группе имело место повышение риска общей смертности [5]. Важно отметить, что в этом исследовании у пациентов без МС, но при наличии у них маскированной АГ, АГ «белого халата» и просто АГ при наблюдении в течение 10 лет отмечалась более высокая частота возникновения МС [6].
В исследовании Progetto Ipertensione Umbria Monitoraggio Ambulatoriale (PIUMA) study у 34% пациентов с АГ имелся МС в сочетании с повышенным риском развития сердечно-сосудистых осложнений (ССО) [7]. В крупном исследовании French population study частота развития МС возрастала по мере повышения уровня АД [8].
Особенности патогенеза
Ключевыми механизмами повышения АД при МС являются инсулинорезистентность (ИР), повышение активности ренин-ангиотензин-альдостероновой системы (РААС) и симпатоадреналовой системы (САС) [2][9-12], задержка натрия [13]. Это происходит на фоне изменения активности предсердного натрийуретического пептида [14][15].
ИР вызывает активацию САС (один из механизмов увеличения частоты сердечных сокращений), РААС (за счет ангиотензина II (АТ II)) и уменьшает продукцию оксида азота [16-19]. Другими важными механизмами патогенеза АГ при МС являются активация системы гипоталамус-надпочечники, повышение уровня лептина, нарушение барорефлекторной регуляции и синдрома обструктивного апноэ сна (СОАС) [13][16][20]. При избыточной массе тела и ожирении усилена реабсорбция натрия в почках [21] и негативное влияние на почки висцеральных жировых отложений [22-26].
ИР. ИР способствует повышению уровня АД за счет влияния на активность центральной симпатической нервной системы и РААС [27], задержки натрия почками [28] и уменьшения инсулин-опосредованной вазодилатации [29].
Воспаление. С-реактивный белок (СРБ) преимущественно образуется в печени в ответ на интерлейкин-6 (ИЛ-6), интерлейкин-1β, фактор некроза опухоли-α (ФНО-α), является маркером системного воспалительного процесса и также может быть использован для оценки сердечно-сосудистого риска (ССР) и эффективности вмешательств [30]. Ряд исследований продемонстрировал связь между повышенным уровнем СРБ, повышением АД [31] и развитием АГ [32]. У относительно здоровых людей повышение пульсового АД на 10 мм рт.ст. ассоциировано с повышением уровня СРБ на 12-15% [33].
Адипонектин продуцируется адипоцитами и обладает противовоспалительными и антиатерогенными свойствами, а также модулирует обмен липидов и углеводов [34]. Чем ниже уровень адипонектина, тем выше уровень систолического АД [35].
Снижение уровня адипонектина наблюдается при ожирении, АГ, ишемической болезни сердца, сахарном диабете (СД) 2 типа и является предиктором риска развития ишемической болезни сердца и инфаркта миокарда [36-38].
ФНО-α не только является маркером воспаления, но и связан с развитием ИР и таким образом влияет на уровень АД [39]. ИЛ-6 имеет положительную корреляцию с ССР, ишемической болезнью сердца, инсультом и сердечной недостаточностью (СН) [40].
Активация РААС. Жировая ткань обладает собственной РААС и адипоциты синтезируют все ее компоненты, активируют рецепторы АТ II, повышая их аффинность к паракринному АТ II [2][41]. Доказана прямая взаимосвязь между уровнем АТ II, активностью ренина, ангиотензинпревращающего фермента плазмы и альдостерона с ИМТ [42][43].
Активация САС. Повышение активности САС от центрального до рецепторного уровня является следствием ИР, лептинорезистентности, повышения уровня АТ II, свободных жирных кислот, внутрипочечного давления и активации почечных механорецепторов и нарушения барорефлекторной регуляции [44-50].
Нарушения барорефлекторной регуляции тесно связаны с изменением уровня лептина [51][52] и активностью рецепторов глюкагоноподобного пептида 1 [53].
Лептинорезистентность. Лептин, секретируемый адипоцитами, обладает прессорным эффектом [54][55] за счет периферической вазоконстрикции, задержки натрия и повышения уровня адренокортикотропного гормона, кортизола и альдостерона [56]. Также лептин активирует рецепторы гипоталамуса для регуляции энергетического баланса через снижение аппетита и повышение энерготрат за счет активации САС [57]. При избыточной массе тела стимулирующий эффект лептина на активность САС в значительной мере обусловлен активацией АТ II [58].
СОАС. Ассоциация между избыточной массой тела, обструктивным апноэ сна и АГ, особенно резистентной АГ, хорошо известна [59]. СОАС играет одну из ведущих ролей в повышения АД или отсутствия его снижения в ночное время и связано с повышением риска ССО (особенно инсульта) и общей смертностью. Всем пациентам с ожирением рекомендуется проведение суточного мониторирования АД (оценка АД в ночное время) и ночной оксиметрии. Снижение веса ассоциировано со снижением степени тяжести СОАС (определяется по значению индекса апноэ-гипопноэ — количество дыхательных событий за час сна) [60]. ИМТ является важным независимым показателем степени десатурации кислорода при СОАС [61][62]. При наличии храпа и СОАС уменьшение массы тела на 10% от исходной может улучшить параметры дыхания на 50%, что сопровождается переходом в более легкую степень тяжести заболевания. В ряде случаев при неосложненном храпе достаточно уменьшить массу тела на 5-7% для того, чтобы полностью устранить храп без каких-либо прочих вмешательств. Кроме того, снижение веса может способствовать снижению риска ССО, хотя крупномасштабные контролируемые исследования по этому вопросу отсутствуют [59]. Эффективным вмешательством для уменьшения выраженности обструктивного апноэ сна является РАР (ПАП)-терапия (неинвазивная вентиляция легких с созданием положительного давления в дыхательных путях (Positive Airway Pressure)), помимо этого, она незначительно (на 1-2 мм рт.ст.) снижает АД [63][64]. РАР (ПАП)-терапия показана при любой форме СОАС при наличии симптомов дневной сонливости, а также выявленных при обследовании коморбидных заболеваниях (АГ, ишемической болезни сердца или нарушения мозгового кровообращения в анамнезе) [65]. Существуют данные о положительном влиянии данного метода терапии на уровень ИР при МС в сочетании с СОАС, а также о возможном влиянии на риск сердечно-сосудистых событий [66][67]. В случае непереносимости или отказа от РАР (ПАП)-терапии необходимо рассмотреть вопрос о назначении ортодонтического лечения апноэ сна или позиционной терапии для взрослых пациентов с МС и СОАС [68][69].
Особенности течения
Наличие МС является независимым фактором риска плохого контроля АД [70]. В исследовании Global Cardiometabolic Risk Profile in Patients with Hypertension Disease (GOOD) study менее трети пациентов с МС достигли целевого уровня АД <140/90 мм рт.ст. [71].
При этом у пациентов с МС имеется более выраженное поражение органов-мишеней (гипертрофия левого желудочка (ГЛЖ), развитие диастолической дисфункции миокарда, повышение сосудистой жесткости, альбуминурия, ретинопатия, увеличение толщины комплекса интима-медиа сонной артерии) [72-76].
Особенности диагностики
При окружности плеча >32 см необходимо использовать манжеты большего размера, в т.ч. при проведении суточного мониторирования АД. Для измерения АД у пациентов с МС необходима манжета большого размера (L) (32-42 см) или комбинированная манжета среднего и большого размера (M/L) (22-42 см). Размер манжетки тонометра должен соответствовать окружности плеча: охватывать не менее 80% окружности и не менее 40% длины плеча. В таблице 1 представлены особенности ведения пациентов при МС в рамках развития континуума от АГ к СН.
Таблица 1
Особенности ведения пациентов с МС в рамках развития континуума от АГ к СН
|
Характеристики АГ у пациентов с метаболическими нарушениями в континууме: ожирение → МС → СД → СНсФВ |
Влияние на тактику ведения |
|
Увеличенная окружность плеча |
Измерение АД с использованием манжеты большего размера (обычно обозначается L (32-42 см) или комбинация двух размеров M-L (22-42 см)) |
|
Более выраженное повышение систолического АД, высокое пульсовое давление |
Комбинированная терапия практически у всех пациентов, начало лечения с двух препаратов |
|
Повышенная вариабельность АД |
Использование препаратов длительного действия |
|
Повышенное ночное АД, отсутствие ночного снижения АД |
Применение препаратов длительного действия. Адекватная терапия тиазидоподобными диуретиками, антагонистами минералокортикоидных рецепторов и при необходимости петлевыми диуретиками. Профилактика и лечение СОАС |
|
Солечувствительность АГ, гиперволемия |
Использование тиазидоподобных диуретиков |
|
Повышенный риск гиперкалиемии |
Периодический контроль уровня калия |
|
Ортостатическая и постпрандиальная гипотензия |
Необходимость измерения АД в положении стоя и после еды, коррекция интенсивности терапии |
|
Трудности в достижении целевого АД, частая резистентная АГ |
Использование нескольких групп антигипертензивных препаратов, включая бета-адреноблокаторы и антагонисты минералокортикоидных рецепторов |
|
Более частое «скрытое повышение АД» по сравнению с общей популяцией |
Проведение внеофисных измерений АД, особенно у пациентов с диабетом и повышенным АД |
Сокращения: АГ — артериальная гипертензия, АД — артериальное давление, МС — метаболический синдром, СД — сахарный диабет, СНсФВ — сердечная недостаточность с сохранной фракцией выброса, СОАС — синдром обструктивного апноэ сна.
Особенности лечения
Всем пациентам с АГ при МС следует проводить немедикаментозное лечение, направленное на существенную модификацию образа жизни, в частности, включающее снижение веса, уменьшение потребления соли, повышение физической активности.
Если снижение веса не может быть достигнуто немедикаментозными методами, следует рассмотреть возможность медикаментозного лечения (предпочтительно с использованием агониста рецепторов глюкагоноподобного пептида-1 из-за его более высокой эффективности в снижении веса и, следовательно, большего снижения АД) или бариатрической хирургии [77].
Пациент с МС в подавляющем большинстве случаев относится к категории высокого и очень высокого риска, что предопределяет необходимость использования комбинированной антигипертензивной терапии со старта лечения [1]. Также, исходя из того, что прибавка на каждый килограмм избыточного веса сопровождается повышением АД на 1 мм рт.ст. и практически у всех пациентов имеется один или несколько факторов, затрудняющих контроль АД (ГЛЖ, ИМТ/ожирение, хроническая болезнь почек (ХБП), предиабет/СД 2 типа, малоподвижный образ жизни) [78][79], целесообразно использовать полнодозовые комбинации антигипертензивных препаратов.
Как правило, у пациента с АГ и МС помимо метаболически синдемичных заболеваний (ИМТ/ожирение, нарушения липидного обмена, ХБП, неалкогольная жировая болезнь печени) имеется и другая коморбидная патология (хроническая СН, СОАС, гиперурикемия, патология опорно-двигательного аппарата, поликистоз яичников), что необходимо учитывать при выборе антигипертензивной терапии. Поэтому можно сформулировать принципы рациональной антигипертензивной терапии при МС [80]. Она должна помимо стандартных целей (достижение целевого АД, органопротекции, снижения риска развития СН, СД 2 типа, ССО и смерти):
- уменьшать ИР;
- уменьшать низкоинтенсивное неинфекционное воспаление;
- стабилизировать/снижать массу тела;
- оказывать положительное влияние на адипокины (лептин, грелин, резистин, адипонектин);
- способствовать коррекции имеющихся нарушений липидного и пуринового обмена;
- снижать гиперактивацию САС и РААС;
- увеличивать выведения натрия;
- оказывать положительное влияние на протромбогенный статус;
- снижать частоту эпизодов СОАС.
Констатируя необходимость комбинированной антигипертензивной терапии при МС, важно понимать хорошо изученные возможности монотерапии конкретными классами препаратов, поскольку их положительные или отрицательные свойства будут проявляться при их использовании в комбинациях.
Диуретики
В post hoc анализах исследования Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT) при разделении пациентов в зависимости от ИМТ (<25, 25-29,9, >30 кг/м2) более выраженное снижение во всех группах было выявлено при использовании хлорталидона в равнении с лизиноприлом и амлодипином [81], но при этом он вызывал повышение уровня глюкозы натощак, а при наличии МС увеличивал частоту развития СД 2 типа [82-84], но без отрицательного влияния на ССР [85][86]. Похожие результаты были получены в исследовании Systolic Hypertension in the Elderly Program (SHEP), в котором на терапии хлорталидоном при развитии СД 2 типа не было выявлено повышения общей и сердечно-сосудистой смертности [87].
В исследовании International Nifedipine GITS Stu-dy Intervention as a Goal in Hypertension Treatment (INSIGHT) частота развития СД 2 типа была достоверно ниже при сравнении с ко-амилоридом (4,3% vs 5,6%, p=0,023) [88]. В исследовании The International Verapamil-Trandolapril Study (INVEST) применение гидрохлоротиазида (ГХТЗ) также повышало риск развития СД 2 типа, причем даже при использовании низких доз [89]. В то же время в исследовании Atherosclerosis Risk in Communities Study (ARIC) у нелеченых пациентов с АГ на терапии ГХТЗ не было выявлено повышения частоты развития СД 2 типа [90]. По результатам метаанализа диуретики имели наиболее негативный эффект в отношении повышения риска развития СД 2 типа по сравнению с бета-адреноблокаторами (ББ), антагонистами кальция (АК) и блокаторами РААС [91].
В исследовании Valsartan Antihypertensive Long-Term Use Evaluation (VALUE) trial СД 2 типа, развившийся на фоне антигипертензивной терапии, ассоциировался с более высокой сердечно-сосудистой смертностью, особенно при СН по сравнению с лицами без СД 2 типа, но она была ниже, чем у пациентов с имеющимся СД 2 типа. На терапии валсартаном риск развития СД 2 типа был ниже, чем при приеме амлодипина, причем в обеих группах риск СД 2 типа увеличивался при совместном приеме с ББ, диуретиками или их комбинации [92]. В исследовании PIUMA study ССР были одинаковыми как при вновь развившемся, так и имеющемся СД 2 типа, однако при приеме тиазидных диуретиков риск СД 2 типа возрастал [93].
Считается, что развитие гипокалиемии при приеме диуретиков опосредованно уменьшает секрецию инсулина. Применение калий-сберегающих диуретиков, использование препаратов калия и комбинирование их с блокаторами РАСС может нивелировать гипергликемический эффект [94].
ББ
Гиперактивация САС при МС делает вполне логичным использование ББ для лечения АГ у этой категории пациентов [95]. Однако необходимо принимать во внимание данные о негативном влиянии «старых» ББ на вес, углеводный и липидный обмен [84][96], а также повышение риска развития СД 2 типа [90][97][98], что требует использования «новых» ББ (бисопролол, карведилол, небиволол), практически лишенных этих эффектов при МС [99], что подтверждено результатами таких исследований, как Glycemic Effects in Diabetes Mellitus Carvedilol-Metoprolol Comparison in Hypertensive (GEMINI) [100-102] и YESTONO study [103].
АК
АК не оказывают негативного влияния на углеводный и липидный обмен. В исследовании European Lacidipine Study on Atherosclerosis (ELSA) study антагонист кальция лацидипин снижал риск развития МС и улучшал течение СД 2 типа в сравнении с ББ атенололом [104]. Исследование OLAS study продемонстрировало снижение риска развития СД 2 типа при комбинации блокатора РААС с амлодипином по сравнению с аналогичной комбинацией с ГХТЗ [105]. В исследовании the Study of Trandolapril-Verapamil SR And Insulin Resistance (STAR) [106] и в долгосрочном расширенном исследовании STAR (STAR-LET) [107] показано выраженное положительное влияние трандолаприла в комбинации с верапамилом в сравнении с лозартаном в комбинации с ГХТЗ на показатели гликемического контроля и частоту развития новых случаев СД 2 типа, не связанное с антигипертензивным эффектом и с наличием в одной из схем сравнения ГХТЗ.
Блокаторы РААС
Тесная корреляция между ИР и повышением активности РААС хорошо известна и обусловлена ухудшением мышечного кровотока с развитием оксидативного стресса и ингибированием эффектов инсулина на клеточном уровне [108]. Поэтому при лечении АГ у пациентов с МС блокаторам РААС отдается предпочтение [99], хотя между ними имеются различия по метаболическим эффектам [109].
Анализ результатов проспективного когортного исследования Cardiovascular Health Study продемонстрировал, что ингибиторы ангиотензинпревращающего фермента (иАПФ) и блокаторы АТ II (БРА) снижают риски ССО у лиц с МС, не имеющих сердечно-сосудистых заболеваний и СД 2 типа [110].
Среди иАПФ наибольшая доказательная база по воздействию на метаболические показатели у пациентов с АГ и МС накоплена для высоколипофильных периндоприла и рамиприла. Периндоприл наглядно продемонстрировал свои преимущества перед эналаприлом и лозартаном по влиянию на уровень лептина, резистина и метаболические показатели у пациентов с АГ и МС в нескольких исследованиях [111-113]. У пациентов с АГ и МС было доказано выраженное ангиопротективное действие и влияние на уровень лептина периндоприла в сравнении с телмисартаном [114], а комбинации периндоприла с индапамидом и с амлодипином оказывали положительное влияние на липидный профиль и метаболические показатели [115-117]. Рамиприл продемонстрировал свои преимущества у пациентов с АГ и МС в исследованиях AASK [118] и НОРЕ [119] (применение рамиприла снижало риск развития новых случаев СД 2 типа (отношение рисков 0,64 и 0,67, соответственно)), результаты исследований DREAM [120] и ADAPT [121] подтвердили положительное влияние рамиприла на углеводный обмен за счет повышения чувствительности тканей к инсулину и усиление утилизации глюкозы тканями вследствие улучшения периферического кровоснабжения. В исследовании HOPE рамиприл численно достиг даже более высокого относительного снижения первичной конечной точки (сердечно-сосудистая смерть, инфаркт миокарда или инсульт) у пациентов с СД 2 типа по сравнению с недиабетической субпопуляцией [119]. В исследованиях ХАРИЗМА [122] и ХАРИЗМА-2 [123] также показана высокая эффективность рамиприла у пациентов с АГ и МС.
БРА также различаются по влиянию на метаболические показатели у пациентов с АГ и МС. Субанализ исследования Treat to Target survey продемонстрировал, что при МС монотерапия ирбесартаном и его комбинация с ГХТЗ улучшает показатели углеводного и липидного обмена, уменьшает окружность талии [124], что связывают со способностью ирбесартана активировать рецепторы, активируемые пероксисомным пролифератором гамма (PPAR-γ) [109], уменьшая ИР и повышая уровень адипонектина [125]. Метаанализ, сравнивавший эффекты БРА и телмисартана (еще одного БРА с PPAR-γ активирующими свойствами), выявил преимущества последнего в уменьшении ИР при сопоставимом снижении АД [126]. Телмисартан не уступал рамиприлу в отношении снижения композитной сердечно-сосудистой смерти, инфаркта миокарда и инсульта с/без госпитализации (первичные и вторичные результаты эффективности) в подгруппе пациентов с СД 2 типа в исследовании ONTARGET [127]. Для азилсартана медоксомила также установлены положительные плейотропные эффекты в условиях наличия МС [128, 129], а данные сравнительных исследований свидетельствуют о наличии у азилсартана [130-133] преимуществ перед другими БРА в достижении контроля АД, улучшении эластичности сосудов, снижении ИР, уровня лептина и неинфекционного воспаления, а также повышении уровня адипонектина у пациентов с МС. Однако данные об органопротективных свойствах азилсартана ограничены небольшим количеством исследований, а исследований с жесткими конечными точками для азилсартана не проводилось [129].
иАПФ, БРА и АК продемонстрировали противовоспалительный эффект при МС, избыточной массе тела и нарушениях углеводного обмена [134][135], а также положительно влияли на уровень высокочувствительного СРБ [134-143]. Среди ББ только небиволол обладает этой способностью [144]. Положительное влияние на адипонектин [145-147], HOMA-IR [148-150], ФНО-α [39][151][152] и ИЛ-6 [40][153][154] оказывают БРА (особенно телмисартан, БРА с PPAR-γ активирующими свойствами). Все эти эффекты блокаторов РААС не связаны с их антигипертензивной активностью [155][156]. Было показано, что у пациентов с АГ и МС рамиприл и валсартан способствуют значительному повышению уровня адипонектина, в то время как метопролол, амлодипин и доксазозин подобным эффектом не обладают [35]. Терапия лозартаном значительно снизила уровень ФНО-α у пациентов с АГ и СД 2 типа [157]. Была продемонстрирована способность иАПФ, БРА и комбинации иАПФ + АК снижать уровень ИЛ-6 [158-160].
Таким образом, иАПФ и БРА обладают противовоспалительным и положительным метаболическим эффектом, однако между препаратами внутри класса имеются существенные различия.
Комбинации антигипертензивных препаратов
Установлено, что двойные антигипертензивные комбинации позволяют в 2,5-3 раза повысить вероятность достижения целевого АД <130/80 мм рт.ст. у пациентов с МС, у которых была неэффективна монотерапия одним из компонентов комбинации [161], причем в более короткие сроки [162]. По данным метаанализа двойные антигипертензивные комбинации при МС в среднем снижают систолическое АД и диастолическое АД на 21 и 13 мм рт.ст., соответственно [163].
При МС антигипертензивная эффективность комбинаций блокатора РААС + АК и РААС + ГХТЗ практически не отличается [105], помимо этого, нет различий по эффективности комбинаций в зависимости от присутствия в них иАПФ или сартанов [164]. Однако комбинации блокаторов РААС с АК снижают риск развития ССО [165], конверсии в СД 2 типа [91][106][166], а также положительно влияют на сосудистую жесткость, уровень общего холестерина, липопротеинов низкой плотности, триглицеридов, маркеров воспаления и протромбогенного статуса, уменьшают ИР и повышают уровень липопротеинов высокой плотности и адипонектина [105][158][164][167] и по влиянию на эти показатели эффективнее компонентов монотерапии. При этом более выраженное положительное влияние оказывают антигипертензивные препараты с положительным влиянием на PPAR-γ рецепторы [105].
У пациентов с избыточной массой тела и СД 2 типа было доказано выраженное нефропротективное действие комбинации периндоприла с индапамидом [168], а тройная фиксированная комбинация периндоприла с индапамидом и амлодипином при длительном приеме (~8 лет) благоприятно влияла на уровень триглицеридов и липопротеинов низкой плотности, снижала риск развития ГЛЖ, СД 2 типа, ССО по сравнению с другими тройными произвольными и комбинациями [115]. При этом эффективность этой комбинации не зависела от ИМТ пациентов [117].
Имеются данные о высокой эффективности ангиотензиновых рецепторов и неприлизина ингибиторов (сакубитрил + валсартан) у пациентов с МС и резистентной АГ [169][170].
Ожирение является одним из важных факторов риска развития резистентной АГ, многочисленные исследования показали, что антигипертензивные средства снижают АД в сопоставимой степени у пациентов с ожирением по сравнению с пациентами без него. Трудности в лечении АГ при МС могут быть связаны с ее сложным патогенезом и необходимостью воздействия на многочисленные механизмы — отсюда необходимость в схемах лечения, включающих в некоторых случаях четыре, пять и более антигипертензивных средств.
Влияние сахароснижающих препаратов на уровень АД
По данным метаанализа [171] применения 21 сахароснижающего препарата из 9 различных классов при лечении СД 2 типа было выявлено, что семаглутид (снижение более чем на 3 мм рт.ст.), лираглутид, дапаглифлозин, эмпаглифлозин, канаглифлозин (снижение более чем на 2,5 мм рт.ст.) в наибольшей степени снижали систолическое АД. Метформин оказывал менее выраженное гипотензивное действие (снижение более чем на 1 мм рт.ст.). Эти же препараты в наибольшей степени снижали вес пациентов. Диастолическое АД снижалось при лечении ингибиторами натрий-глюкозного котранспортера 2 типа, семаглутидом и пиоглитазоном (снижение более чем на 0,5 мм рт.ст.). Остальные сахароснижающие препараты гипотензивным эффектом практически не обладали. Схожие результаты были получены и в другом метаанализе [172]. При этом необходимо отметить, что у антагонистов рецепторов глюкагоноподобного пептида 1 (семаглутида) и ингибиторов натрий-глюкозного котранспортера 2 типа имеются важные при сочетании МС и АГ способности, наряду со снижением массы тела, уменьшать риск развития СН, прогрессирования ХБП и неалкогольной жировой болезни печени [173-175].
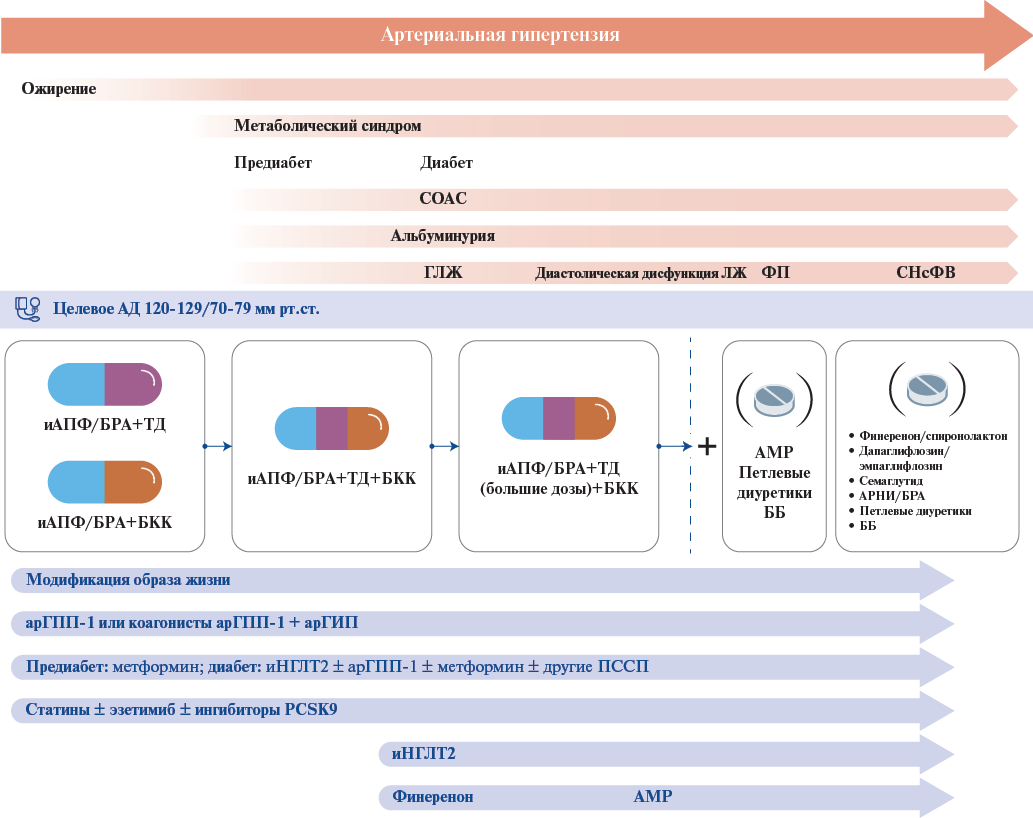
На рисунке 1 представлена концепция ведения пациента с АГ и коморбидной патологией в рамках МС.

Рис. 1. Концепция ведения пациента с АГ и коморбидной патологией в рамках МС.
Сокращения: АД — артериальное давление, АМР — антагонисты минералокортикоидных рецепторов, АРНИ — ангиотензиновых рецепторов и неприлизина ингибиторы, арГПП-1 — антагонисты рецепторов глюкагоноподобного пептида-1, арГИП — антагонисты рецепторов глюкозозависимогой инсулинотропного пептида, ББ — бета-адреноблокаторы, БКК — блокаторы кальциевых каналов, БРА — блокаторы рецепторов ангиотензина, ГЛЖ — гипертрофия левого желудочка, иАПФ — ингибиторы ангиотензинпревращающего фермента, иНГЛТ2 — ингибиторы натрий-глюкозного котранспортера 2 типа, ЛЖ — левый желудочек, ПССП — пероральные сахароснижающие препараты, СНсФВ — сердечная недостаточность с сохранной фракцией выброса, СОАС — синдром обструктивного апноэ сна, ТД — тиазидоподобные диуретики, ФП — фибрилляция предсердий, PCSK9 — пропротеиновая конвертаза субтилизин-кексинового типа 9.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Кобалава Ж.Д., Конради А.О., Недогода С.В. Артериальная гипертензия при метаболическом синдроме. Российский кардиологический журнал. 2025;30(1S):6536. https://doi.org/10.15829/1560-4071-2025-6536
Скопировать