Влияние отмены длительной СРАР-терапии на течение обструктивного апноэ сна
Обструктивное апноэ во сне (ОАС) является очень распространенным в популяции заболеванием, характеризующимся преходящим коллапсом верхних дыхательных путей во время сна и следующими за этим гипоксемией, колебаниями внутригрудного давления и фрагментацией сна. Наиболее широко цитируемое исследование, Wisconsin Sleep Cohort (Висконсинская когорта), показало в среднем 10%- ую распространенность умеренной и тяжелой форм болезни (значения индекса апноэ/гипопноэ (ИАГ) >15 эп/ч) среди популяции в возрасте 30-70 лет — 13% среди мужчин и 6% среди женщин [1].
Метод лечения путем создания постоянного положительного давления в верхних дыхательных путях (аббревиатура, используемая в печати — CPAPтерапия) в настоящее время является методом выбора во многих клинических ситуациях при лечении ОАС [2][3]. Механизм действия этого метода заключается в создании постоянного положительного давления и направлен на преодоление пассивного коллапса верхних дыхательных путей [3]. Эта терапия очень эффективна в устранении других патологических видов дыхания во сне (синдром гиповентиляции, синдром повышенной резистентности верхних дыхательных путей, храп, в некоторых случаях — центральное апноэ сна) и быстро нормализует их последствия [4]. Рандомизированные исследования у пациентов с ОАС средней и тяжелой степени показали, что СРАР-терапия уменьшает чрезмерную дневную сонливость, улучшает качество жизни [5-9] и внимательность при вождении транспортных средств [10]. В свою очередь, сердечно-сосудистая заболеваемость и смертность, как было показано в отдельных работах, снижается при использовании данного вида терапии не <4 ч за ночь [11].
Эффективность такого лечения зависит прежде всего от корректного использования метода (не <4 ч и >70% ночей пользования). Даже у пациентов с высокой приверженностью к терапии применение метода СРАР от ночи к ночи может сильно варьировать [12][13], вплоть до полного прекращения лечения. С другой стороны, часть больных с ОАС в течение первого года терапии самостоятельно прекращают лечение.
Данные о состоянии болезни после прекращения CPAP-терапии в доступной литературе ограничены и противоречивы. Некоторые исследователи полагают, что апноэ не сразу возвращается к исходному состоянию в течение первых ночей и даже недель после отмены лечения [14-16]. Эти исследования показывают, что могут быть остаточные эффекты использования CPAP, которые улучшают состояние верхних дыхательных путей. Кроме того, преходящая десатурация кислорода, характерная для ОАС, при отмене терапии может быть менее выражена, чем до начала терапии. В других исследованиях было показано, что резкая отмена CPAP-терапии вызывает немедленный возврат болезни к прежним уровням тяжести [17-20].
Таким образом, в настоящее время остаются открытыми вопросы, в какой степени рецидивирует ОАС после отмены СРАР-терапии, от каких факторов будет зависеть степень последующего рецидива и возможно ли предложить той части больных, у которых после курсового лечения СРАР снижается исходная тяжесть болезни, другие лечебные стратегии нарушений дыхания во сне.
Материал и методы
Изучаемая когорта. Было проведено наблюдательное обсервационное когортное исследование в течение 12 мес. В исследование включались пациенты с пароксизмальной формой фибрилляции предсердий (ФП), прошедшие катетерное лечение ФП в период с 2016 по 2018гг в отделе нарушений ритма ФГБУ НМИЦ ТПМ Минздрава РФ. Начиная с 10 сут. после проведения операции всем пациентам было проведено кардиореспираторное мониторирование сна (КРМ) в течение одной ночи для диагностики нарушений дыхания во время сна, а затем пациентам с выявленным ОАС тяжелых степеней инициирована терапия постоянным положительным давлением в верхних дыхательных путях (СРАР-терапия) в автоматическом режиме на 12 мес. Исследуемая когорта включила в себя 40 пациентов в возрасте от 37 до 75 лет. После года постоянной СРАР-терапии она была прервана, и через 1-2 дня было проведено повторное КРМ для оценки степени рецидива ОАС.
Исследование было одобрено Этическим Комитетом ФГБУ НМИЦ ТПМ Минздрава РФ. До включения в исследование все пациенты подписали информированное согласие.
В исследование не включались пациенты, у которых было наличие в анамнезе хронической сердечной недостаточности 2 функционального класса и выше, с декомпенсацией основных заболеваний, кардиомиопатиями любого генеза, с обструктивной болезнью легких, с нейромышечными заболеваниями; с имеющимся центральным апноэ сна, определяемым на момент проведения КРМ как >50% от всех патологических дыхательных событий. Кроме того, критерием исключения считался добровольный отказ от участия в исследовании.
Диагностика обструктивного апноэ сна и подбор СРАР-терапии. Диагностика нарушения дыхания во сне проводилась при помощи портативного прибора для кардиореспираторного мониторирования нарушения дыхания во сне (Astrocard, Медитек, Россия). Данный прибор является прибором 3-го диагностического уровня, одобренным и рекомендованным Европейским Респираторным Обществом для объективной диагностики ОАС [21]. Прибор позволяет регистрировать 4 канала, которые включают в себя дыхательный поток, дыхательные движения грудной клетки или брюшной стенки, электрокардиограмму и уровень сатурации О2. После окончания исследования полученные данные были сохранены, а затем просмотрены в ручном режиме специалистом по медицине сна при помощи программного обеспечения Somno-Studio (Медитек, Россия). С учетом текущих определений и рекомендаций по диагностике ОАС Американской Академии Медицины Сна (ААSM) [22] обструктивное апноэ определялось как прекращение воздушного потока на 90% и более от исходного продолжительностью 10 сек. и более при сохранении дыхательных усилий. Обструктивное гипопноэ определялось как снижение (но не полное прекращение) воздушного потока на 30% и более от исходного уровня продолжительностью >10 сек., которое сопровождалось падением насыщения уровня кислорода в крови на 3% и более при сохранении дыхательных усилий. Гипоксемия ночью определялась как снижение среднего уровня насыщения кислорода крови <92%. Надир десатурации определялся как минимальное снижение уровня кислорода за ночь исследования. Степень тяжести обструктивного апноэ сна определялась по наличию ИАГ, который отражает количество эпизодов апноэ/гипопноэ за час исследования. Границей нормы явилось значение ИАГ <5 эп/ч. Степень тяжести ОАС была определена как мягкая степень при значении ИАГ от 5 до 14 эп/ч, как средняя степень тяжести при значении ИАГ от 15 до 30 эп/ч, как тяжелая степень при значении ИАГ >30 эп/ч.
Неинвазивная вентиляция легких во сне проводилась с применением респираторного устройства для обеспечения постоянного положительного давления в верхних дыхательных путях (аппараты для СРАРтерапии, ResMed Autoset S9, Австралия). Пробная СРАР-терапия инициировалась в режиме автоматического подбора. Перед ночью пробной терапии проводился подбор лицевого интерфейса для лечения (выбор соответствующего типа маски), устанавливались диапазоны лечебного давления и осуществлялся инструктаж пациента по пользованию прибором. Длительность пробной СРАР-терапии составила от 1 до 4 сут. По окончании пробной СРАР-терапии данные переносились в программное обеспечение ResScan (ResMed, Австралия). Эффективной считалась терапия, в результате которой была достигнута либо полная ремиссия обструктивного апноэ сна (остаточный ИАГ <5 эп/ч), либо уменьшение количества эпизодов апноэ на 50% и более от исходного значения. Далее в ручном режиме проводилась коррекция настроек прибора для длительного использования СРАР-терапии. Пациенты получали соответствующие рекомендации по использованию прибора в домашних условиях (частота применения не <5 дней в нед. и длительность терапии не <4 ч в течение ночи) и эксплуатации увлажнителя, носовой маски и других комплектующих. Проводился контроль показателей лечения СРАР через 3, 6 и 12 мес. после начала терапии.
В течение 12 мес. из исследования выбыло 7 пациентов (2 на этапе подбора, 3 на визите через 3 мес. и 2 на визите через 6 мес.). Причинами выбытия из исследования явились: субъективная непереносимость лечения — 2 человека, добровольный отказ от участия в исследовании — 4 человека, невозможность использования лечения по личным причинам — 1 человек).
Через 12 мес. у окончивших исследование 33 пациентов СРАР-терапия была прекращена, после отмены лечения на 1-2 день было проведено повторное КРМ, полученные результаты обрабатывались аналогично протоколу первого исследования.
Статистический анализ результатов исследования. Количественные переменные описывались следующими показателями: числом пациентов, средним арифметическим значением (М), стандартным отклонением от среднего арифметического значения (?), 25-м и 75-м процентилями, медианой. Качественные переменные описывались абсолютными и относительными частотами. Различия считались статистически значимыми при достигнутом уровне p<0,05.
Для количественных переменных проводился тест по Колмогорову-Смирнову на соответствие нормальному закону распределения. Оценка полученных результатов проводилась с использованием методов параметрической и непараметрической статистики: ?2-критерия Пирсона, двустороннего критерия Фридмана, непарного t-критерия Стьюдента, непараметрических критериев Манна-Уитни, Вилкоксона, Краскела-Уоллиса. Для определения взаимного влияния показателей использовали корреляционный анализ Спирмена.
Расчет выполнен на персональном компьютере с использованием приложения Microsoft Excel и пакета статистического анализа данных Statistica 10 for Windows (StatSoft Inc., USA).
Результаты
В таблице 1 приведены базовые характеристики группы до начала лечения. 55% обследованных пациентов имели различные степени ожирения, в группе было приблизительное равенство обоих полов (мужчин было 52,5%). Средний возраст группы составил 59,3±8,2 лет, преобладали лица старше 60 лет (52,8%) (в этом возрасте наличие болезни выявляется у мужчин и женщин с одинаковой частотой), отмечалось сравнительно малое количество курящих (22,5%). Превалирующее большинство пациентов имели в анамнезе гипертоническую болезнь и получали гипотензивную терапию (92,3% и 82,5%, соответственно). Также у 62,5% включенных в исследование было увеличено левое предсердие (>40 мм, фактор риска рецидива ФП).
Таблица 1
Характеристика группы, получавшей СРАР-терапию

Сокращения: ГБ — гипертоническая болезнь, ИМТ — индекс массы тела, ЛП — левое предсердие, ФП — фибрилляция предсердий.
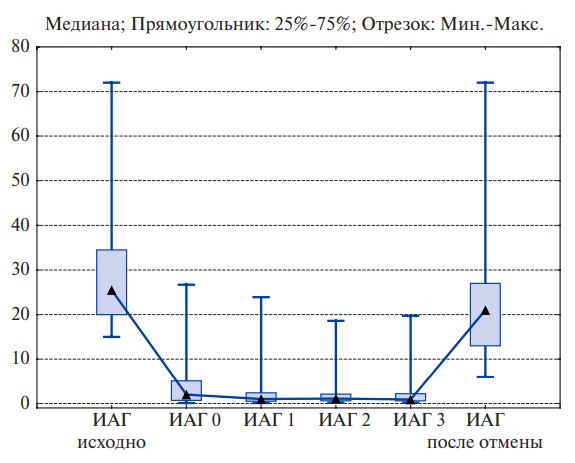
Как показано на рисунке 1, СРАР-терапия в течение периода пробного подбора перевела в полную ремиссию средние и тяжелые формы ОАС (статистические различия по двустороннему критерию Фридмана р=0,001). В одном случае количество апноэ снизилось на 50% от исходного, что также является критерием успешной СРАР-терапии. Ремиссия заболевания сохранялась в течение всех последующих визитов. Однако отмена СРАР-терапии во всех случаях привела к немедленному рецидиву ОАС — медиана значения ИАГ составила 21 [ 13; 27 ] эп/ч (хотя значение ИАГ снизилось по сравнению с исходными значениями (24 [ 20; 34 ]), статистически значимой разницы не получено).

Рис. 1. Динамика ИАГ сна до, на этапах и после отмены СРАР-терапии.
Сокращение: ИАГ — индекс апноэ/гипопноэ.
Также никакой значимой положительной динамики (рис. 2) не было отмечено в показателях среднего уровня и минимального значения (надира) кислорода в ночное время после острой отмены СРАР-терапии.

Рис. 2. Динамика среднего значения О2 и минимального значения О2 (надир) до и после лечения СРАР-терапии.
Мы провели парный анализ группы по сравнению исходной степени тяжести ОАС до лечения и после отмены СРАР-терапии (рис. 3). В группе с исходной средней степенью тяжести ОАС у 10 пациентов (52,6%) после отмены СРАР степень тяжести снизилась до легкой, у 8 (42,1%) не изменилась, а у одного пациента стала тяжелой. В группе с исходно тяжелым ОАС перехода в легкую степень не произошло ни у одного пациента (степень тяжести либо не изменилась (28,6%), либо перешла в категорию средней тяжести (71,4%).

Рис. 3. Значения степени тяжести после прерывания лечения в зависимости от исходного показателя.
Корреляционный анализ степени тяжести ОАС, уровней сатурации, роста, веса, индекса массы тела, наличия гипертонической болезни показал, что существует статистически значимая зависимость степени тяжести болезни, конечного значения ИАГ и надира десатурации от массы тела (до и после терапии) (r=0,396, 0,411 и -0,488; r=0,358, 0,398 и -0,44, соответственно, р<0,05). Нужно отметить, что статистически значимой корреляции между комплаентностью к терапии (время пользования за ночь и % дней использования за отчетный период) и рецидивом болезни после отмены терапии мы не получили.
Обсуждение
В современных рекомендациях достаточно подробно прописаны клинические ситуации назначения СРАР-терапии, однако ее длительность, возможность полной отмены или замены на другой тип терапии не оговорены [3].
Прекращение CPAP-терапии изучалось в нескольких исследованиях, в которых продолжительность прерывания лечения составила от одной ночи до 2 нед. Некоторые исследователи сообщают о рецидиве ОАС после отмены СРАР терапии, однако с меньшей степенью выраженности, чем до начала лечения. Например, Криббс с коллегами установили, что отмена CPAP на одну ночь привела к тому, что ИАГ в среднем составил 34 эп/ч по сравнению с 57 эп/ч до лечения [23]. Другие авторы показали возврат к исходным показателям ИАГ в первую же ночь отмены CPAP-терапии. Однако он сопровождался меньшим падением уровня кислорода во сне после первой ночи отмены. В дальнейшем через 1 нед. без терапии уровень О2 вернулся к исходному уровню тяжести [16]. Рандомизированное исследование, сравнивающее отмену CPAP на более длительный срок (2 нед. с последующим продолжением терапии), показало быстрый рецидив ОАС, характеризующийся возвратом к исходному значению ИАГ в течение первой же ночи после отмены терапии, но при этом менее выраженное падение уровня сатурации в первую ночь отмены [15]. В недавнем исследовании было отмечено, что ОАС вообще не рецидивировало у 1/3 пациентов после 4 ночей отмены CPAP, это относилось к пациентам с исходно менее тяжелой ОАС и меньшей массой тела [14]. Это исследование находится в ряду подтверждающих отсутствие рецидива ОАС во время острой отмены CPAP.
В нашем исследовании мы не получили столь выраженного ответа после 12 мес. СРАР-терапии, хотя среднее значение ИАГ и снизилось по сравнению с исходным, но это снижение не было статистически значимым. Также не было показано достоверного улучшения газового состава крови. Ни среднее значение кислорода за ночь, ни надир десатурации не изменились после проведенной СРАР-терапии сразу после ее отмены. В целом наши данные не отличались от данных большинства предшествующих исследований, т.к. без лечения показатели степени тяжести апноэ (ИАГ) и газового состава крови неизменно возвращались к исходным через достаточно короткий промежуток времени (от 1-2 дней до 2 нед.).
Какие же факторы теоретически могли уменьшить степень рецидива ОАС после отмены лечения? Есть работы, показывающие, что снижение выраженности ОАС может просто отражать известную вариабельность между разными ночами, которая, в свою очередь, определяет рецидив в более низких диапазонах степени тяжести болезни [24-26]. Однако эта внутренняя вариабельность становится менее вероятной или полностью отсутствует при тяжелой степени ОАС. Тем не менее — при очень тяжелом исходном состоянии болезни длительная СРАРтерапия может способствовать регрессии к средним значениям ИАГ. Этот факт нашел отражение и в нашем исследовании, когда большая часть пациентов с тяжелой степенью ОАС (71,4%) перешла в группу средней тяжести.
Можно было ожидать, что у пациентов с увеличением возраста и наличием ожирения ремиссия ОАС после отмены СРАР-терапии будет маловероятна. Этот факт подтверждается нашими данными (у 55% обследованных пациентов индекс массы тела был >30 кг/м2, а средний возраст группы составил 59,3±8,2 лет).
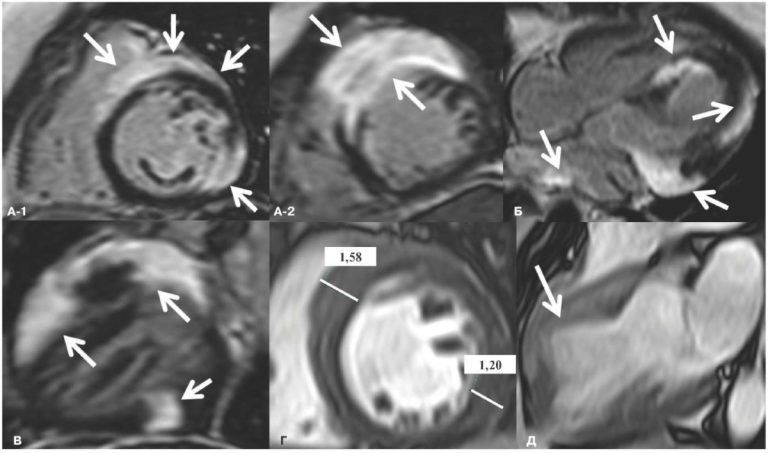
Кроме того, на тяжесть апноэ сна могут влиять такие факторы, как отек в верхних дыхательных путях под влиянием хронической баротравмы — периодического храпа при апноэ [27], переход и локализация тканевой жидкости во время сна на спине в область шеи [28], нарушение дыхательных сенсорных афферентных рефлексов [29] и мышечная слабость подъязычной мышцы [30]. Можно ожидать воспроизводимый эффект CPAP-терапии на степень тяжести апноэ, если в результате ее действия достигается снижение воздействия этих факторов. В некоторых исследованиях после длительного использования CPAP-терапии ее эффект оценивался при помощи магнитно-резонансной томографии [31]. Был продемонстрирован анатомический ремоделирующий эффект применения неинвазивной вентиляции во сне на структуры верхних дыхательных путей. Также в ряде работ было показано, что CPAP-терапия может уменьшать влияние контроля дыхательного центра при апноэ и снижать дыхательные реакции, которые отвечают за дыхательную нестабильность верхних дыхательных путей [32][33].
Последним фактором, влияющим на возможность ремиссии после отмены СРАР-терапии, является длительность и регулярность ее применения. В нашем исследовании 12-мес. использование СРАРтерапии не показало достоверного влияния на степень ремиссии после отмены лечения.
В нашем исследовании есть определенные ограничения. Во-первых, мы не проводили полисомнографическое исследование с записью структуры сна. Известно, что отмена СРАР-терапии отрицательно влияет на архитектуру сна, приводит к увеличению представленности стадий бодрствования и поверхностной стадии медленноволнового сна и к снижению времени пародоксального сна (REMсна). Нестабильность сна с частыми пробуждениями и реакциями ЭЭГ-активации обычно усугубляет течение ОАС [34]. Во-вторых, нами не оценивались дневные функции (прежде всего сонливость днем) после отмены СРАР-терапии. Данные влияния отмены СРАР-терапии на объективную и субъективную дневную сонливость противоречивы. В исследованиях [12] было показано, что при отмене СРАР-терапии сонливость сразу же возвратилась к своим долечебным уровням. Это было одинаково как для тяжелой, так и для умеренной степени ОАС. Напротив, Sforza с коллегами [35] обнаружили, что субъективная сонливость не вернулась к исходным уровням перед началом лечения. Хотя возможно, что различия могут объясняться влиянием на конечный результат эффектом похудения у испытуемых.
Есть также данные, что отмена CPAP-терапии показала связь рецидива ОАС с нарушением функции эндотелия, увеличением концентрации катехоламинов в моче, повышением артериального давления и частоты сердечных сокращений, т.е. возобновлением повышенной симпатической активности, характерной для не леченного ОАС [15][36].
Вопрос замены или полного прекращения СРАРтерапии при снижении степени тяжести ОАС после лечения в литературе освещен крайне недостаточно. С одной стороны, пациенты, которые наблюдались в нашей работе, требуют постоянной курации нарушений дыхания во сне, т.к. ОАС у них сочетается с пароксизмальной формой ФП, которая потребовала хирургического вмешательства. Современные исследования говорят о высокой частоте встречаемости обструктивных нарушений дыхания во сне у пациентов с разными формами ФП [37][38]. Настоящие рекомендации и согласительные документы рассматривают ОАС как фактор риска развития и/или рецидива ФП и предлагают постоянное долгосрочное лечение СРАР с целью снижения рисков возникновения ФП на этапе послеоперационного лечения [39][40]. В клинических рекомендациях по другим видам лечения ОАС [41] возможна замена СРАР-терапии на внутриротовые устройства в случаях средней и тяжелой формы ОАС при невозможности продолжать лечение СРАР по различным причинам.
Таким образом, на настоящий момент нет убедительных доказательств полной отмены терапии ОАС либо по достижению определенного времени от начала терапии, либо при достижении ремиссии болезни. Как показало наше исследование и большинство работ, цитируемых нами, полного излечения от нарушений дыхания при прерывании лечения при терапии разной длительности не происходит, и ОАС рецидивирует в той или иной степени в ближайшее время после отмены СРАР-терапии. Поэтому продолжение СРАРтерапии в настоящее время остается единственной возможностью достижения полной и контролируемой ремиссии ОАС. Замена СРАР-терапии на другой метод лечения ОАС теоретически возможна, но требует проведения дополнительных исследований, доказывающих эффективность такой замены.
Заключение
В нашем исследовании при прерывании терапии после 12 мес. использования СРАР полного излечения от нарушений дыхания во сне не зарегистрировано ни в одном случае. ОАС рецидивировало сразу после отмены СРАР-терапии (на 1-2 день). Тяжесть рецидива заболевания зависела от исходной степени тяжести болезни. На настоящее время продолжение СРАР-терапии остается единственной возможностью достижения полного контроля за ОАС как за фактором риска развития ФП.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Агальцов М.В., Драпкина О.М. Влияние отмены длительной СРАР-терапии на течение обструктивного апноэ сна. Российский кардиологический журнал. 2021;26(2S):4314. https://doi.org/10.15829/1560-4071-2021-4314
Скопировать