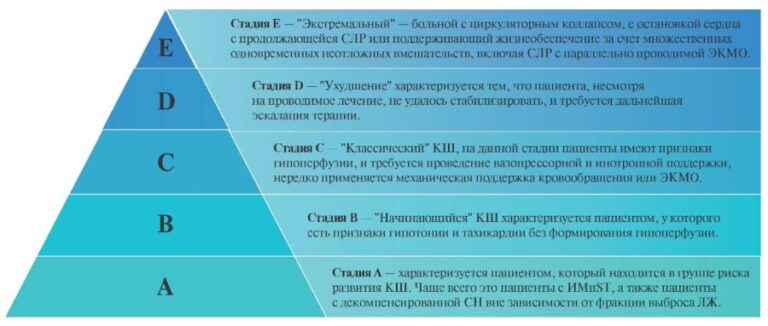
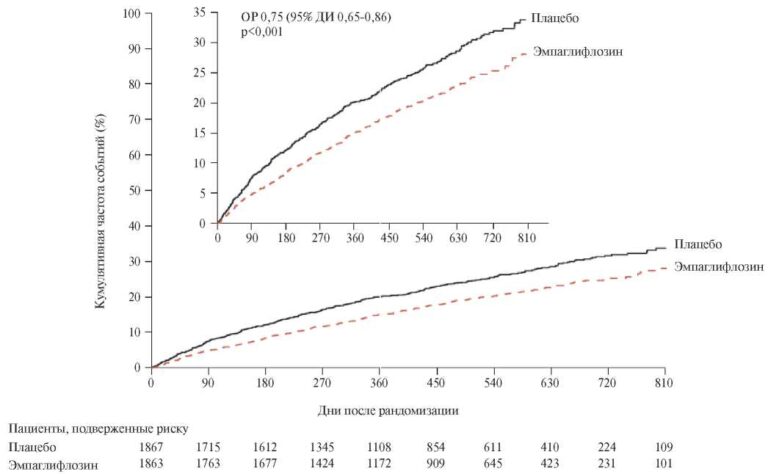
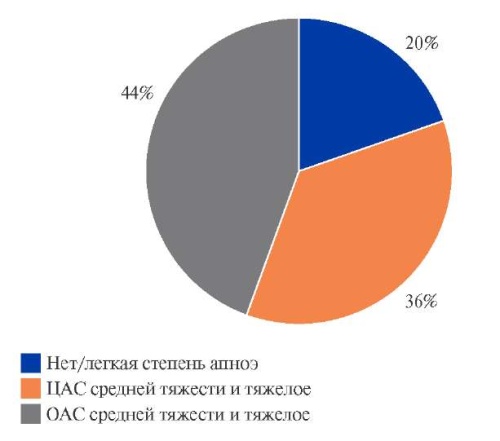
Систематический обзор и метаанализ сравнения бимаммарного коронарного шунтирования in situ с композитным бимаммарным шунтированием: непосредственные результаты и 30-ти дневная летальность
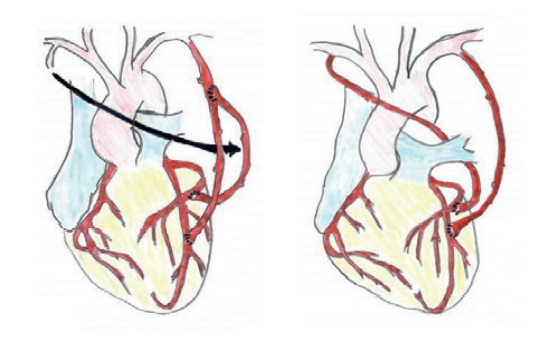
Коронарное шунтирование (КШ) остается одним из методов лечения больных с ишемической болезнью сердца [1]. Отдаленная выживаемость и большие сердечно-сосудистые события зависят от используемых кондуитов при КШ [2][3]. Маммарно-коронарное шунтирование передней межжелудочковой артерии улучшает отдаленную проходимость кондуита и выживаемость [4][5]. Были предприняты усилия для увеличения этих преимуществ за счет увеличения количества артериальных трансплантатов, включая правую внутреннюю грудную артерию (ПВГА), которая гистологически идентична левой внутренней грудной артерии (ЛВГА) и продемонстрировала дополнительные преимущества в виде улучшения выживаемости и свободы от стенокардии, инфаркта миокарда (ИМ), независимо от того как использовались внутренние грудные артерии (ВГА) (в виде свободного кондуита и применяется в виде композитного шунта (рис. 1 А) или in situ (рис. 1 Б, В, Г)) [6][7]. Однако, в зависимости от анатомии коронарных артерий и технических особенностей, ПВГА in situ может иметь недостаточную длину для шунтирования коронарной артерии боковой стенки, неадекватный кровоток из-за стеноза подключичной артерии или случайного повреждения. В этих случаях ПВГА может использоваться как свободный трансплантат и применяться как композитный графт, хирургические аспекты такого шунтирования хорошо описаны в соответствующих руководствах [8][9]. Существуют единичные исследования сравнения бимаммарного коронарного шунтирования (БиМКШ) in situ с композитным шунтированием [10-20].

Рис. 1. БиМКШ при помощи композитного графта или in situ [9]. А — композитное, Б — in situ (ЛВГА in situ к ПМЖА, а ПВГА in situ (над аортой) к ВТК), В — in situ (ЛВГА in situ к ПМЖА, а ПВГА in situ (под аортой через поперечный синус) к ВТК), Г — in situ (ЛВГА in situ к ВТК, а ПВГА in situ к ВТК).
Цель нашего метаанализа — сравнить непосредственные результаты и 30-ти дневную летальность БиМКШ in situ с композитным БиМКШ.
Материал и методы
Систематический обзор и метаанализ выполнены в соответствии с международными рекомендациями (PRISMA) [21] (рис. 2). Для поиска статей использовалась стратегия PICO:
- пациент (Patient) — пациенты старше 18 лет;
- вмешательство (Intervention) — применение БиМКШ in situ;
- сравнение (Comparison) — БиМКШ с композитным графтом;
- исходы (Outcomes) — непосредственные результаты и 30-ти дневная летальность.

Рис. 2. Дизайн исследования PRISMA для данного исследования.
Источники данных. Поиск литературы проводили в следующих базах: PubMed, Google Scholar, Web of Science с 1990 по 2020гг на предмет всех исследований, в которых использовалась терминология “bilateral internal mammary artery” (бимаммарная артерия) или “bilateral internal thoracic artery” (две ВГА), или “right internal mammary artery” (правая маммарная артерия), или “right internal thoracic artery” (правая внутренняя грудная артерия), или “bilateral internal mammary artery in situ versus composite” (БиМКШ in situ против композитного), в заголовке или аннотации.
Отбор исследований. Мы включили все исследования, сравнивающие БиМКШ in situ с композитным БиМКШ (когда одну из маммарных артерий использовали в качестве свободного трансплантата) у пациентов с ишемической болезнью сердца, в которых были известны непосредственные послеоперационные результаты (инсульт, периоперационный ИМ, постоперационная фибрилляция предсердий (ПОФП), медиастинит, выполнения рестернотомии по поводу кровотечения, острое почечное повреждение, госпитальная летальность) и 30-ти дневная летальность.
Критерии исключения:
- исследования, в которых не сообщалось о клинических исходах,
- данные были опубликованы только в виде аннотации,
- работы, опубликованные не на английском языке.
Извлечение данных и оценка качества. Два рецензента независимо друг от друга извлекли данные, включая подробности публикаций, критерии включения/исключения, демографические данные пациентов, дооперационные факторы риска, описание используемых вмешательств, определения результатов и событий, объем выборок. Системные ошибки публикаций оценивались с помощью воронкообразного графика. Асимметричность графика свидетельствовала о системной ошибке публикации.
Анализ данных. Для обсервационных, т.е. наблюдательных, исследований, в которых сообщалось как о данных до “псевдорандомизации” (Propensity-score matching), так и после “псевдорандомизации”, мы предпочитали использовать данные после “псевдорандомизации”. Все анализы проводились с помощью программного обеспечения Review Manager (RevMan версии 5.2; Cochrane Collaboration, Оксфорд, Великобритания). Для периоперационных исходов с аналогичным последующим наблюдением между группами логарифмические отношения рисков (ОР) были выведены для бинарных исходов и взвешенных средних различий (MD) для количественных показателей. Проверка статистической неоднородности исследований осуществлялась с помощью Q-теста на основе ?2. Модель случайных эффектов была принята при Р<0,1 в тесте ?2 и I2>40%, модель фиксированного эффекта при Р?0,1 в тесте ?2 и I2 ?40%.
Результаты
Первоначальная стратегия поиска дала 1204 ссылки из PubMed, Google Scholar, Web of Science, 10 из них были включены в данный систематический обзор и метаанализ, в которых принимало участие 8489 больных (табл. 1).
Таблица 1
Демографическая характеристика исследований

Сокращения: Комп. — композитное, Обс. — обсервационное, РКИ — рандомизированное контролируемое исследование, ФП — фибрилляция предсердий.
Описание включенных исследований и пациентов. Были проведены 2 рандомизированных контролируемых исследования (РКИ) (n=705 пациентов) [18][20], 4 наблюдательных исследования, сопоставленные по шкале предрасположенности, т.е. с “псевдорандомизацией” (Propensity score matching (PSM)) (n=4267) [10][12][14][17], и 4 нескорректированных обсервационных исследования (n=3517) [11][15][16][19], которые соответствовали критериям включения. РКИ [18][20] не были слепыми, одно из наблюдательных исследований было проспективным [15], а остальные исследования [10][11][12][14][16][17][19] были ретроспективными. В большинстве исследований группы пациентов были сопоставимы по основным дооперационным демографическим показателям. В одном из исследований в группе, где выполнялось композитное БиМКШ было статистически значимо больше больных с фракцией выброса левого желудочка ?35%, больше больных с сахарным диабетом и с повторным вмешательством [11]. В другом исследовании в группе где выполнялось композитное БиМКШ было статистически значимо больше женщин [19]. Более подробная дооперационная характеристика включенных больных описана в таблицах 1 и 2.
Таблица 2
Эхокардиографические и ангиографические параметры исследований

Сокращения: Комп. — композитное, ЛКА — левая коронарная артерия, РКИ — рандомизированное контролируемое исследование, ФВ ЛЖ — фракция выброса левого желудочка.
Операционные детали. Сравнивая БиМКШ in situ c композитным БиМКШ, мы обнаружили, что общее количество наложенных дистальных анастомозов в группе, где выполнялось in situ, было статистически значимо меньше, чем в группе с композитным шунтированием (MD=0,23 с 95% доверительным интервалом (ДИ) 0,15-0,32; р<0,001) (рис. 3). А также меньше наложенных дистальных анастомозов с ВГА в группе in situ, чем в группе с композитным шунтированием (MD=0,3 с 95% ДИ 0,15-0,45; р=0,0001) (рис. 4). Но не было статистически значимой разницы во времени ишемии миокарда между группами (3 мин с 95% ДИ -3,23-9,79; р=0,32) (рис. 5). Большинство этих анализов демонстрируют неоднородность от умеренной до высокой. Оперативные параметры отражены в таблицах 3 и 4.
Таблица 3
Оперативные детали исследований

Примечание: * — cеквенциальные анастомозы с ВГА.
Сокращения: БиМКШ — бимаммарное коронарное шунтирование, ВГА — внутренняя грудная артерия, ИК — искусственное кровообращение, Комп — композитное, КШ — коронарное шунтирование, Комп. — композитное, РКИ — рандомизированное контролируемое исследование.

Рис. 3. График Forest plot, построенный по данным метаанализа для сравнения количества общих дистальных анастомозов.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 4. График Forest plot, построенный по данным метаанализа для сравнения количества дистальных анастомозов с ВГА.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 5. График Forest plot, построенный по данным метаанализа для сравнения времени ишемии миокарда.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.
Таблица 4
Использование дополнительных кондуитов

Сокращения: БПВ — большая подкожная вена, ЖСА — желудочно-сальниковая артерия, Комп. — композитное, ЛА — лучевая артерия, РКИ — рандомизированное контролируемое исследование, ЭГА — эпигастральная артерия.
Ранние послеоперационные результаты. Не было статистически значимой разницы между группами в частоте развития периоперационного инсульта (RR=0,5 с 95% ДИ 0,63-1,74; р=0,85) (рис. 6), ИМ (RR=1,1 с 95% ДИ 0,66-1,85; р=0,71) (рис. 7), медиастинита (RR=0,86 с 95% ДИ 0,62-1,20; р=0,38) (рис. 8), выполнении рестернотомии по поводу кровотечения (RR=1,29 с 95% ДИ 0,75-2,21; р=0,36) (рис. 9), острое почечное повреждение (ОПП) (RR=1,24 с 95% ДИ 0,84-1,84; р=0,29) (рис. 10), но частота ПОФП была статистически значимо меньше в группе где in situ (RR=1,23 с 95% ДИ 1,04-1,44; р=0,01) (рис. 11).

Рис. 6. График Forest plot, построенный по данным метаанализа для сравнения частоты возникновения периоперационного инсульта.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 7. График Forest plot, построенный по данным метаанализа для сравнения частоты возникновения периоперационного ИМ.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 8. График Forest plot, построенный по данным метаанализа для сравнения частоты возникновения медиастинита.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 9. График Forest plot, построенный по данным метаанализа для сравнения частоты рестернотомия по поводу кровотечений.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 10. График Forest plot, построенный по данным метаанализа для сравнения частоты возникновения ОПП.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 11. График Forest plot, построенный по данным метаанализа для сравнения частоты возникновения постоперационной ФП.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.
Летальность. Не было статистически значимой 0 разницы между группами в госпитальной летальности (RR=1,08 с 95% ДИ 0,67-1,75; р=0,75) (рис. 12) и 30-ти дневной летальности (RR=1,19 с 95% ДИ 0,81-1,75; р=0,38) (рис. 13). Все конечные точки проиллюстрированы на рис. 14.

Рис. 12. График Forest plot, построенный по данным метаанализа для сравнения частоты госпитальной летальности.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 13. График Forest plot, построенный по данным метаанализа для сравнения частоты 30-ти дневной летальности.
Сокращение: БиМКШ — бимаммарное коронарное шунтирование.

Рис. 14. Иллюстрация непосредственных результатов, госпитальной и 30-ти дневной летальности при БиМКШ in situ и композитном БиМКШ.
Сокращение: ИМ — инфаркт миокарда, ФП — фибрилляция предсердий, RR — относительный риск.
Обсуждение
Это второй систематический обзор и метаанализ сравнения двух наиболее распространенных методик при БиМКШ, первый был опубликован в 2017г Yanagawa B, et al. [22]. Данные авторы проанализировали 8 исследований, в которые были включены 5910 больных. Не было статистически значимой разницы в послеоперационных осложнениях (периоперационный ИМ, инсульт), в госпитальной, 30-ти дневной и отдаленной летальности, а также в больших сердечно-сосудистых событиях, повторной реваскуляризации, ИМ в отдаленном периоде и сердечно-сосудистой смертности. В post hoc анализе в подгруппах систематический обзор показал возможное снижение смертности от всех причин и реваскуляризации в группе in situ в исследованиях со среднесрочным наблюдением <5 лет.
Neragi-Miandoab S, et al. [23] провели небольшое проспективное РКИ сравнение БиМКШ композитного графта со свободным аортокоронарным графтом. По данным интраоперационной флоуметрии транзиторное время потока статистически значимо больше в группе со свободным аортокоронарным шунтом (38,3±13,5 мл vs 22,1±9,5 мл), р<0,01.
Nakajima H, et al. [24], сравнивая методики наложения проксимальных анастомозов при композитном БиМКШ (“I” vs “Y” графта), сообщили об увеличении антеградного кровотока при использовании “I” графтов по сравнению с “Y” графтом (92,5% vs 89,7%, P=0,049). Таким образом, эти авторы предполагают, что “Y”-трансплантат может быть более подвержен конкурентному кровотоку.
Композитные графты при БиМКШ требуют большего внимания к коронарной анатомии, включая степень проксимального стеноза и размер коронарного перфузионного резерва. В некоторых случаях композитная методика может привести к конкурентному кровотоку, но позволяет накладывать больше дистальных анастомозов. Однако мы в своем метаанализе не нашли разницы между двумя методиками при выполнении БиМКШ.
Таким образом, мы не обнаружили явного преимущества одной стратегии над другой.
Ограничения исследования. В наш систематический обзор включено небольшое количество исследований и пациентов, только меньшая часть из этих исследований является РКИ. Следовательно, трудно прийти к окончательным выводам из-за ограниченных данных. В частности, данные из обсервационных исследований следует интерпретировать с осторожностью, поскольку даже в согласованных когортах, вероятно, существует высокая степень систематической ошибки отбора при распределении пациентов по одному из методов. Вероятно, что не все пациенты в каждом из обсервационных исследований могут подходить даже для обеих методик и в рамках каждого исследования неясно, насколько результаты зависели от хирургов, а не от самой техники. Также нами не проводилось сравнение отдаленных результатов этих двух методик.
Заключение
При композитном БиМКШ накладывалось больше дистальных анастомозов с ВГА, при этом время ишемии миокарда не отличалось между группами. Мы не обнаружили статистически значимой разницы в частоте периоперационного ИМ, инсульта, медиастините, ОПП, выполнения рестернотомии по поводу кровотечения, госпитальной летальности и 30-ти дневной летальности. Но в то же время ОР развития ПОФП был статистически значимо меньше при использовании обеих ВГА in situ.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Энгиноев С.Т., Кондратьев Д.А., Магомедов Г.М., Екимов С.С., Зеньков А.А., Мотрева А.П., Кадыралиев Б.К., Чернов И.И., Тарасов Д.Г. Систематический обзор и метаанализ сравнения бимаммарного коронарного шунтирования in situ с композитным бимаммарным шунтированием: непосредственные результаты и 30-ти дневная летальность. Российский кардиологический журнал. 2021;26(2S):4504. https://doi.org/10.15829/1560-4071-2021-4504
Скопировать