Применение акселерометров в частотно-адаптивных кардиостимуляторах
Аннотация
Хронотропная некомпетентность — нарушение способности сердца адекватно увеличивать частоту сокращений в ответ на физическую нагрузку — широко распространена у пациентов с брадиаритмиями и сердечной недостаточностью.
Частотно-адаптивные электрокардиостимуляторы, оснащённые сенсорными технологиями, представляют собой эффективный инструмент компенсации хронотропной недостаточности. Среди различных типов сенсоров наиболее широко применяются акселерометры — миниатюрные устройства, чувствительные к изменениям положения тела и уровню физической активности.
Современные разработки в области кардиостимуляции, включая беспроводные (leadless) капсульные электрокардиостимуляторы, демонстрируют расширенное применение акселерометров не только для определения уровня активности, но и для регистрации механических событий сердечного цикла, таких как сокращения предсердий, обеспечивая атриовентрикулярную синхронность у пациентов с нарушениями проводимости.
Целью обзора является анализ современных данных литературы, посвящённых применению акселерометрических датчиков в частотно-адаптивных кардиостимуляторах. Приоритет отдавался работам, содержащим оценки эффективности применения акселерометрических датчиков и сравнительный анализ различных сенсорных решений в системах частотно-адаптивной стимуляции.
Имплантируемые кардиостимуляторы с адаптивной частотой предназначены для устранения брадикардии и хронотропной недостаточности.
Хронотропная недостаточность относится к неспособности сердца адаптировать (увеличить до 85% максимальной частоты сердечных сокращений (ЧСС) по возрасту) свою частоту для улучшения сердечного выброса в ответ на метаболические потребности во время физической нагрузки и/или стресса. При этом расстройстве генерируется недостаточная ЧСС относительно потребностей организма, что приводит к недостаточному кровоснабжению, усталости, одышке, снижению толерантности к физической нагрузке и снижению качества жизни. Хронотропная недостаточность является независимым предиктором серь-
езных неблагоприятных сердечно-сосудистых событий и общей смертности. Это расстройство часто связано с другими дисфункциями сердечно-сосудистой системы, включая сердечную недостаточность. Имплантируемые кардиостимуляторы успешно используются для лечения некоторых из этих дисфункций [1, 2].
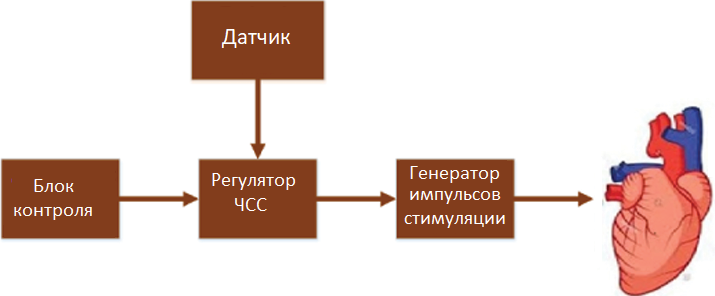
Для решения этих проблем современные электро-кардиостимуляторы (ЭКС) оснащаются датчиками, реагирующими на физиологические изменения: пьезоэлектрический датчик, датчиками активности (акселерометры), датчиками вентиляции легких, измерителями сократимости миокарда, анализом импеданса и др. Ранее использовались в большом объеме пьезоэлектрические датчики, в дальнейшем начали использовать акселерометры. На рисунке 1 представлены принципы работы различных датчиков, их конструкция, методы обработки сигнала и алгоритмы адаптивной стимуляции, а также роль и сравнительный анализ в первую очередь пьезоэлектрического датчика и акселерометра [1, 3].
Физические основы и конструкции датчиков в кардиостимуляторе
В кардиостимуляторах первых поколений использовали пьезоэлектрический датчик вибрации — изгибаемый консольный баллон с грузом, например кристалл, прикрепленный к внутренней стенке корпуса стимулятора (Medtronic Activitrax и др.). Такой датчик реагировал на сотрясения и движения грудной клетки, порождая электрический сигнал при сгибе пьезоэлемента. Однако отклик пьезодатчика зависел от положения устройства и окружающих тканей, требовалась калибровка под каждого пациента.
Акселерометр — это датчик ускорения, измеряющий изменение скорости объекта [4]. В основе работы большинства современных акселерометров лежит микромеханическая структура (МЭМС): микроскопический инерционный груз, подвешенный на упругих элементах (мембранах, балках) внутри кремниевого чипа [5]. При ускорении устройства инерционный груз смещается, и датчик преобразует это смещение в электрический сигнал пропорционально ускорению. В современных МЭМС-акселерометрах часто применяется емкостной принцип: отклонение кремниевой структуры меняет емкость конденсатора, что фиксируется встроенной электроникой. Существуют также акселерометры на основе пьезорезистивного эффекта и пьезоэлектрические микроэлементы [6]. Конструкции акселерометров в медицинских имплантах должны быть миниатюрными, надежными и мало энергопотребляющими, а также устойчивыми к длительной работе в замкнутом герметичном объёме (рис. 2).
Впоследствии производители перешли на интеграцию трёхосевых МЭМС-акселерометров, устанавливаемых на печатной плате генератора импульсов. Пример — сенсор OmniSense в устройствах St. Jude Medical или акселерометры Medtronic последних поколений. Эти датчики имеют фиксированную собственную массу и потому менее зависят от особенностей тела пациента; они дают более воспроизводимый и пропорциональный сигнал ускорения. Как правило, используется чувствительность по одной оси — обычно переднезадней оси, совпадающей с основным направлением движения туловища при ходьбе. Тем не менее акселерометр фактически улавливает все ускорения корпуса устройства, включая гравитацию и вибрации окружения. Для борьбы с артефактами современные сенсоры нередко реализуют многоосевую чувствительность с объединённым выходом. Например, патент Medtronic (Moberg, 1998) раскрыл конструкцию акселерометра с консольной балкой и смещённым грузом, чувствительного сразу по нескольким осям, но с одним выходным сигналом (рис. 3). Такой датчик на основе пьезополимерной пленки имел выход ~1 В/g, что значительно выше прежних ~10 мВ/g у пьезокристаллов. Повышенная чувствительность улучшает регистрацию слабых движений пациента [7, 8].
Помимо акселерометров в корпусе ЭКС, разрабатывались и альтернативные конструкции1 [9, 10]. В 1990-х годах предложен датчик кардиальной сократимости — акселерометр, размещенный в самом конце электрода внутри сердца. Датчик пикового эндокардиального ускорения установлен в герметичную капсулу на кончике эндокардиального электрода. Он улавливает микровибрации, возникающие при работе сердца — в частности, вибрацию миокарда во время изоволюмической сократимости (тоны сердца). Конструкция капсулы сделана жесткой, чтобы исключить артефакты от сдавления электрода миокардом — акселерометр реагирует только на инерционные силы сокращающегося сердца. Электронный модуль в электроде предварительно обрабатывает сигнал и передает его по проводнику в генератор. Исследования Rickards и его коллег (PACE, 1996) продемонстрировали, что пик эндокардиального ускорения коррелирует с максимальной скоростью нарастания давления в желудочке, т.е. с силой сокращения миокарда. Таким образом, акселерометр в конце электрода позволяет оценивать инотропное состояние сердца. Компания Sorin (Италия) внедрила датчик пикового эндокардиального ускорения в свои системы, назвав эту технологию Son R. Преимущество такого датчика — способность реагировать как на физическую нагрузку, так и на эмоциональный стресс, поскольку измеряется непосредственно гемодинамическое изменение (сила сокращений). Однако требуется специальный датчик-электрод, совместимый лишь с определёнными моделями ЭКС, и на практике такие решения использовались ограниченно [10].
Датчик минутной вентиляции — сенсор, который рассчитывает частоту кардиостимуляции на основе частоты дыхания и дыхательного объема легких [11]. Может использоваться как физиологический датчик повышенной метаболической потребности, связанной со стрессом или физической нагрузкой. Минутная вентиляция легких может быть измерена путем оценки внутригрудного импеданса, соотношения газа в крови и тканях на протяжении всего дыхательного цикла. В кардиостимуляторах минутная вентиляция легких основана на мониторинге изменений внутригрудного импеданса, измеряемых в цепи между генератором импульсов и наконечником ЭКС. К сожалению, этот датчик имеет свои ограничения. Он подвержен нарушениям и изменениям внутригрудного импеданса, которые не связаны с физической и эмоциональной нагрузкой. Точность измеряемых показателей может быть снижена в ситуациях, когда тело находится в разном положении (сидя или лежа), а также в зависимости от вида нагрузки (бег или езда на велосипеде). Этот датчик также имеет ограниченное применение у пациентов с респираторными заболеваниями. Существенным недостатком этого решения является его подверженность помехам, связанным с другим медицинским оборудованием. Нарушения контроля ЧСС возникали у пациентов с системами искусственной вентиляции легких и суточного мониторинга сердечного ритма, а также во время чреспищеводной эхокардиографии. Эта система также была успешно апробирована на педиатрических пациентах [12].
Датчик интервала QT также используется для адаптации частоты стимуляции к метаболическим потребностям организма. Он основан на измерении интервала QT. При нагрузке физической или эмоциональной интервал QT укорачивается, вследствие — частота стимуляции будет увеличиваться. Датчик имеет свои недостатки: реакция значительно запаздывает во времени, некорректное определение значений интервала QT при использовании лекарственных препаратов, невосприятие зубца Т при остром инфаркте миокарда. Этот сенсор лучше использовать с акселерометрами для дополнения друг друга и более точного отображения значений (рис. 4).
В обзоре Dell’Orto S, et al. отмечается, что специальные сенсорные электроды в целом уступили по надежности и простоте обычным датчикам активности в корпусе и ныне применяются скорее для мониторинга гемодинамики, а не для частотной адаптации. Современные кардиостимуляторы в подавляющем большинстве используют акселерометры, расположенные в корпусе, иногда в сочетании с другим сенсором для повышения физиологической адаптации ЧСС [13].

Рис. 1. Схема кардиостимулятора с частотной адаптацией сердечных сокращений.
Примечание: исключая датчик, остальное представляет собой базовую блок-схему кардиостимулятора. Блок контроля (чувствительный блок) регистрирует внутренние импульсы пациента с брадикардией, генератор сигналов возбуждения подает стимулы к мышцам сердца, а регулятор частоты сердечных сокращений контролирует длительность подаваемого.
Сокращение: ЧСС — частота сердечных сокращений.

Рис. 2. Схема конструкции генератора импульсов с встроенным датчиком активности на основе акселерометра и пьезоэлектрического кристалла.

Рис. 3. Модель механического акселерометра.
Примечание: при увеличении ускорения, масса будет растягивать пружину. По закону Гука можно с легкостью найти ускорение системы: a= , где k — коэффициент упругости пружины, δx — ее растяжение и m — масса груза. Используя три перпендикулярно расположенных датчика, можно узнать ускорение предмета по 3-м осям и, зная начальные условия, определить положение тела в пространстве.

Рис. 4. График зависимости нагрузки, ЧСС и интервала QT.
Примечание: при увеличении нагрузки укорачивается интервал QT, при укорочении интервала QT увеличивается ЧСС после обработки информации в ЭКС.
Сокращения: ЧСС — частота сердечных сокращений, ЭКС — электрокардиостимулятор.
Считывание сигнала и обработка данных акселерометра
Акселерометр генерирует электрический сигнал (аналоговый), характер которого связан с движениями пациента. В кардиостимуляторе этот сигнал проходит через каскад обработки: предварительное усиление и фильтрация, аналого-цифровое преобразование и алгоритмы выделения параметров движения. Главная задача — определить интенсивность физической активности на основе шума и вибраций, измеренных датчиком, и скорректировать ее с требуемой частотой стимуляции сердца. Различные производители реализовали схожие подходы к выделению показателя «уровня активности»: обычно измеряется частота и амплитуда колебаний корпуса ЭКС. Например, в первых устройствах Medtronic с пьезодатчиком подсчитывали число вибрационных импульсов, превышающих заданный порог, за определенное время; затем по числу импульсов вычислялась требуемая прибавка к частоте стимуляции. В таких системах врач программировал две ключевые настройки: чувствительность датчика (порог) — минимальную амплитуду движения, при которой оно учитывается, и крутизну (наклон) реакции — степень увеличения ЧСС при росте активности [14-16].
Современные устройства используют более сложные алгоритмы. Medtronic применяет метод «скользящего порога»: устройство динамически подстраивает порог детекции под фоновые условия [1]. Мелкие частые вибрации (например, при езде в автомобиле) отфильтровываются повышением порога, тогда как резкие сильные ускорения (характерные для шагов, бега) фиксируются и учитываются. Это снижает ложные срабатывания на внешние вибрации. Далее, алгоритм подсчитывает счётчик активности — условное число «шагов/толчков» в единицу времени, скорректированное по амплитуде сигналов. На основании этого рассчитывается сенсорная частота, т.е. рекомендуемая ЧСС стимуляции. Реализация обычно задаётся в виде двухфазной или трехфазной кривой зависимости частоты от уровня активности. Например, в алгоритмах Medtronic имеется диапазон с умеренными нагрузками, в котором ЧСС повышается до некоторого среднего уровня, и диапазон с более интенсивными нагрузками, где ЧСС приближается к верхнему пределу. Врач настраивает три точки: нижний порог частоты, целевую частоту для обычной активности и максимальную частоту при нагрузке. Алгоритм распределяет требуемое число шагов/с между этими зонами.
Отдельно программируются динамические характеристики: время реакции — как быстро начинается разгон ЧСС при обнаружении активности, и время восстановления — как медленно ЧСС возвращается к базовой после прекращения движения. Например, в кардиостимуляторах Boston Scientific задаются эти параметры в секундах, позволяющие сглаживать резкие изменения. Кроме того, многие современные ЭКС имеют автономную автонастройку датчика. Так, устройства St. Jude (Abbott) могут работать в автоматическом режиме для порога и наклона: за 18 ч покоя они автоматически определяют фоновый уровень сигналов и выставляют оптимальный порог чувствительности; а по вариации активности за неделю — подбирают крутизну так, чтобы ~1% времени пациента приходилось на высокие нагрузки (чтобы использовать резерв ЧСС). Medtronic в своих моделях Kappa/Adapta вводила функцию оптимизации физической активности: прибор ежедневно сравнивает полученный профиль частоты с некоторым целевым (нормальным для данного возраста/пола) и постепенно подстраивает чувствительность сенсора, ускоряя или замедляя реакцию. Świerżyńska E, et al. автоматически оптимизировали настройки сенсора под дневную активность пациента, что дало более физиологичный ответ ЧСС при тестах ходьбы по сравнению с устройствами, где датчик настраивался вручную [1].
Система считывания акселерометра также распознаёт паттерн сигнала, помимо амплитуды. В патенте US5649968A (Thacker et al., 1997) предложен анализ формы сигнала акселерометра для различения типов нагрузки — например, ходьба по ровной, в гору или с горы дают разные соотношения положительных/отрицательных колебаний [6]. Устройство сравнивает морфологию сигнала движения и способно «подправлять» частоту стимуляции, делая её более адекватной конкретному типу упражнения. Такой подход повышает специфичность сенсора, хотя и усложняет обработку. В целом же основная стратегия остаётся такой: датчик движения обеспечивает быстрый прирост ЧСС при начале активности, но требует фильтрации артефактов и ограничения чрезмерной реакции. Акселерометры чрезвычайно чувствительны к любым механическим движениям тела, но имеют некоторые недостатки — «нефизиологичность» (реагируют только на движения, а не на истинную метаболическую потребность), отсутствие отклика на психоэмоциональный стресс и ложные срабатывания при движениях без нагрузки (например, езда в транспорте, сильный кашель). Именно поэтому оптимальная система часто комбинирует сигнал акселерометра с другим сенсором [17, 18].
Алгоритмы адаптивной стимуляции и роль акселерометра
Алгоритм частотной адаптации в кардиостимуляторе — это программа, которая по выходным данным датчиков определяет, до какого значения повысить частоту стимуляции сердца. Проще говоря, акселерометр сообщает устройству «пациент движется интенсивно», и ЭКС увеличивает частоту импульсов в заданных пределах. Базовый принцип — линейное или ступенчатое увеличение ЧСС пропорционально уровню активности. Однако практическая реализация значительно сложнее из-за разнообразия условий. Современные алгоритмы включают несколько механизмов:
- Порог чувствительности и коэффициент реагирования: как упомянуто, этими параметрами задаётся базовая кривая «нагрузка-ЧСС» [11, 13]. Правильная настройка крайне важна — недостаточная чувствительность приведёт к слабому ответу (пациент ощущает усталость при нагрузке), а чрезмерная — к «гиперхронотропии» (ненужному учащению пульса). Клинические испытания, проведенные Candinas со своими коллегами, продемонстрировали, что акселерометры способны более точно и быстро подбирать частоту стимуляции под уровень усилия, чем старые пьезокристаллические датчики. В исследовании Srivastava R, et al. [2] было проведенопрямое сравнение двух типов сенсоров: оказалось, что акселерометр обеспечивает прирост частоты примерно на 90% быстрее, чем пьезоэлектрический датчик (рис. 5). Это подтверждает, почему акселерометры вытеснили прежние решения.
- Ограничение максимальной частоты: алгоритмы учитывают программируемый верхний предел (например, 140 уд./мин) и возрастной максимум пациента. Даже если датчик «хочет» более высокую ЧСС, стимуляция не превысит безопасный предел. Кроме того, во избежание резких скачков, многие ЭКС вводят плавное насыщение — при достижении зоны высоких нагрузок прибавка ЧСС замедляется.
- Двойные сенсоры: чтобы компенсировать недостатки одного датчика, часто комбинируют два. Самая распространённая пара — акселерометр и датчик минутной вентиляции легких. Акселерометр обеспечивает мгновенный начальный отклик (разгон ЧСС при старте движения), а сенсор вентиляции легких (измеряющий дыхательный объем/частоту по изменению грудного импеданса) даёт более специфическую и пропорциональную реакцию, соответствующую реальной потребности в кислороде. В комбинации ускоренный, но «слепой» датчик активности дополняется медленным, но физиологичным датчиком метаболизма. Алгоритм таких систем реализует согласование сигналов: либо усреднение, либо приоритизацию. Например, в системе Boston Scientific оба сенсора активны и устройство усредняет рассчитанные ими требуемые частоты или отдает предпочтение тому, чей сигнал убедительнее, в разных диапазонах ЧСС. При низких нагрузках большую значимость получает акселерометр, при возрастании усилия — больший вклад вносит вентиляционный сенсор (поскольку на высоких уровнях последний точнее отражает потребность). Также реализована взаимная проверка: прирост частоты происходит лишь если оба датчика согласны или доминирующий датчик активен, что предотвращает ложные срабатывания (например, при внешних вибрациях акселерометра без увеличения вентиляции, ЧСС не повысится). Клинические исследования (например, DUSISLOG, 2006) показали, что у пациентов с двойным сенсором достигается наиболее близкий к естественному профиль ЧСС при нагрузке, с ошибкой <10% от нормального синусового ритма (рис. 6)2.
- Закрытый контур: альтернативный подход — не измерять движение или дыхание, а отслеживать непосредственно гемодинамический отклик сердца [19]. Пример — технология замкнутого цикла стимуляции от Biotronik, использующая измерение внутрисердечного импеданса через электрод для оценки изменений сократимости миокарда. Повышение контрактильной функции сердца при стрессе (физическом или эмоциональном) вызывает снижение импеданса, и стимулятор увеличивает ЧСС на основе этой обратной связи. Закрытый контур считается более «физиологичным» методом, способным реагировать и на эмоции, и на разные виды нагрузки. Механизм исключает в большей степени вазовагальные эпизоды синкопе, увеличивая силу сокращения сердца на пресинкопальной фазе, что является физиологической реакцией для их предотвращения. Активация замкнутого цикла стимуляции в этом механизме позволяет поддерживать минутный объем в момент снижения давления. После частота стимуляции сердца возвращается постепенно к начальным значениям в соответствии с программой стимуляции. Из-за принципа, лежащего в основе датчика, у 88% пациентов с вазовагальными эпизодами отмечалось снижение синкопальных симптомов (рис. 6).
Однако и у него есть ограничения — например, у пациентов после инфаркта импедансный отклик может быть слабым. В контексте нашей темы важно, что акселерометр в таких системах тоже часто присутствует (для подстраховки): например, устройства Biotronik с замкнутым циклом стимуляции всё равно имеют акселерометр на случай, если импедансный сигнал недостаточен при резком движении. Таким образом, акселерометр остаётся ключевым компонентом большинства адаптивных алгоритмов, либо как основной, либо как вспомогательный сенсор3.
На рисунке 7 изображены схематически отличия в работе замкнутого цикла стимуляции и акселерометра. Закрытый контур способен реагировать и увеличивать ЧСС, на незначительные изменения во время эмоциональной нагрузки, приема лекарственных препаратов, чего не может акселерометр.
Роль акселерометра в оценке активности пациента сводится к тому, что он выступает простым суррогатным индикатором физической нагрузки. Датчик измеряет движение тела — параметр непосредственно не равный потребности в сердечном выбросе, но тесно связанный с ней при типичных повседневных действиях. Благодаря высокой чувствительности акселерометр способен раньше других сенсоров зафиксировать начало активности: он реагирует практически мгновенно на шаги, изменение положения, вибрацию мышц. В то же время он не различает причину движения — отсюда и ложные срабатывания. Инженеры решили эту проблему сочетанием алгоритмов: фильтрацией частот, задержкой реакции (требуется несколько подряд «шагов», чтобы повысить ЧСС, во избежание реакции на единичные движения) и возможностью быстрого снижения ЧСС, если движение прекратилось (чтобы не перегружать сердце зря).
Отдельно стоит упомянуть акселерометр в беспроводных кардиостимуляторах, таких как Medtronic Micra (рис. 8). Эти миниатюрные капсульные стимуляторы тоже оснащены акселерометром. В однокамерной версии (Micra VR, режим VVIR) акселерометр служит единственным датчиком для частотной адаптации, ускоряя ритм при повышении интенсивности вибраций тела во время нагрузок. Более того, в усовершенствованной модели Micra AV акселерометр задействован дважды: он не только отслеживает активность пациента, но и регистрирует механические колебания, связанные с работой предсердий. Micra AV работает в режиме VDD, пытаясь сохранять AV-синхронизм без предсердного электрода. Для этого акселерометр «слушает» звук/вибрацию потока крови через атриовентрикулярные клапаны после сокращения предсердий — по тонким сотрясениям при открытии митрального клапана алгоритм определяет момент предсердной систолы и вовремя вызывает стимулирование QRS комплекса. Таким образом, достигается синхронная работа желудочка, управляемая собственным предсердием пациента, без наличия предсердного электрода (поскольку капсула лишь в желудочке). Это новейшее применение акселерометра демонстрирует его универсальность: по сути, миниатюрный датчик ускорения внутри сердца исполняет роль фонендоскопа, различая тоны клапанов и обеспечивая адаптацию ритма к физиологии сердечного цикла. Ограничение такого подхода — он годится только при сохранном синусовом ритме (Micra AV не стимулирует предсердие), но тем не менее для многих пациентов с атриовентрикулярной блокадой эта технология значительно улучшила синхронизацию и толерантность к нагрузке2 [18].

Рис. 5. Сравнение отклика пьезоэлектрического датчика и акселерометра.

Рис. 6. Схема алгоритма замкнутого цикла стимуляции.
Сокращения: АД — артериальное давление, ХН — хронотропная недостаточность, ЧСС — частота сердечных сокращений.

Рис. 7. Схема изменений артериального давления и ЧСС на стимуляции по замкнутому циклу и стимуляции с помощью акселерометра.
Сокращения: АД — артериальное давление, ЧСС — частота сердечных сокращений.

Рис. 8. Наглядное расположения кардиостимулятора Medtronic Micra.
Заключение
Акселерометр прочно занял место основного сенсора в адаптивных кардиостимуляторах благодаря простоте конструкции, быстроте отклика и миниатюрности. Он обеспечивает повышение ЧСС при физической активности пациента, тем самым имитируя естественную работу синусового узла и улучшая переносимость нагрузок у пациентов с брадикардиями и хронотропной некомпетентностью. Физически акселерометр представляет собой чувствительный элемент, измеряющий ускорение (в современных приборах — микромеханический кремниевый датчик). В кардиостимуляторах применяются как одиночные датчики ускорения, так и их комбинации с другими сенсорами (дыхания, импеданса, электрокардиография), что позволяет преодолеть ограничения каждого метода и достичь более физиологичного реагирования. Развитие алгоритмов обработки сигнала — от простого порогового детектора шагов до интеллектуальных систем с автокалибровкой и анализом формы сигнала — существенно повысило точность и надежность акселерометра.
1 Ellenbogen K, Caszala K. Sensor technology and rate responsiveness. Medscape. https://www.medscape.org/viewarticle/724645.
2 Basic cardiac pacing, pacemaker functions and settings [Internet]. ECGWaves (ECG & Echo Learning). 2020. Available from: https://ecgwaves.com/topic/basic-cardiac-pacing-pacemaker-functions-and-settings/.
3 ClinicalTrials.gov NCT05549544: Clinical Efficacy of Left Bundle Branch Area Pacing for Patients With Permanent Atrial Fibrillation and Heart Failure (LBBAP-AFHF) [Internet]. Bethesda (MD): National Library of Medicine (US); 2022. Available from: https://clinicaltrials.gov/study/NCT05549544.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Аванесян Г.А., Филатов А.Г., Сатюкова А.С., Панагов З.Г., Яхьяев Я.Б. Применение акселерометров в частотно-адаптивных кардиостимуляторах. Российский кардиологический журнал. 2025;30(3S):6703. https://doi.org/10.15829/1560-4071-2025-6703. EDN: YDFKOH
Скопировать