Спонсорский материал
Клиническое значение оценки метаболизма и перфузии миокарда правого желудочка с помощью позитронно-эмиссионной томографии, совмещенной с компьютерной томографией, у пациентов с легочной артериальной гипертензией
Аннотация
Легочная артериальная гипертензия (ЛАГ) — гемодинамическое и патофизиологическое состояние, сопровождающееся высокой летальностью вследствие правожелудочковой сердечной недостаточности. Современные методы обследования констатируют уже произошедшее ремоделирование и дисфункцию миокарда правого желудочка. Поиск неинвазивных методов диагностики, позволяющих выявлять ранние признаки маладаптации миокарда правого желудочка, критически важен для адекватной стратификации риска летальности и оценки эффекта терапии с целью выбора оптимальной стратегии ведения и улучшения прогноза у пациентов с ЛАГ.
Обзор посвящен применению позитронной эмиссионной томографии, совмещенной с компьютерной томографией (ПЭТ/КТ) у пациентов с ЛАГ. ПЭТ/КТ позволяет анализировать механизмы развития заболевания на уровне тканевого метаболизма и перфузии, что недоступно при использовании традиционных методов диагностики. В перспективе ПЭТ/КТ может стать важным инструментом научного поиска новых мишеней терапии и персонализированного подхода к лечению пациентов с ЛАГ.
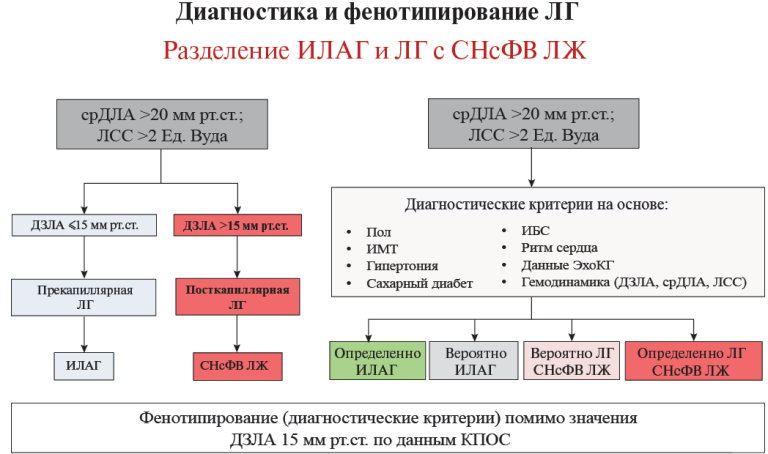
Легочная гипертензия (ЛГ) — гемодинамическое и патофизиологическое состояние, характеризующееся повышением среднего давления в легочной артерии (срДЛА) ≥20 мм рт.ст., определяемое во время катетеризации правых камер сердца (КПКС) в состоянии покоя [1]. Для легочной артериальной гипертензии (ЛАГ) характерно повышение легочного сосудистого сопротивления (ЛСС) >2 ед. Вуда при нормальном давлении заклинивания в легочной артерии (давление заклинивания в легочной артерии <15 мм рт.ст.). ЛГ может возникать как первичное заболевание (идиопатическая ЛАГ (ИЛАГ)) или быть ассоциированной с другими заболеваниями. Считается, что в основе патогенеза ЛАГ лежит дисфункция эндотелия легочных артерий с нарушением синтеза вазодилататоров (оксид азота, простациклин I2) и избыточного образования эндотелина-1, обладающего мощной вазоконстрикторной и пролиферативной активностью [2]. Ремоделирование интра- и преацинарных легочных артерий неразрывно связано с процессами воспаления и ангиогенеза [3]. Формирование плексиформных изменений усугубляет редукцию эффективного микроциркуляторного русла. Уменьшение просвета легочных артерий сопровождается повышением ЛСС и ростом давления в легочной артерии. Инвазивная оценка гемодинамики малого круга кровообращения является золотым стандартом верификации ЛГ и ее гемодинамического варианта, а также определения тяжести и прогноза ЛАГ [1]. Однако основной причиной летальности пациентов с ЛАГ является правожелудочковая сердечная недостаточность (СН). Выявление дисфункции миокарда правого желудочка (ПЖ) на ранних этапах маладаптивного ремоделирования, до развития клинических проявлений и своевременная эскалация ЛАГ-специфической терапии остается актуальной проблемой ведения пациентов с ЛАГ. Индивидуальные возможности миокарда ПЖ по преодолению повышенного давления в легочной артерии определяют течение ЛАГ [4], что, в свою очередь, обусловлено особенностями строения и задачами ПЖ.
Методология исследования
Поиск публикаций осуществлялся в научных базах данных PubMed, Wiley Online Library и eLibrary. По результатам проведенного поиска отобрано 15 публикаций, отражающих применение позитронной эмиссионной томографии, совмещенной с компьютерной томографией (ПЭТ/КТ) в диагностике ЛАГ, опубликованных в период с 2005 по 2025гг. Для формирования поисковых запросов использовались ключевые слова и их комбинации: «легочная гипертензия», «легочная артериальная гипертензия», «позитронно-эмиссионная томография», «метаболизм», «перфузия», «правый желудочек», «[ 18F]-фтордезоксиглюкоза».
Результаты
Анатомия и физиология ПЖ
ПЖ и левый желудочек (ЛЖ) сердца имеют различное эмбриологическое происхождение. ЛЖ и серповидная трубка формируется из первичного сердечного поля, ПЖ и выходной тракт развивается из клеток вторичного сердечного поля [5]. Дифференцировка кардиомиоцитов контролируется определенными генами. Например, ген Paired-Like Homeodomain 2 (PITX2) определяет лево-правую асимметрию, гены Heart and Neural Crest Derivatives Expressed (HAND1 и HAND2) влияют на развитие ЛЖ и ПЖ, соответственно [6].
У плода и новорожденного ПЖ представляет собой камеру с толстыми стенками, совершающую работу в условиях высокого сопротивления сосудов легких. Толщина стенок обоих желудочков увеличивается параллельно и достигает ~3,5 мм к моменту рождения. После рождения легочное сопротивление снижается, и толщина стенки ПЖ остается ~4 мм, тогда как миокард ЛЖ сталкивается с большей постнагрузкой, что приводит к увеличению толщины стенки ЛЖ до ~11 мм [7].
В экспериментальных исследованиях на животных моделях обнаружены морфофункциональные различия между кардиомиоцитами желудочков: клетки ЛЖ по сравнению с миоцитами ПЖ характеризуются большей длиной, шириной и общими размерами, а также большей амплитудой сокращения, кинетикой сокращения и расслабления [8][9]. Кроме того, митохондрии ПЖ продуцируют больше активных форм кислорода [9]. Эти данные позволяют предположить, что ЛЖ и ПЖ обладают различными механизмами адаптации к нагрузкам.
Структура миокарда желудочков также различается. Свободная стенка ПЖ представлена в основном поперечными волокнами и небольшой долей субэндокардиальных продольных волокон. В ЛЖ эндокардиальные и эпикардиальные волокна формируют спиральную структуру, дополненную циркулярными волокнами в среднем слое. Следовательно, миокард ПЖ тоньше по сравнению с миокардом ЛЖ (примерно одна треть ЛЖ) [6]. Наряду с различиями в анатомии, ПЖ имеет более высокое содержание внеклеточного матрикса по сравнению с ЛЖ [10], что делает его более комплаентным к возврату венозной крови без существенного повышения конечного диастолического давления к норме. ПЖ имеет серповидную форму, тогда как ЛЖ — конусообразную. ПЖ разделен на три сегмента: приносящий отдел, включающий трикуспидальный клапан, хорды и папиллярные мышцы; верхушка; выносящий отдел (конус или инфундибулум). ПЖ сокращается перистальтической волной от синуса к конусу [11]. Поверхностный слой миокардиальных волокон ПЖ связан с волокнами ЛЖ, что объясняет движение свободной стенки ПЖ в сторону межжелудочковой перегородки во время систолы. Более глубокий слой вертикально ориентированных волокон обеспечивает продольное укорочение ПЖ, что используется в эхокардиографии (ЭхоКГ) для оценки функции ПЖ с помощью измерения амплитуды систолического движения кольца трикуспидального клапана (tricuspid annular plane systolic excursion, TAPSE). TAPSE <18 мм ассоциировано с неблагоприятным прогнозом у пациентов с ЛАГ. Комбинированный параметр TAPSE/систолическое давление в легочной артерии (СДЛА) (норма >0,55 мм/мм рт.ст.) тесно связан с сопряжением ПЖ и легочной артерии (ПЖ-ЛА) и прогнозирует исход заболевания [12]. Tello K, et al. (2018) проанализировали клиническую значимость соотношения TAPSE/СДЛА у 290 пациентов с ЛАГ [13]. Соотношение TAPSE/СДЛА <0,19 мм/мм рт.ст. было ассоциировано с более худшими показателями гемодинамики и физической работоспособности по сравнению с пациентами, имевшими более высокий показатель TAPSE/СДЛА (0,19-0,32 мм/мм рт.ст. и >0,32 мм рт.ст., соответственно). Учитывая тесную взаимосвязь показателя сопряжения ПЖ-ЛА с выживаемостью пациентов с ЛАГ, клиническими и гемодинамическими показателями, соотношение TAPSE/СДЛА было внесено в шкалу стратификации риска летальности ESC/ERS2022 в качестве одного из предикторов летальности [1]. Другим показателем систолической функции ПЖ является скорость движения латеральной части фиброзного кольца трикуспидального клапана (TAPSV или S’, см/с), который определяется с помощью тканевой допплерографии. Значение S′ >10,5 см/сек ассоциировано с сохранной систолической функцией ПЖ [14].
Различия в анатомическом строении ПЖ и ЛЖ отражаются на их перфузии. Благодаря низкому давлению в легочной артерии (в норме 20% от системного артериального давления) и ЛСС (в норме 10% от системного сосудистого сопротивления), ПЖ потребляет меньше кислорода по сравнению с ЛЖ [6]. В отличие от ЛЖ, у которого перфузия осуществляется преимущественно во время диастолы, кровоснабжение ПЖ происходит на протяжении всего сердечного цикла. Данная характеристика перфузии ПЖ является преимуществом для поддержания адекватной доставки кислорода к миокарду. Однако при наличии острой или хронической ЛГ систолическое давление ПЖ повышается, что приводит к фазовому распределению кровотока, аналогичному таковому в ЛЖ [15]. Van Wolferen SA, et al. (2008) измерили перфузию правой коронарной артерии (ПКА) у пациентов с ЛГ (5 пациентов с ИЛАГ, 9 пациентов с хронической тромбоэмболической ЛГ (ХТЭЛГ)) и 11 пациентов из контрольной группы с помощью магнитно-резонансной томографии (МРТ) с использованием количественной оценки кровотока (МР-флоуметрия) [16]. Авторы выявили, что перфузия ПКА эквивалентна между диастолой и систолой у пациентов контрольной группы, тогда как у пациентов с ЛГ кровоток по ПКА становится двухфазным с уменьшением систолического и увеличением диастолического кровотока. Превышение потребности ПЖ в кислороде над возможностями перфузии ведет к развитию ишемии ПЖ. В условиях гипоксии миокард переключается с окислительного фосфорилирования на анаэробный гликолиз. Несмотря на временную компенсацию, низкая эффективность увеличения кровоснабжения миокарда ПЖ приводит к истощению энергетических ресурсов при прогрессирующей гипертрофии миокарда ПЖ в условиях ЛАГ. Как следствие, клетки ПЖ переходят в режим гибернации [17].
Повышенная постнагрузка является основной причиной гипертрофии ПЖ и, в конечном счете, его недостаточности при ЛАГ. Переход от адаптивной гипертрофии ПЖ к маладаптивной не имеет резкой границы, а скорее отражает последовательные стадии истощения компенсаторных возможностей сердца [18, 19]. ПЖ изначально адаптируется к увеличению постнагрузки, его стенки утолщаются, сохраняя функцию и структуру. Однако устойчивая перегрузка давлением не позволяет ПЖ поддерживать адаптивную гипертрофию, и в конечном счете развивается маладаптивная гипертрофия. Данное состояние характеризуется дилатацией полости, фиброзом и нарушением сократительной функции, что приводит к снижению сердечного выброса, прогрессированию СН и ухудшению прогноза. Маладаптивная гипертрофия миокарда ПЖ также сопровождается метаболическими нарушениями, такими как переход на анаэробный гликолиз, что снижает энергетическую эффективность кардиомиоцитов. Данные изменения можно выявить с помощью ПЭТ/КТ с радиофармацевтическим лекарственным препаратом (РФЛП) 2-фтор-[ 18F]-2-дезокси-D-глюкозой ([ 18F]-ФДГ) [7].
Современные возможности диагностики ремоделирования миокарда ПЖ
Неспецифический характер жалоб в дебюте ЛАГ, наличие сопутствующей патологии левых камер сердца, респираторной системы, ожирения приводят к позд- ней диагностике заболевания. По данным современного научного регистра ЛГ США USPHSR, верификация ЛАГ в среднем составляет 1,9 лет от момента появления первых жалоб [20]. Подавляющее большинство пациентов ЛАГ на момент обращения в референтный центр ЛГ имеют симптомы и ЭхоКГ признаки дисфункции миокарда ПЖ [21], что определяет прогноз и эффективность лечения. В настоящее время диагностика ЛАГ и стратификация риска летальности представляет мультимодальный подход, включающий оценку клинической симптоматики, переносимости физической нагрузки, инвазивной гемодинамики, лабораторных маркеров СН (N-концевого промозгового натрийуретического пептида (NT-proBNP)), ремоделирования правых камер сердца и сократительной способности миокарда ПЖ [1]. Определены прогностические показатели ремоделирования и сократительной способности миокарда ПЖ и их значения, соответствующие критериям низкого, промежуточного и высокого рисков летальности (табл. 1) [1][12].
В рекомендациях по ведению пациентов с ЛГ ЭхоКГ с допплерографическим анализом представлена не только в качестве основного скринингового метода диагностики ЛГ [22-24], но и исследования, позволяющего характеризовать тяжесть и прогноз ЛАГ (табл. 1). Преимуществами ЭхоКГ являются неинвазивность, воспроизводимость и широкая доступность. Однако сложная геометрическая форма ПЖ затрудняет адекватную оценку его морфологии и функции. Золотым стандартом исследования структуры и функции ПЖ считается МРТ сердца. Благодаря превосходному пространственному разрешению и контрастному усилению МРТ преодолевает ограничения, связанные со сложной геометрией и трабекулярностью ПЖ, позволяет точно оценить объем, фракцию выброса (ФВ) и другие функциональные параметры. Метод также позволяет проводить трехмерную (3D) визуализацию в режиме реального времени, количественно оценивать кровоток (включая регургитацию на клапанах) и выявлять сложные врожденные аномалии. Помимо этого, МРТ позволяет охарактеризовать структурные изменения миокарда и внекардиальных образований [25]. Основными преимуществами МРТ являются отсутствие ионизирующего излучения и высокая точность. Однако длительность проведения исследования, несовместимость с некоторыми имплантированными устройствами и высокая стоимость ограничивают широкое внедрение МРТ сердца в клиническую практику у пациентов с ЛАГ. Следует отметить хорошую способность МРТ в дифференциации пациентов ЛАГ низкого и промежуточного риска летальности [26], что в особенности актуально с учетом текущих национальных рекомендаций по ведению пациентов с ЛАГ [12], в которых для пациентов низкого риска летальности определена стартовая монотерапия ЛАГ-специфическим препаратом. Но остается вопрос, насколько общепринятые методы исследования и стратификация риска летальности адекватно объективизируют состояние миокарда ПЖ.
Изменение метаболизма миокарда ПЖ при ЛАГ
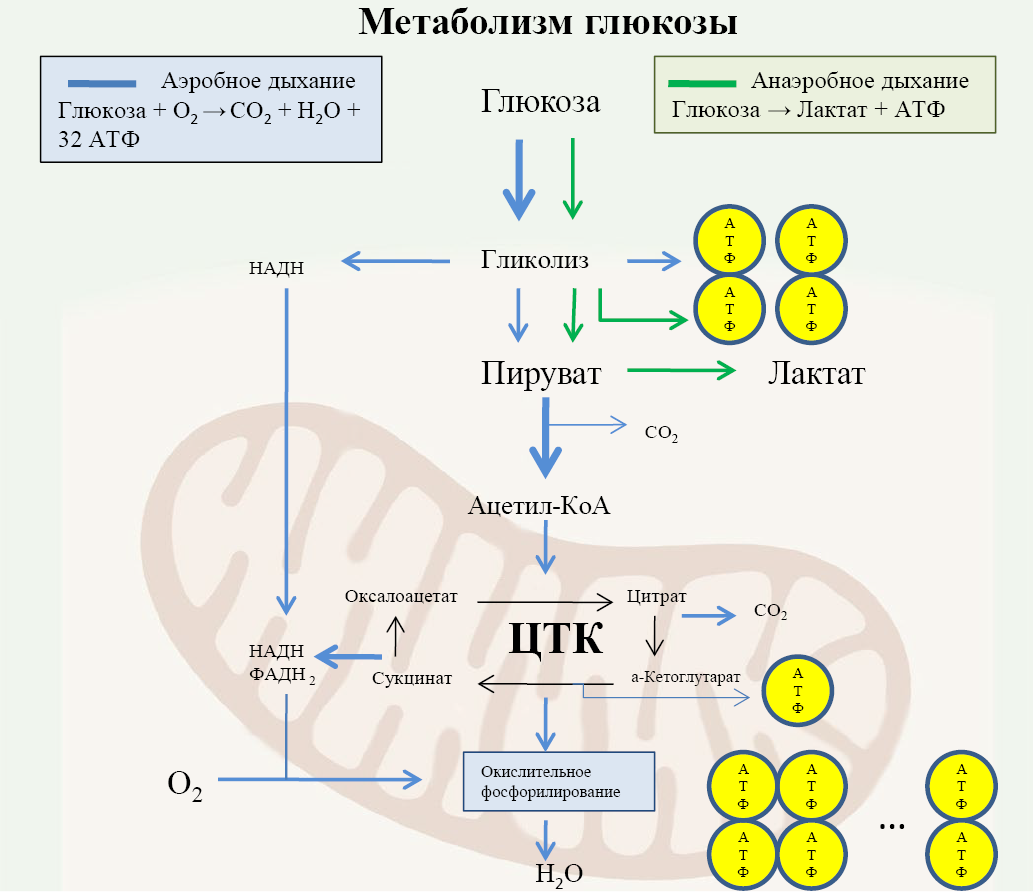
Окисление свободных длинноцепочечных жирных кислот является основным источником продукции аденозинтрифосфата (АТФ) (60-90%) в кардиомиоцитах. При этом метаболизм глюкозы составляет 10-40% от общего потребления метаболических субстратов с целью синтеза АТФ [7]. При ЛАГ происходит ремоделирование митохондрий в кардиомиоцитах миокарда ПЖ, что приводит к переходу от митохондриального окислительного фосфорилирования к цитоплазматическому гликолизу. Данный переход наблюдается в эндотелиальных клетках и гладкомышечных клетках легочной артерии, выделенных из легких с ЛАГ in vitro, а также из миокарда ПЖ и легких пациентов с ЛАГ in vivo и в животных моделях ЛАГ [27]. Глюкоза транспортируется через мембрану в цитозоль клетки посредством глюкозотранспортного белка 1 типа (Glut-1). В цитоплазме кардиомиоцита глюкоза претерпевает метаболическое превращение в гликолитическом каскаде биохимических реакций с образованием пировиноградной кислоты. Пировиноградная кислота является субстратом для митохондриальной пируватдегидрогеназы, при воздействии которой в ходе окислительного декарбоксилирования происходит образование ацетил-КоА — входного субстрата цикла трикарбоновых кислот, и выработка молекул АТФ в дыхательной цепи на мембранах митохондрий (рис. 1). При ЛАГ происходит активация киназы, ингибирующей действие пируватдегидрогеназы, что приводит к снижению окислительного фосфорилирования, уменьшению выработки АТФ и, как следствие, нарушению сократительной способности миокарда ПЖ. Метаболический сдвиг в кардиомиоцитах ПЖ в сторону гликолиза вызывает увеличение внутриклеточного транспорта глюкозы. Увеличение потребности кардиомиоцита ПЖ в глюкозе можно оценить с помощью ПЭТ/КТ с [ 18F]-ФДГ, которая является синтетическим аналогом глюкозы [29].
Таблица 1
Показатели ЭхоКГ и МРТ сердца, используемые для стратификации риска летальности у пациентов с ЛАГ [1][12]
| Факторы прогноза (оценка 1-летней летальности) | Низкий риск (<5%) | Промежуточный риск (5-20%) | Высокий риск (>20%) |
| Параметры | |||
| ЭхоКГ | Площадь правого предсердия <18 см2
Отсутствие выпота в перикарде TAPSE/СДЛА >0,32 мм/мм рт.ст. |
Площадь правого предсердия 18-26 см2
Минимальный перикардиальный выпот TAPSE/СДЛА 0,19-0,32 мм/мм рт.ст. |
Площадь правого предсердия >26 см2
Умеренный или выраженный перикардиальный выпот TAPSE/СДЛА <0,19 мм/мм рт.ст. |
| МРТ | Фракция выброса ПЖ >54%
Ударный индекс >40 мл/м2 Индекс конечно-систолического объема ПЖ <42 мл/м2 |
Фракция выброса ПЖ 37-54%
Ударный индекс 26-40 мл/м2 Индекс конечно-систолического объема ПЖ 42-54 мл/м2 |
Фракция выброса ПЖ <37%
Ударный индекс <26 мл/м2 Индекс конечно-систолического объема ПЖ >54 мл/м2 |
Сокращения: МРТ — магнитно-резонансная томография, ПЖ — правый желудочек, ЭхоКГ — эхокардиография, TAPSE/СДЛА — соотношение амплитуды систолического движения кольца трикуспидального клапана к систолическому давлению в легочной артерии.

Рис. 1. При нормальных условиях, пируват преобразуется в ацетил-КоА, метаболизируемый в цикле трикарбоновых кислот (ЦТК).
Примечание: продукты ЦТК используются в окислительном фосфорилировании, обеспечивая синтез 32 молекул АТФ на одну молекулу глюкозы. При ЛАГ происходит метаболический сдвиг с окислительного фосфорилирования на анаэробный гликолиз, в ходе которого синтезируются 2 молекулы АТФ. Адаптировано с модификациями из [28].
Сокращения: АТФ — аденозинтрифосфат, ЦТК — цикл трикарбоновых кислот.

Рис. 2. Примеры ПЭТ/КТ изображений с [ 18F]-ФДГ: (А) пациент без ЛГ (контрольная группа); (Б) пациент с ЛАГ.
Примечание: визуализируется повышенное накопление радиофармпрепарата [ 18F]-ФДГ в миокарде правого желудочка при ЛАГ (красная стрелка) по сравнению с миокардом ПЖ у пациента без ЛГ (желтая стрелка) (собственные данные).

Рис. 3. Накопление [ 18F]-ФДГ миокардом ПЖ в зависимости от категории риска летальности ESC/ERS 2022 у пациентов с ИЛАГ (верхний ряд — МРТ пациентов с ИЛАГ в зависимости от категории риска летальности; средний ряд — ПЭТ/КТ с [ 18F]-ФДГ; нижний ряд — показатели КПКС в соответствии с категорией риска летальности) [42].
Сокращения: ЛСС — легочное сосудистое сопротивление, среднее ДЛА — среднее давление в легочной артерии.
ПЭТ/КТ
На сегодняшний день нет общепринятого стандартизированного протокола выполнения ПЭТ/КТ сердца у пациентов с ЛАГ с целью выявления метаболических нарушений, ассоциированных с дисфункцией ПЖ. В зарубежных исследованиях представлены различные методики выполнения ПЭТ/КТ и алгоритмы подготовки, которые можно условно разделить на две группы: 1) после периода голодания и 2) на фоне усиления физиологического захвата глюкозы в миокарде. В случае выполнения ПЭТ/КТ после периода голодания (от 4 до 12 ч) время накопления РФЛП от момента инъекции до начала ска-нирования составляет 40-180 мин по данным разных авторов [30-38]. При использовании пероральных нагрузочных протоколов также наблюдаются существенные методологические различия между исследователями: углеводная нагрузка составляет 50-75 г глюкозы за 30-60 мин до инъекции [ 18F]-ФДГ с началом сканирования через 35-60 мин [39]. При проведении исследования метаболических изменений в миокарде ПЖ на фоне эугликемического-гиперинсулинемического клэмпа соблюдается единый принцип подготовки пациентов, но могут наблюдаться отличия в периодичности заборов крови и оценки уровня гликемии [32][40]. В исследовании, выполненном нами, у 30 пациентов с ИЛАГ проводилась пункция кубитальной вены с установкой периферического катетера для одновременной инфузии 20% глюкозы и инсулина короткого действия (40 мЕд/мин/м2) [41]. Уровень гликемии контролировали каждые 5 мин, корректируя скорость введения глюкозы для поддержания нормогликемии (5 ммоль/л). Через 1 ч после начала инфузии внутривенно вводили [ 18F]-ФДГ (5 МБк/кг), а через 40 мин выполняли электрокардиографически-синхронизированное ПЭТ/КТ сканирование. Согласно данным зарубежной литературы, в некоторых исследованиях используется препарат аципимокс (производное никотиновой кислоты). Его механизм действия включает снижение концентрации свободных жирных кислот в плазме крови и усиление метаболизма глюкозы кардиомиоцитами. Например, в исследовании Kazimierczyk R, et al. (2021) пациентам за 1 ч до ПЭТ перорально давали аципимокс (250 мг), а за 2 ч до инъекции [ 18F]-ФДГ углеводно-белковую нагрузку, для стимуляции поглощения глюкозы миокардом [42].
У пациентов с ЛАГ отмечается повышенное накопление [ 18F]-ФДГ в миокарде ПЖ, что напрямую связано с метаболическим сдвигом в кардиомиоцитах. При визуальной оценке изображений ПЭТ/КТ сердца определяется значимая разница в уровне поглощения [ 18F]-ФДГ в миокарде ПЖ у пациентов контрольной группы и у пациентов с ЛАГ (рис. 2).
Saygin D, et al. (2017) обнаружили достоверно больший уровень накопления [ 18F]-ФДГ в ПЖ и в легких у 30 пациентов с ЛГ (из них 9 пациентов с ИЛАГ) по сравнению с 8 здоровыми контролями [30]. У пациентов с ЛГ уровень соотношения [ 18F]-ФДГ ПЖ к ЛЖ коррелировал с показателями ЭхоКГ, такими как объем правого предсердия и давление правого предсердия, конечно-систолическая и конечно-диастолическая площади ПЖ, систолическое давление ПЖ, TAPSE и глобальная пиковая систолическая деформация миокарда ПЖ. Наряду с оценкой метаболической активности миокарда ПЖ осуществлялись попытки оценки метаболизма в паренхиме легких, где источниками потребления глюкозы являются эндотелиальные и гладкомышечные клетки легочной артерии. У пациентов с ЛГ интенсивность аккумуляции [ 18F]-ФДГ в паренхиме легких была достоверно выше по сравнению с контрольной группой, однако достоверные корреляционные взаимосвязи между уровнем накопления РФЛП и показателями ЭхоКГ отсутствовали. Авторы пришли к выводу, что измерение стандартизованного уровня захвата РФЛП (SUV) в легочной паренхиме не позволяет оценить тяжесть ЛГ, и использование этого параметра в клинических целях представляется малоперспективным.
Can М, et al. (2011) изучали метаболизм глюкозы в миокарде ПЖ у 23 пациентов с ЛАГ и 16 пациентов контрольной группы [31]. В группе пациентов с ЛАГ соотношение полуколичественного показателя SUV ПЖ к ЛЖ достоверно положительно коррелировало с уровнем мозгового натрийуретического пептида (BNP), уровнем СДЛА, соотношением площадей ПЖ/ЛЖ, индексом Tei, и имело отрицательную корреляционную взаимосвязь с величиной TAPSE и дистанцией в тесте 6-минутной ходьбы (ТШХ). Результаты исследования продемонстрировали взаимосвязь между тяжестью перегрузки миокарда ПЖ, увеличением метаболического запроса и дисфункцией миокарда ПЖ. Однако малая выборка пациентов не позволила выделить четкие пороговые показатели SUV [ 18F]-ФДГ, характерные для определенного уровня давления в легочной артерии или сократительной способности миокарда ПЖ.
Аналогичные результаты были получены Молоковой Е. Р. и др. (2022) [32]. 25 пациентов с подтвержденной ХТЭЛГ и 23 контрольных пациента без ЛГ прошли ПЭТ/КТ с двумя РФЛП: [ 18F]-ФДГ для оценки метаболизма глюкозы и [ 13N]-аммония для изучения перфузии миокарда. У пациентов с ХТЭЛГ и сердечным индексом (СИ) <2 л/мин/м2 наблюдалось более высокое значение отношения накопления [ 18F]-ФДГ и [ 13N]-аммония в миокарде ПЖ к ЛЖ (SUV ПЖ/SUV ЛЖ) по сравнению с пациентами с СИ >2 л/мин/м2. В исследовании выявлена прямая связь с показателями поглощения [ 18F]-ФДГ миокардом ПЖ с параметрами КПКС (СДЛА, срДЛА, диастолическое давление в легочной артерии, ЛСС, центральное венозное давление), ЭхоКГ параметрами (размеры ПЖ, расчетное давление в легочной артерии) и уровнем NT-proBNP, при этом наблюдалась обратная корреляция с дистанцией в ТШХ, функциональными показателями ЛЖ (конечный диастолический размер, ударный объем) и ПЖ (TAPSE, TASV), сатурацией кислорода в смешанной венозной крови. Аналогично, накопление [ 13N]-аммония в миокарде ПЖ положительно коррелировало с давлением в ЛА и ЛСС, но отрицательно — с размерами левого предсердия, параметрами ЛЖ (конечный диастолический размер, ударный объем, индекс массы миокарда ЛЖ) и сердечным выбросом, при этом клинико-лабораторные маркеры (дистанция в ТШХ, NT-proBNP) не продемонстрировали значимой связи с показателями перфузии.
Ohira H, et al. (2016) оценивали метаболизм глюкозы и жирных кислот в миокарде ПЖ у 17 пациентов с ЛАГ (9 — ИЛАГ, 8 — ЛАГ при заболеваниях соединительной ткани) с помощью ПЭТ/КТ с [ 18F]-ФДГ и с РФЛП на основе жирной кислоты — [ 18F]-6-тиогептадекановой кислотой (ФТГК) [33]. Поглощение [ 18F]-ФДГ и соотношение ФДГ/ФТГК в ПЖ достоверно положительно коррелировали с срДЛА и ЛСС. Уровень накопления обоих РФЛП демонстрировал достоверную отрицательную корреляционную взаимосвязь с ФВ ПЖ, определенную с помощью МРТ. Эти данные подтверждают взаимосвязь между метаболическим ремоделированием миокарда ПЖ со сдвигом в сторону гликолиза и окислением жирных кислот с гемодинамической перегрузкой, дисфункцией и маладаптацией миокарда ПЖ. Помимо этого, для оценки перфузии миокарда ПЖ этим же пациентам было проведено ПЭТ/КТ с [ 13N]-аммонием. Авторы использовали визуальный анализ перфузионно-метаболического несоответствия в миокарде ПЖ, т.к. у пациентов с ЛАГ на данный момент не существует стандартизированных методов оценки полуколичественных показателей, характеризующих интенсивность накопления РФЛП. У всех пациентов с тяжелой ЛГ (срДЛА ≥50 мм рт.ст.) выявлено перфузионно-метаболическое несоответствие в миокарде ПЖ с преобладанием метаболизма глюкозы над перфузией миокарда ПЖ, характерное для состояния гибернации. В то же время Ahmadi А, et al., Ohira H, et al. [28, 33] отмечают, что прогнозирование тяжести ЛГ на основе результатов перфузионной ПЭТ/КТ сердца вызывает трудности, т.к. паттерн распределения перфузионного РФЛП в миокарде ПЖ в условиях нормального давления в системе легочной артерии до сих пор неизвестен.
Hagan G, et al. (2011) оценивали накопление [ 18F]-ФДГ в паренхиме легких, проксимальных отделах легочных артерий и в миокарде ПЖ у 14 пациентов с ЛГ (8 пациентов с ИЛАГ и 6 пациентов с ХТЭЛГ) и 6 пациентов из контрольной группы [34]. У пациентов с ИЛАГ наблюдались достоверно более высокие значения аккумуляции [ 18F]-ФДГ в паренхиме легких и в ПЖ по сравнению с контрольной группой. При этом достоверных различий в накоплении [ 18F]-ФДГ в клетках проксимальных отделов легочной артерии между пациентами с ХТЭЛГ, ИЛАГ и в контрольной группе не обнаружено. Авторы предположили, что отсутствие значимого увеличения захвата РФЛП в проксимальных отделах легочных артерий обусловлено локализацией патологического процесса в мелких субсегментарных легочных артериях у пациентов с ЛАГ. Усиленное накопление РФЛП в паренхиме легких может быть связано с изменениями гликолитического метаболизма в эндотелиальных клетках при ИЛАГ или увеличением количества клеток, вовлеченных в воспалительный процесс.
В исследовании Sumer C, et al. (2024) выполнено сравнение интенсивности аккумуляции [ 18F]-ФДГ в миокарде ПЖ у 30 пациентов контрольной группы и 17 пациентов с ЛГ (10 — с ЛАГ, 7 — с ХТЭЛГ) [35]. У пациентов с ЛГ выявлена прямая зависимость между метаболизмом глюкозы в правых отделах сердца и показателями гемодинамики, установленными с помощью инвазивных методик: срДЛА и давлением в правом предсердии. Через 6 мес. после ЛАГ-специфической терапии повторно оценивали накопление [ 18F]-ФДГ в миокарде ПЖ у пациентов с ЛГ. Авторы отметили снижение аккумуляции [ 18F]-ФДГ в ПЖ на фоне лечения, которое не достигло статистической значимости по сравнению с исходными данными. Вероятно, отсутствие динамики показателей метаболизма миокарда ПЖ обусловлено незначимым снижением срДЛА и ЛСС через 6 мес. ЛАГ-специфической терапии и с уменьшением выборки к моменту контрольного ПЭТ/КТ вследствие смерти 5 пациентов с ЛГ.
В исследовании Oikawa М, et al. (2005) у 24 пациентов с ЛГ (15 — с ЛАГ, 9 — с ХТЭЛГ) выявлены положительные корреляционные взаимосвязи между уровнем накопления [ 18F]-ФДГ в миокарде ПЖ и уровнем ЛСС, срДЛА, давления в правом предсердии, содержанием BNP в сыворотке крови [36]. Корреляций между накоплением [ 18F]-ФДГ в миокарде ПЖ и толщиной его стенки или массой обнаружено не было. Данное заключение авторы объясняют тем, что метаболические изменения в ПЖ не всегда сопровождаются структурной перестройкой. По их мнению, сердце способно адаптировать метаболизм субстратов быстрее, чем изменять свою структуру. Непрерывная внутривенная терапия эпопростенолом была начата у 10 пациентов с ЛАГ, находившихся в тяжелом состоянии (функциональный класс III или IV). Через 3 мес. лечения у пациентов со снижением ЛСС >30%, наблюдалось снижение накопления [ 18F]-ФДГ в миокарде ПЖ, что коррелировало со степенью уменьшения срДЛА.
Fang W, et al. (2012) проанализировали показатели аккумуляции [ 18F]-ФДГ в миокарде ПЖ у 24 пациентов с ИЛАГ и 43 пациентов с ЛАГ, ассоциированной с врожденными пороками сердца [37]. Отношение накопления [ 18F]-ФДГ в миокарде ПЖ к накоплению РФЛП в миокарде ЛЖ достоверно коррелировало со срДЛА и ЛСС, отрицательно — с СИ. Кроме того, у 9 пациентов (3 с ИЛАГ и 6 с ЛАГ, ассоциированной с врожденными пороками сердца) после 6 мес. терапии силденафилом авторы зарегистрировали достоверное уменьшение этого показателя.
В проспективном исследовании Li W, et al. (2015) отношение накопления [ 18F]-ФДГ между миокардом ПЖ и ЛЖ служило независимым предиктором выживаемости у 45 пациентов с ИЛАГ [38]. Авторы сравнили два протокола сканирования: натощак (≥8 ч голодания), и после глюкозной нагрузки (50 г глюкозы перорально за 30 мин до инъекции [ 18F]-ФДГ). Оба протокола сканирования зарегистрировали накопление [ 18F]-ФДГ в миокарде желудочков. Однако данные, полученные при ПЭТ/КТ с глюкозной нагрузкой, обладали лучшей прогностической способностью в оценке функции ПЖ по сравнению с результатами ПЭТ/КТ, выполненной натощак. Авторы предполагают, что глюкозная нагрузка не только увеличивает общий захват [ 18F]-ФДГ, но избирательно подчеркивает различия между желудочками, усиливая контраст метаболической дисфункции ПЖ.
Tatebe S, et al. (2014) изучили прогностическую значимость накопления [ 18F]-ФДГ миокардом ПЖ у пациентов с ЛГ [39]. Среди 27 пациентов с ЛГ (18 — с ЛАГ и 9 — с ХТЭЛГ) у 15 было зарегистрировано клиническое ухудшение течения ЛГ, а в 11 случаях наступил летальный исход. Группа с ухудшением течения ЛАГ характеризовалась более высоким содержанием BNP в сыворотке крови, высоким функциональным классом, средним давлением в правом предсердии и легочной артерии, а также признаками тяжелого ремоделирования ПЖ по данным МРТ с увеличением массы миокарда ПЖ и тенденцией к снижению ФВ ПЖ. У пациентов с ухудшением течения ЛАГ регистрировался достоверно более высокий показатель накопления [ 18F]-ФДГ в свободной стенке ПЖ, скорректированный на эффект частичного объема (cRV-SUV) по сравнению с пациентами без ухудшения. Хотя не проводился прямой корреляционный анализ между cRV-SUV и показателями МРТ, функциональными, лабораторными, гемодинамическими параметрами; авторами была обнаружена статистически достоверная взаимосвязь между повышенным накоплением [ 18F]-ФДГ в ПЖ и уменьшением времени до наступления ухудшения течения ЛАГ. Результаты исследования демонстрируют клиническое значение применения ПЭТ/КТ с ФДГ для долгосрочного прогнозирования исходов у пациентов с ЛГ.
В настоящее время опубликованы единичные работы о прогностической значимости соотношения [ 18F]-ФДГ SUV ПЖ/SUV ЛЖ у пациентов с ЛАГ. Кроме того, отсутствие достаточного количества пациентов и периода наблюдения, разнородность исследуемых когорт пациентов в отношении этиологии ЛГ, возраста, используемых методов оценки тяжести ЛГ, существенно затрудняет интерпретацию данных.
В исследовании Kazimierczyk R, et al. (2021) оценивали соотношение полуколичественных показателей SUV ПЖ/SUV ЛЖ при гибридной ПЭТ/МРТ с [ 18F]-ФДГ у 26 пациентов с ЛАГ [40]. Когорта пациентов включала 17 пациентов с ИЛАГ/наследственной ЛАГ, 4 пациента с ЛАГ, ассоциированной с диффузными заболеваниями соединительной ткани, 5 пациентов с ЛАГ, ассоциированной с врожденными пороками сердца. Контрольная группа была представлена 12 пациентами без ЛГ. Часть пациентов с ЛАГ (n=12) получали ЛАГ-специфическую терапию на момент проведения исследования. Смерть, ухудшение функционального класса (по классификации Всемирной организации здравоохранения), госпитализация из-за прогрессирования ЛАГ или правожелудочковой СН использовались в качестве комбинированной конечной точки. У пациентов с ЛАГ регистрировалось значительное повышение соотношения SUV ПЖ/SUV ЛЖ (медиана 1,02) по сравнению с контрольной группой (медиана 0,16). Пациенты с SUV ПЖ/SUV ЛЖ >1 демонстрировали более выраженное снижение ФВ ПЖ по данным МРТ, повышение срДЛА и увеличение ЛСС. Также важно отметить, что у пациентов, достигших клинических конечных точек, отмечалось более высокое соотношение SUV ПЖ/SUV ЛЖ (1,21 vs 0,53) и сниженная ФВ ПЖ (37,9±5,2% vs 46,8±5,7%) при отсутствии статистически достоверных различий в показателях инвазивной гемодинамики. Авторы пришли к выводу, что исходные изменения в метаболизме ПЖ могут предшествовать развитию дисфункции ПЖ вследствие выраженной гемодинамической перегрузки правых камер сердца. Поскольку сочетание высокого исходного захвата глюкозы миокардом ПЖ и низкой ФВ ПЖ ассоциировалось с худшим прогнозом, единое гибридное исследование ПЭТ/МРТ позволило идентифицировать пациентов с более высоким риском неблагоприятных событий. При достижении комбинированной конечной точки пациентам проводилась эскалация ЛАГ-специфической терапии, что сопровождалось значимым уменьшением соотношения SUV ПЖ/SUV ЛЖ (на 33,9%) и коррелировало с улучшением ключевых гемодинамических показателей — повышением СИ, снижением срДЛА и ростом ФВ ПЖ по данным МРТ в динамике. Таким образом, эскалация ЛАГ-специфической терапии у пациентов с неблагоприятными прогностическими маркерами (исходное соотношение SUV ПЖ/SUV ЛЖ >1,0, ФВ ПЖ <40%) привело к снижению патологического захвата глюкозы в ПЖ [42].
В проведенном нами исследовании (2025) оценка метаболизма и перфузии миокарда ПЖ с применением ПЭТ/КТ с [ 18F]-ФДГ и ПЭТ/КТ с [ 13N]-аммонием проанализирована у 30 пациентов с ИЛАГ в зависимости от принадлежности к группам риска летальности шкалы ESC/ERS 2022 (рис. 3) [41].
Существенным отличием от других исследований была нозологическая однородность группы, ИЛАГ; невключение в исследование пациентов с сопутствующей патологией левых камер сердца, респираторной системы; и исследование как метаболизма, так и перфузии миокарда ПЖ. Другой особенностью данного исследования было включение большого числа пациентов с ИЛАГ с положительным вазореактивным тестом, которые преимущественно формировали группу низкого риска летальности и имели признаки легкой легочной васкулярной болезни с незначительным ремоделированием миокарда ПЖ по данным МРТ. Пациенты низкого риска летальности имели наименьшие показатели аккумуляции [ 18F]-ФДГ миокардом ПЖ по сравнению с пациентами промежуточного и высокого риска летальности. Более того, в группе низкого риска летальности уровень соотношения SUVПЖ/SUVЛЖ [ 18F]-ФДГ был сопоставим с контрольной группой без ЛАГ, однако показатель перфузии миокарда ПЖ был значительно выше по сравнению с контролями без ЛАГ. Полученные результаты мы интерпретировали как компенсацию метаболического запроса миокарда ПЖ за счет увеличения кровотока миокарда ПЖ у пациентов с ИЛАГ низкого риска. Мы соотнесли метаболизм миокарда ПЖ к перфузии и оказалось, что у пациентов с ИЛАГ промежуточного и высокого риска летальности наблюдалось прогрессирующее увеличение метаболического запроса при отсутствии прироста перфузии миокарда. Данное исследование было первой попыткой охарактеризовать уровень накопления [ 18F]-ФДГ и [ 13N]-аммония миокардом ПЖ в зависимости от категории риска летальности ESC/ERS 2022. Кроме того, мы подтвердили достоверные корреляционные взаимосвязи между показателями метаболизма и перфузии миокарда и уровнем срДЛА, ЛСС, показателями ремоделирования миокарда ПЖ (МРТ). В этой связи наибольший интерес, на наш взгляд, представляет группа низкого риска летальности, где, несмотря на статус низкого риска, вариабельность цифр срДЛА может быть существенной. Сохранение высокого срДЛА является основным фактором прогрессирования ремоделирования миокарда ПЖ и в конечном итоге, декомпенсации правожелудочковой СН и смерти [43]. ПЭТ/КТ остается дорогостоящим и нераспространенным диагностическим методом. У пациентов с промежуточным и высоким риском летальности неинвазивные методы (МРТ, ЭхоКГ, NT-proBNP) обычно достаточны для принятия решения об эскалации терапии. Мы полагаем, что в перспективе ПЭТ/КТ с [ 18F]-ФДГ будет наиболее целесообразно выполнять у пациентов с ИЛАГ с критериями низкого риска летальности как при первичной диагностике, так и при отсутствии возможности выполнения КПКС в периоде наблюдения для своевременной эскалации ЛАГ-специфической терапии. Однако необходимы дальнейшие исследования с большим числом пациентов для определения клинической значимости пороговых значений накопления [ 18F]-ФДГ в миокарде ПЖ с учетом этиологии ЛАГ, гемодинамики и ремоделирования правых камер сердца.
Заключение
Уровни накопления [ 18F]-ФДГ и [ 13N]-аммония миокардом ПЖ достоверно взаимосвязаны с тяжестью гемодинамической перегрузки у пациентов с ЛАГ и ремоделированием миокарда ПЖ. Необходимо продолжение работы над стандартизацией протоколов сканирования и накопления данных с целью определения пороговых значений ПЭТ/КТ с [ 18F]-ФДГ и [ 13N]-аммонием в зависимости от категорий риска летальности у пациентов с различной этиологией ЛАГ для адекватной стратификации риска и определения стратегии лечения. Возможность оценки метаболических и перфузионных отношений на тканевом уровне может помочь в поиске новых мишеней для терапевтического воздействия у пациентов с ЛАГ.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Маланова А.С., Гончарова Н.С., Рыжкова Д.В. Клиническое значение оценки метаболизма и перфузии миокарда правого желудочка с помощью позитронно-эмиссионной томографии, совмещенной с компьютерной томографией, у пациентов с легочной артериальной гипертензией (обзор литературы). Российский кардиологический журнал. 2025;30(2S):6495. https://doi.org/10.15829/1560-4071-2025-6495. EDN: XIYPJE
Скопировать