Эмпаглифлозин: путь от контроля гликемии к снижению сердечно-сосудистой смертности и госпитализаций по причине сердечной недостаточности
В 2021г на конгрессе Европейского общества кардиологов были представлены новые рекомендации по диагностике и лечению острой и хронической сердечной недостаточности (ХСН). Одним из ключевых вопросов, получивших новое решение в рекомендациях, стал алгоритм ведения пациентов с ХСН с низкой фракцией выброса (ФВ) левого желудочка (ХСНнФВ). В базовую терапию ХСНнФВ с классом рекомендаций I и уровнем доказательности А вошли блокаторы ренин-ангиотензиновой системы — ингибиторы ангиотензинпревращающего фермента (иАПФ) или антагонисты рецепторов ангиотензина и ингибиторы неприлизина (АРНИ), или блокаторы рецепторов ангиотензина II (БРА), а также бета-блокаторы (ББ), антагонисты минералокортикоидных рецепторов (АМКР) и ингибиторы натрийглюкозного котранспортера 2 типа (иНГЛТ2) [1]. Если традиционные подходы к лечению пациентов с ХСНнФВ предполагали нейрогуморальную блокаду при помощи иАПФ/БРА/АРНИ, ББ и АМКР, давно и успешно применяющихся при ХСН, то иНГЛТ2 включены в состав базовой терапии впервые. На протяжении последнего десятилетия иНГЛТ2 применяются у пациентов с сахарным диабетом 2 типа (СД2) для контроля уровня гликемии [2-4]. Хорошо известно, что СД2 относится к числу важнейших факторов развития и прогрессирования атеросклеротических сердечно-сосудистых заболеваний (ССЗ) и ХСН [5-7]. Длительный интенсивный контроль гликемии показал некоторое снижение риска развития сердечно-сосудистых осложнений [8], однако в ряде исследований не наблюдалось позитивного влияния на сердечно-сосудистый прогноз пациентов сахароснижающих препаратов [9-11]. Закономерно встал вопрос об изучении их возможности повлиять на риск развития сердечно-сосудистых событий и ХСН. В исследованиях EMPA-REG OUTCOME, CANVAS и DECLARE-TIMI 58 у пациентов с СД2 и выявленными ССЗ или факторами сердечно-сосудистого риска, получавших иНГЛТ2 (эмпаглифлозин, канаглифлозин, дапаглифлозин), было продемонстрировано снижение риска неблагоприятных сердечно-сосудистых осложнений, а также развития или ухудшения течения ХСН без учащения случаев гипогликемии по сравнению с группой плацебо [12- 14]. В более позднем исследовании эртуглифлозина VERTIS-CV у пациентов с СД2 и атеросклеротическими ССЗ было показано снижение риска госпитализаций по причине ХСН [15]. Однако только для эмпаглифлозина было показано снижение общей и сердечно-сосудистой смертности, что нашло отражение в действующей инструкции к препарату [12].
В исследовании EMPA-REG OUTCOME комбинированная первичная конечная точка включала сердечно-сосудистую смерть, нефатальные инфаркт миокарда (ИМ) и инсульт. В ключевую вторичную конечную точку входили компоненты первичной конечной точки и случаи госпитализации по поводу нестабильной стенокардии. Дополнительными заранее определенными конечными точками были сердечнососудистую смерть, ИМ, инсульт, общая смертность, госпитализация по поводу ХСН и комбинированная почечная конечная точка [16]. В группах пациентов, получавших эмпаглифлозин, было установлено значимое снижение относительного риска развития событий комбинированной первичной конечной точки на 14% (р=0,04), снижение риска сердечно-сосудистой смерти на 38% (р<0,001), риска смерти от любой причины — на 32% (р<0,001) и риска госпитализаций по причине ХСН — на 35% (р<0,002) [12].
Столь значительные преимущества эмпаглифлозина и других иНГЛТ2, полученные в больших многоцентровых рандомизированных клинических исследованиях, вызвали большой интерес к изучению механизмов действия этого класса препаратов в целом и каждого из них в отдельности. Особое внимание уделяется отличным от сахароснижающего действиям, которые могли бы объяснить полученные результаты. Были изучены такие гемодинамические эффекты, как снижение уровня артериального давления, преднагрузки и постнагрузки [17-19]. Эмпаглифлозин продемонстрировал способность уменьшать сосудистое сопротивление [20]. Весьма важным эффектом иНГЛТ2 является снижение симпатической активности [21][22]. Кроме того, в результате рандомизированных контролируемых исследований установлена способность иНГЛТ2 уменьшать массу миокарда левого желудочка (ММЛЖ). Эмпаглифлозин в исследовании EMPA-HEART продемонстрировал существенное влияние на ремоделирование левого желудочка (ЛЖ), выраженное в снижении индекса ММЛЖ у пациентов с СД2 и ишемической болезнью сердца [23]. Авторы сделали предположение, что снижение ММЛЖ могло послужить одним из механизмов улучшения прогноза у пациентов с СД2 и ССЗ в исследовании EMPA-REG OUTCOME. Исследование DAPA LVH также показало по данным магнитно резонансной томографии снижение ММЛЖ у пациентов с СД2 и гипертрофией ЛЖ, получавших дапаглифлозин, что может быть результатом известного натрийуреза и диуреза, свойственного иНГЛТ2 [24]. Именно этот механизм, по мнению ряда исследователей, лежит в основе позитивного влияния иНГЛТ2 на гемодинамику [25][26]. Кроме того, наблюдается в большей мере уменьшение интерстициальной, чем внутрисосудистой жидкости и повышение гематокрита, способствующее лучшей доставке к тканям кислорода [27-30]. В свою очередь, натрийурез регулирует тубулогломерулярную обратную связь, снижая давление в клубочках и, в конечном итоге, защищая почку [31].
Еще одним из описанных механизмов действия иНГЛТ2 является их способность влиять на активность мембранных Na+/H+-обменников (NHE) изоформ 1 и 3. Повышение активности NHE описано при ХСН и СД2 [31][32]. В эксперименте эмпаглифлозин подавлял активность NHE в кардиомиоцитах крыс и кроликов [33]. Подавление активности эмпаглифлозином изоформы 1 NHE на животных моделях сердечной недостаточности (СН) с сохраненной ФВ, не зависимо от наличия сахарного диабета, снижало явления клеточного апоптоза [34] и улучшало клеточный обмен Са2+, обусловленный повышением активности Са2+-АТФазы саркоплазматического ретикулума с последующим улучшением диастолической функции ЛЖ [35]. Благотворное влияние эмпаглифлозина на систолическую функцию и ремоделирование миокарда реализуется через улучшение энергетического метаболизма, повышение выработки глюкагона и кетонового ?-гидроксибутирата, увеличивая тем самым энергетические возможности миокарда [27][36-39].
Известно, что гиперурикемия является независимым фактором риска развития ХСН, в т.ч. СН с сохраненной ФВ ЛЖ [40][41]. В метаанализе Zhao Y, et al. (2018) было показано быстрое и устойчивое снижение уровня мочевой кислоты при назначении иНГЛТ2 [42]. В последние годы воспаление и фиброз рассматриваются в числе патогенетических механизмов развития ХСН [43]. Кардиопротективный эффект эмпаглифлозина на модели ХСН проявился в снижении экспрессии циклооксигеназы-2 и интерлейкина-1? не зависимо от наличия диабета [44]. На модели реперфузионного повреждения миокарда и гипоксии уменьшение площади ИМ и улучшение сократимости, вызванное эмпаглифлозином, было опосредовано его влиянием на сигнальные пути АМФ-активированной протеинкиназы [45].
Таким образом, все известные на сегодняшний день эффекты иНГЛТ2 весьма разнообразны и требуют объемного описания. В 2020г было опубликовано мнение экспертов Ассоциации сердечной недостаточности Европейского общества кардиологов, где различные механизмы были систематизированы с выделением четырех основных групп: сосудистые и гемодинамические эффекты, почечные эффекты, кардиальные эффекты и метаболические эффекты [46]. Одновременно с изучением различных механизмов иНГЛТ2 были спланированы многоцентровые рандомизированные клинические исследования ХСНнФВ. В 2019г были представлены результаты исследования DAPA-HF, продемонстрировавшие преимущество дапаглифлозина у пациентов с ХСНнФВ не зависимо от наличия СД2 [47]. В большую программу исследований эмпаглифлозина EMPOWER в т.ч. вошли исследования EMPEROR-Reduced и EMPEROR-Preserved, посвященные изучению сердечно-сосудистых исходов у пациентов с СД2 и без СД2 и ФВ ЛЖ ?40% (EMPEROR-Reduced) и >40% (EMPEROR-Preserved) [48][49].
В рандомизированное двойное слепое плацебо контролируемое исследование EMPEROR-Reduced было включено 3730 пациентов старше 18 лет с ХСН с ФВ ЛЖ ?40%, II-IV функционального класса по классификации NYHA, госпитализацией по причине ХСН в последние 12 мес., повышением уровня N-терминального промозгового натрийуретического пептида (NT-proBNP) и скоростью клубочковой фильтрации (рСКФ) >20 мл/мин/1,73 м2. Все пациенты получали лечение по поводу ХСН иАПФ/БРА/АРНИ, ББ, АМКР. В группу, получавшую эмпаглифлозин в дозе 10 мг/сут., вошли 1863 пациента, в группу плацебо — 1887 пациентов. Первичная конечная точка включала в себя смерть от сердечно-сосудистых причин или госпитализации по причине СН. Вторичными конечными точками были: первая или повторные госпитализации по причине СН, угловой коэффициент изменения рСКФ по сравнению с исходным уровнем (расчет проводился по формуле CKD-EPI). По демографическим и клиническим характеристикам группы не отличались друг от друга. В обеих группах СД2 страдали 49,8% пациентов, ФВ ЛЖ ?30% была у 73% и NT-proBNP ?1000 пг/мл была у 79% пациентов. В группе эмпаглифлозина 70,5% пациентов получали иАПФ или БРА, АРНИ получали 18,5%, ББ — 94,7% и АМКР — 70,1% пациентов. Таким образом, большая часть включенных в исследование пациентов получала рекомендованную лекарственную терапию ХСН. Кардиовертердефибрилятор был имплантирован у 31% пациентов и ресинхронизирующая терапия проведена 11,8% пациентов. Медиана наблюдения составила 16 мес.
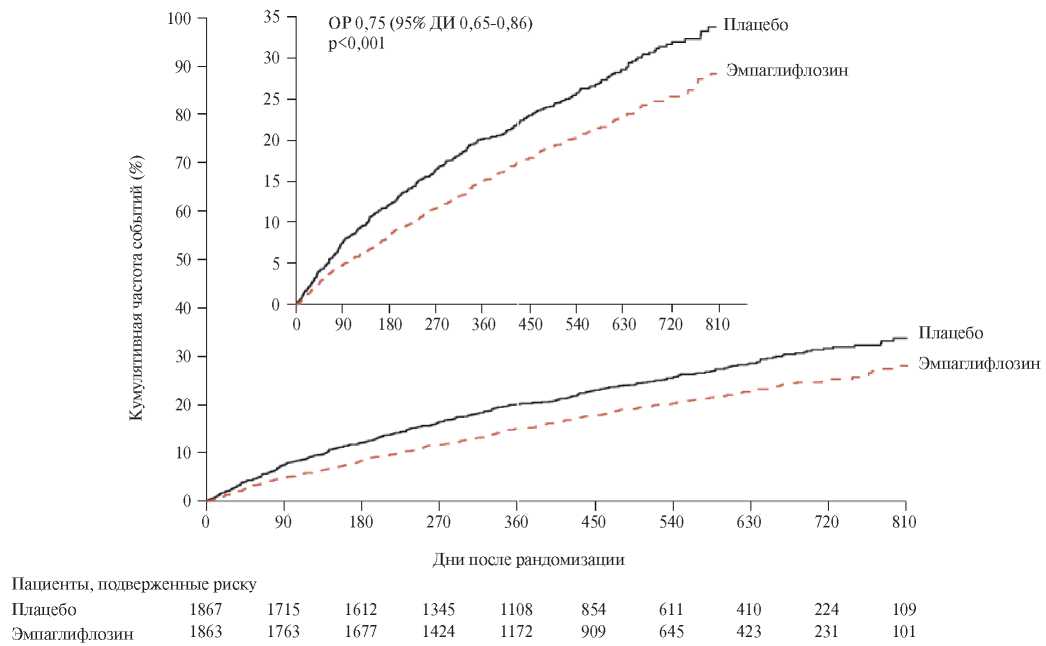
Первичная конечная точка развилась у 19,4% пациентов в группе эмпаглифлозина и у 24,7% в группе плацебо (отношение рисков (ОР) 0,75; 95% доверительный интервал (ДИ) 0,65-0,86; р<0,001) (рис. 1). Таким образом, относительный риск наступления первичной конечной точки в группе эмпаглифлозина был на 25% ниже, чем в группе плацебо. Столь существенное преимущество эмпаглифлозина было достигнуто в основном за счет снижения риска госпитализаций (ОР 0,69; 95% ДИ 0,59-0,81), хотя и в отношении смерти от сердечно-сосудистых причин наблюдалось снижение относительного риска на 8%. Обращает на себя внимание факт преимущества эмпаглифлозина во всех подгруппах пациентов, которое не зависело от пола, возраста пациента, наличия СД2, функции почек, причины развития ХСН и ряда других факторов. Наконец, эффективность эмпаглифлозина не зависела от лекарственной терапии ХСН — приема пациентами АМКР и АРНИ.

Рис. 1. Первичная конечная точка. Смерть от сердечно-сосудистых причин или госпитализации по причине ХСН.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Число всех госпитализаций по причине СН было ниже в группе эмпаглифлозина и составило 388 vs 553 (ОР 0,70; 95% ДИ 0,58-0,85, р<0,001) в группе плацебо (рис. 2). Снижение относительного риска любой госпитализации по причине ХСН составило 30%. В субанализе клинической стабильности была также показана меньшая частота госпитализаций, потребовавших внутривенного введения вазопрессоров и диуретиков пациентам в группе эмпаглифлозина. Авторы сделали заключение о снижении у пациентов с ХСНнФВ, получавших эмпаглифлозин, риска и общего количества случаев ухудшения СН как в стационарных, так и амбулаторных условиях, при этом положительные эффекты наблюдались сразу после начала лечения и сохранялись в течение всего периода терапии [50]. Другая вторичная конечная точка была посвящена изучению функции почек. Скорость снижения рСКФ в течение периода лечения была медленнее в группе эмпаглифлозина, чем в группе плацебо (-0,55 мл/мин/1,73 м2 в год vs -2,28 мл/мин/1,73 м2 в год), составив разницу между группами в 1,73 мл/мин/1,73 м2 в год (95% ДИ 1,10- 2,37; р<0,001) (рис. 3). На первичную и вторичные конечные точки не влияло и наличие признаков задержки жидкости при включении пациентов в исследование [51].

Рис. 2. Первичная и повторная госпитализации по причине ХСН.
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.

Рис. 3. Изменения рСКФ.
Сокращения: ДИ — доверительный интервал, рСКФ — расчетная скорость клубочковой фильтрации.
Среди результатов заранее запланированного анализа результатов исследования EMPEROR-Reduced хочется отметить снижение на 50% риска развития комбинированной почечной конечной точки, включавшей в себя потребность в хроническом диализе или в пересадке почки, или устойчивое снижение рСКФ <15 мл/мин/1,73 м2 (ОР 0,50; 95% ДИ 0,32-0,77). Вторичный анализ исследования, посвященный зависимости эффективности эмпаглифлозина от определенного по Канзасскому опроснику качества жизни пациентов показал, что эмпаглифлозин снижал риск сердечно-сосудистой смерти или госпитализации по поводу СН во всем диапазоне исходного состояния качества жизни и обеспечивал раннее устойчивое и клинически значимое снижение бремени симптомов и улучшение качества жизни пациентов [52].
Особо хочется отметить высокую безопасность эмпаглифлозина. В группе пациентов и с СД2 и без СД2, получавших эмпаглифлозин, в сравнении с группой плацебо не наблюдалось роста доли случаев симптомной гипотонии, кетоацидоза и гипогликемии. В группе эмпаглифлозина было больше случаев генитальных инфекций, чем в группе плацебо (31 случай (1,7%) и 12 случаев (0,6%), соответственно), что объясняется характерной для всех иНГЛТ2 глюкозурией. Соблюдение правил гигиены является эффективным способом профилактики урогенитальных инфекций.
Таким образом, исследование EMPEROR-Reduced показало, что применение у пациентов с ХСНнФВ эмпаглифлозина ведет к эффективному и безопасному снижению риска сердечно-сосудистой смерти или госпитализации по поводу ХСН и замедлению прогрессирования ухудшения функции почек, независимо от наличия или отсутствия СД2, и позволило включить эмпаглифлозин в состав базовой четырехкомпонентной терапии ХСНнФВ.
Отношения и деятельность. Материал подготовлен при поддержке ООО “Берингер Ингельхайм”.
Чтобы читать статью войдите с логином и паролем от scardio.ru
Ключевые слова
Для цитирования
Хасанов Н.Р. Эмпаглифлозин: путь от контроля гликемии к снижению сердечно-сосудистой смертности и госпитализаций по причине сердечной недостаточности. Российский кардиологический журнал. 2021;26(4S):4807. https://doi.org/10.15829/1560-4071-2021-4807
Скопировать